Analizar la eficacia y seguridad de las dosis bajas de factor activador del plasminógeno (rt-PA) en el tratamiento de las trombosis venosas y/o arteriales en niños
Pacientes y métodosEstudio clínico prospectivo observacional en el que se estudiaron 18 pacientes de edades comprendidas entre 1 mes y 11 años que recibieron tratamiento fibrinolítico en perfusión intravenosa continua con dosis bajas de rt-PA. (0,01-0,06mg/kg/h).
ResultadosUn 94% de los pacientes mejoraron con el tratamiento con dosis bajas de rt-PA (72% con resolución completa del trombo y 22% resolución parcial). Un paciente presentó una hemorragia grave y precisó suspender el tratamiento. La incidencia de efectos secundarios graves fue baja (5%).
ConclusionesEl tratamiento con dosis bajas de rt-PA (0,01-0,05mg/kg/h) es efectivo en un elevado porcentaje de niños con trombosis aguda arterial y/o venosa y con un relativo bajo porcentaje de riesgo de sangrado.
To analyse the efficacy and side effects of low doses of tissue plasminogen activator for the treatment of acute arterial and/or venous thrombosis in children.
Patients and methodsProspective observational clinical study. 18 children between 1 months and 11 years treated with low doses (0.01-0.06mg/kg/h) of continuous intravenous thrombolytic therapy with t-PA were studied.
ResultsA total of 94% of patients improved with low doses t-PA (72% complete resolution of the thrombosis and 22% partial resolution). One patient suffered a severe haemorrhage secondary to t-Pa and had to stop the treatment. The incidence of severe side effects was low (5%)
ConclusionsThrombolytic therapy with low doses of t-PA (0.01-0.05mg/kg/h) is effective in a high percentage of children with acute arterial and/or venous thrombosis and produces a relatively low frequency of side effects.
Las trombosis intravasculares constituyen un problema cada vez más frecuente en niños, principalmente en los niños hospitalizados en las unidades de cuidados intensivos pediátricos1–5.
Las causas más frecuentes de trombosis son la canalización vascular arterial o venosa, el cateterismo para realizar estudios hemodinámicos y la cirugía cardiaca5,6, siendo mucho menos frecuentes las trombofilias hereditarias1,6.
Las consecuencias principales de una trombosis intravascular son la isquemia del tejido u órgano afectado por la obstrucción, la propagación del trombo y embolización del mismo y el riesgo de infección5,7,8. La trombosis de una fístula sistémico-pulmonar, que es el conducto vascular artificial que se implanta con más frecuencia en la infancia, produce isquemia pulmonar e hipoxemia grave, que pueden llevar al fallecimiento del paciente.
Los fármacos antitrombóticos más utilizados son la heparina, los anticoagulantes orales, los antiagregantes y los fibrinolíticos5,9. Los fibrinolíticos producen una resolución del trombo de forma más rápida y eficaz que la heparina. Actúan activando el plasminógeno y produciendo la degradación de la fibrina y fibrinógeno, dando lugar a los productos de degradación del fibrinógeno (PDF) y el dímero-D.
El tratamiento fibrinolítico es útil para desobstruir catéteres trombosados (intravasculares o peritoneales) o lisar coágulos de grandes vasos y está indicado cuando fracasa la anticoagulación o cuando es preciso el reestablecimiento del flujo de forma urgente, como en el caso de infarto agudo de miocardio, tromboembolismo pulmonar o cerebral, y trombosis aguda arterial o venosa con importante repercusión clínica1,2,4,6,9,10.
El factor activador del plasminógeno recombinante (rt-PA) es una glucoproteína obtenida por ingeniería genética que tiene un efecto más rápido que la uroquinasa sobre las trombosis intravasculares y presenta una vida media más corta. Sin embargo, el rt-PA produce mayor número de complicaciones hemorrágicas4,6,8.
En niños existen pocos estudios que hayan analizado la eficacia y seguridad del rt-PA y no se conoce bien cuál es la dosis más adecuada1–4,6–8,11. Existen dos pautas de tratamiento: la dosis estándar (0,1-0,5mg/kg/h) y la dosis baja (0,01-0,05mg/kg/h). Algunos autores han encontrado que las dosis bajas tienen una efectividad similar a la dosis estándar con menor incidencia de efectos secundarios1–4,6,7,11.
Para valorar el efecto del tratamiento, se deben realizar controles periódicos de coagulación, objetivando una elevación del tiempo parcial de tromboplastina, tiempo de trombina parcialmente activado, y del D-dímero y PDF, y una disminución del fibrinógeno1,4,6,8,9.
El efecto adverso más frecuente derivado del uso de fibrinolíticos es el sangrado. Las complicaciones hemorrágicas están relacionadas con el tiempo de tratamiento y las dosis mayores del mismo. En ocasiones, es leve por zonas de punción, pero en otros casos puede ser importante y precisar la suspensión del tratamiento1–4,6.
El objetivo de nuestro estudio ha sido valorar la eficacia y la seguridad del tratamiento con dosis bajas de rt-PA de la trombosis arterial o venosa en niños.
Pacientes y métodosSe realizó un estudio observacional, prospectivo, con intervención. Se incluyó en el estudio a los niños críticos de 1 mes a 16 años ingresados en el servicio de cuidados intensivos pediátricos en los que se realizó tratamiento fibrinolítico con rt-PA entre 2005 y 2009. Los pacientes fueron incluidos en el estudio tras el consentimiento informado de sus padres o tutores.
Las indicaciones de tratamiento de rt-PA fueron: evidencia o sospecha clínica de trombosis intravascular (arterial o venosa) asociada o no a catéter, trombosis endocavitaria, tromboembolismo pulmonar y coagulación intravascular diseminada.
El diagnóstico de trombosis se realizó mediante diagnóstico clínico (en caso de trombosis arterial, palidez y frialdad de las extremidades con disminución del pulso por riego inadecuado; y en caso de trombosis venosa, tumefacción y edema), ecografía, y/o veno o arteriografía.
La administración de rt-PA se realizó como perfusión continua intravenosa sistémica. con dosis bajas (0,01-0,06mg/kg/h). Previo al tratamiento con rt-PA, se administró plasma fresco congelado (dosis 10ml/kg) para asegurar unos niveles de fibrinógeno y plasminógeno óptimos y disminuir el riesgo de sangrado.
El tratamiento se finalizó cuando se produjo la resolución o mejoría significativa de la sintomatología clínica, se objetivó la resolución parcial o total del trombo y/o aparecieron efectos secundarios importantes. Durante el tratamiento se evitaron en la medida de lo posible procedimientos invasivos como inyecciones intramusculares, sondaje vesical y canalización de vías arteriales y venosas centrales.
En cada paciente se recogieron datos demográficos (edad, sexo, peso), clínicos (diagnóstico, antecedentes, cirugía o cateterismo reciente, canalización vascular), analíticos (hemoglobina, plaquetas, estudio de coagulación, D-dímero), tratamientos (anticoagulantes, antiagregantes, fibrinolíticos), dosis y duración del tratamiento, Durante el tratamiento se realizó monitorización clínica y analítica, realizándose controles seriados (hemograma y coagulación) antes, durante y 12-24 h después del tratamiento.
La efectividad del tratamiento se valoró mediante la mejoría de la sintomatología clínica (recuperación del pulso periférico y perfusión de la extremidad) y la disminución y/o desaparición del trombo por ecografía y/o radiografía. Se definió lisis completa como la resolución del trombo en un 95%, y lisis parcial en un 50-95%1,6.
Se registraron la aparición de efectos secundarios: hemorragia, necesidad de hemoderivados y la mortalidad secundaria al tratamiento. Se definió hemorragia grave como un sangrado a nivel intracraneal o retroperitoneal, o aquel que tuvo repercusión hematológica precisando transfusión de concentrado de hematíes. La hemorragia leve se definió como sangrado a nivel de puntos de punción, epistaxis, sangrado de la mucosa oral, hematuria, melena o hematomas, que no producía alteración hematológica ni hemodinámica12.
Se realizó análisis estadístico de los resultados mediante el programa SPSS, versión 16.0. utilizando el test exacto de Fisher y el test no paramétrico de Wilcoxon para la comparación de variables. Se consideró significativa una p<0,05.
ResultadosDurante el periodo de estudio, 18 pacientes de edades comprendidas entre los 33 días de vida y los 11 años y media de 38 meses fueron tratados con rt-PA. Un 44% eran menores de un año; 17 pacientes presentaban cardiopatías congénitas en los que se había realizado cirugía o cateterismo y un paciente presentaba síndrome de Klippel-Feil.
Seis pacientes presentaban trombosis venosa, 5 arterial y 2 ambas simultáneamente. En dos existía trombosis del conducto de Fontán, en dos de fístulas sistémico-pulmonares y en una un trombo en aurícula derecha.
Catorce pacientes habían sido sometidos a una cirugía previa: 3 cirugía de Glenn, 6 cirugía de Fontán, 2 cierre de comunicación interventricular o interauricular, 1 cirugía correctora de tetralogía de Fallot y 2 cirugía de válvula mitral. En 12 niños la trombosis estaba relacionada con el catéter, en uno con cateterismo (y en 5 casos fue posquirúrgica).
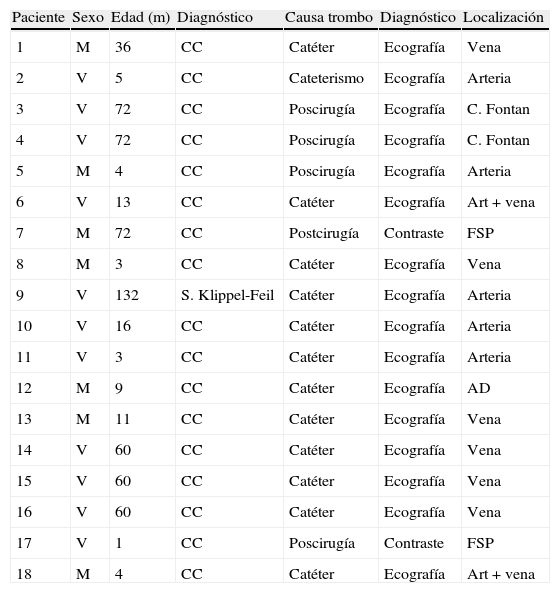
El diagnóstico se realizó por ecografía en 16 pacientes y en 2 mediante el cateterismo con contraste. La tabla 1 resume las características clínicas de los pacientes, la localización del trombo y el método diagnóstico utilizado.
Características clínicas, localización del trombo y métodos diagnósticos
| Paciente | Sexo | Edad (m) | Diagnóstico | Causa trombo | Diagnóstico | Localización |
| 1 | M | 36 | CC | Catéter | Ecografía | Vena |
| 2 | V | 5 | CC | Cateterismo | Ecografía | Arteria |
| 3 | V | 72 | CC | Poscirugía | Ecografía | C. Fontan |
| 4 | V | 72 | CC | Poscirugía | Ecografía | C. Fontan |
| 5 | M | 4 | CC | Poscirugía | Ecografía | Arteria |
| 6 | V | 13 | CC | Catéter | Ecografía | Art+vena |
| 7 | M | 72 | CC | Postcirugía | Contraste | FSP |
| 8 | M | 3 | CC | Catéter | Ecografía | Vena |
| 9 | V | 132 | S. Klippel-Feil | Catéter | Ecografía | Arteria |
| 10 | V | 16 | CC | Catéter | Ecografía | Arteria |
| 11 | V | 3 | CC | Catéter | Ecografía | Arteria |
| 12 | M | 9 | CC | Catéter | Ecografía | AD |
| 13 | M | 11 | CC | Catéter | Ecografía | Vena |
| 14 | V | 60 | CC | Catéter | Ecografía | Vena |
| 15 | V | 60 | CC | Catéter | Ecografía | Vena |
| 16 | V | 60 | CC | Catéter | Ecografía | Vena |
| 17 | V | 1 | CC | Poscirugía | Contraste | FSP |
| 18 | M | 4 | CC | Catéter | Ecografía | Art+vena |
AD: aurícula derecha; CC: cardiopatía congénita; FSP: fístula sistémico-pulmonar; NV: no valorable.
Los 18 pacientes recibieron dosis bajas de rt-PA (0,01-0,06mg/kg/h), con una media de 0,026 y DS (0,011). En 14 de ellos se administró un bolo previo de 0,05-0,1mg/kg; 13 pacientes habían recibido otro tratamiento (heparina, antiagregantes o uroquinasa) antes del rt-PA. En 16 pacientes (88,9%) se administró plasma fresco congelado previamente a la rt-PA y en 9 (50%) se administró heparina en perfusión continua de forma conjunta con el rt-PA, dosis media 21 U/kg/h, DS 15,6. La duración media del tratamiento fue de 32 h (DS 14), rango 6 a 48 h.
El tratamiento fue efectivo en un 94% de los niños. En todos los pacientes se comprobó la resolución del trombo por ecografía excepto en uno que se consideró tratamiento efectivo por la clínica que presentó el paciente tras el tratamiento. En un paciente tratado con dosis de 0,05mg/kg/h se finalizó el tratamiento por sangrado a través del tubo endotraqueal con anemización, precisando transfusión de concentrado de hematíes.
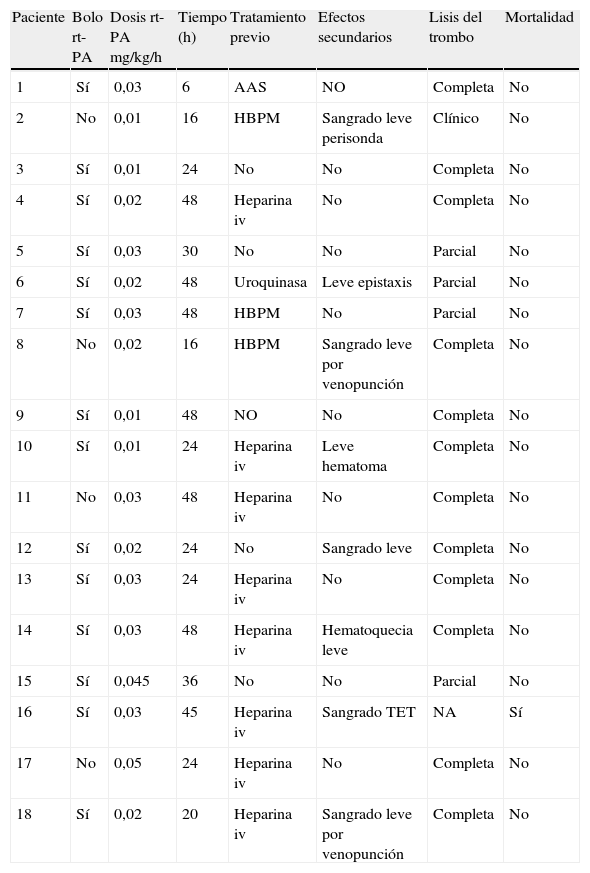
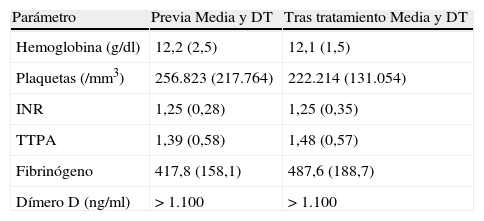
La mortalidad fue del 5,5% (1 paciente). La tabla 2 recoge el tratamiento de los pacientes y su evolución clínica y la tabla 3 los resultados de los controles analíticos previos, durante y tras el tratamiento. No se encontraron diferencias significativas entre los valores antes y después del tratamiento en ninguno de los parámetros.
Tratamiento y evolución clínica
| Paciente | Bolo rt-PA | Dosis rt-PA mg/kg/h | Tiempo (h) | Tratamiento previo | Efectos secundarios | Lisis del trombo | Mortalidad |
| 1 | Sí | 0,03 | 6 | AAS | NO | Completa | No |
| 2 | No | 0,01 | 16 | HBPM | Sangrado leve perisonda | Clínico | No |
| 3 | Sí | 0,01 | 24 | No | No | Completa | No |
| 4 | Sí | 0,02 | 48 | Heparina iv | No | Completa | No |
| 5 | Sí | 0,03 | 30 | No | No | Parcial | No |
| 6 | Sí | 0,02 | 48 | Uroquinasa | Leve epistaxis | Parcial | No |
| 7 | Sí | 0,03 | 48 | HBPM | No | Parcial | No |
| 8 | No | 0,02 | 16 | HBPM | Sangrado leve por venopunción | Completa | No |
| 9 | Sí | 0,01 | 48 | NO | No | Completa | No |
| 10 | Sí | 0,01 | 24 | Heparina iv | Leve hematoma | Completa | No |
| 11 | No | 0,03 | 48 | Heparina iv | No | Completa | No |
| 12 | Sí | 0,02 | 24 | No | Sangrado leve | Completa | No |
| 13 | Sí | 0,03 | 24 | Heparina iv | No | Completa | No |
| 14 | Sí | 0,03 | 48 | Heparina iv | Hematoquecia leve | Completa | No |
| 15 | Sí | 0,045 | 36 | No | No | Parcial | No |
| 16 | Sí | 0,03 | 45 | Heparina iv | Sangrado TET | NA | Sí |
| 17 | No | 0,05 | 24 | Heparina iv | No | Completa | No |
| 18 | Sí | 0,02 | 20 | Heparina iv | Sangrado leve por venopunción | Completa | No |
AAS: ácido acetilsalicílico; HBPM: heparina de bajo peso molecular; NA: no analizada por fallecimiento del paciente; TET: tubo endotraqueal.
Evolución de los parámetros analíticos
| Parámetro | Previa Media y DT | Tras tratamiento Media y DT |
| Hemoglobina (g/dl) | 12,2 (2,5) | 12,1 (1,5) |
| Plaquetas (/mm3) | 256.823 (217.764) | 222.214 (131.054) |
| INR | 1,25 (0,28) | 1,25 (0,35) |
| TTPA | 1,39 (0,58) | 1,48 (0,57) |
| Fibrinógeno | 417,8 (158,1) | 487,6 (188,7) |
| Dímero D (ng/ml) | > 1.100 | > 1.100 |
INR: índice normalizado internacional; TTPA: tiempo de tromboplastina activado.
Diferencias no significativas en ninguno de los parámetros al comparar antes y después del tratamiento.
La frecuencia de trombosis en pacientes pediátricos está aumentando en los últimos años1–5. Por ello, el tratamiento fibrinolítico es cada vez más utilizado.
Los agentes fibrinolíticos se clasifican en: de primera generación, como la uroquinasa y estreptoquinasa, que producen una activación inespecífica del plasminógeno; de segunda generación, como el activador recombinante tisular del plasminógeno (rt-PA o Actylise), y de tercera generación, el reteplasa o mini rt-PA, la TNK-PA, la estafiloquinasa y los anticuerpos monoclonales9,10. Los fibrinolíticos actualmente más utilizados en pacientes pediátricos son la uroquinasa y el rt-PA. La estreptoquinasa no está recomendada porque puede producir reacciones alérgicas y desarrollar anticuerpos frente al tratamiento4,6.
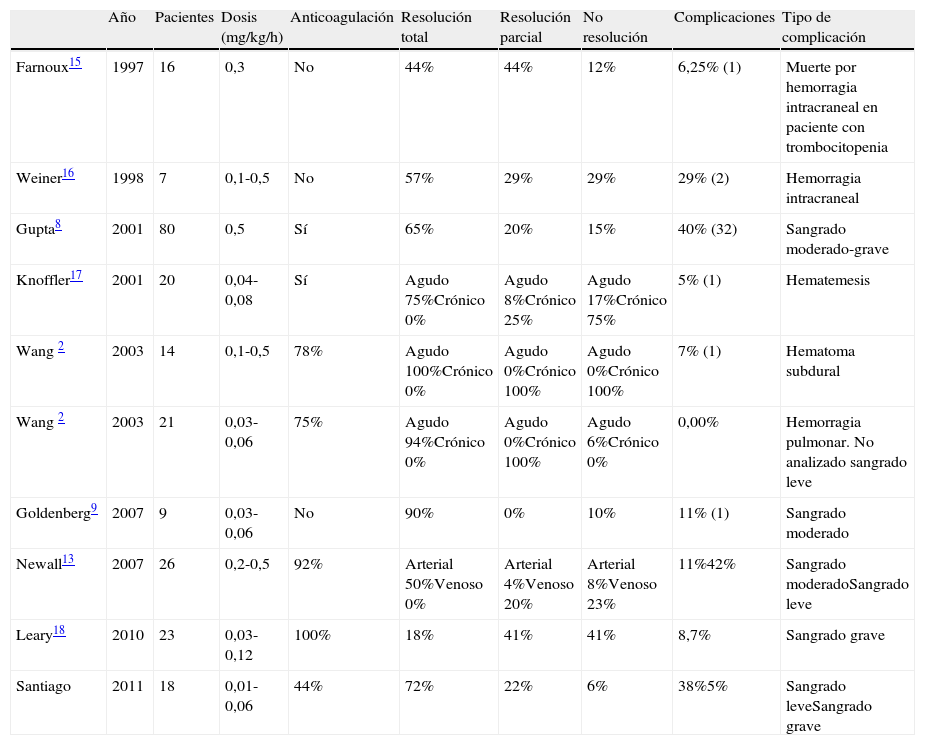
La experiencia con tratamiento con rt-PA en niños todavía es escasa1–4,6,7,11,13–18. La tabla 4 compara los resultados de los trabajos realizados en niños con rt-PA.
Comparación de los estudios de utilización de rt-PA en niños
| Año | Pacientes | Dosis (mg/kg/h) | Anticoagulación | Resolución total | Resolución parcial | No resolución | Complicaciones | Tipo de complicación | |
| Farnoux15 | 1997 | 16 | 0,3 | No | 44% | 44% | 12% | 6,25% (1) | Muerte por hemorragia intracraneal en paciente con trombocitopenia |
| Weiner16 | 1998 | 7 | 0,1-0,5 | No | 57% | 29% | 29% | 29% (2) | Hemorragia intracraneal |
| Gupta8 | 2001 | 80 | 0,5 | Sí | 65% | 20% | 15% | 40% (32) | Sangrado moderado-grave |
| Knoffler17 | 2001 | 20 | 0,04-0,08 | Sí | Agudo 75%Crónico 0% | Agudo 8%Crónico 25% | Agudo 17%Crónico 75% | 5% (1) | Hematemesis |
| Wang 2 | 2003 | 14 | 0,1-0,5 | 78% | Agudo 100%Crónico 0% | Agudo 0%Crónico 100% | Agudo 0%Crónico 100% | 7% (1) | Hematoma subdural |
| Wang 2 | 2003 | 21 | 0,03-0,06 | 75% | Agudo 94%Crónico 0% | Agudo 0%Crónico 100% | Agudo 6%Crónico 0% | 0,00% | Hemorragia pulmonar. No analizado sangrado leve |
| Goldenberg9 | 2007 | 9 | 0,03-0,06 | No | 90% | 0% | 10% | 11% (1) | Sangrado moderado |
| Newall13 | 2007 | 26 | 0,2-0,5 | 92% | Arterial 50%Venoso 0% | Arterial 4%Venoso 20% | Arterial 8%Venoso 23% | 11%42% | Sangrado moderadoSangrado leve |
| Leary18 | 2010 | 23 | 0,03-0,12 | 100% | 18% | 41% | 41% | 8,7% | Sangrado grave |
| Santiago | 2011 | 18 | 0,01-0,06 | 44% | 72% | 22% | 6% | 38%5% | Sangrado leveSangrado grave |
Nuestro estudio demuestra que el tratamiento con rt-PA a dosis baja es efectivo en el tratamiento de la trombosis aguda, arterial, venosa o de conductos, lo que coincide con lo referido por otros autores. La efectividad encontrada en nuestro estudio es similar a la referida previamente en otros trabajos (tabla 4).
Las dosis bajas de rt-PA son tan efectivas como las dosis altas con menores efectos secundarios1–4,6,7,11. Sin embargo, un estudio reciente ha encontrado que algunos pacientes que no responden con dosis de 0,03 a 0,06 sí lo hacen al aumentar la dosis a 0,12 mg/kg/h18.
Nuestro estudio demuestra que el tratamiento fibrinolítico con rt-PA a dosis bajas es muy efectivo como tratamiento de la trombosis aguda arterial y venosa en el niño. Aunque no se ha realizado una comparación entre las dosis altas y bajas de rt-PA, con los datos de nuestro estudio y los referidos en la literatura, consideramos que no existe justificación ética para realizar un estudio comparativo que incluya a pacientes tratados con dosis altas de rt-PA.
El efecto adverso más frecuente derivado del uso de fibrinolíticos es el sangrado. Las complicaciones hemorrágicas están relacionadas con el tiempo de tratamiento y las dosis más elevadas. La incidencia de efectos secundarios con dosis bajas de RT-PA fue significativamente menor que con la dosis alta1–4,6,7,11. En nuestra experiencia previa, 3 de 5 pacientes tratados con dosis altas de heparina presentaron sangrado importante que precisó la suspensión del tratamiento. La importancia de la hemorragia puede variar desde leve en los puntos de punción, a muy importante y precisar la suspensión del tratamiento1–4,6.
La incidencia de efectos secundarios graves en nuestro estudio es similar a la descrita en la literatura2,3,8,9,15–18. Sin embargo, aunque con dosis bajas de rt-PA la frecuencia de efectos secundarios sea menor, es necesario realizar un cuidadoso seguimiento clínico y analítico de todos los niños que reciben tratamiento fibrinolítico por el riesgo de presentar hemorragias graves.
Concluimos que el tratamiento con rt-PA en dosis bajas (0,01-0,05mg/kg/h) es efectivo para el tratamiento de la trombosis aguda en niños y produce menos efectos secundarios que las dosis altas. En nuestro estudio, la efectividad del tratamiento no se relacionó con la edad, la duración del tratamiento, la administración concomitante de heparina ni la evolución de los controles de coagulación.
FinanciaciónEl estudio ha sido realizado con la ayuda de la Red de Salud Materno Infantil y del Desarrollo SAMID RD08/0072 del Instituto Carlos III del VI programa marco Nacional 2008-2011.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A las enfermeras y médicos del Servicio de Cuidados Intensivos Pediátricos del Hospital General Universitario Gregorio Marañón y al Dr. José Luis Zunzunegui, de la Sección de Cardiología Pediátrica, por su colaboración en el estudio.