A día 1 de mayo de 2020, la enfermedad por coronavirus SARS-CoV-2 (COVID-19) ha afectado a más de 3.181.000 de personas en todo el mundo y causado más de 220.000 muertes. Aproximadamente un 1% de los casos ocurren en niños menores de 10 años, mayoritariamente con un curso clínico leve1. Los pacientes oncológicos sometidos a quimioterapia podrían ser más vulnerables a las complicaciones asociadas a la COVID-19, como han sugerido Liang et al.2, pero los datos en pacientes oncológicos pediátricos son escasos3.
Presentamos el caso de un niño de 20 meses de edad, diagnosticado 2 meses antes de leucemia linfoblástica aguda B de alto riesgo con reordenamiento de KMT2A-MLLT3.
Al final del segundo bloque en la fase de inducción, el paciente desarrolló neutropenia febril en ausencia de síntomas respiratorios o cualquier otro signo de infección focal. Dada la alta prevalencia de COVID-19 en España, además de los cultivos de sangre y orina se realizó una prueba para la detección de SARS-CoV-2 mediante reacción en cadena de la polimerasa con transcripción inversa en tiempo real (RT-PCR) en muestra de aspirado nasofaríngeo, cuyo resultado fue negativo. Se inició antibioterapia empírica con piperacilina-tazobactam y amikacina, de acuerdo con las guías locales para el manejo de la neutropenia febril. A las 12h del ingreso el paciente desarrolló taquipnea y se escucharon crepitantes en base izquierda a la auscultación. En este momento se repitió la RT-PCR para detección del SARS-CoV-2 test, con resultado positivo, mientras que la radiografía de tórax fue normal. Horas después, el paciente desarrolló hipoxemia que requirió oxigenoterapia, y se inició tratamiento con hidroxicloroquina y azitromicina orales, como han propuesto Gautret et al.4. En los hemocultivos obtenidos al ingreso se detectó la presencia de Streptococcus mitis, por lo que se interrumpió la amikacina y se inició tratamiento con vancomicina. Debido a la aplasia posquimioterapia, se realizó transfusión de glóbulos rojos y plaquetas. No hubo signos de inestabilidad hemodinámica, coagulopatía, sobrecarga hídrica, fallo renal o hepático. En los 6 días siguientes el niño se mantuvo hipoxémico con distrés respiratorio y fiebre a diario, requiriendo oxigenoterapia de alto flujo (flujo máximo de 2l/kg/min con FiO2 del 30-40%). Una radiografía de tórax adicional reveló la presencia de una condensación hiliar y basal izquierda.
Dada la persistencia de la neutropenia febril, se inició tratamiento empírico con anfotericina B liposomal y se realizó el despistaje de infección fúngica, que fue negativo.
Ante la sospecha de un síndrome de liberación de citoquinas (SLC), descrito previamente como un predictor de COVID grave5, se monitorizaron los niveles de proteína C reactiva (PCR), interleucina-6 (IL-6) y ferritina (fig. 1) y se administró una única dosis de tocilizumab, un anticuerpo monoclonal humanizado dirigido contra el receptor de la IL-6 humana.
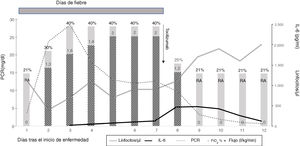
Evolución desde el inicio de la enfermedad. Las líneas representan el recuento linfocitario (linfocitos/μl) y los parámetros analíticos relacionados con el síndrome de liberación de citoquinas: proteína C reactiva (PCR) (mg/dl) e interleucina-6 (IL-6) (pg/ml); las barras representan la oxigenoterapia (l/kg/min) y la FiO2 (%). Tras el tratamiento con tocilizumab, la fiebre desapareció, y a las 24h se retiró la oxigenoterapia. AA: aire ambiente (FiO2 al 21%).
Tras administrarse la dosis de tocilizumab, la fiebre desapareció de inmediato con resolución de todos los síntomas respiratorios, pudiéndose retirar la oxigenoterapia 24h después. Los niveles de PCR disminuyeron y comenzó la recuperación hematológica. Los niveles de IL-6 aumentaron en los primeros días, alcanzando un máximo de 478pg/ml al noveno día del ingreso (segundo día tras la dosis de tocilizumab), para luego disminuir al tercer día de la administración de tocilizumab, como se había descrito en modelos de artritis reumatoide. Los niveles de ferritina continuaron aumentando tras la dosis de tocilizumab, con un pico de 1,600ng/ml a los 11 días del ingreso (5 días tras la dosis de tocilizumab). Otros biomarcadores relacionados con el SLC, como los triglicéridos, la lactato deshidrogenasa o el fibrinógeno fueron normales, como lo fue la procalcitonina. No se observaron efectos secundarios relacionados con el tocilizumab.
La antibioterapia se completó en una semana. El niño recibió el alta a los 14 días del ingreso tras la recuperación hematológica, momento en el que estaba libre de síntomas de COVID-19 y el examen físico fue normal.
A los 14 días de la resolución de los síntomas, una nueva prueba para la detección de SARS-CoV-2 mediante RT-PCR en muestra de aspirado nasofaríngeo resultó negativa, y se reanudó la quimioterapia.
El caso presentado ilustra el curso clínico de la COVID-19 grave en un paciente oncológico pediátrico, incluyendo el desarrollo de SLC tras el inicio de síntomas causados directamente por la infección por SARS-CoV-2. Aunque la bacteriemia por Streptococcus mitis asociada y las transfusiones de plaquetas podrían haber influenciado el desarrollo de síndrome de distrés respiratorio agudo, se sospechó del SLC porque la fiebre y los síntomas respiratorios del paciente no mejoraron a pesar de recibir medidas de soporte y antibioterapia adecuadas. A ello hay que sumar que la resolución total de la fiebre y los síntomas respiratorios tras la administración de una única dosis de tocilizumab se ajustaron al patrón descrito en casos graves de COVID-19 en adultos6.
Para concluir, aunque la mayoría de los pacientes pediátricos con COVID-19 muestran síntomas leves, los niños con cáncer pueden desarrollar COVID-19 grave, en cuyo caso se debería evaluar la posibilidad del SLC y contemplar el uso de tocilizumab tras excluir infección bacteriana o fúngica. Es aconsejable repetir las pruebas de SARS-COV-2 en casos con fuerte sospecha y resultados iniciales negativos, sobre todo en pacientes inmunocomprometidos con infección grave.
Nuestro agradecimiento a Magda Campins y al equipo del servicio de medicina preventiva y epidemiología por su consejo en el manejo de la enfermedad y su participación en un valioso intercambio de opiniones.