Los monitores de apneas detectan anomalías en la frecuencia cardíaca y respiratoria, sin utilidad demostrada para el diagnóstico de alteraciones respiratorias relacionadas con el sueño en los niños como se pensaba en su origen.
ObjetivoDescribir el tipo de pacientes que se monitorizan, durante cuánto tiempo y la evolución de los mismos.
Materiales y métodosEstudio descriptivo retrospectivo de los pacientes con monitorización cardiorrespiratoria domiciliaria controlados, desde octubre del 2008 hasta septiembre del 2012, en consultas externas de un hospital materno-infantil de tercer nivel.
ResultadosDurante el periodo de estudio fueron incluidos 88 pacientes, el 58% de ellos de sexo masculino, con una mediana de edad de 15,5 días y durante un periodo de 4,7 meses. El motivo de monitorización fue en un 20,5% por antecedente de muerte súbita, sin encontrar patología subyacente; un 25% por apnea de la prematuridad; un 20,5% por episodio aparentemente letal, y un 14.8% por atragantamiento. Otras causas suponen el 19,3% (apnea/hipopnea, desaturaciones y respiración periódica). De estos 3 últimos grupos, en el 50% se registraron eventos patológicos: reflujo patológico (9), apneas de la prematuridad (2), causa neurológica (3) y apneas de causa desconocida (10).
ConclusionesLa sospecha de apnea del lactante es un motivo de consulta que crea gran preocupación tanto a la familia como al pediatra. La monitorización domiciliaria es útil en la detección de alteraciones en la frecuencia cardíaca y respiratoria pero es necesario limitar sus indicaciones y realizar un buen seguimiento de estos pacientes, evitando el abuso de otras pruebas complementarias o tratamientos.
Home apnea monitors detect abnormalities in cardiac and respiratory frequency, but their use in the diagnosis of respiratory -related sleep disturbances in children has not been demonstrated, as was originally thought.
ObjectiveTo describe the type of patients being monitored, for how long and their outcome.
Material and methodsA retrospective descriptive study was conducted on patients with controlled home cardiorespiratory monitoring from October 2008 to September 2012 in the Outpatient department of a Maternity tertiary hospital.
ResultsDuring the study period 88 patients were included, 58% of them were male, with a median age of 15.5 days, and followed up for a period of 4.7 months. The reason for monitoring was due to a history of sudden death without finding underlying pathology in 20.5%, 25% due to apnea of prematurity, 20.5% due to apparent life-threatening event, and 14.8% due to choking. Other causes accounted for 19.3% (apnea/hypopnea, desaturation and periodic breathing). Of these last three groups, pathological events were observed in 50% of them: reflux disease (9), apnea of prematurity (2), neurological causes (3), and apnea of unknown cause (10).
ConclusionsSuspected infant apnea is a cause for consultation that creates a great deal of concern to the family and the pediatrician. Home monitoring is useful in detecting changes in cardiac and respiratory frequency, but is necessary to limit its indications and ensure proper monitoring of these patients, avoiding the abuse of other tests or treatments.
Los monitores de apneas son aparatos diseñados para detectar alteraciones en la frecuencia cardíaca y la respiratoria en relación con apneas y no para el diagnóstico de alteraciones respiratorias relacionadas con el sueño en los niños1.
El uso de monitores de apneas domiciliarios se inició hace más de 30 años durante la época en que la apnea prolongada se proponía como causa hipotética del síndrome de muerte súbita del lactante (SMSL). Fueron diseñados para intentar proteger a los lactantes de la muerte identificando episodios de apnea central o bradicardia, avisando a los padres para que intervinieran antes de que el evento fuera fatal.
Posteriormente, diversos estudios han concluido que la apnea no está relacionada con el SMSL y que los monitores no evitarían una muerte súbita2.
El miedo a la muerte súbita de los lactantes lleva a los padres y facultativos, para proteger a los niños en situación de riesgo, a monitorizarlos, con el desafortunado resultado de una falsa sensación de seguridad que ofrece un dispositivo diseñado para detectar un tipo limitado de acontecimientos.
En nuestro centro, el control de monitorización de apnea se lleva haciendo desde 1997, inicialmente en contexto de evitar la muerte súbita, pero evolucionando posteriormente a otras indicaciones.
El objetivo de este trabajo es hacer una descripción de qué tipo de pacientes se monitorizan, durante cuánto tiempo y la evolución de los mismos.
Material y métodosSe trata de un estudio descriptivo retrospectivo de los pacientes con monitorización cardiorrespiratoria domiciliaria controlados, desde octubre del 2008 hasta septiembre del 2012, en consultas externas de un hospital materno-infantil de tercer nivel.
La selección de los pacientes se realizó mediante la revisión retrospectiva de la historia clínica informatizada y/o en papel de todos los pacientes con motivo de consulta o diagnóstico final relacionado de apneas. De estos, se seleccionaron los pacientes que habían sido seguidos en consultas externas con monitorización de apneas y se recogieron variables epidemiológicas, clínicas y de manejo.
Definiciones3:
Apnea: episodio inexplicado de cese de la respiración durante un tiempo mayor o igual de 20 s o un periodo más corto si se acompaña de bradicardia, cianosis, palidez o hipotonía marcada.
Respiración periódica: patrón respiratorio con pausas que duran entre 3 y 20 s entre las que se intercalan periodos de respiración normal.
Episodio aparentemente letal (EAL): aquel evento agudo que asusta al observador y que consiste en una combinación de apnea ≥ 20 s, cambio del color de la piel y del tono muscular, y que requiere estimulación enérgica o reanimación.
SMSL: muerte repentina que es inexplicada por la historia y en la que no se demuestra una causa de muerte en la evaluación post mortem.
Los pacientes seguidos por apnea de la prematuridad fueron aquellos remitidos desde la unidad de Neonatología y los incluídos como EAL fueron aquellos casos en los que durante su periodo de observación en la planta de hospitalización se registraron eventos patológicos en la monitorización.
Los datos extraídos se almacenaron y procesaron en una base de datos relacional Microsoft Access (Microsoft Corporation, Redmond, EE. UU.).
El análisis estadístico se realizó con el programa SPSS 20.0 (SPSS Inc., Chicago, EE. UU.). Las variables fueron en su mayoría dicotómicas y nominales y se expresaron en forma de porcentajes, números absolutos, medias con desviaciones estándar (DE) y medianas con percentiles (p25-75).
Las comparaciones entre grupos para variables cualitativas se realizaron con tablas de contingencia, comparando por medio de la prueba de la chi cuadrado. Las comparaciones entre grupos para variables cuantitativas se realizaron empleando el test paramétrico t de Student para muestras independientes.
ResultadosEn el periodo de estudio, el tiempo de seguimiento fue de 47 meses, desde octubre del 2008 hasta septiembre del 2012. En total, se recogieron 88 pacientes, el 57,9% de sexo masculino, con una mediana edad al inicio de la monitorización de 15,5 días (p25-p75 de 2 a 54.2 días) y monitorizados durante una mediana de 4,7 meses (p25-75 de 2,4 a 8,1 meses).
El motivo de monitorización fue en un 20,5% de los casos por antecedente de muerte súbita, un 20,5% por episodio aparentemente letal, un 25,0% por apnea de la prematuridad y 14,8% por atragantamiento. Otras causas suponen el 19,2% (apnea/hipopnea, desaturaciones y respiración periódica).
Se describen los resultados divididos para cada uno de los 3 grupos de seguimiento: apnea de la prematuridad, antecedente de muerte súbita y EAL, incluyendo en este último también atragantamiento y otras causas.
De los 22 pacientes en seguimiento por apnea de la prematuridad derivados de Neonatología (25,0%), el tiempo medio ± DE de monitorización fue de 5,6 ± 3,1 meses. Del total de estos pacientes, un 86,4% (19 pacientes) estuvo a tratamiento con cafeína una media de 2,6 ± 1,2 meses por registros compatibles con apneas de la prematuridad y/o respiración inmadura. De estos pacientes, el 68,2% tenía una edad gestacional entre 32,0-36+6, un 18,2% entre 28,0 y 31+6 semanas de gestación (SG) y otro 13,6% eran menores de 28 SG.
Dieciocho pacientes (50,0% sexo masculino) fueron seguidos por antecedente de muerte súbita, durante una mediana de 8,1 meses (p25-75, 3.5-11). En estos pacientes se realizaron diferentes estudios complementarios: la evaluación cardiológica se practicó en 15 niños (83,3%), neuroimagen en 8 (44,4%) y cribado metabólico en 4 (22,2%). En ninguno de ellos se detectó patología, aunque en uno de los pacientes se detectaron apneas con bradicardia con resolución espontánea. Uno de los pacientes falleció por una broncoaspiración accidental 4 meses después de suspender la monitorización.
Del tercer grupo de pacientes (48) que incluye EAL, atragantamiento y otras causas, al 85,4% se le realizó evaluación cardiológica, de los cuales 5 fueron patológicos (3 foramen oval permeable, una agenesia de vena cava inferior y una comunicación interventricular). A 5 pacientes se les realizó Holter ECG, siendo todos normales. Al 37,5% se le practicó tránsito gastrointestinal, estando alterado en 6 de ellos (33,3%). La videofluoroscopia se indicó en 6 con alteración en 2 casos. A 37 pacientes (77,1%) se les realizó neuroimagen, que resultó alterada en 4 (quiste aracnoideo, 2 con signos de hipoxia por EHI severa, retraso de mielinización). El EEG se realizó en 16 niños (33,3%), siendo patológico en 2 casos. En 16 se disponía de polisomnografía, con resultado alterado en 4 de ellos. En el 62,5% se practicó el cribado metabólico, siendo normal en todos los casos. En el 50,0% (24) de los pacientes de este grupo no se registraron nuevos eventos durante la monitorización. El diagnóstico final de los que sí presentaron eventos patológicos fue de reflujo patológico en 9 pacientes, apneas de la prematuridad en 2, en 3 la causa fue de origen neurológico y en 10 pacientes se detectaron apneas sin hallarse la causa de estas que se autolimitaron. Aunque solo 2 pacientes fueron diagnosticados de apneas de la prematuridad, 8 casos recibieron cafeína por sospecha de respiración inmadura y a pesar de detectar reflujo patológico en 9, recibieron tratamiento 12 pacientes.
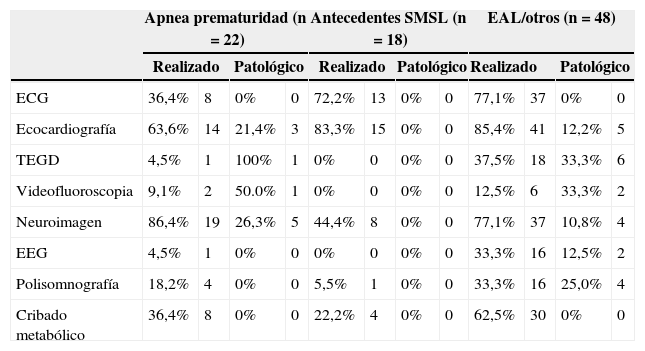
En la tabla 1 se resumen todas las exploraciones complementarias realizadas en cada uno de los grupos y sus resultados.
Pruebas realizadas en nuestro estudio según el motivo de seguimiento
| Apnea prematuridad (n=22) | Antecedentes SMSL (n=18) | EAL/otros (n=48) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Realizado | Patológico | Realizado | Patológico | Realizado | Patológico | |||||||
| ECG | 36,4% | 8 | 0% | 0 | 72,2% | 13 | 0% | 0 | 77,1% | 37 | 0% | 0 |
| Ecocardiografía | 63,6% | 14 | 21,4% | 3 | 83,3% | 15 | 0% | 0 | 85,4% | 41 | 12,2% | 5 |
| TEGD | 4,5% | 1 | 100% | 1 | 0% | 0 | 0% | 0 | 37,5% | 18 | 33,3% | 6 |
| Videofluoroscopia | 9,1% | 2 | 50.0% | 1 | 0% | 0 | 0% | 0 | 12,5% | 6 | 33,3% | 2 |
| Neuroimagen | 86,4% | 19 | 26,3% | 5 | 44,4% | 8 | 0% | 0 | 77,1% | 37 | 10,8% | 4 |
| EEG | 4,5% | 1 | 0% | 0 | 0% | 0 | 0% | 0 | 33,3% | 16 | 12,5% | 2 |
| Polisomnografía | 18,2% | 4 | 0% | 0 | 5,5% | 1 | 0% | 0 | 33,3% | 16 | 25,0% | 4 |
| Cribado metabólico | 36,4% | 8 | 0% | 0 | 22,2% | 4 | 0% | 0 | 62,5% | 30 | 0% | 0 |
Las comparaciones entre grupos no dieron resultados estadísticamente significativos.
DiscusiónEl neumocardiograma es útil en la detección de eventos patológicos relacionados con cambios en la frecuencia cardiaca y respiratoria. No obstante, tras décadas de monitorización domiciliaria, las controversias sobre su eficacia hacen que las recomendaciones de su uso sean restringidas. Deben utilizarse con cautela cuando se quiere descartar otras patologías o utilizar como sistema de seguridad de otros eventos durante el sueño4.
Hace más de 25 años se inició la utilización de monitores de apneas domiciliarios en una época en que la apnea prolongada se proponía como causa hipotética del SMSL. La idea inicial de estos monitores era un sistema diseñado de detección de bradicardias o pausas respiratorias mantenidas que avisara a los padres y evitar de esta forma un suceso fatal en aquellos niños con factores de riesgo. Posteriormente, múltiples estudios han concluido que apnea prolongada no está relacionada con el SMSL y que los monitores no evitarían una muerte súbita5,6. Los factores que sí que han demostrado asociarse a un mayor riesgo de muerte súbita están consensuados por profesionales de diferentes partes del mundo y que pueden ser prevenidos son dormir boca abajo y el tabaco materno pre y posnatal4,7.
Epidemiológicamente, no ha habido cambio en la incidencia de SMSL en relación con el uso de los monitores durante las últimas décadas6, pero en la práctica sigue constituyendo un reto para el médico en muchas ocasiones saber cuándo indicarlo, durante cuánto tiempo y el seguimiento de estos pacientes. En el estudio de Hunt et al.8 se especula que cambios cardiorrespiratorios sutiles detectados por los monitores podrían preceder en horas a eventos patológicos (apnea o bradicardia extrema). Sin embargo, la AAP y la AEP4 recomiendan que la monitorización domiciliaria no se utilice como método para prevenir el SMSL, pero se acepta su posible utilidad para la rápida detección de apnea central en algunas situaciones y patologías específicas.
Los motivos de monitorización cardiorrespiratoria en nuestro centro, y similares a los de muchos centros y contemplados según algunas guías clínicas3, son fundamentalmente el antecedente de hermano fallecido de muerte súbita, apneas de la prematuridad y antecedente de episodio aparentemente letal. Otras patologías respiratorias dependientes de tecnología para una buena ventilación, no se registran en nuestro estudio. De esta forma, en esta serie se evalúan las pruebas diagnósticas que se realizan en cada uno de ellos, incluyendo evaluación cardiológica, TGE, videofluoroscopia, EEG, neuroimagen y cribado metabólico.
En cuanto a los niños en seguimiento por apnea de la prematuridad en nuestra serie, el mayor número de pacientes monitorizados tienen una edad gestacional entre 32-36+6. En la revisión del 2001 de Zhaoy et al.9 se comenta que la incidencia es inversamente proporcional a la edad gestacional, afectando a casi todos los menores de 29 semanas. Quizás esta discrepancia se deba a que en los prematuros más extremos la apnea se resuelve antes de precisar seguimiento puesto que la apnea de la prematuridad es un problema madurativo y autolimitado, aunque hay que tener en cuenta la menor proporción total de prematuros extremos. En este mismo estudio, se considera que a partir de la semana 36-40 posgestacional suelen desaparecer la mayoría, en comparación con otras publicaciones en las que prolongan el periodo hasta la semana 43 posgestacional2. Sin embargo, el tiempo de monitorización en nuestro trabajo en pacientes con apnea de la prematuridad fue probablemente excesivo, de 5,6 meses.
Respecto a los niños en seguimiento por antecedente de hermano fallecido de muerte súbita del lactante, todas las pruebas diagnósticas realizadas fueron normales, realizándose sobre todo evaluación cardíaca (83,3%). El tiempo de seguimiento medio fue de 8,1 meses, posiblemente en relación con el grado de angustia de los padres, prolongándose más meses en algún caso. Varias revisiones apuntan que a partir de los 6 meses disminuye el riesgo de SMSL10 y en los casos graves hasta los 9 meses, estando indicada la retirada del monitor al menos 2 meses después de la edad del fallecimiento del hermano3. El hecho de detectar tan solo un registro patológico nos debe plantear revisar esta actitud.
Según la revisión de Hally et al.11, el 7% de los niños que mueren por SMSL presentaban historia de EAL. A pesar de que algunas madres de niños con SMSL refieren un EAL previo más frecuentemente que aquellas madres de niños control, esto constituye una pequeña proporción de los casos de SMSL. En nuestra revisión, ninguno de los niños en seguimiento presentó recurrencia y ninguno falleció.
Existe en la bibliografía información referente a los factores de riesgo en la anamnesis y exploración física que nos indiquen que un paciente tiene riesgo de presentar un EAL y que sería candidato de monitorización de apneas domiciliaria12. Los factores de riesgo identificados incluirían: antecedente de prematuridad, múltiples EAL y sospecha de maltrato. En cuanto al EAL entendido según la definición de 19873, el rendimiento de las pruebas diagnósticas realizadas es dudoso y, antes de indicar la monitorización de apneas, está indicado un estudio etiológico que descarte aquellas patologías que pueden ser la causa y tengan tratamiento3. No existe actualmente un protocolo de manejo claro de los lactantes con EAL y son necesarios nuevos estudios más potentes para su establecimiento. Según apuntan Weiss et al. en su estudio prospectivo del 201013, el rendimiento de las pruebas diagnósticas después de un EAL es globalmente bajo y solo cuando hay un elevado índice de sospecha, este aumenta. Los test de cribado para RGE, meningitis, bacteriemia o convulsiones tienen un bajo rendimiento en aquellos niños sin factores de riesgo en los antecedentes o hallazgos sugestivos en la exploración física12. En nuestra serie, el EEG se realizó en el 33,3% de los EAL y solo en 2 casos fueron patológicos. En el último estudio previamente comentado, refieren que esta prueba tiene un rendimiento del 4,5%, en comparación con otros trabajos que potencian la inclusión del EEG como prueba de primera línea de EAL al considerar que un total del 11% de estos tienen como diagnóstico final convulsiones14. En nuestra serie, se objetiva un registro alterado en el 4,2% del total de EAL, aunque algunos de estos pacientes presentan algunos otros síntomas y signos que hacían pensar en patología de base.
Otro ejemplo es la evaluación cardiológica. Existe bibliografía que resalta el papel del ECG como una herramienta potencialmente útil en el diagnóstico de EAL causados por alteraciones del ritmo15. En nuestro estudio, se realizó en el 85,4% de los pacientes que presentaron EAL, siendo patológica en el 12,2% de las realizadas. Sin embargo, los hallazgos en el ecocardiograma no justificaban la clínica de EAL.
En referencia a la neuroimagen como prueba de primera elección, el estudio de Weiss et al.13 previamente comentado, considera que esta debe reservarse para aquellos casos en los que existe una alta sospecha clínica de patología neurológica. En nuestra serie, se realizó al 77,1%, siendo patológica en 4 casos en los que existía algún otro signo acompañante por lo que su empleo como prueba de cribado podría valorarse individualmente.
Por otro lado, el cribado metabólico está incluido en el estudio básico de EAL en muchos trabajos14. En nuestra serie, se realizó al 62,5% de los EAL y en el 22,2% de los pacientes en seguimiento por antecedente de muerte súbita, siendo negativo en todos los casos. Aunque exista bibliografía que defiende su realización por tratarse de una prueba inocua y barata10,14,16, su realización sistemática es cuestionable sobre la base de los resultados de nuestro estudio.
De todas las pruebas complementarias realizadas en nuestro estudio, se puede extraer que la mayoría resulta ser negativas y las que se informan como alteradas suelen ser insuficientes para justificar la causa de la apnea. De esta manera, el mejor abordaje sería probablemente la realización de determinados exámenes complementarios solo en función del contexto clínico, en lugar de establecer un listado de pruebas a efectuar en todos ellos.
Las limitaciones de nuestro estudio son que se trata de un estudio retrospectivo, con los inconvenientes que ello conlleva, y que la muestra corresponde a niños con monitorización domiciliaria, perdiéndose aquellos casos de niños que presentaron un EAL que fue estudiado y no precisó monitorización.
En conclusión, la sospecha de apnea del lactante es un motivo de consulta que crea gran preocupación tanto a la familia como al pediatra y la indicación de monitor de apneas es una cuestión controvertida. Sabemos que es útil en la detección de alteraciones en la frecuencia cardíaca y respiratoria pero es necesario limitar sus indicaciones y realizar un correcto seguimiento de estos pacientes ya que en muchas ocasiones se tiende a la sobreutilización. Debe revisarse fundamentalmente la indicación en los pacientes con antecedentes de un hermano fallecido por muerte súbita, examinar los factores de riesgo establecidos para EAL y limitar el tiempo de utilización en aquellos con apnea de la prematuridad. También es importante evitar el abuso de otras pruebas complementarias o tratamientos innecesarios y realizar estudios de mayor relevancia en lo que se refiere a indicaciones de las exploraciones, la duración de los tratamientos y monitorización, y el seguimiento de pacientes con factores de riesgo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.