La neutropenia cíclica es una enfermedad congénita hereditaria poco frecuente. Hasta el año 2002, había únicamente 194 casos registrados1. Una mutación del gen de la proteína elastasa del neutrófilo (ELA2)2 localizado en el cromosoma 19, produce un defecto en la granulopoyesis. Esto ocasiona neutropenia en sangre periférica cada 3 a 4 semanas3. Estos episodios se acompañan de fiebre, estomatitis aftosa, gingivitis, faringitis o adenopatías cervicales. En un 10% de los casos se producen infecciones graves, como neumonía, sepsis o peritonitis4. La neutropenia cíclica evoluciona habitualmente hacia neutropenia crónica2.
Se recomienda el tratamiento con G-CSF (granulocyte-colony stimulating factor ‘factor estimulante de colonias de granulocitos’) recombinante5,6. Con este tratamiento se disminuye la duración de la neutropenia y se reduce el riesgo de infecciones bacterianas graves.
A continuación se expone el caso de un niño de 5 años que, desde el primer año de vida, presentaba episodios mensuales consistentes en fiebre elevada, aftas bucales y afectación del estado general. Estos episodios evolucionaban a su curación de forma lenta (4 o 5 días) tras tratamiento empírico con antibiótico de amplio espectro.
Como antecedentes personales destacaban faringoamigdalitis, otitis media aguda de repetición, salmonelosis y varicela a los 2 años con gran repercusión cutánea, así como gastroenteritis agudas esporádicas, bruxismo sin parasitosis e hiperhidrosis desde los 3 años. El niño fue amigdalectomizado a los 2 años y reintervenido un año más tarde por persistencia de tejido amigdalar. No tenía antecedentes familiares de interés.
Se observaban múltiples aftas en la mucosa oral y labial junto con adenopatías subangulomandibulares, el resto de la exploración física fue normal.
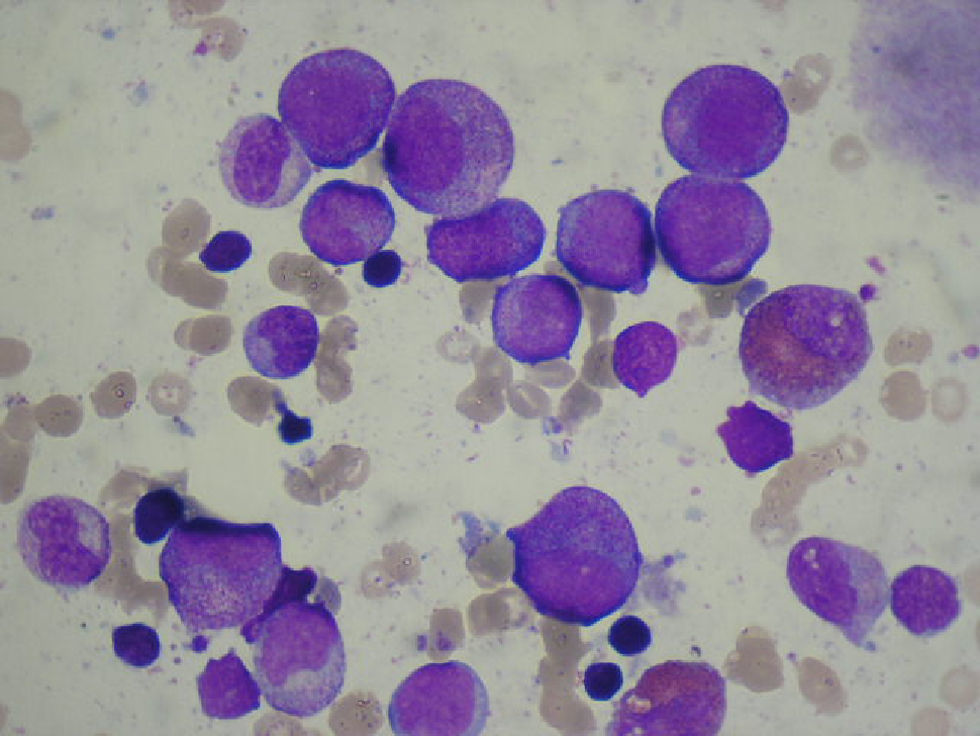
Las pruebas complementarias incluyeron bioquímica con glucosa, urea, creatinina, sodio, potasio y cloro, y coagulación; los resultados fueron normales. La proteína C reactiva fue de 16mg/l. Se realizó un estudio inmunológico completo, en el que se analizaron parámetros de inmunidad humoral (inmunoglobulinas [Ig] G, A, M, y subclases de IgG), la producción de anticuerpos (polisacáridos, proteínas), el complemento (vías clásica y alternativa), la inmunidad celular (producción de citocinas y respuesta proliferativa) y función de los neutrófilos (mieloperoxidasa intraneutrófilos, quimiotaxis, generación de anión superóxido y capacidad de fagocitosis de Escherichia Coli). Todos los resultados fueron normales. En el hemograma se observó una cifra de leucocitos de 5,1 × 109/l (0,29 × 109/l de neutrófilos, 3,7 × 109/l de linfocitos y 0,9 × 109/l de monocitos), así como series roja y plaquetaria normales. En hemogramas anteriores se habían encontrado cifras de neutrófilos de hasta 0,07 × 109/l. Se realizó aspirado de médula ósea y se observó detención madurativa de los metamielocitos, con normalidad en el resto de las series hematopoyéticas (fig. 1). Se realizaron un estudio inmunofenotípico y un estudio citogenético, que fueron normales.
Se observan distintas células de la serie granulocítica neutrófila. Las más grandes son los promielocitos; algo más pequeños y con el núcleo algo más excéntrico se obsevan los mielocitos; las siguientes células en la fase madurativa del neutrófilo son los metamielocitos que se aproximan a la forma de cayado, sin que se evidencie ninguna célula en esta última fase.
Se realizó el diagnóstico de neutropenia cíclica y se administró tratamiento con G-CSF (Filgastrim®) en dosis subcutáneas de 5mcg/kg/día, subcutánea durante 2 días, en los períodos de neutropenia. Posteriormente se administró G-FSC cuando aparecían los síntomas. Hubo una mejoría clínica muy llamativa, sobre todo durante el primer año, ya que disminuyó la sintomatología infecciosa y se acortaron mucho los períodos sintomáticos. A partir del año de seguimiento ha empezado a ser menos efectiva.
La neutropenia cíclica es un síndrome neutropénico bien conocido aunque se trate de una enfermedad poco frecuente. Hasta el año 2002 había únicamente 194 casos registrados1. Puede presentarse de manera esporádica, pero hasta en un tercio de los casos se trata de formas familiares que muestran un patrón de herencia autonómico dominante7. Una mutación del gen de la elastasa del neutrófilo es la causante de la alteración de la granulopoyesis, que produce una interrupción periódica de la producción celular en la médula ósea8–10. Esta mutación puede seguir el mencionado patrón autonómico dominante o presentarse de novo, como ocurre en esta mujer, en la que no se hallaron otros casos de la enfermedad en la familia.
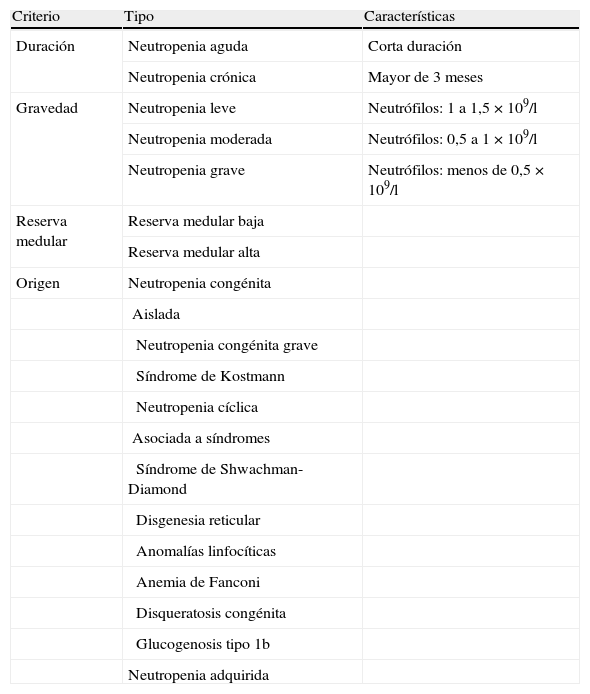
Hay diversas causas (congénitas o adquiridas) de neutropenia y distintas formas de clasificación de éstas (tabla 1). Las neutropenias congénitas graves pueden aparecer aisladas o formar parte de diversos síndromes11,12. La neutropenia cíclica se enmarca entre las neutropenias congénitas.
Clasificación de las neutropenias
| Criterio | Tipo | Características |
| Duración | Neutropenia aguda | Corta duración |
| Neutropenia crónica | Mayor de 3 meses | |
| Gravedad | Neutropenia leve | Neutrófilos: 1 a 1,5 × 109/l |
| Neutropenia moderada | Neutrófilos: 0,5 a 1 × 109/l | |
| Neutropenia grave | Neutrófilos: menos de 0,5 × 109/l | |
| Reserva medular | Reserva medular baja | |
| Reserva medular alta | ||
| Origen | Neutropenia congénita | |
| Aislada | ||
| Neutropenia congénita grave | ||
| Síndrome de Kostmann | ||
| Neutropenia cíclica | ||
| Asociada a síndromes | ||
| Síndrome de Shwachman-Diamond | ||
| Disgenesia reticular | ||
| Anomalías linfocíticas | ||
| Anemia de Fanconi | ||
| Disqueratosis congénita | ||
| Glucogenosis tipo 1b | ||
| Neutropenia adquirida |
Se considera neutropenia cuando hay un número absoluto de neutrófilos menor de 1,5 × 109/l. Se define neutropenia crónica grave cuando hay un número absoluto de neutrófilos menor de 0,5 × 109/l que persiste meses o años.
El diagnóstico de neutropenia cíclica se realiza al observar cifras de neutrófilos menores de 0,2 × 109/l de forma cíclica cada 3 semanas, con una duración de 3 a 6 días11,12. Además puede asociarse a monocitosis. En ocasiones, pueden producirse variaciones cíclicas en el resto de las células de la sangre periférica, que pueden coincidir o no con la neutropenia.
El cuadro clínico habitual se presenta con episodios recurrentes (cada 3 o 4 semanas) consistentes en fiebre e infecciones orofaríngeas o cutáneas. También la neutropenia crónica benigna puede presentar un patrón cíclico, pero nunca con la misma regularidad que la neutropenia cíclica.
Al realizar un aspirado de médula ósea, la neutropenia muestra al inicio un aumento rápido de promielocitos y mielocitos, como le ocurrió a esta mujer. Posteriormente hay un aumento de las formas maduras. Tras 2 semanas, solamente se observan formas maduras, con una ausencia casi completa de sus precursores.
El tratamiento con G-CSF recombinante es esencial en los niños que presentan neutropenia cíclica5,6. Su aplicación durante períodos de neutropenia grave y ante la aparición de los síntomas, mejora sustancialmente la calidad de vida de los sujetos y reduce la duración de los episodios, la intensidad de los síntomas y el riesgo de complicaciones bacterianas13,14.