La fibrosis quística (FQ) es una enfermedad multisistémica, de carácter progresivo, que afecta la calidad de vida del paciente. Las manifestaciones clínicas respiratorias se relacionan principalmente con su morbimortalidad, siendo la fisioterapia respiratoria (FTR) un pilar importante para la mejora del aclaramiento mucociliar1. Los dispositivos de insuflación-exuflación mecánica (IEM) generan un flujo suficientemente alto como para proporcionar un cizallamiento en las vías aéreas que desprende y moviliza las secreciones hacia el exterior. La IEM ha demostrado su eficacia en la mejora del aclaramiento de las vías respiratorias en pacientes con enfermedades neuromusculares2, y aunque existen evidencias sobre su uso en bronquiectasias sin FQ3, su aplicación en niños con FQ precisa de estudios que así la avalen1.
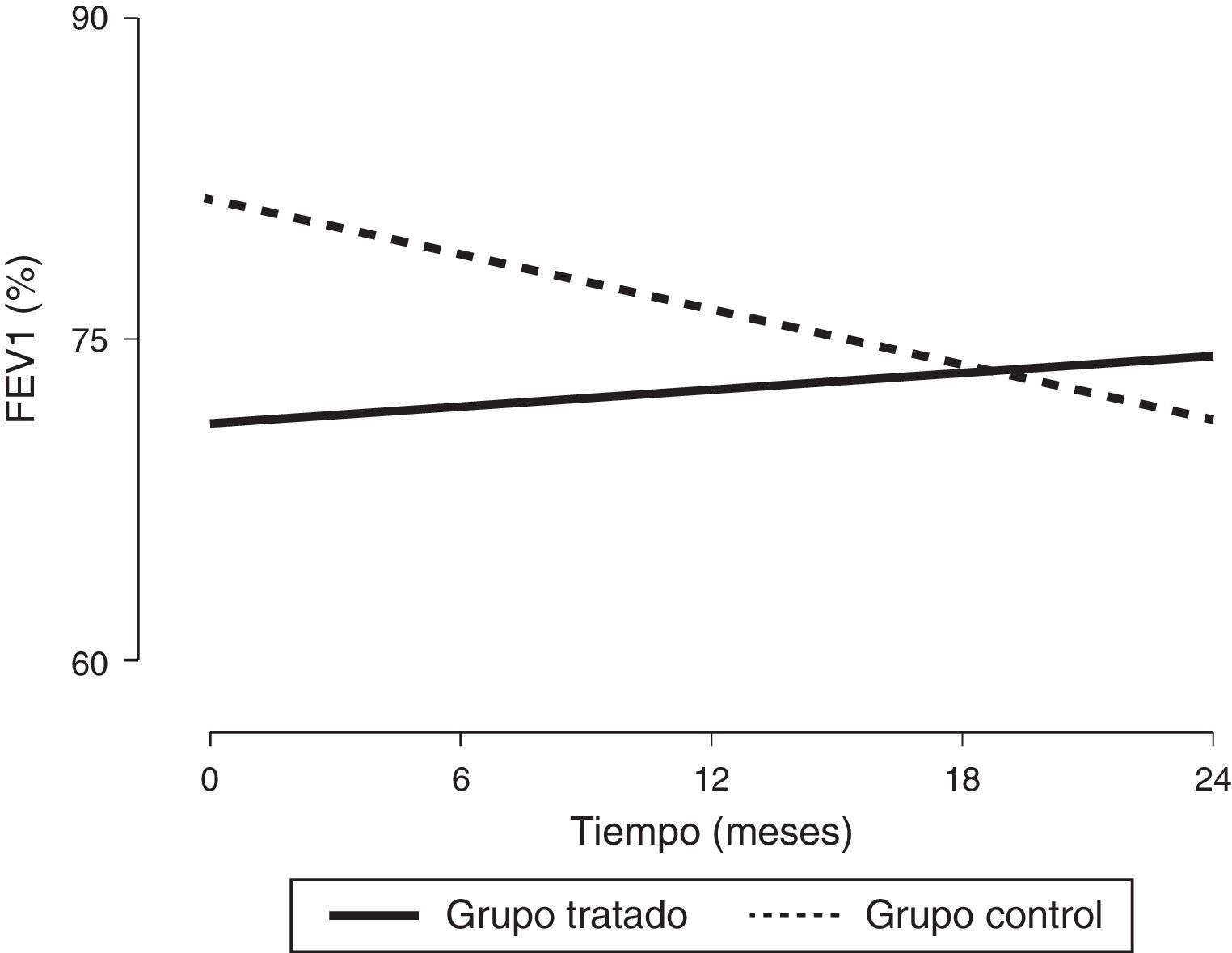
Con el objetivo de evaluar el efecto de IEM sobre la función pulmonar en niños diagnosticados de FQ, nos planteamos un estudio prospectivo de 24 meses que compara la combinación FTR, incluida en el abordaje terapéutico habitual, más IEM (grupo tratado, n=9) frente a la FTR (grupo control, n=11); cumpliendo en cada caso todos los criterios de inclusión y ninguno de exclusión (tabla 1). Los procedimientos utilizados se realizaron tras obtención del consentimiento informado de los padres. La intervención se efectuó cada 21 días, durante 45min. Se desarrollaron 3 ciclos de 6-8 respiraciones por decúbito (tiempo de insuflación 5s, tiempo de exhalación 5s, tiempo de pausa 2s; presiones utilizadas +30/−35 cmH2O; aparato CoughAssist®, Philips). Para mejorar la eliminación de la obstrucción bronquial se aplicaron presiones abdominales. Antes y después de cada sesión se monitorizó la pulsioximetría. Para la valoración de la función pulmonar se llevó a cabo espirometría basal forzada según normativa SEPAR a los 6, 12, 18 y 24 meses tras el inicio de la intervención, considerándose mejora el incremento de al menos un 5% en FVC (%) y FEV1 (%); y deterioro, una reducción ≥5% (tabla 1). De los 9 pacientes tratados, se excluyeron 2, por miedo al dispositivo y por no asistencia, respectivamente. Aun partiendo de una función pulmonar más deteriorada que el grupo control, tras la intervención, se observó una tendencia a la elevación de FEV1 (%) mantenida en el tiempo (fig. 1), siendo dicho incremento estadísticamente significativo para FVC (%); de hecho, la mejora de FEV1 (%), correlacionó de forma positiva y significativa con recibir FTR (r=0,47 y p<0,05) y con la mejora de FVC (%), (r=0,72 y p<0,05). En el grupo control, FEV1 (%) y FVC (%) disminuyeron de manera estadísticamente significativa. Las características clínicas de los pacientes se presentan en la tabla 1. Los resultados obtenidos con el estimador de Kaplan-Meier para comprobar las variaciones en el parámetro FEV1 (%) entre grupos están en concordancia con la mejoría que presentan los pacientes que reciben el tratamiento a estudio, ya que se estima una diferencia de 6 meses entre ambos grupos a favor del grupo tratado (p<0,05). Con respecto al estado nutricional, no se observan diferencias significativas en IMC entre ambos grupos, evolución presentada en la población pediátrica de FQ en los últimos años4.
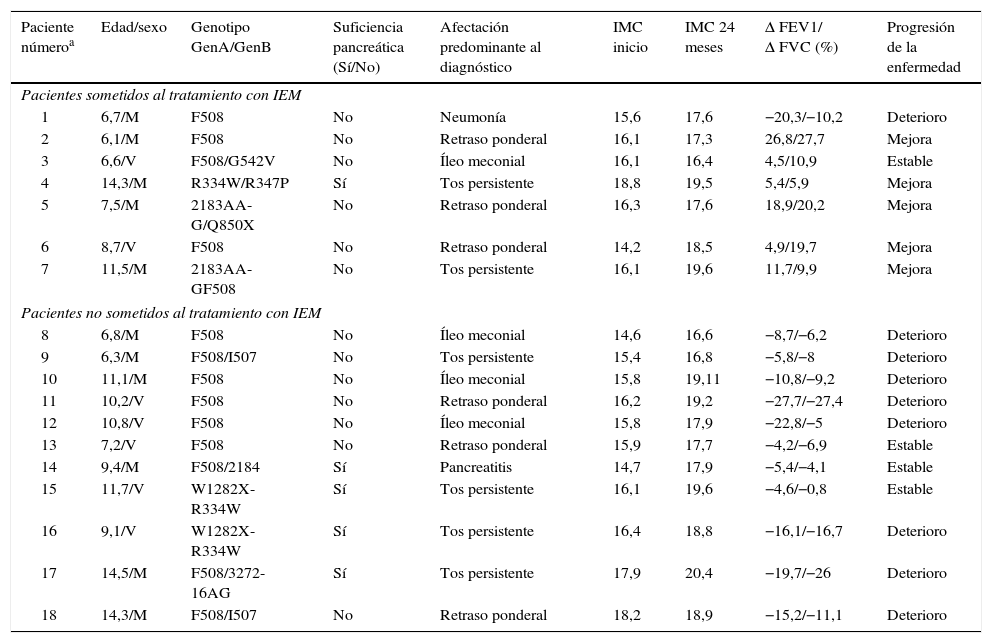
Características clínicas de los pacientes
| Paciente númeroa | Edad/sexo | Genotipo GenA/GenB | Suficiencia pancreática (Sí/No) | Afectación predominante al diagnóstico | IMC inicio | IMC 24 meses | Δ FEV1/ Δ FVC (%) | Progresión de la enfermedad |
|---|---|---|---|---|---|---|---|---|
| Pacientes sometidos al tratamiento con IEM | ||||||||
| 1 | 6,7/M | F508 | No | Neumonía | 15,6 | 17,6 | −20,3/−10,2 | Deterioro |
| 2 | 6,1/M | F508 | No | Retraso ponderal | 16,1 | 17,3 | 26,8/27,7 | Mejora |
| 3 | 6,6/V | F508/G542V | No | Íleo meconial | 16,1 | 16,4 | 4,5/10,9 | Estable |
| 4 | 14,3/M | R334W/R347P | Sí | Tos persistente | 18,8 | 19,5 | 5,4/5,9 | Mejora |
| 5 | 7,5/M | 2183AA-G/Q850X | No | Retraso ponderal | 16,3 | 17,6 | 18,9/20,2 | Mejora |
| 6 | 8,7/V | F508 | No | Retraso ponderal | 14,2 | 18,5 | 4,9/19,7 | Mejora |
| 7 | 11,5/M | 2183AA-GF508 | No | Tos persistente | 16,1 | 19,6 | 11,7/9,9 | Mejora |
| Pacientes no sometidos al tratamiento con IEM | ||||||||
| 8 | 6,8/M | F508 | No | Íleo meconial | 14,6 | 16,6 | −8,7/−6,2 | Deterioro |
| 9 | 6,3/M | F508/I507 | No | Tos persistente | 15,4 | 16,8 | −5,8/−8 | Deterioro |
| 10 | 11,1/M | F508 | No | Íleo meconial | 15,8 | 19,11 | −10,8/−9,2 | Deterioro |
| 11 | 10,2/V | F508 | No | Retraso ponderal | 16,2 | 19,2 | −27,7/−27,4 | Deterioro |
| 12 | 10,8/V | F508 | No | Íleo meconial | 15,8 | 17,9 | −22,8/−5 | Deterioro |
| 13 | 7,2/V | F508 | No | Retraso ponderal | 15,9 | 17,7 | −4,2/−6,9 | Estable |
| 14 | 9,4/M | F508/2184 | Sí | Pancreatitis | 14,7 | 17,9 | −5,4/−4,1 | Estable |
| 15 | 11,7/V | W1282X-R334W | Sí | Tos persistente | 16,1 | 19,6 | −4,6/−0,8 | Estable |
| 16 | 9,1/V | W1282X-R334W | Sí | Tos persistente | 16,4 | 18,8 | −16,1/−16,7 | Deterioro |
| 17 | 14,5/M | F508/3272-16AG | Sí | Tos persistente | 17,9 | 20,4 | −19,7/−26 | Deterioro |
| 18 | 14,3/M | F508/I507 | No | Retraso ponderal | 18,2 | 18,9 | −15,2/−11,1 | Deterioro |
FEV1 (%): volumen espiratorio forzado en el primer segundo expresado en porcentaje; FVC (%): capacidad vital forzada expresado en porcentaje; IEM: insuflación-exuflación mecánica; IMC: índice de masa corporal (kg/m2); M: mujer; V: varón; Δ: incremento en los parámetros de función pulmonar.
Los valores de FEV1 (%) y FVC (%) se expresaron como porcentaje del valor teórico para sujetos de la misma edad, peso y altura, según la población española de referencia.
Los pacientes incluidos en la tabla cumplieron los siguientes criterios de inclusión y ninguno de los de exclusión. Criterios de inclusión: diagnóstico de FQ según los criterios diagnósticos internacionalmente aceptados; seguir controles periódicos en las consultas de la unidad de FQ; edad comprendida entre 6-14 años; capacidad para realización de prueba de función respiratoria; entender el objetivo del estudio y firmar el consentimiento informado. Criterios de exclusión: pacientes con riesgo radiológico o clínico para sufrir neumotórax o neumomediastino; pacientes con barotrauma en el mes previo al ingreso en el estudio; antecedentes de hemoptisis masiva o amenazante; pacientes trasplantados o en lista de espera para trasplante.
Evolución de la función pulmonar (expresada como FEV1%) desde el inicio del estudio, hasta el final de la intervención.
FEV1 (%): volumen espiratorio forzado en el primer segundo expresado en porcentaje. Los valores se expresaron como porcentaje del valor teórico para sujetos de la misma edad, peso y altura según la población española de referencia.
Las características clínicas de los pacientes son concordantes con las descritas4, aunque los parámetros espirométricos en el grupo tratado están por debajo de lo registrado en la literatura4,5, situación que posiblemente influyó en la decisión de participar en el estudio. Como indica la tabla 1, mientras que ningún paciente del grupo control mostró mejoría en su función pulmonar después de 24 meses, de los 7 pacientes tratados, 5 mejoraron su función pulmonar tras la intervención, uno la mantuvo estable y solo en un paciente empeoró. El FEV1 (%) en el grupo tratado tiende a mejorar durante la intervención (fig. 1), mientras que en el grupo control se observa la evolución natural de la FQ, es decir, una disminución progresiva de la función pulmonar5. Según estos resultados, la FTR planteada podría enlentecer la evolución de la enfermedad. En este estudio, no observamos efectos secundarios relacionados con la utilización del dispositivo, siendo la técnica utilizada segura y bien tolerada. Solo se registró en alguna ocasión irritación de la faringe y dolor de cabeza debido a la tos, efectos no relacionados con los 2 abandonos producidos. Concluimos que, esta es la primera serie de casos pediátricos que describe el uso de la combinación de FTR convencional y la técnica instrumental de IEM en pacientes con FQ, demostrando una mejora en la función pulmonar de al menos 2 años de evolución. En consecuencia, podría ser una buena herramienta preventiva del deterioro de la función respiratoria en esta población, siendo necesario el desarrollo de estudios multicéntricos que permitan establecer conclusiones basadas en la evidencia.
A la Asociación contra la Fibrosis Quística de Málaga.