La terapia con células CAR-T supone un claro reto al sistema de salud y a la manera de abordar los problemas hemato-oncológicos. El artículo titulado «Inmunoterapia con células CAR-T en hemato-oncología pediátrica»1 del Grupo de Inmunoterapia y Terapias Avanzadas de la Sociedad Española de Hematología y Oncología Pediátricas realiza una interesante revisión de los aspectos más relevantes de la implantación de la terapia con linfocitos T que expresan un receptor antigénico quimérico (CAR-T) en el arsenal terapéutico de opciones frente a las enfermedades linfoproliferativas de estirpe B CD19+.
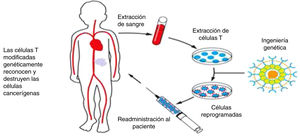
Las células CAR-T son linfocitos T modificados genéticamente para que expresen un receptor dirigido frente a un antígeno tumoral. De esta forma la célula CAR-T, sin mediación del complejo mayor de histocompatibilidad, puede atacar y destruir la célula tumoral (fig. 1). Las células CAR-T frente al antígeno CD19 (CART19), presente en las células de estirpe B, pueden eliminar las células tumorales en leucemias y linfomas B. Ha sido precisamente en pacientes pediátricos con leucemia linfoblástica de precursores B con enfermedad muy avanzada y sin apenas opciones curativas donde las CAR-T han demostrado mayor eficacia. Y es precisamente un ensayo clínico internacional, en el que participó un centro español, con pacientes pediátricos y adultos jóvenes con LLA el que llevó a la aprobación de tisagenlecleucel, uno de los constructos CAR-T comerciales2. También en nuestro país, se ha desarrollado un CART19 de producción académica3 y un ensayo clínico fase I con pacientes adultos y pediátricos cuyos resultados se publicarán próximamente.
Producción y administración de células CART. Se obtienen los linfocitos del paciente mediante leucoaféresis. Ex vivo se separan los linfocitos T, se expanden y se modifican genéticamente para que expresen un receptor de células T quimérico (Chimeric antigen receptor) que reconoce un antígeno tumoral (CD19 en el caso de las CART19) y se reinfunden después al paciente.
La aprobación por las autoridades regulatorias de tisagenlecleucel y axicabtagene ciloleucel (las 2 propuestas comerciales de CAR-T frente a CD19 para el tratamiento de la leucemia linfoblástica aguda de precursores B en niños y adultos jóvenes y del linfoma difuso de células grandes B del adulto), ha impulsado la puesta en marcha del «Plan Nacional de Terapias Avanzadas-Medicamentos CAR-T» en España. En este se resalta no solo la conveniencia de identificar los centros más adecuados para su administración, sino que se hace especial énfasis en la necesidad de que algunos de estos hospitales se transformen para que su actividad asistencial permita disponer de capacidad para la fabricación propia de este tipo de inmunoterapias personalizadas. Los hospitales especializados en hemato-oncología pediátrica tienen por tanto el importante reto de evolucionar hacia un modelo asistencial que integre esta inmunoterapia génica y celular, orientándose a disponer de capacidad propia para gestionar todos los aspectos relativos al uso, fabricación y administración de estos nuevos tratamientos. En este sentido, la experiencia en España de un CAR-T académico y ensayo clínico con pacientes adultos y pediátricos ha demostrado la viabilidad de este tipo de terapia en nuestro medio3.
Más allá de la descripción de qué son y cómo funcionan los CAR-T y su importancia para entender su comportamiento en los pacientes, el artículo incide en aspectos fundamentales para su uso terapéutico. Entre los elementos más peculiares se recoge el papel fundamental de la colaboración coordinada de diversas especialidades hospitalarias, concepto recogido bajo el término de la multidisciplinariedad de los equipos CAR-T. Si bien la lista puede parecer larga (hematólogos, inmunólogos, intensivistas, pediatras, neurólogos, oncólogos, biólogos, farmacólogos, farmacéuticos hospitalarios, expertos en regulación y sistemas de calidad, enfermería,…), después de más de un año de implantación de este plan de abordaje, se constata que todos estos actores son imprescindibles para una atención eficaz y eficiente de los pacientes.
El artículo también aborda la opción de fabricación y manejo directo («académico») de estas propuestas que tienen y deben tener un amplísimo campo para la mejora continua. La regulación actual de los fármacos busca estabilizar los sistemas de producción, pero los CART como la mayoría de las terapias celulares-génicas tienen la obligación de adaptarse rápidamente para ofrecer la propuesta terapéutica con más prestaciones. Es importante asumir mecanismos para la introducción de mejoras (que en las terapias avanzadas son casi ilimitadas) y solo la producción y ensayo en condiciones académicas puede permitir la optimización de la terapia celular. Por ello, resulta importante dotar a los centros de profesionales y medios, incluyendo una regulación más específica que no bloquee, sino que permitan esta «fabricación y desarrollo» de propuestas académicas que lleven a tener acceso a CAR nuevos. El ámbito académico permite con mayor agilidad perfeccionar e innovar CAR, implementar nuevas propuestas de producción, manejo, y definir acciones clínicas específicas que lleven a demostrar de manera más rápida y concluyente opciones de uso con la máxima eficacia para los enfermos. Además, puede dirigirse a la investigación de CAR destinados al tratamiento de enfermedades poco prevalentes, como lo son, entre otras, las oncológicas en la edad pediátrica, en las que la industria farmacéutica puede tener menor interés en su desarrollo.
Por último, más allá de las consideraciones económicas alrededor de la inmunoterapia CART que puede poner en compromiso a sistemas públicos universales de salud como el nuestro, la opción de desarrollo de los productos «junto al paciente» tiene otras importantes ventajas. Por un lado, facilita su gestión, ya que la fabricación de CART en el propio centro puede reducir los tiempos de producción, que es esencial en pacientes con enfermedad oncológica avanzada. También tiene menor impacto ecológico que el CART comercial, en relación a las emisiones de CO2 debidas al transporte de las células, dado que entre el centro de producción de los CART comerciales y el hospital puede haber distancias de miles de kilómetros. Por otro lado, la fabricación local también puede resultar importante ante crisis como la de COVID-19, que en la actualidad pone en jaque a muchos pacientes oncológicos4. Las dificultades de las comunicaciones a distancia tensionan fuertemente la atención por problemas diversos, entre los que se incluyen el desabastecimiento de productos cuando estos se fabrican lejos del paciente. Propuestas in house descentralizadas como las de CART académicos proporcionan una flexibilidad que, ante crisis como la actual, deben y pueden facilitar el acceso a estas terapias que se usan como última opción en una encrucijada vital a los pacientes, con una connotación claramente muy especial en pacientes pediátricos.
Las células CAR-T constituyen un gran avance y una revolución en el tratamiento de algunos cánceres hematológicos. La investigación frente a nuevas dianas y mecanismos para combatir barreras importantes en su uso en otro tipo de tumores sólidos y puede abrir una nueva forma de tratar el cáncer y posiblemente otras enfermedades, como las autoinmunes entre otras. La constitución de un grupo de inmunoterapia en la Sociedad Española de Hematología y Oncología Pediátrica resulta de gran importancia para que los avances en estas terapias lleguen de forma rápida a los pacientes pediátricos.
Han contribuido a través de las brcacs PI18/000775 y AC18/00072 (CE_ERA Net_Nanomed18) del Instituto de Salud Carlos III con Fondos FEDER y también por «Fundació bancària la Caixa» (3922-19 FCRB).