Estudio epidemiológico para evaluar el desarrollo antropométrico en niños diagnosticados de enuresis nocturna primaria monosintomática según las distintas opciones terapéuticas.
Pacientes y métodosSerie de casos longitudinal en el que se incluyeron 548 niños de 5 a 10 años de edad. Se evaluaron sus parámetros antropométricos en el momento del diagnóstico y tras uno y 2 años de tratamiento.
ResultadosLos sujetos con enuresis nocturna primaria monosintomática no presentan alteraciones antropométricas cuando se comparan sus datos con los valores estándar de talla, peso e IMC. En general, tras 2 años de tratamiento de la enuresis no se observan alteraciones en los mencionados parámetros (excepto una disminución en el peso en el caso de los niños). Solo se encontró una disminución en la talla y en el peso en aquellos niños sometidos a terapia conductual con o sin alarma, hallazgos que dadas las limitaciones del estudio no consideramos significativos. La odds ratio de curación tras uno y 2 años de tratamiento se multiplica por 1,41 (IC 95%: 0,85-2,34) y 1,52 (IC 95%: 0,86-2,70) cuando se compara la desmopresina (y observación) con todas las demás opciones.
ConclusionesEn el presente estudio, antes y después del tratamiento de la enuresis nocturna primaria monosintomática, los niños presentan una talla, peso e IMC similares a los de los niños sanos españoles de su misma edad y sexo. La desmopresina parece aumentar la probabilidad de curación tras uno y 2 años de tratamiento, pero estos datos deberían ser corroborados en futuros ensayos clínicos aleatorizados.
An epidemiological study was conducted to assess the anthropometric development in children diagnosed with primary monosymptomatic nocturnal enuresis, depending on the treatment option selected.
Patients and methodsA longitudinal series of cases including 548 children aged 5-10 years. Anthropometric parameters of children were assessed at diagnosis, and after one and two years of treatment.
ResultsChildren with primary monosymptomatic nocturnal enuresis showed no anthropometric changes when their data were compared to the standard deviation score of height, weight, and body mass index (BMI). Overall, no changes were seen in the above mentioned parameters after two years of treatment for enuresis (except for a weight standard deviation score (SDS) decrease in boys). We only found a decrease in the size and weight in those children undergoing behavioral therapy with or without an alarm, findings that, given the limitations of the study, were not considered significant. The odds ratio for cure after one and two years of treatment was 1.41 (95% CI: 0.85-2.34) and 1.52 (95% CI: 0.86-2.70) for desmopressin (and watchful waiting) as compared to all other options.
ConclusionsIn this study, children had SDS values of height, weight, and BMI similar to healthy children of the same age and sex before and after treatment for primary monosymptomatic nocturnal enuresis. Desmopressin appeared to increase the probability of cure after one and two years of treatment, however these data should be corroborated in future randomized clinical trials.
La enuresis es un trastorno mucho más frecuente de lo que, en general, pueden percibir los pediatras de atención primaria. Es una enfermedad que está infradiagnosticada, bien por la tolerancia de los padres, los propios médicos, bien porque en muchas ocasiones se oculta por vergüenza. Se trata de una condición que genera además problemas psicosociales en el niño que la padece, que se acentúan a medida que este es mayor y supone una carga familiar, de trabajo y económica1.
La prevalencia de la enuresis nocturna es de un 10-20% en niños de 5 años, de un 5-10% en niños de 7 años y de un 5-7% en los de 10 años, según los diferentes autores, persistiendo en un 1% de los casos en la edad adulta. La enuresis es aproximadamente 2 veces más frecuente en niños que en niñas2–6.
La etiopatogenia de este trastorno todavía no está del todo aclarada. La teoría fisiopatológica más aceptada propone que existiría un retraso en la maduración de las funciones de control del sistema nervioso central sobre la vejiga durante la noche, unido a deficiencias en el control endocrino nocturno (pulsatilidad de la vasopresina o ADH)7,8. Otras teorías sugieren como posibles causas la falta de desarrollo de una capacidad vesical adecuada, patrones de sueño anómalos, factores emocionales o conductuales y defectos en el entrenamiento vesical, todos ellos unidos en muchas ocasiones a una historia familiar de enuresis nocturna9–11. Este origen multifactorial ha sugerido que la población de niños enuréticos puede presentar una mayor incidencia de retrasos en el desarrollo antropométrico, que afectarían fundamentalmente al crecimiento pudiendo observarse repercusiones sobre la talla final de estos niños12. Teniendo en cuenta que los niños enuréticos pueden tener percentiles más bajos de peso y talla que los controles sanos, se ha observado que dichas alteraciones se pueden asociar a retrasos en la maduración ósea, sin embargo, los mecanismos responsables de dicho retraso todavía no han sido aclarados13,14.
Algunos autores atribuyeron estos posibles retrasos en el desarrollo antropométrico y en la maduración ósea observados en los niños con enuresis a retrasos en la maduración de ciertas funciones reguladoras del sistema nervioso central13.
Las patologías que presentan un componente psicosocial se asocian muchas veces al aislamiento del paciente, déficit de habilidades sociales, disminución de la autoestima, trastornos del comportamiento, etc., como es el caso de la enuresis nocturna. Estos factores, a su vez, pueden alterar patrones de sueño, ritmos circadianos y ejes endocrinos, como el somatotropo. Se ha observado que los pacientes con talla baja de componente psicosocial pueden presentar déficit idiopático de hormona de crecimiento (GH) o resistencia a la la misma, trastorno que puede ser aislado o afectar a otros ejes hipotálamo-hipofisarios15.
En el presente estudio epidemiológico y prospectivo hemos evaluado los parámetros atropométricos de los niños con enuresis nocturna primaria monosintomática (ENPM) y, por primera vez, su evolución durante dos años en función del tratamiento recibido.
Pacientes y métodosEntre febrero de 2006 y marzo de 2009 se reclutaron a 548 niños con diagnóstico de ENPM en 159 centros de atención primaria y hospitales de toda España. Cada participante en el estudio tuvo la oportunidad de incluir un máximo de 5 enuréticos escogidos al azar entre los pacientes atendidos. A los 2 años del estudio, se evaluaron 363 pacientes. Los criterios de inclusión incluían niños/as de edades comprendidas entre los 5 y los 10 años y que cumplieran los criterios de ENPM de la International Children's Continence Society (Sociedad Internacional de Continencia de los Niños [ICCS])16 modificados por Espino17, debiéndose disponer de datos antropométricos históricos (talla, peso, índice de masa corporal [IMC]) para evaluar la velocidad de crecimiento en el momento del diagnóstico. Los principales criterios de exclusión eran: antecedentes de parto pretérmino o postérmino, padecer patologías o síndromes que pudieran afectar al crecimiento, recibir tratamiento crónico con fármacos, padecer cuadros de malabsorción, hipercatabolismo o malnutrición crónicos u obesidad (IMC>27).
Tras obtener el consentimiento informado de los padres y en línea con el diseño epidemiológico del estudio, cada investigador prescribió el tratamiento para la ENPM que consideró más oportuno y quedó registrado como la «intención de tratar» en el cuaderno de recogida de datos. Con fines prácticos se agruparon los tratamientos en los siguientes: observación y medidas higiénico-dietéticas, terapia de conducta/psicoterapia asociada o no a alarma, desmopresina sola o con observación, desmopresina junto con terapia de conducta y otras opciones (anticolinérgicos, antidepresivos). Las tablas de referencia fueron las publicadas por la Fundación Orbegozo en el año 200218. Los datos de la media de peso, talla e IMC de estas tablas han sido utilizados como grupo control para el cálculo de las DE de los diferentes grupos de la muestra estudiada.
El estudio contó con la aprobación de un comité ético y se llevó a cabo cumpliendo las normas de buenas prácticas clínicas y la declaración de Helsinki.
Visitas de seguimientoEl día en que se diagnosticaba a los niños de ENPM el pediatra debía recoger datos sobre los antecedentes familiares de sus padres (aspectos antropométricos y enuréticos), se recogían datos de talla, peso, velocidad de crecimiento y se decidía el tratamiento para la patología. Además se recogían datos sobre la prevalencia de problemas familiares, escolares, de alimentación así como trastornos del sueño. Cada investigador debía realizar un seguimiento de los niños tras uno y 2 años de tratamiento.
Análisis estadísticoSe evaluaron los 548 pacientes que fueron incluidos en el estudio. El análisis epidemiológico estadístico se realizó sobre estos pacientes y los datos finales de crecimiento sobre los 363 pacientes controlados durante los 2 años del estudio; los grupos de tratamiento fueron los marcados por el investigador como «intención de tratar» en el momento del reclutamiento.
Las variables cuantitativas que se distribuían de acuerdo a una curva normal (test de Kolmogorov-Smirnov) se expresaron mediante su media y desviación estándar mientras que las que no se distribuían de esta manera se expresaron con su mediana y rango intercuartílico. Las variables cualitativas se representan mediante su distribución de frecuencias.
Las comparaciones entre grupos se realizaron mediante una prueba ANOVA en el caso de que se cumpliera el supuesto de homogeneidad de varianzas o mediante una prueba de Kruskal Wallis en el caso contrario. Para evaluar los distintos parámetros antropométricos a lo largo de los 2 años de seguimientos se realizó un test de medidas repetidas.
Las variables cualitativas se compararon con el test X2 o test de Fisher, calculándose las correspondientes medidas de asociación (odds ratio) y ajustándose modelos de regresión logística para controlar los factores de confusión.
Se rechazó la hipótesis nula de igualdad de grupos cuando la p era menor de 0,05. El análisis estadístico se realizó con el programa SPSS 14.0 (SPSS INC Chicago, IL)
ResultadosDatos epidemiológicosLos investigadores participantes tenían una media de 21,38 (18,74) casos de ENPM diagnosticados entre los pacientes asignados en su cupo. De estos, aproximadamente el 70% eran niños y el 30% niñas y un 66,46% (29,21) estaban en tratamiento.
Los médicos participantes admitieron en un 88,14% (32,47%) de los casos que la edad de los pacientes influye a la hora de tomar una decisión de prescribir un determinado tratamiento u otro.
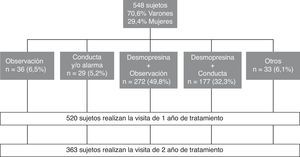
Resultados basalesEn la figura 1 se puede observar la evolución de los pacientes a lo largo de todo el estudio. Podemos destacar que los investigadores participantes en el estudio prefirieron como principales opciones de tratamiento la desmopresina junto con observación (49,8%) seguido de la desmopresina junto con la terapia conductual (32,3%), dato recogido como «intención de tratar». Veintiocho de los 548 niños que empezaron el estudio no fueron evaluados tras un año de tratamiento. De ellos, 363 llegaron a visita final (2 años). Los motivos por lo que se perdió el seguimiento fueron diversos, siendo el más frecuente el abandono voluntario del estudio o el cambio de residencia tanto del investigador como del paciente.
Los pacientes incluidos en los distintos grupos de tratamiento eran comparables en lo que respecta a las características basales (tabla 1). Destaca el hecho de que la edad media al diagnóstico de la enuresis era de aproximadamente 6,5 años. Cabe resaltar la fuerte comorbilidad que presenta la ENPM con la hipertrofia de amígdalas y vegetaciones adenoideas (HAVA).
Datos demográficos de los pacientes. Los datos se expresan en media (desviación estándar) o en frecuencia (%)
| Observación | Conducta y/o alarma | Desmopresina+observación | Desmopresina+conducta | Otros | |
| Peso al nacimiento (kg) | 3,21 (0,29) | 3,31 (0,34) | 3,19 (0,48) | 3,26 (0,43) | 3,36 (0,42) |
| Longitud al nacimiento (cm) | 49,99 (2,21) | 50,13 (1,36) | 49,84 (2,14) | 49,80 (2,01) | 50,26 (1,60) |
| Sexo del paciente | |||||
| Varón | 20 (57,1%) | 22 (84,6%) | 186 (69,4%) | 128 (73,6%) | 26 (74,3%) |
| Mujer | 15 (42,9%) | 4 (15,4%) | 82 (30,6%) | 46 (26,4%) | 9 (25,7%) |
| Peso del padre (kg) | 82,1 (9,0) | 79,0 (7,1) | 79,8 (10,6) | 81,0 (8,7) | 78,92 (11,2) |
| Talla del padre (cm) | 173,8 (5,6) | 174,7 (5,7) | 174,9 (6,0) | 175,1 (6,5) | 172,7 (8,2) |
| Peso de la madre (kg) | 63,3 (9,6) | 61,9 (9,1) | 61,6 (9,0) | 63,8 (11,0) | 64,8 (10,4) |
| Talla de la madre | 163,0 (6,1) | 162,7 (5,0) | 162,3 (5,9) | 162,4 (9,8) | 161,3 (6,3) |
| HAVA | 5 (15,2%) | 5 (23,8%) | 21 (9,1%) | 20 (12,7%) | 2 (6,5%) |
| Medicación concomitantea | 0 (0%) | 0 (0%) | 8 (3,1%) | 3 (1,9%) | 1 (3,0%) |
| Demanda asistencia | 18 (51,4%) | 15 (57,7%) | 211 (80,2%) | 129 (74,6%) | 25 (71,4%) |
| Diagnósticado en nuestro servicio | 17 (48,6%) | 11 (42,3%) | 50 (19,0%) | 44 (25,4%) | 7 (20,0%) |
| Remitido por otro médico | 0 (0%) | 0 (0%) | 2 (0,8%) | 0 (0%) | 3 (8,6%) |
| Edad | 6,4 (1,2) | 6,3 (1,1) | 7,05 (1,3) | 6,90 (1,2) | 7,21 (1,4) |
HAVA: hipertrofia de amígdalas y vegetaciones adenoideas.
No se encontraron diferencias significativas en los parámetros evaluados.
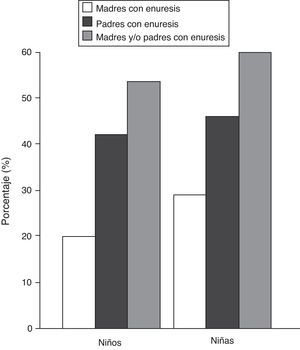
En lo que respecta a las características de los padres, se advierte que existe un alto porcentaje de sujetos enuréticos cuyos padres sufrieron enuresis (fig. 2). Así, el riesgo de sufrir enuresis si habían tenido una madre enurética se multiplica por 1,681 [IC 95% 1,087-2,599; p<0,05] en el caso del sexo femenino. En términos globales podemos decir que aproximadamente el 60% de las niñas y el 55% de los niños diagnosticados de ENPM en este estudio tenían, al menos, un progenitor enurético.
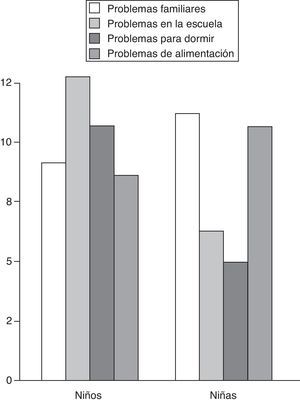
En la figura 3 se observa que, antes de ser diagnosticada la enuresis, está ligada en un alto porcentaje de casos a problemas en ambos sexos. En los niños destacan los problemas escolares y en las niñas los familiares y los de alimentación.
En cuanto a las características basales podemos comprobar que tanto el peso, como la talla como el IMC que presentaban los sujetos en el momento del diagnóstico de ENPM eran normales para su edad y sexo, como se puede comprobar en la tabla 2 que expresa los resultados en desviación estándar estandarizada (SDS).
Datos antropométricos basales. Los datos se expresan en mediana (percentil 25, percentil 75)
| Hombre | Mujer | |||||
| Mediana | P25 | P75 | Mediana | P25 | P75 | |
| SDS talla | 0,30 | -0,45 | 1,06 | 0,21 | -0,50 | 0,93 |
| SDS peso | -0,01 | -0,49 | 0,71 | 0,04 | -0,46 | 0,83 |
| SDS IMC | -0,08 | -0,63 | 0,46 | 0,06 | -0,44 | 0,77 |
| Vel. de Crec. Talla (cm) | 6,0 | 5,5 | 7,0 | 6,0 | 5,0 | 7,0 |
| Vel. de Crec. Peso (kg) | 3,00 | 2,00 | 4,00 | 3,00 | 2,15 | 4,00 |
SDS: desviación estándar estandarizada.
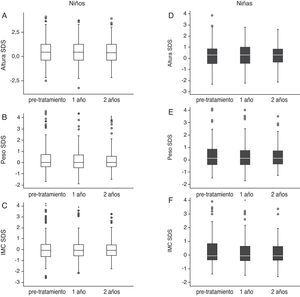
Si expresamos los datos antropométricos en términos de SDS, observamos que no se aprecian cambios en la talla (fig. 4) ni en niños ni en niñas. De la misma manera, el IMC y el peso no se ven alterado tras 2 años de tratamiento de la ENPM (fig. 4).
A: evolución de la SDS de talla en niños; B: evolución de la SDS de peso en niños; C: evolución de la SDS del IMC en niños; D: evolución de la SDS de talla en niñas; E: evolución de la SDS de peso en niñas; F: evolución de la SDS de IMC en niñas. No se observan diferencias significativas en ningún caso. IMC: índice de masa corporal; SDS: desviación estándar estandarizada.
Si estratificamos la evolución de los parámetros anteriormente descritos en función del tipo de tratamiento recibido, encontramos que, en el grupo tratado con terapia conductual con o sin alarma asociada experimenta una disminución significativa en el SDS de talla y de peso tras 2 años de tratamiento (tabla 3) aunque desde un punto de vista clínico este dato no es relevante (-0,26 SDS en 2 años). Además, en el grupo tratado con otras opciones de tratamiento se observa una disminución significativa en la SDS de peso tras 2 años de tratamiento. En todos los demás grupos no se observaron alteraciones significativas.
Evolución de los parámetros antropométricos según las distintas opciones de tratamiento. Los datos se expresan en mediana (percentil 25, percentil 75)
| Talla | Peso | Índice de masa corporal | p | |||||||
| Pretratamiento | 1 año | 2 años | Pretratamiento | 1 año | 2 años | Pretratamiento | 1 año | 2 años | ||
| Global | 0,22(-0,45; 1,05) | 0,28(-0,45; 0,99) | 0,29(-0,47; 0,92) | -0,01(-0,49; 0,73) | 0,04(-0,49; 0,70) | -0,01(0,47; 0,59) | -0,05(-0,59; 0,53) | -0,03(-0,54; 0,53) | -0,05(-0,53; 0-53) | ns |
| Observación | -0,16(-0,70; 0,57) | -0,23(-0,63; 0,89) | -0,43(-0,80; 0,49) | -0,06(-0,55; 0,61) | -0,10(-0,38; 0,49) | -0,23(-0,48; 0,63) | -0,06(-0,45; 0,53) | -0,02(-0,52; 0,44) | -0,19(-0,40; 0,83) | ns |
| Conductaa | 0,22(-0,23; 1,05) | 0,15(-0,45; 0,85) | -0,04(-0,71; 0,48) | 0,18(-0,40; 0,73) | -0,14(-0,34; 0,48) | -0,06(-0,44;0,39) | -0,20(0,54; 0,68) | -0,26(-0,57; 0,46) | 0,10(-0,67; 0,51) | <0,05* |
| Desmopresinab | 0,34(-0,45; 1,10) | 0,29(-0,47; 1,02) | 0,35(-0,45; 1,07) | 0,04(-0,49; 0,67) | 0,04(-0,55; 0,63) | 0,02(-0,47; 0,52) | -0,05(-0,59; 0,45) | -0,08(-0,57; 0,45) | -0,04(-0,54; 0,49) | ns |
| Desmopresinac | 0,29(-0,42; 1-04) | 0,33(-0,45; 1,00) | 0,41(-0,45; 0,86) | -0,03(-0,45; 0,83) | 0,06(-0,43; 0,81) | 0,03(-0,43; 0,65) | -0,09(-0,60; 0,50) | -0,01(-0,45; 0,52) | -0,06(-0,50; 0,55) | ns |
| Otros | 0,17(-0,56; 0,71) | 0,34(-0,42; 0,88) | 0,33(-0,32; 0,86) | 0,18(-0,49; 1,12) | 0,12(-0,55; 0,79) | -0,01(-0,56; 0,75) | 0,23((-0,70; 1,07) | 0,16(0,65; 0,95) | 0,13(-0,70; 0,73) | <0,05** |
Uno de los objetivos secundarios más importantes del estudio consistía en comprobar la eficacia de las distintas opciones terapéuticas elegidas por los médicos. Como criterio de curación se aplicó el 100% de noches secas tras 3 meses sin tratamiento. La tasa de curación tras un año de tratamiento se produce de manera mayoritaria en el grupo tratado con desmopresina y observación, siendo dicha tasa de un 58% durante el primer año de tratamiento y de un 80,6% durante el segundo año.
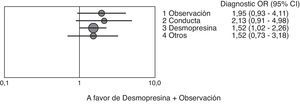
En la figura 5 se puede observar que la probabilidad de curación durante el primer año de tratamiento se multiplica por 1,52 (IC 95%:1,02-2,26; p<0,05) cuando se utiliza desmopresina+observación si se compara con el tratamiento con desmopresina y terapia conductual, mientras que en la figura 6 destaca el hecho de que la probabilidad de curación durante los 2 primeros años de tratamiento se multiplica por 2,86 (IC 95%:1,24-6,59) cuando se utiliza desmopresina+observación si se compara con terapia observacional y de conducta asociada o no a alarma.
En términos globales podemos decir que la odds de curación tras uno y 2 años de tratamiento se multiplica por 1,41 (IC 95%: 0,85-2,34) y 1,52 (IC 95%: 0,86-2,70) cuando se compara la desmopresina (y observación) con todas las demás opciones.
SeguridadDurante los 2 años de tratamiento se produjeron 2 interrupciones por efectos secundarios. Una en el grupo de observación y terapia de conducta, y otra en el grupo de otras opciones, concretamente en un sujeto tratado con anticolinérgicos.
DiscusiónLa enuresis nocturna es un problema común entre la población pediátrica cuya etiología no ha sido todavía totalmente clarificada. Las causas más aceptadas de la enuresis nocturna son un tamaño reducido de la vejiga unido a alteraciones en los patrones normales del sueño. Además se ha relacionado con factores de comportamiento así como con un retraso en la maduración funcional del sistema nervioso central7,19. Nuestro estudio viene a confirmar alguno de estos hallazgos ya que, por ejemplo, hemos encontrado un gran porcentaje tanto de niños como de niñas en los que la enuresis nocturna estaba asociada a problemas familiares y escolares así como a trastornos de la alimentación y del sueño. En este último apartado destaca el hecho de que un 11,1% de los niños que se incluyeron en el estudio padecía HAVA, una patología que ya había sido relacionada con la enuresis en un pequeño número de trabajos anteriores al nuestro20.
Otro de los hallazgos más importantes de nuestro estudio es la confirmación del fuerte patrón de «heredabilidad» que presenta la enuresis. En este sentido, en el 40% de los sujetos incluidos en el estudio se puede hablar de que su progenitor paterno había sufrido enuresis en su infancia. Por otro lado, se encontraron antecedentes maternos de enuresis en el 30% de las niñas y en el 20% de los niños con enuresis incluidos en el estudio. Esta diferencia nos da a entender que en el caso del sexo femenino existe una mayor influencia genética de transmisión de madres a hijas que en el caso de los padres a los hijos varones.
Uno de los objetivos más importantes de nuestro trabajo era el comprobar si los niños con enuresis nocturna no tratada presentaban alteraciones en los parámetros antropométricos cuando se comparaban con niños sanos, ya que, en estudios previos se habían descrito retrasos en la edad y en la densidad mineral ósea12. Dejando a parte los aspectos genéticos, la gran prevalencia de trastornos psicosociales que hemos encontrado en los niños con enuresis podría ser una de las explicaciones de la mencionada hipótesis inicial de nuestro estudio, ya que se sabe que los pacientes con talla baja de componente psicosocial pueden presentar un déficit idiopático de GH o una resistencia a la acción de la misma15. Sin embargo, en nuestro estudio hemos encontrado que los niños españoles con enuresis presentan una talla, peso e IMC acordes con respecto a los parámetros de normalidad para su edad (SDS). Este dato, aparentemente contradictorio, coincide con los encontrados en otros estudios como, por ejemplo, el publicado por Dundaroz et al. en el que, a pesar de encontrar retrasos en la edad ósea en niños con enuresis nocturna no hallaron diferencias en la talla y en el peso13. Asimismo en un estudio más reciente21 en el que se incluyó un reducido número de niños con enuresis nocturna primaria (n=27) y de niños control (n=19), tampoco se encontraron diferencias ni en la edad ósea, ni en el peso ni en la talla.
No obstante, hay que señalar también que los niños incluidos en nuestro estudio tenían edades comprendidas entre los 5 y los 10 años aproximadamente, y que por lo tanto, quizá no habríamos dejado tiempo a que la ENPM actúe sobre los parámetros antropométricos.
Sería interesante, por consiguiente, estudiar también a un subgrupo de niños con ENPM y edades cronológicas más avanzadas y que no hayan recibido tratamiento, para valorar sus estándares de talla, peso e IMC. En este subgrupo habríamos dejado más tiempo actuar a las variables psicosociales, y probablemente sería más fácil poder encontrar alteraciones en los parámetros antropométricos con respecto a la población control de su misma edad.
De esta manera, el retraso en la edad ósea en los niños que sufren esta patología puede reflejar un retraso madurativo en las funciones del sistema nervioso central que no se manifestaría en los parámetros antropométricos.
Otro de los objetivos del presente trabajo, y que no ha sido descrito hasta el momento en la literatura científica, es comprobar la evolución de los distintos parámetros antropométricos de los niños enuréticos en función de las diferentes opciones de tratamiento elegidas por el médico. Llegados a este punto, encontramos que el tratamiento de la enuresis no produce ningún compromiso en la evolución de la talla de los niños/as con la enfermedad en estudio. Sí se observa, por otro lado, una disminución significativa en la SDS de peso únicamente en los individuos de sexo masculino.
Sin embargo, si analizamos los resultados más en detalle encontramos que aquellos niños en los que se optó por llevar a cabo una terapia observacional y de conducta asociada o no a la alarma presentaban disminuciones en la talla y el peso tras uno y 2 años de tratamiento. Esto no ocurre así con ninguna de las otras opciones de tratamiento. Dada la relatividad y limitaciones de nuestro estudio entendemos que estos datos carecen de relevancia clínica (-0,26 SDS) aunque hipotéticamente podrían atribuirse a que una de las implicaciones que suelen tener tanto la terapia conductual como la alarma son el despertar al niño por la noche para que orine. Este acto podría tener como consecuencia una alteración en el pico de secreción nocturna de GH22.
Con respecto a los objetivos secundarios, cabe destacar que la desmopresina, bien sea sola (junto con observación) bien en combinación con la terapia conductual es la opción que consigue una mayor tasa de curación tras un año de tratamiento. Además tras 2 años de tratamiento con desmopresina y observación se multiplica la probabilidad de curación por 2,86 (p<0,05) si se compara con la terapia de observación por sí sola. Este hallazgo es el primero de estas características que se encuentra en un número tan importante de pacientes (363) aunque ya había sido descrito en estudios anteriores23–25.
Aunque este estudio debería ser tomado como una hipótesis debido a las limitaciones de su diseño epidemiológico y la escasa relevancia clínica de los resultados, podemos decir, como conclusiones, que en nuestro estudio los niños con ENPM diagnosticados y tratados con edades comprendidas entre los 5 y 10 años aproximadamente presentan unos parámetros antropométricos (talla, peso e IMC) acordes con su edad y sexo, y que el tratamiento global de la ENPM no parece afectar de manera clínicamente relevante a los mencionados parámetros. Además, la opción mayoritaria para el tratamiento de la ENPM es la desmopresina, tanto unida a observación como a terapia conductual, siendo la primera la que más tasa de curación obtiene tras uno y 2 años de seguimiento.
Por último, nuestros datos avalan la necesidad de efectuar un diagnóstico y tratamiento precoces de la ENPM, lo que sin duda contribuiría a evitar las repercusiones psicosociales que puede desencadenar este trastorno en la vida de los niños que la padecen.
Conflicto de InteresesFerring SAU fue promotor del estudio. Los investigadores recibieron una compensación económica acorde al número de pacientes incluidos en el estudio.
Francisco Ponce (Mairena de Alcor), Antonio Escobar (San Hilario), Natividad Canales (Lebrija), María Antonia Reina (Lebrija), Inmaculada Martín (Los Palacios), Elena Valera (Los Palacios), Gabriel Pou (Carmona), Enrique Maqueda (Gines), Juan José Silva (Gerena), Ramón Roldán (Guillena), Francisco Calderón (Bollullos del Condado), José Antonio Delgado (Castilleja de la Cuesta), Manuel Haro (Almorrón), Ana Pérez (Alora), Izilda Molina (Tiro Pichón), Miguel Ángel Diego (Campanillas), Elisa Márquez (Marbella), M. del Mar Lillo (Estepona), Pilar Valdés (Arroyo Miel), Eufrasia García (Alhaurín Grande), Patricia Pérez (La Cala Moral), Eduardo Torres (El Palo), Encarnación Martín (La Palmilla), Francisco Carrillo (San Andrés), Fuensanta Costa (Lorca Centro), Juan José Vigueras (Mariano Yago), Francisco Navarro (Vistabella), Pascual Santos (Caravaca), Servicio Pediatría (San Javier), Servicio Pediatría (Huercal Overa), Juan Cayetano Canovas (Beniel), María Luisa Camps (Espinardo), Manuel García (La Consolación), María Paz Ortuño (San Antón), Sebastián Lorente (Totana), Antonio Iofrio (Los Dolores), Bernardo Cervantes (La Unión), Monserrat Montes (Colón), Isabel Muriel (Colón), Amparo Cabez (Poniente), Amancio Gómez (Poniente), Reyes Martínez (Fuensanta), Carmen de la Torre (Levante Norte), Ruth Capitán (Santa Rosa), Miriam González (Levante Sur), Josefa Toledano (Levante Sur), José Murcia (Magdalena), Adolfo Ramírez (El Valle), Raúl Cordero (San Felipe), Manuel Escobar (El Progreso), Luis Valbuena (La Solana), Margarita Tomico (Humans), José M. Obeo (Illescas), Rosa María Bernal (Abrantes), María Teresa Garde (Polígono), José María de Cea (Severo Ochoa), Jesús Jordán (Vicente Soldevilla), Pilar García (San Juan de la Cruz), Luis Rubio (Valdebernardo), Beatriz Serrano (Orcasitas), Virginia del Rey (Coronel de Palma), Marien Llorente (Los Alpes), Benjamín Herranz (Torrejón de Ardoz), Eva Escribano (Móstoles), Carlos Montachez (Bohadilla del Monte), Pedro Rincón (La Chopera), Encarnación Santos (Cebreros), M. Ángeles Bascones (Estrecho de Corea), María Villa (Pascual Rodríguez), Javier Lassaletta (Pascual Rodríguez), José Sepúlveda (San Vicente), Antonio Tosao (El Cabo), Francisco Javier García (Las Lomas), M. Carmen Belda (Villena Ii), Santiago Barrios (El Toscar), Encarna Ortuño (Marina Española), Manuel López (Orihuela), Javier Bru (Altabix), Gloria María Fraga (Sant Pau), Pilar Broto (Llefia), Juan Verges Brotons (Badalona), Rosa M. Isnard (Germans Trias I Pujol), Pilar Cerdá (Fondo), Xavier Vallbona (Lliça D¿Amunt), Jose M. Martínez (Pumarín-Naranco), Venancio Martínez (El Llano), M. Dolores Grión (Sagrado Corazón), Juan Blanco (Pola de Siero), Fernando Fueyo (Pola de Siero), Angeles Hernández (Natahoyo), Encarnación Diez (Pumarín-Naranco), Begoña Domínguez (Otero), Jacinto Martínez (El Coto), Marta López (Contrueces), Santiago Rodríguez (Terrassa Nord), Hortensia Pallares (Gava), José Molina (Viladecans), Vicens Morales (Vilafranca), Rosalia Casas (Consulta Privada El Prat), Enrique Ferrer (Navarcles), Erwin Amaya (Sant Andreu de la Barca), Inmaculada Cid (Amadeu Torner), Carles Flaquer (Montclar), Ana Tomas (Bobila), Holman Shedden (Castellbel I El Vilar), Eduardo Zabala (Llibertat), Gabriela Ricoma (Jaume I), M. Jesus Blasco (Valdefierro), M. Jesús Alcazar (Calatayud), Teresa Arana (Sagasta), Carmen Puig (Actur Norte), José M. Aranda (H. Ernest Lluch), Héctor Colán (Hnos. Ibarra), M. Jose Agusti (Sta. Mª de Pla), Pedro Oros (Casetas), Carlos Chérrez (Azpilagaña), Alberto Díaz (Villava), Jesus Soria y Mercedes Elizalde (Orcoyen), Emma de la Fuente (San Vicente), Pedro Núñez (Matiko), Miguel Ángel Martinez (Las Arenas), Fernando Urzainqui (Berriozar), Marta Pérez (Castaños), Lourdes Aramburu (Antiguo), Cesar Ruiz (Parquesol), Luis Rodríguez (Huerta del Rey), Pedro de la Serna (Pinilla-Trobajo), Javier Polo Diez (Pizarrales), Mercedes Miguélez (Puerta Nueva), José Martín (Santa Marta), Benito de Dios (Santa Marta), Esperanza Casas (Delicias), Puerto Llorente (Son Gotleu), Edelmiro Vergés (Binissalem), Gloria Pérez (Rafal del Palma), Nicolás Torres (Galdar), Luisa María Torres (La Matanza), Ana Bretón (Los Silos), Margarita Monge (Ravelo), José María Baldo (Quart de Poblet), M. José Sanz (Quart de Poblet), Julia Ruiz (CS Sedaví), Adnan Qaisi (CS Benetusser), Silvia Sánchez (CS Picaña), Rosalía Piñeiro (Coia), Carlos Maíz (Ventorrillo), Manuel Pumarega (La Estrada), Manuel Sampedro (Amb. Novoa), Elena Álvarez (San José), Luisa Bujan (Garda), Elisa Barrios (Catalina Santana Vega), Susana Peñarroja (Vall D¿Uxó), Lourdes Jordano (Huerta de la Reina) y Vicente García (Carrus).
Los miembros del grupo EDANE se listan en el anexo 1.