El estudio se llevó a cabo para estimar la carga de enfermedad de la gripe confirmada por laboratorio en niños menores de 15 años.
Pacientes y métodosLos niños que acudieron al Hospital Universitario de Basurto con síntomas de infección respiratoria aguda y/o fiebre aislada entre noviembre de 2010 y mayo de 2011 fueron incluidos en el estudio (NCT01592799). Se tomaron 2muestras de secreción nasofaríngea: una para un test de diagnóstico rápido en el Servicio de Urgencias y otra para análisis en laboratorio con reacción en cadena de la polimerasa en tiempo real y cultivo viral.
ResultadosSe seleccionó a un total de 501 niños, de los que 91 fueron hospitalizados. El diagnóstico de gripe se confirmó en 131 (26,1%); 120/410 (29,3%) fueron tratados ambulatoriamente y 11/91 (12,1%), hospitalizados. En 370/501 niños (73,9%) el resultado no fue positivo. La proporción de otros virus respiratorios fue 145/501 (28,9%) casos y de coinfección con otro virus respiratorio además de gripe de 7/501 (1,4%). Los tipos de virus de gripe fueron: A (H1N1 y H3N2) 53,2% (67/126); B (Victoria y Yamagata) 46,0% (58/126); A+B 0,8% (1/126). El coste médico directo medio asociado con cada caso de gripe confirmada fue de 177,00€ (N=131). No se observaron diferencias estadísticamente significativas entre el coste asociado con gripe A o B.
ConclusiónCasi la mitad de los casos fueron virus de gripe B. La administración de una vacuna que incluya tipos A y B de gripe debería reducir la carga de la enfermedad.
This study was undertaken to estimate the burden of morbidity associated with laboratory-confirmed influenza in children below 15 years of age.
Patients and methodsChildren presenting with acute respiratory infection and/or isolated fever at the Basurto University Hospital, Bilbao, Spain between November 2010 and May 2011 were included in this study (NCT01592799). Two nasopharyngeal secretion samples were taken from each; one for a rapid influenza diagnostic test in the emergency department, and the second for laboratory analysis using real-time polymerase chain reaction and viral culture.
ResultsA total of 501 children were recruited, of whom 91 were hospitalized. Influenza diagnosis was confirmed in 131 children (26.1%); 120 of 410 (29.3%) treated as outpatients and 11 of 91 (12.1%) hospitalized children. A total of 370 of 501 children (73.9%) had no laboratory test positive for influenza. The proportion of subjects with other respiratory viruses was 145/501 (28.9%) cases and co-infection with the influenza virus plus another respiratory virus was detected in 7/501 (1.4%) cases. Influenza virus types were: A (H1N1 and H3N2) 53.2% (67/126); B (Victoria and Yamagata) 46.0% (58/126); A+B 0.8% (1/126). The median direct medical costs associated with each case of laboratory-confirmed influenza was €177.00 (N=131). No significant differences were observed between the medical costs associated with influenza A and B.
ConclusionAlmost half of the cases were influenza virus B type. The administration of a vaccine containing influenza A and B types to children below 15 years of age might reduce the overall burden of the illness.
La gripe es una enfermedad respiratoria aguda provocada por el virus de la gripe, asociada a un amplio abanico de manifestaciones clínicas que abarca desde procesos autolimitados de las vías respiratorias altas hasta repercusiones sistémicas y complicaciones potencialmente mortales1,2. La gripe suele presentarse en epidemias estacionales anuales, aunque en ocasiones puede ser pandémica. La Organización Mundial de la Salud (OMS) estima que la incidencia global de la gripe es de 3a 5millones de casos anuales, que causan aproximadamente 300.000 muertes cada temporada, de las que más de 40.000 ocurren en la Unión Europea1,3. Los lactantes, los niños con enfermedades subyacentes y los adultos mayores de 65 años son los grupos más susceptibles a las formas graves de la enfermedad2–4. No obstante, la mayor morbilidad se observa en la edad pediátrica, y los niños son los principales transmisores de la infección. La gripe infantil también comporta costes económicos y sociales considerables4-6.
Los tipos de virus de la gripe que afectan más comúnmente a los seres humanos son el A y el B. Las epidemias anuales suelen deberse a variantes menores de ambos grupos7, de manera que casi todos los niños se infectan en los primeros años de vida y desarrollan inmunidad exclusivamente a esa cepa concreta del virus. El virus influenza A puede infectar a diversas especies de animales y, por consiguiente, en ocasiones causa pandemias y preocupa más a las autoridades sanitarias que el virus influenza B, que solo afecta a los seres humanos2,8,9. Como el virus de la gripe A muestra una variación considerable, se clasifica en subtipos con base en sus antígenos de membrana hemaglutinina (HA) y neuraminidasa (NA). Divergencias antigénicas y genéticas han llevado a la distinción de 2linajes del virus de la gripe B: Victoria y Yamagata, que llevan cocirculando por todo el mundo desde los años ochenta8,10. Es difícil predecir qué linaje va a prevalecer en la siguiente temporada de la gripe11.
La vacunación contra la gripe es un método eficaz para prevenir la infección y sus complicaciones4. Aunque es difícil calcular la incidencia real de la enfermedad por la naturaleza inespecífica de su clínica12, resulta esencial obtener datos precisos sobre la carga de la enfermedad y los costes médicos asociados a la gripe para desarrollar la estrategia de vacunación más apropiada. En España, los datos disponibles son escasos, de ahí que el presente estudio se diseñara para cuantificar el número de visitas a servicios de urgencias y de hospitalizaciones, así como los costes médicos directos atribuibles a casos de gripe confirmada por laboratorio en niños menores de 15 años que acudieron al hospital con infecciones respiratorias agudas (IRA) o fiebre aislada durante la temporada de gripe.
Pacientes y métodosDiseño y población de estudioEstudio prospectivo (NCT01592799) realizado en el Hospital Universitario de Basurto (Bilbao, España), centro de nivel terciario con un servicio de urgencias generales, entre noviembre de 2010 y mayo de 2011 (con posterioridad a la pandemia de gripe de 2009), conforme a los principios de buena práctica clínica, la Declaración de Helsinki y los estándares locales. El protocolo de estudio fue aprobado por el Comité Ético institucional, y se obtuvo el consentimiento informado de los padres o tutores legales de los niños menores de 12 años y de los niños de mayor edad antes de su inclusión en el estudio.
Se seleccionó a niños de menos de 15 años de edad que acudieron al servicio de urgencias con una IRA durante una temporada de gripe (definida como el período transcurrido entre el primer y el último caso de gripe confirmada por laboratorio), independientemente de que fueran o no admitidos al hospital. La IRA se definió como la presencia de al menos uno de los siguientes síntomas: dolor de garganta (en niños ≥3 años), rinorrea, tos y/o dificultad respiratoria, y/o fiebre aislada (temperatura oral ≥37,5°C; axilar ≥37,5°C; rectal ≥38°C, timpánica ajustada para temperatura oral ≥37,5°C o timpánica ajustada para temperatura rectal ≥38°C)13.
Se obtuvieron 2 muestras clínicos (frotis faríngeo y/o nasofaríngeo) de cada paciente y se revisaron sus historias clínicas (incluyendo vacunaciones previas, medicación concomitante, síntomas asociados a IRA o fiebre y hallazgos del examen físico). Los datos fueron recogidos directamente por cada pediatra en el formulario de datos clínicos del estudio. En pacientes hospitalizados, la información sobre la evolución clínica de la enfermedad y el tratamiento recibido se completó al alta.
Aproximadamente al mes de la visita inicial al hospital, se contactó telefónicamente con las familias para llevar a cabo una entrevista de seguimiento. Se obtuvo información concerniente a la evolución clínica de la enfermedad, la necesidad de asistencia médica adicional, el uso de medicamentos sin receta tras el alta hospitalaria; el número de días de ausencia escolar y el número de contactos domiciliarios que habían desarrollado síntomas gripales posteriormente.
Utilizando la información de la base de datos administrativa del hospital, se calcularon los costes médicos asociados a síndromes gripales, incluyendo los costes del manejo médico en el servicio de urgencias, de hospitalización, y de los recursos empleados en el diagnóstico y tratamiento de la enfermedad y sus complicaciones.
Procedimientos de laboratorioPara identificar los casos de gripe de manera precoz se realizó inmediatamente un test diagnóstico rápido (Xpect Flu A&B, Remel, Lenexa, Kansas, EE. UU.) en una de las muestras de secreciones nasofaríngeas obtenidas en el servicio de urgencias. Con independencia del resultado, se almacenaron las muestras restantes a 4°C para su transporte al laboratorio del Instituto Valenciano de Microbiología en medio con solución salina de Hanks balanceada (buffer HEPES 1M, gelatina al 0,5%, bicarbonato de sodio al 7,5%, y antibióticos [penicilina, estreptomicina y anfotericina B]) para analítica confirmatoria mediante cultivo viral y reacción de cadena de la polimerasa en tiempo real (RT-PCR). Para esta última determinación, se extrajo el ARN total mediante el Maxwell 16 Viral Total Nucleic Acid Purification Kit (Promega, Madison, Wisconsin, EE. UU.), que se amplificó mediante RT-PCR múltiple con cebadores sentido y antisentido y sondas de etiquetado doble FAM-BHQ-1 o HEX-BHQ-1 para identificar los virus de la gripe de tipo A14 y de tipo B15, respectivamente.
Análisis estadísticoEl tamaño muestral estimado requería la inclusión de 500 sujetos atendidos en el servicio de urgencias con clínica de IRA y/o fiebre aislada con base en una proporción esperada de infección por virus de la gripe confirmada por laboratorio del 5 al 20% de los sujetos. El hospital registra los costes médicos de cada tratamiento y servicio asistencial recibido por los pacientes. Los costes médicos directos de los casos pediátricos de gripe confirmada por laboratorio se calcularon con base en los datos administrativos del hospital, tomando en consideración: diagnóstico, manejo médico y tratamiento antigripal, visitas al servicio de urgencias, costes de hospitalización, costes específicos de estancia en planta y costes de unidad de cuidados intensivos (UCI). Los intervalos de confianza (IC) del 95% se calcularon con el software Proc-StatXact (Cytel, Cambridge, Massachusetts, EE. UU.). Las pruebas empleadas para comparar los grupos con resultados positivos y negativos para el virus de la gripe fueron el test de Mann-Whitney para variables ordinales y continuas y el test exacto de Fisher para variables categóricas.
Se llevaron a cabo análisis adicionales para evaluar el coste médico directo, los síntomas y la necesidad posterior de servicios de salud asociados a la gripe de tipos A o B.
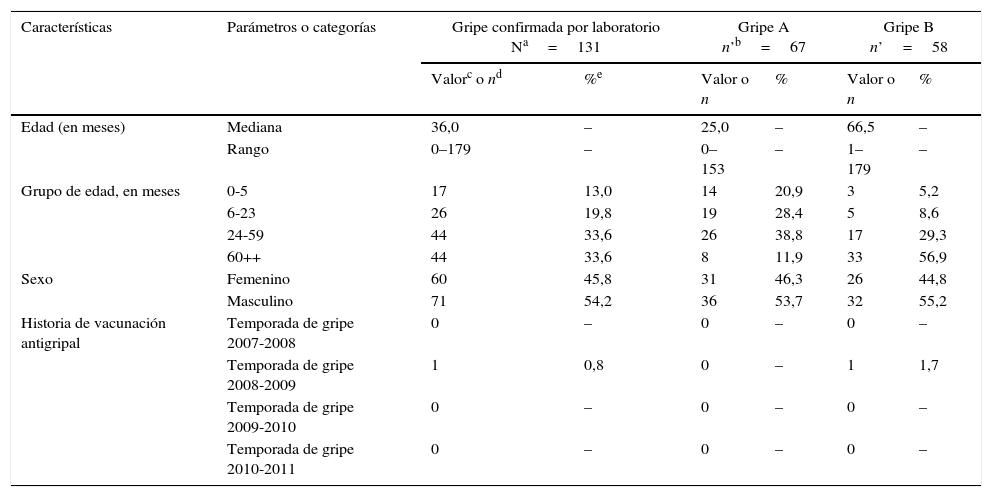
ResultadosSe seleccionó a 501 niños entre noviembre de 2010 y abril de 2011. Como había suficientes datos para evaluar todos los casos, se incluyó a todos los sujetos en el análisis final. Aunque 410 de los niños solo recibieron atención en el servicio de urgencias, 91 tuvieron que ser hospitalizados. El diagnóstico de gripe fue confirmado por laboratorio (mediante test diagnóstico rápido, cultivo o RT-PCR, todos los cuales se realizaron en cada sujeto) en el 26,1% de los niños (131/501; IC del 95%: 22,4-30,2), es decir 29,3% de los ninos que solamente acudieron al servicio de urgencias (120/410; IC del 95%: 24,9-33,9) y 12,1% de los ninos que fueron hospitalizados (11/91; IC del 95%: 6,2-20,6). La edad mediana de los niños con gripe confirmada por laboratorio fue de 36,0 meses (rango: 0-179 meses) y el 54,2% fueron varones (tabla 1).
Características demográficas de niños con gripe confirmada por laboratorio (N=131)
| Características | Parámetros o categorías | Gripe confirmada por laboratorio Na=131 | Gripe A n’b=67 | Gripe B n’=58 | |||
|---|---|---|---|---|---|---|---|
| Valorc o nd | %e | Valor o n | % | Valor o n | % | ||
| Edad (en meses) | Mediana | 36,0 | – | 25,0 | – | 66,5 | – |
| Rango | 0–179 | – | 0–153 | – | 1–179 | – | |
| Grupo de edad, en meses | 0-5 | 17 | 13,0 | 14 | 20,9 | 3 | 5,2 |
| 6-23 | 26 | 19,8 | 19 | 28,4 | 5 | 8,6 | |
| 24-59 | 44 | 33,6 | 26 | 38,8 | 17 | 29,3 | |
| 60++ | 44 | 33,6 | 8 | 11,9 | 33 | 56,9 | |
| Sexo | Femenino | 60 | 45,8 | 31 | 46,3 | 26 | 44,8 |
| Masculino | 71 | 54,2 | 36 | 53,7 | 32 | 55,2 | |
| Historia de vacunación antigripal | Temporada de gripe 2007-2008 | 0 | – | 0 | – | 0 | – |
| Temporada de gripe 2008-2009 | 1 | 0,8 | 0 | – | 1 | 1,7 | |
| Temporada de gripe 2009-2010 | 0 | – | 0 | – | 0 | – | |
| Temporada de gripe 2010-2011 | 0 | – | 0 | – | 0 | – | |
No se tuvieron en cuenta los niños con un test rápido positivo para los tipos A y B.
Dentro de los 131 casos de gripe confirmada por laboratorio, los test indicaron que 126 estaban infectados por virus de la gripe de tipo A o B: 67 (53,2%) dieron positivo al tipo A, 58 (46,0%) al tipo B y uno (0,8%) resultó positivo a ambos tipos. Los resultados de la RT-PCR cuantitativa para la gripe de tipo A mostraron que alrededor del 87% tenían el subtipo H1N1 y el 13% el subtipo H3N2. Del total de 501 niños, 370 (73,9%) no tuvieron resultados positivos para virus de la gripe. Por lo general, los niños con resultados positivos para el tipo B fueron de mayor edad que aquellos infectados por el tipo A (tabla 1). En los niños con resultados positivos para el tipo B, las proporciones de los linajes Victoria y Yamagata fueron del 96,6% (56/58) y del 3,4% (2/58), respectivamente.
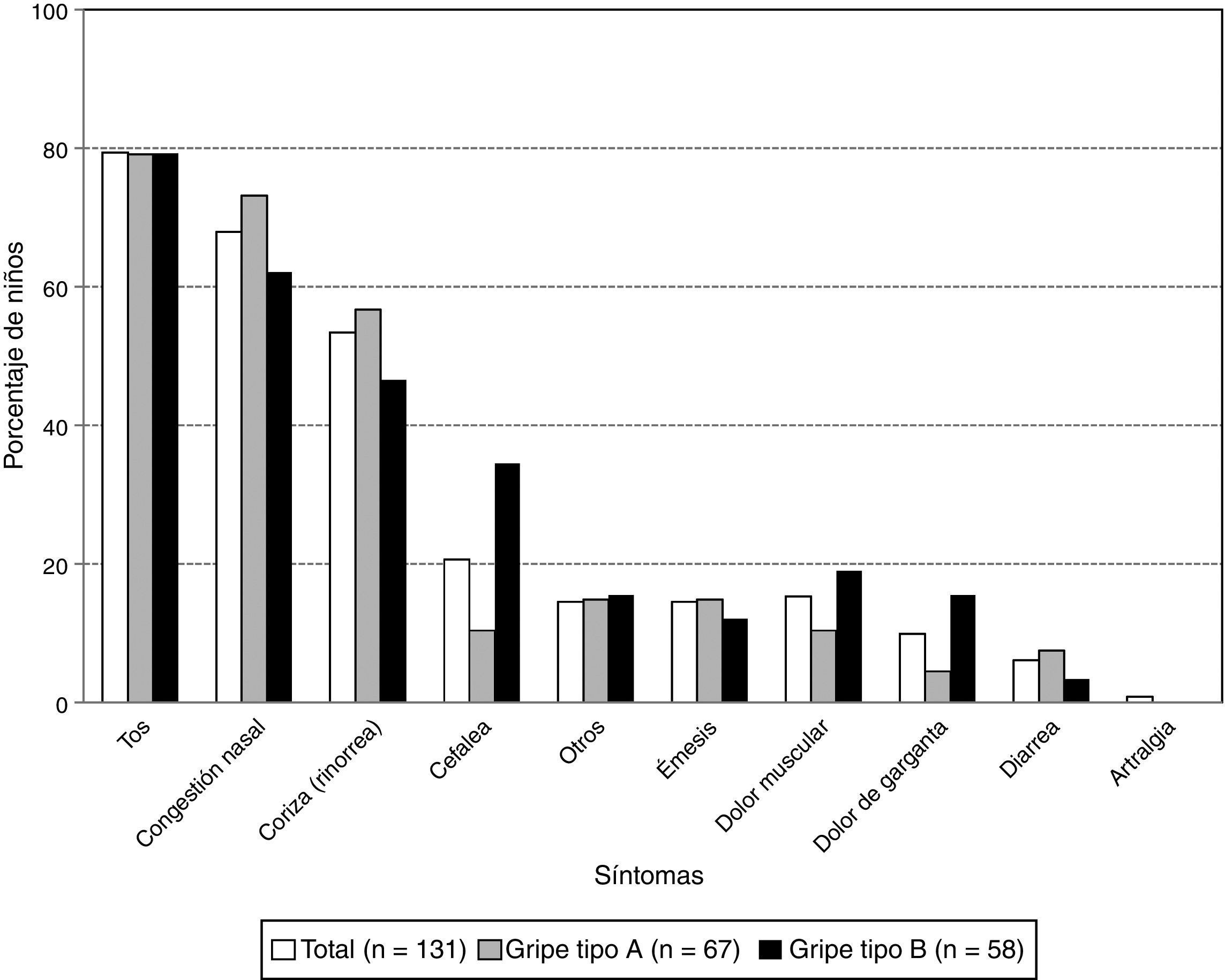
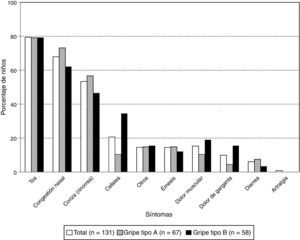
La tos fue el síntoma más frecuente en niños con gripe confirmada por laboratorio (79,4%: 104/131), seguida de congestión nasal (67,9%: 89/131) y rinorrea (53,4%: 70/131). No encontramos diferencias significativas en la frecuencia de estos síntomas entre los niños diagnosticados con distintos tipos de virus (fig. 1). Sin embargo, hubo un número significativamente menor de casos con cefalea en niños con gripe A que en niños con gripe B (10,4%: 7/67 y 34,5%: 20/58; p=0,0019).
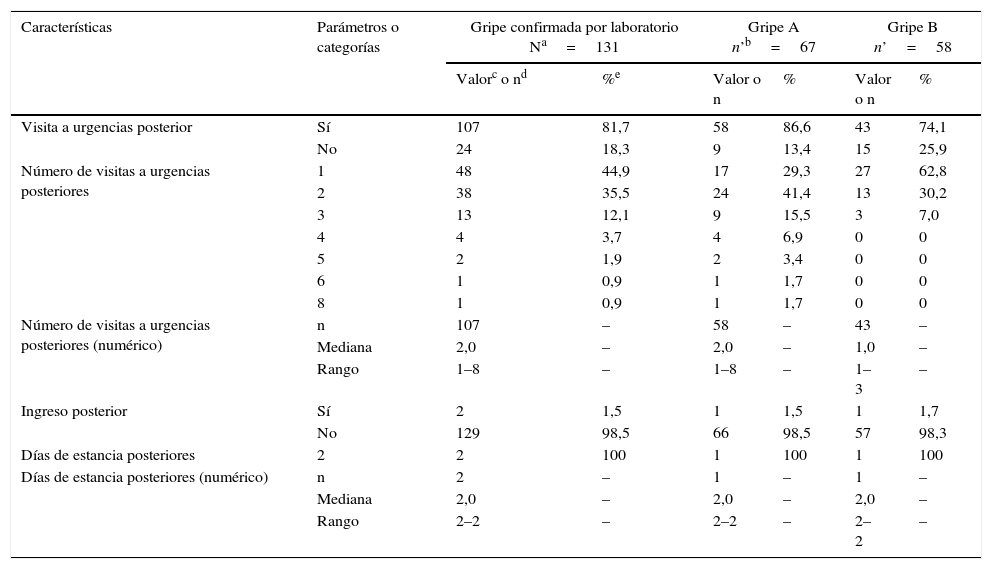
De los 131 casos de gripe confirmada por laboratorio, 107 (81,7%) necesitaron ser reevaluados en el servicio de urgencias tras el alta, y 2(1,5%) tuvieron que ser ingresados (tabla 2). Casi todos los pacientes hicieron visitas de seguimiento, independientemente de los resultados de la analítica: el 81,7% de los sujetos con resultados positivos para gripe y el 87,0% de los sujetos con resultados negativos (p=0,1477). Entre los casos de gripe, las proporciones de pacientes con gripe A (86,6%) y con gripe B (74,1%) que hicieron visitas de seguimiento fueron similares (p=0,1104). En el momento del último contacto, casi todos los niños (93,1%: 122/131) se habían repuesto, mientras que el 6,9% (9/131) seguían recuperándose.
Ingresos y visitas a urgencias posteriores en casos de gripe confirmada por laboratorio (N=131)
| Características | Parámetros o categorías | Gripe confirmada por laboratorio Na=131 | Gripe A n’b=67 | Gripe B n’=58 | |||
|---|---|---|---|---|---|---|---|
| Valorc o nd | %e | Valor o n | % | Valor o n | % | ||
| Visita a urgencias posterior | Sí | 107 | 81,7 | 58 | 86,6 | 43 | 74,1 |
| No | 24 | 18,3 | 9 | 13,4 | 15 | 25,9 | |
| Número de visitas a urgencias posteriores | 1 | 48 | 44,9 | 17 | 29,3 | 27 | 62,8 |
| 2 | 38 | 35,5 | 24 | 41,4 | 13 | 30,2 | |
| 3 | 13 | 12,1 | 9 | 15,5 | 3 | 7,0 | |
| 4 | 4 | 3,7 | 4 | 6,9 | 0 | 0 | |
| 5 | 2 | 1,9 | 2 | 3,4 | 0 | 0 | |
| 6 | 1 | 0,9 | 1 | 1,7 | 0 | 0 | |
| 8 | 1 | 0,9 | 1 | 1,7 | 0 | 0 | |
| Número de visitas a urgencias posteriores (numérico) | n | 107 | – | 58 | – | 43 | – |
| Mediana | 2,0 | – | 2,0 | – | 1,0 | – | |
| Rango | 1–8 | – | 1–8 | – | 1–3 | – | |
| Ingreso posterior | Sí | 2 | 1,5 | 1 | 1,5 | 1 | 1,7 |
| No | 129 | 98,5 | 66 | 98,5 | 57 | 98,3 | |
| Días de estancia posteriores | 2 | 2 | 100 | 1 | 100 | 1 | 100 |
| Días de estancia posteriores (numérico) | n | 2 | – | 1 | – | 1 | – |
| Mediana | 2,0 | – | 2,0 | – | 2,0 | – | |
| Rango | 2–2 | – | 2–2 | – | 2–2 | – | |
No se tuvieron en cuenta los niños con un test rápido positivo para los tipos A y B.
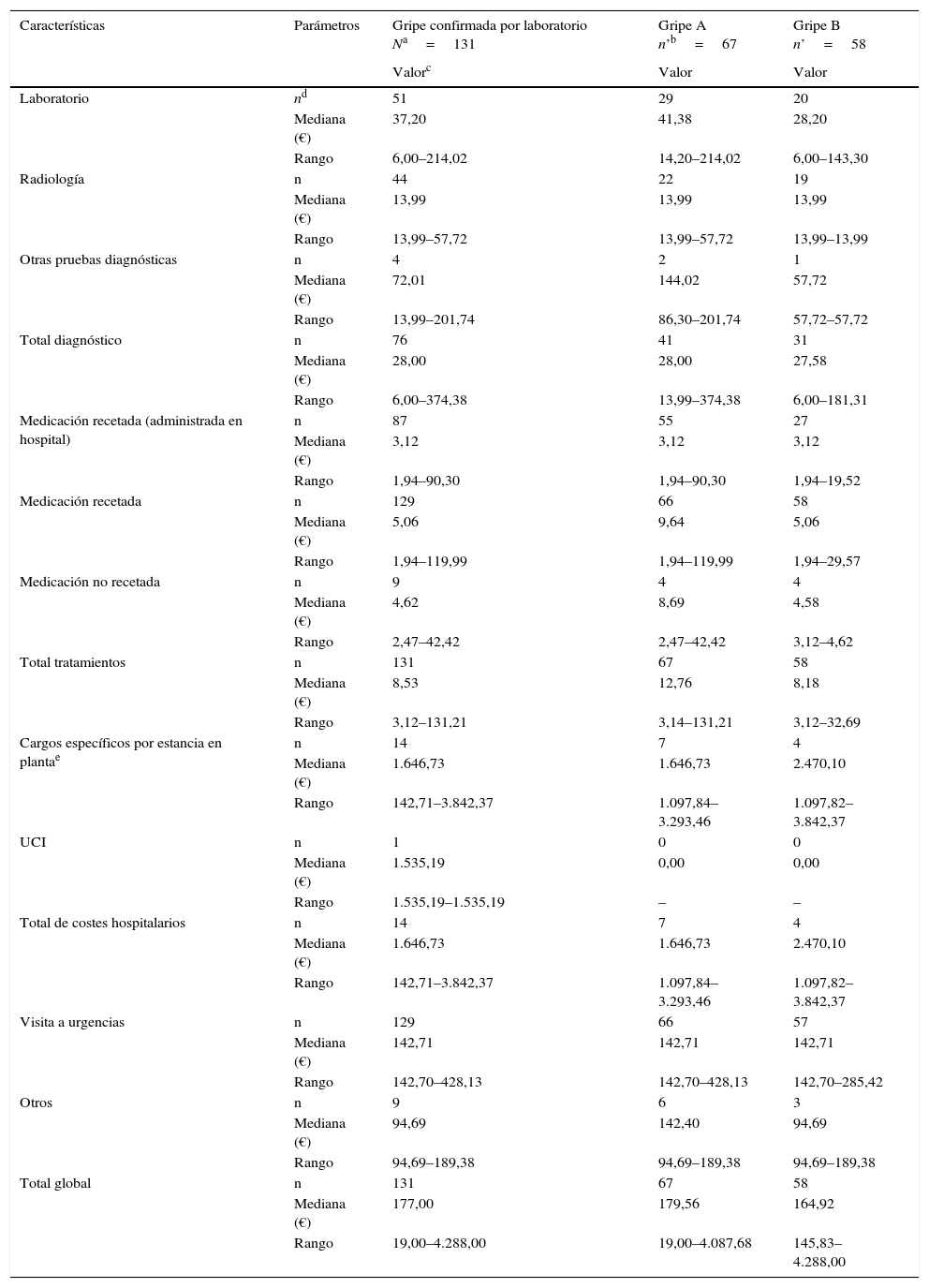
La mediana global de los costes médicos directos totales asociados con cada caso de gripe confirmada por laboratorio fue 177,00€ (rango: 19,00-4.288,00€). No se observaron diferencias significativas entre los costes médicos asociados con la gripe A (179,56€; rango: 19,00-4.087,68) y con la gripe B (164,92€; rango: 145,83-4.288,00) (tabla 3). El rango de los costes se asocia al rango del tratamiento recibido; la mayoría de los pacientes habían hecho una visita al servicio de urgencias (mediana 142,71€) y todos los pacientes recibieron medicamentos con o sin receta (mediana 8,53€). Alrededor del 60% de los pacientes incurrió en costes relacionados con el diagnóstico (mediana 28,00€), aproximadamente el 10% de los pacientes incurrió en costes considerables por la estancia en planta (mediana 1.646,73€) y un paciente incurrió en costes considerables por la estancia en la UCI (mediana 1.535,19€).
Costes médicos totales medianos (en euros) asociados con casos de gripe confirmada por laboratorio (N=131)
| Características | Parámetros | Gripe confirmada por laboratorio Na=131 | Gripe A n’b=67 | Gripe B n’=58 |
|---|---|---|---|---|
| Valorc | Valor | Valor | ||
| Laboratorio | nd | 51 | 29 | 20 |
| Mediana (€) | 37,20 | 41,38 | 28,20 | |
| Rango | 6,00–214,02 | 14,20–214,02 | 6,00–143,30 | |
| Radiología | n | 44 | 22 | 19 |
| Mediana (€) | 13,99 | 13,99 | 13,99 | |
| Rango | 13,99–57,72 | 13,99–57,72 | 13,99–13,99 | |
| Otras pruebas diagnósticas | n | 4 | 2 | 1 |
| Mediana (€) | 72,01 | 144,02 | 57,72 | |
| Rango | 13,99–201,74 | 86,30–201,74 | 57,72–57,72 | |
| Total diagnóstico | n | 76 | 41 | 31 |
| Mediana (€) | 28,00 | 28,00 | 27,58 | |
| Rango | 6,00–374,38 | 13,99–374,38 | 6,00–181,31 | |
| Medicación recetada (administrada en hospital) | n | 87 | 55 | 27 |
| Mediana (€) | 3,12 | 3,12 | 3,12 | |
| Rango | 1,94–90,30 | 1,94–90,30 | 1,94–19,52 | |
| Medicación recetada | n | 129 | 66 | 58 |
| Mediana (€) | 5,06 | 9,64 | 5,06 | |
| Rango | 1,94–119,99 | 1,94–119,99 | 1,94–29,57 | |
| Medicación no recetada | n | 9 | 4 | 4 |
| Mediana (€) | 4,62 | 8,69 | 4,58 | |
| Rango | 2,47–42,42 | 2,47–42,42 | 3,12–4,62 | |
| Total tratamientos | n | 131 | 67 | 58 |
| Mediana (€) | 8,53 | 12,76 | 8,18 | |
| Rango | 3,12–131,21 | 3,14–131,21 | 3,12–32,69 | |
| Cargos específicos por estancia en plantae | n | 14 | 7 | 4 |
| Mediana (€) | 1.646,73 | 1.646,73 | 2.470,10 | |
| Rango | 142,71–3.842,37 | 1.097,84–3.293,46 | 1.097,82–3.842,37 | |
| UCI | n | 1 | 0 | 0 |
| Mediana (€) | 1.535,19 | 0,00 | 0,00 | |
| Rango | 1.535,19–1.535,19 | – | – | |
| Total de costes hospitalarios | n | 14 | 7 | 4 |
| Mediana (€) | 1.646,73 | 1.646,73 | 2.470,10 | |
| Rango | 142,71–3.842,37 | 1.097,84–3.293,46 | 1.097,82–3.842,37 | |
| Visita a urgencias | n | 129 | 66 | 57 |
| Mediana (€) | 142,71 | 142,71 | 142,71 | |
| Rango | 142,70–428,13 | 142,70–428,13 | 142,70–285,42 | |
| Otros | n | 9 | 6 | 3 |
| Mediana (€) | 94,69 | 142,40 | 94,69 | |
| Rango | 94,69–189,38 | 94,69–189,38 | 94,69–189,38 | |
| Total global | n | 131 | 67 | 58 |
| Mediana (€) | 177,00 | 179,56 | 164,92 | |
| Rango | 19,00–4.288,00 | 19,00–4.087,68 | 145,83–4.288,00 |
No se tuvieron en cuenta los niños con un test rápido positivo para los tipos A y B.
UCI: unidad de cuidados intensivos.
La mayoría de los niños con gripe confirmada por laboratorio (71,8%: 94/131) faltaron al colegio o a la guardería. La ausencia media fue de 6,6 días (rango: 1-15). La ausencia escolar se registró en el 62,7% (42/67) de los niños con gripe A y en el 81,0% (47/58) de los niños con gripe B. La proporción de contactos domiciliarios con síntomas de tipo gripal, IRA y/o fiebre durante el período de estudio fue significativamente mayor en el grupo de niños con gripe confirmada por laboratorio (25,8%; IC del 95%: 21,2-31,1) que en el resto de los niños (17,5%; IC del 95%: 15,0-20,2; p=0,0032). La proporción de contactos domiciliarios que desarrollaron síndrome gripal fue mayor en los niños con gripe A que en los niños con gripe B (31,7%; IC del 95%: 25,0-39,3 versus 20,0%; IC del 95%: 14,3-27,1).
Entre los otros patógenos respiratorios que fueron aislados en el 28,9% de los casos (145/501), el detectado con mayor frecuencia fue el virus respiratorio sincitial (VRS), presente en 52 (10,4%) de los aislados (VRS A: 37; VRS B: 12; A+B: 3), seguido por rinovirus en 40 (8,0%) aislados y adenovirus en 30 (6,0%) aislados. Las edades medianas de los niños infectados con estos patógenos fueron 6,0 meses (VRS; rango: 0-178 meses), 15,5 meses (rinovirus, rango: 0-164 meses) y 25,0 meses (adenovirus, rango: 2-146 meses). Nueve sujetos con gripe confirmada por laboratorio (6,9%: 9/131) presentaban coinfección con otros virus. Cuatro patógenos (adenovirus, bocavirus, coronavirus y VRSA) se aislaron en combinación con el virus de la gripe tipo A, y 3(un coronavirus y 2VRSB) en combinación con el virus de la gripe de tipo B. Las manifestaciones clínicas más frecuentes en niños infectados con estos patógenos fueron tos, congestión nasal y rinorrea. La mayor incidencia de complicaciones correspondió a los sujetos con infección por VRS (71,2%: 37/52), en los que la bronquiolitis fue la complicación más importante (64,9%: 24/37). La tasa de ingreso también fue mayor en estos pacientes (54,0%: 20/37).
DiscusiónCada año, la mayor incidencia de la gripe se da en la población pediátrica. De hecho, se han publicado incidencias globales de hasta 49,4 casos por cada 1.000 menores de 15 años16. En nuestro hospital universitario, la gripe se confirmó por laboratorio en el 26,1% de los niños menores de 15 años que presentaron síntomas compatibles con infecciones de tipo gripal. Esto es consistente con Matias et al. (2011), que describieron que el 32,3% de los niños que presentaban IRA o fiebre aislada tuvieron resultados positivos para gripe13.
En la población pediátrica, la gripe da lugar a un número elevado de visitas a servicios de urgencias, ingresos hospitalarios y ausencias escolares, y representa una considerable carga económica anual. Así, en nuestro estudio en un centro hospitalario el coste médico total mediano asociado con la gripe fue de 177€ por caso. Una estrategia vacunal apropiada podría reducir dicha carga.
Como ya se había observado en España13, los niños en nuestro estudio con resultados positivos para gripe B eran de mayor edad que los niños con resultados positivos para gripe A (edad mediana: 66,5 meses versus 25,0 meses, respectivamente). Estos resultados son similares a los obtenidos en un estudio realizado en Finlandia entre 1980 y 1999, en el que las edades medias correspondientes fueron 4,2 años (gripe B) y 2,0 años (gripe A; p<0,001)17.
Entre los años 2001 y 2011, la proporción de cepas del tipo B entre todos los virus circulantes en Europa osciló entre el 1,0 y el 59,8% en cada temporada de gripe10. No obstante, según el informe más reciente del Centro Europeo para la Prevención y el Control de las Enfermedades, el virus de la gripe de tipo B predominó en España en 2013, y afectó al 18,6% de la población total española con una incidencia de 14,5 casos por cada 100.000 habitantes18. En el presente estudio, la proporción de niños con gripe confirmada por laboratorio infectados con el tipo B fue del 46,0%. Este resultado es similar al observado por Matias et al. en un estudio con diseño parecido, en el que el virus de la gripe de tipo B se detectó en el 47,7% de los casos de gripe confirmados por laboratorio en España (N=477)13. La proporción de casos correspondiente a cada uno de los tipos varía cada temporada y en función de la localización geográfica.
La vacunación es un método efectivo para prevenir la infección por el virus de la gripe y sus repercusiones, como por ejemplo sus complicaciones y su carga económica. En la temporada 2010-2011, la OMS recomendó la inclusión de las siguientes cepas en la vacuna trivalente para el hemisferio norte: 2virus de la gripe de tipo A (cepa análoga a A/California/7/2009 [H1N1]; y cepa análoga a A/Perth/16/2009 [H3N2]) y un virus de la gripe tipo B de linaje Victoria (cepa análoga a B/Brisbane/60/2008)19. En nuestro estudio, la mayoría de los casos de tipo B confirmados por laboratorio correspondieron a la cepa del linaje Victoria. Por lo tanto, el linaje del tipo B recomendado para la vacuna correspondió al tipo B circulante durante la temporada de gripe 2010-2011. No obstante, cualquiera de los 2linajes del tipo B (Victoria o Yamagata) puede predominar en cada temporada7,11, y aunque en nuestro estudio la proporción de cepas de linaje Yamagata (3,4%) fue muy baja, se ha observado una gran variabilidad entre temporadas. Por ejemplo, en la temporada 2006-2007 el 5,5% de las cepas de tipo B eran de linaje Yamagata, mientras que en la 2007-2008 el porcentaje ascendió al 40%20. Cabe destacar que la OMS recomendó el uso de vacunas tetravalentes (es decir, con cepas del tipo A y de ambos linajes del tipo B) para la temporada 2012-2013 en el hemisferio norte21.
Este estudio tiene limitaciones que podrían afectar a la interpretación de sus resultados. En primer lugar, todos los niños se reclutaron a través de un servicio de urgencias hospitalario, en donde los casos atendidos tienden a ser más graves y tratados mediante un número mayor de pruebas diagnósticas que los casos manejados en atención primaria. Por otro lado, la disponibilidad de test diagnósticos rápidos implica una reducción en la proporción de niños que presentan fiebre aislada y que acaban siendo ingresados, en comparación con cuando los test no están disponibles. Es posible que los síntomas registrados durante las entrevistas de seguimiento realizadas por teléfono fueran infradeclarados. Por último, el estudio se realizó durante una única temporada de gripe y, por lo tanto, sus hallazgos pueden infravalorar o sobrevalorar la carga de enfermedad de la gripe en otras temporadas. Además, como las proporciones de los virus de la gripe de tipo A y B y de los distintos linajes pueden variar, sería de interés explorar la situación durante varias temporadas.
Resumiendo, la gripe resulta en una carga de enfermedad y costes médicos asociados considerables en la población pediátrica todos los años. Los casos de gripe causados por cepas de tipo A y por cepas de tipo B parecen ocasionar una carga similar en términos de costes incurridos en servicios de urgencias e ingresos hospitalarios, que podría aminorarse con una estrategia vacunal apropiada. Las proporciones de los virus de la gripe de tipo A y de tipo B en la temporada 2010-2011 fueron similares, y en nuestro estudio se detectaron los 2linajes del tipo B (Victoria y Yamagata) en los casos de gripe confirmada por laboratorio, aunque con un porcentaje bajo del linaje Yamagata. En la temporada de gripe correspondiente a este estudio, el ajuste entre las cepas vacunales y las cepas circulantes fue adecuado, ya que la vacuna protegía de cepas del tipo A y de cepas del tipo B de linaje Victoria. Sin embargo, en temporadas en las que hay un desajuste entre cepas vacunales y circulantes es probable que la vacuna ofrezca una protección menor. Teniendo en cuenta la carga de enfermedad de la gripe observada en este estudio, la administración a niños menores de 15 años de vacunas que contengan cepas del tipo A y de los linajes del tipo B podría contribuir a reducir la carga global de enfermedad. Dada la dificultad de predecir qué cepas virales van a estar involucradas en temporadas de gripe futuras, el uso de vacunas tetravalentes, que protegen de cepas de tipo B de ambos linajes además de proteger de cepas de tipo A, proporcionaría la protección más amplia posible.
FinanciaciónGlaxoSmithKline Biologicals promovió y financió la realización del estudio (NCT01592799), el análisis de datos, y la elaboración y publicación del manuscrito.
Autoría/colaboradoresTodos los autores de este artículo de investigación han participado directamente en el diseño, implementación o análisis, e interpretación del estudio, y han revisado y aprobado la versión final remitida para publicación. Todos los autores tuvieron acceso irrestricto a los datos y asumen la responsabilidad de la integridad y la precisión del análisis. Todos los autores contribuyeron en igual medida al desarrollo del manuscrito.
Conflicto de interesesGarcía-Martínez J.A., McCoig C., García-Corbeira P., Devadiga R. y Tafalla M. son empleados del grupo empresarial GSK. McCoig C., García-Corbeira P. y Tafalla M. han recibido acciones del grupo empresarial GSK como parte de su remuneración laboral. Arístegui J. ha recibido honorarios del grupo empresarial GSK como investigador en el estudio, como consultor en un Advisory Board de vacunas pediátricas y para cubrir gastos de transporte, alojamiento y participación como ponente en eventos científicos. Garrote E. y Rementería J. declaran pagos a sus instituciones respectivas para la realización de estudios por el grupo empresarial GSK. Ortiz-Lana N. declara no tener conflicto de intereses.
Queremos expresar nuestro agradecimiento a los participantes del estudio, a todos los investigadores, enfermeras y al resto del equipo por su diversa contribución al estudio. A Harshith Bhat (GSK) por su contribución a la escritura del manuscrito, a Jérémie Dedessus le Moutier (Business & Decision Life Sciences en representación de GSK) por la coordinación del manuscrito y el asesoramiento técnico durante su elaboración, a Roeland Van Kerckhoven (Keyrus Biopharma en representación de GSK) y a Grégory Leroux (Business & Decision Life Sciences en representación de GSK) por la coordinación del manuscrito, a Preethi Govindarajan (GSK) por la ayuda en el formateo y a Julia Donnelly (manager de publicación freelance en representación de GSK) por la edición del texto.
Presentación como póster en el VII Congreso de la Asociación Española de Vacunología, del 25 al 27 de noviembre de 2013, Cáceres (España).