Ivacaftor es un potenciador de la proteína reguladora de la conductancia transmembrana de la fibrosis quística (CFTR) que ha demostrado en ensayos clínicos mejoría del estado nutricional y la función pulmonar de pacientes con fibrosis quística con mutación G551D. El objetivo de este estudio es describir la evolución en la vida real de niños tratados con ivacaftor.
MétodosSe describe la evolución en vida real de 4 niños con fibrosis quística con genotipo F508del/G551D comparando los datos durante el tratamiento con ivacaftor respecto a la situación basal y al año previo al tratamiento.
ResultadosSe analizan 4 niños de entre 6 y 14 años, incluyendo uno con diagnóstico reciente de fibrosis quística y otro con infección persistente por Mycobacterium abscessus (M. abscessus) y aspergilosis broncopulmonar alérgica (ABPA) recurrente. El volumen espiratorio forzado en el primer segundo (FEV1) basal fue del 58,5-81,8% del predicho y recibieron ivacaftor 24 meses de media (rango 12-30 meses). Todos los pacientes tuvieron una mejoría significativa y mantenida de la función pulmonar. Respecto a la situación basal, el z-score del peso mejoró 1,53 puntos y el z-score del índice de masa corporal (IMC) 1,6 puntos. Comparado con el año previo al tratamiento con ivacaftor, disminuyeron la frecuencia de aislamientos de Pseudomonas aeruginosa (P. aeruginosa) (−0,4/paciente/año) y el número de exacerbaciones respiratorias (−1,8/paciente/año). La dosis de lipasa ajustada por kilo disminuyó progresivamente en todos los pacientes. Un paciente resolvió durante el tratamiento la infección por M. abscessus y la ABPA.
ConclusionesLos niños con fibrosis quística y mutación F508del/G551D tratados con ivacaftor mostraron en la vida real mejoría de la función pulmonar, el estado nutricional, las exacerbaciones respiratorias, los aislamientos de P. aeruginosa y la dosis de enzimas pancreáticas.
Ivacaftor is a cystic fibrosis transmembrane conductance regulator (CFTR) potentiator that has been shown to improve the nutritional status and lung function of cystic fibrosis patients with the G551D mutation in clinical trials. The objective of this study was to describe the real-world progress of children receiving ivacaftor.
MethodsWe describe the real-world progress of four children with cystic fibrosis and the F508del/G551D genotype comparing data during ivacaftor treatment with baseline and with the year before commencing treatment.
ResultsOur sample comprised 4 children aged between 6 and 14 years and including one with a recent diagnosis of CF and other with persistent Mycobacterium abscessus (M. abscessus) and recurrent allergic bronchopulmonary aspergillosis. The baseline FEV1 was 58.5% to 81.8% of the predicted value, and ivacaftor was taken for a mean 24 months (range, 12-30 months). All patients experienced a significant and sustained improvement in lung function. Compared to baseline, the weight z-score improved by 1.53 points, and the BMI z-score by 1.6 points. Compared to the year before starting ivacaftor, the frequency of Pseudomonas aeruginosa (P. aeruginosa) isolates decreased (−0.4/patient/year), as did the number of respiratory exacerbations (−1.8/patient/year). The weight-adjusted dose of lipase per kilogram decreased progressively in all patients. In 1 patient, a previously persistent M. abscessus infection and recurrent allergic bronchopulmonary aspergillosis resolved during treatment.
ConclusionsChildren with cystic fibrosis and the F508del/G551D genotype receiving treatment with ivacaftor experienced a real-world improvement in lung function, nutritional status, respiratory exacerbations, isolation of P. aeruginosa, and dose of pancreatic enzymes.
La fibrosis quística (FQ) es la enfermedad hereditaria autosómica recesiva con pronóstico vital acortado más común en la población caucásica. Tiene una incidencia que generalmente oscila entre 1/2000 y 1/6000 recién nacidos vivos1. La enfermedad es causada por una mutación en el gen que codifica la proteína reguladora de la conductabilidad transmembrana de la fibrosis quística (CFTR), que regula el canal de transporte iónico dependiente de CFTR. Se han descrito más de 2000 mutaciones del CFTR, siendo la G551D (Gly551Asp, c.1652G>A) responsable de hasta el 4% de los pacientes a nivel mundial2,3. Esta mutación conlleva una disminución significativa en la apertura del canal CFTR, lo que a su vez provoca una reducción considerable del transporte de cloro en la superficie de las células epiteliales4.
El ivacaftor es un potenciador de la proteína CFTR que aumenta el transporte de cloro al incrementar la probabilidad de la apertura del canal CFTR en pacientes con mutaciones de clase III como la G551D5,6. Dos ensayos de fase III han comparado la utilidad del ivacaftor (150mg/12h) respecto a placebo durante 48 semanas en niños mayores de 12 años y adultos (STRIVE)7 y en niños de 6 a 11 años (ENVISION)8. En ambos estudios, el grupo tratado con ivacaftor experimentó mejoras significativas en el FEV1, la concentración de cloro en sudor y el peso corporal. Un estudio de extensión posterior (PERSIST) con seguimiento de pacientes tratados con ivacaftor durante 96 semanas adicionales confirmó la mejoría clínica y no encontró efectos adversos significativos9.
No obstante, estos estudios tenían las limitaciones características de los ensayos clínicos. Se excluyó a pacientes con enfermedades o aislamiento de microorganismos que pudieran actuar como factores de confusión, a pacientes con exacerbaciones o cambios de tratamiento en las semanas precedentes, y a pacientes previamente tratados con fármacos inhibidores o inductores del citocromo P450 3A.
El objetivo del presente estudio fue analizar la evolución de niños tratados con ivacaftor 2,5 años después de su comercialización en el Reino Unido.
MétodosEl estudio se realizó en el Royal London Hospital, un centro de referencia para la FQ en el este de Londres que maneja más de 100 niños con FQ. Durante el seguimiento, se recogieron datos sobre medidas antropométricas, la dosis de enzimas pancreáticas, los ciclos de antibióticos, la frecuencia del aislamiento de microorganismos y la función pulmonar, así como muestras clínicas (esputo, frotis faríngeo). En los pacientes tratados con ivacaftor también se realizaron determinaciones seriadas de transaminasas y cloro en sudor antes de iniciarse el tratamiento y a las 6 semanas, 6 meses, un año y 2 años de tratamiento. Para calcular los valores de referencia sobre el predicho del FEV1 (FEV1%), la capacidad vital forzada (FVC%) y los mesoflujos (FEF25%-75%) se utilizaron las ecuaciones propuestas por la Global Lung Function Initiative. El z-score del peso, talla e IMC se calculó con las tablas publicadas por la Organización Mundial de la Salud.
Se incluyeron todos los pacientes menores de 17 años con una o más mutaciones G551D tratados con ivacaftor entre enero de 2013 y junio de 2015, independientemente de la duración del tratamiento. La dosis administrada fue de 150mg/12h una vez al día, o dos veces por semana en caso de tratamiento concomitante con fármacos inhibidores de citocromo P450 3A.
Se incluyeron todos los datos recogidos durante el tratamiento con ivacaftor y los del año previo cuando estaban disponibles. El análisis se basó en los valores basales y los últimos valores obtenidos durante el tratamiento con ivacaftor. También se calcularon los valores medios de los datos recogidos durante el tratamiento, agrupados en intervalos de 6 meses. Las comparaciones se realizaron con el valor basal (definido como el valor registrado más recientemente antes de administrarse la primera dosis de ivacaftor) o el primer valor disponible, así como con el valor medio del año previo al inicio del tratamiento.
El análisis estadístico se realizó con el software SPSS 19.0. El nivel de significación estadística se estableció en p <0,05. La media y desviación estándar (DE) de los datos agrupados a intervalos de 6 meses y la de los obtenidos el año previo al tratamiento se compararon mediante análisis de varianza.
ResultadosSe incluyeron 4 pacientes de 6 a 14 años de edad que habían recibido ivacaftor durante una media de 24 meses (12 meses, 24 meses, 30 meses, 30 meses). Todos eran heterocigotos F508del/G551D y tenían insuficiencia pancreática (tabla 1). En dos pacientes se inició tratamiento con ivacaftor cuando fue autorizado en el Reino Unido en enero de 2013; el paciente 3 tuvo que esperar hasta que cumplió los 6 años en mayo de 2013. El estado clínico de los pacientes al inicio de ivacaftor era muy variado. El paciente 1 había sido diagnosticado de aspergilosis broncopulmonar alérgica (ABPA) con varias recaídas en los 5 años anteriores, así como en los primeros meses de tratamiento con ivacaftor, que se trataron repetidamente con prednisolona junto con itraconazol o voriconazol. Este paciente había también sido diagnosticado de enfermedad pulmonar por M. abscessus 7 meses antes de iniciarse el tratamiento con ivacaftor, con aislamiento recurrente de M. abscessus asociado a deterioro de la función pulmonar y hallazgos patológicos en la tomografía computarizada (TC). Había recibido tratamiento de erradicación con antibioterapia intensiva intravenosa, nebulizada y oral conforme a las recomendaciones vigentes. No obstante, el paciente continuó teniendo cultivos positivos a M. abscessus antes de iniciarse el tratamiento con ivacaftor a pesar de la terapia de mantenimiento nebulizada y oral. En los primeros meses, el paciente recibió dosis reducidas de ivacaftor dos veces por semana debido al tratamiento concomitante con claritromicina y voriconazol. Durante el tratamiento con ivacaftor, se negativizaron los cultivos de M. abscessus y no tuvo más episodios de ABPA. A los 6 meses se interrumpió el tratamiento con claritromicina y voriconazol y el paciente comenzó a recibir la pauta estándar de ivacaftor con dosis diarias. A la finalización del estudio, el paciente llevaba 21 meses sin presentar M. abscessus ni ABPA.
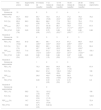
Características clínicas de los pacientes
| Paciente 1 | Paciente 2 | Paciente 3 | Paciente 4 | |
|---|---|---|---|---|
| Sexo | Varón | Varón | Mujer | Mujer |
| Edad al diagnóstico | 2 años | 2 meses | 2 años | 13 años |
| Cloro en sudor al diagnóstico, mmol/l | 126 | 96 | 99 | 90 |
| Genotipo | F508del/G551D | F508del/G551D | F508del/G551D | F508del/G551D |
| Insuficiencia pancreática | Sí | Sí | Sí | Sí |
| Edad al inicio de ivacaftor | 10 años | 7 años | 6 años | 14 años |
| Duración de tratamiento con ivacaftor | 30 meses | 30 meses | 24 meses | 12 meses |
| Microrganismos detectados al inicio de ivacaftor | Mycobacterium abscessus | No | No | No |
| Número de aislamientos de Pseudomonas aeruginosa en el año previo al tratamiento con ivacaftor | 1 | 0 | 1 | Sin datos |
En el caso de la paciente 3, no se dispuso de datos fiables de espirometría hasta los 6 meses de tratamiento con ivacaftor. La paciente 4 se diagnosticó de fibrosis quística a los 13 años y comenzó tratamiento con ivacaftor junto con el inicio de la terapia multidisciplinar de la enfermedad y un ciclo de antibioterapia intravenosa. En la actualidad los 4 pacientes continúan recibiendo tratamiento con ivacaftor.
La función pulmonar —y especialmente el FEV1 y los mesoflujos— mejoró en los 4 pacientes, y esta mejora se mantuvo durante todo el seguimiento (tabla 2). Los valores basales de FEV1% oscilaron entre el 58,5 y el 81,8%. Al comparar los últimos valores registrados durante el tratamiento con los valores basales (en el caso del paciente 3, el primer valor fiable), se observó una mejoría global del FEV1% de 25,72 puntos porcentuales. Cuando comparamos los valores finales con los valores medios del año anterior a iniciar el tratamiento en los pacientes 1 y 2, observamos una mejoría global del FEV1% de 18,85 puntos porcentuales. Cuando se incluyeron en el análisis todos los valores de la función pulmonar obtenidos durante el tratamiento, la mejoría global en el FEV1% fue de 11,96 puntos porcentuales respecto al valor basal.
Parámetros de función pulmonar antes de y durante el tratamiento con ivacaftor
| Año previo | Espirometría basal | 0-6 meses de ivacaftor | 7-12 meses de ivacaftor | 13-18 meses de ivacaftor | 19-24 meses de ivacaftor | 25-30 meses de ivacaftor | Última espirometría | |
|---|---|---|---|---|---|---|---|---|
| Paciente 1 | ||||||||
| Número de espirometrías | 10 | 9 | 5 | 2 | 4 | 4 | ||
| FEV1 (%) | 64,7 (10,8) | 63,9 | 60,7 (5,6) | 70,4 (15,6) | 81,3 (4,0)* | 77,2 (2,0)* | 76,8 (1,5)* | 78,2 |
| FVC (%) | 85,9 (5,6) | 86,3 | 88,4 (6,6) | 86,2 (7,4) | 77,8 (5,8) | 78,0 (3,3)* | 76,4 (2,0)* | 77,5 |
| FEF25-50 (%) | 29,7 (14,1) | 34,2 | 27,1 (6,6) | 45,18 (30,3) | 86,1 (4,1)*** | 74,9 (11,1)*** | 77,0 (8,9)*** | 87,5 |
| FEV1/FVC | 0,64 (7,8) | 0,63 | 0,59 (6,8) | 0,70 (13,7) | 0,89 (2,2)*** | 0,85 (5,5)*** | 0,86 (1,7)*** | 0,86 |
| Paciente 2 | ||||||||
| Número de espirometrías | 10 | 2 | 3 | 3 | 2 | 3 | ||
| FEV1 (%) | 69,6 (10,2) | 81,8 | 88,1 (3,5)** | 89,1 (0,4)** | 81,4 (5,0)* | 87,3 (2,6)** | 89,8 (3,5)** | 93,8 |
| FVC (%) | 74,1 (7,5) | 85 | 89,2 (0)** | 89,1 (1,8)** | 82,5 (5,0)* | 87,0 (3,5)* | 87,8 (2,9)** | 90,4 |
| FEF25-50 (%) | 55,6 (19,7) | 71,4 | 80,6 (14,1)* | 91,3 (3,5)** | 72,5 (4,9)* | 84,4 (4,7)** | 95,4 (13,0)*** | 100,1 |
| FEV1/FVC | 0,83 (5,4) | 0,85 | 0,88 (3,7) | 0,88 (1,5) | 0,86 (0,8) | 0,87 (1,1) | 0,88 (2,926) | 0,90 |
| Paciente 3 | ||||||||
| Número de espirometrías | 1 | 2 | 3 | 3 | ||||
| FEV1 (%) | 70,3 | 64,6 (2,4) | 84,8 (4,3) | 84,5 (11,2) | 97,4 | |||
| FVC (%) | 92,2 | 81,2 (0,49) | 106,3 (5,6) | 105,2 (9,2) | 108 | |||
| FEF25-50 (%) | 26,6 | 40,0 (6,2) | 49,63 (15,6) | 50,9 (21,9) | 73,5 | |||
| FEV1/FVC | 0,69 | 0,72 (2,8) | 0,72 (5,6) | 0,72 (9,7) | 0,8 | |||
| Paciente 4 | ||||||||
| Número de espirometrías | 2 | 3 | ||||||
| FEV1 (%) | 58,5 | 75,1 (7,2) | 101,2 (5,9) | 108 | ||||
| FVC (%) | 84,2 | 89,4 (0,4) | 110 (11,3) | 122,9 | ||||
| FEF25-50 (%) | 14,7 | 41,4 (8,7) | 72,4 (15,4) | 72,4 | ||||
| FEV1/FVC | 0,62 | 0,75 (6,9) | 0,82 (4) | 0,78 | ||||
FEF: flujo espiratorio; FEV1: volumen espiratorio forzado en el primer segundo; FVC: capacidad vital forzada.
Datos expresados como frecuencias absolutas o media (DE).
La significación estadística se calculó con respecto al año previo a iniciarse el tratamiento:
La mejoría global de los mesoflujos al final del seguimiento fue de 46,65 puntos porcentuales respecto a los valores basales. La FVC% mejoró en 3 de los pacientes durante el tratamiento, mientras que el cociente FEV1/FVC mejoró significativamente en uno. La mejoría global de la FVC% al final del seguimiento fue de 12,75 puntos porcentuales con respecto al valor basal.
El estado nutricional, evaluado mediante el z-score del IMC, mejoró progresivamente en todos los pacientes durante el tratamiento con ivacaftor (tabla 3). La mejoría absoluta de la puntuación z-score en la última evaluación antropométrica durante el tratamiento en comparación con los valores basales fue de 1,6 puntos. Cuando agrupamos los valores de los pacientes 1, 2 y 3 al final del seguimiento y los comparamos con los valores del año previo al inicio del tratamiento, observamos un aumento de 0,50 puntos en el z-score medio. Cuando se incluyeron todos los valores registrados en los pacientes 1-3 durante el tratamiento, encontramos una mejoría similar en el z-score (1,37 puntos con respecto al valor basal, y 0,54 con respecto al año previo).
Datos nutricionales y dosis de lipasa antes del inicio y durante el tratamiento con ivacaftor
| Año previo | Valor basal | 0-6 meses de ivacaftor | 7-12 meses de ivacaftor | 13-18 meses de ivacaftor | 19-24 meses de ivacaftor | 25-30 meses de ivacaftor | Último | |
|---|---|---|---|---|---|---|---|---|
| Paciente 1 | ||||||||
| Peso, z-score | 0,85 (2,44) | 0,50 | 0,59 (0,21) | 0,67 (0,46) | 1,27 (0,02) | 1,33 | 1,20 (0,11)* | 1,11 |
| IMC, z-score | 0,79 (0,07) | 0,68 | 0,46 (0,31) | 0,73 (0,64) | 1,5 (0,04)*** | 1,5 | 1,4 (0,14)** | 1,29 |
| Talla, z-score | 0,61 (0,41) | 0,04 | 0,51 (0,05) | 0,30 (0,06) | 0,41 (0) | 0,52 | 0,43 (0,06) | 0,35 |
| Lipasa/kg | 5416,7 | 6157,6 (304) | 5826,4 (273,1) | 4938,1 (118,4) | 3813,1 (502,3) | 3049,7 (231,3) | 3295,7 | |
| Paciente 2 | ||||||||
| Peso, z-score | –0,23 (0,13) | –0,16 | –0,12 (0,07) | 0,2 (0,04)* | 0,11 (0,04) | 0,08 (0,23) | 0,32 (0,13)** | 0,41 |
| IMC, z-score | 0,34 (0,24) | 0,60 | 0,58 (0,10) | 0,9 (0,28) | 0,76 (0,28) | 0,65 (0,22) | 0,88 (0,18) | 1,01 |
| Talla, z-score | –0,76 (0,16) | –0,98 | –0,91 (0,01) | –0,81 (0,05) | –0,80 (0,01) | –0,71 (0,12) | –0,62 (0,02) | –0,64 |
| Lipasa/kg | 11688,3 | 8462,3 (760,5) | 7577,9 (43,5) | 7187 (251,7) | 6849,7 (504,8) | 5371,4(260,4) | 5187,3 | |
| Paciente 3 | ||||||||
| Peso, z-score | –1,69 (0,32) | –2,15 | –1,22 (0,04) | –0,97 (0,01)* | –0,97 (0,04)* | –1,05 (0,06)* | –1,1 | |
| IMC, z-score | –0,12 (2,39) | –0,49 | 0,56 (0,01)* | 0,69 (0,01)** | 0,57 (0,25)* | 0,34 (0,12) | 0,21 | |
| Talla, z-score | –2,16 (0,22) | –2,41 | –2,3 (0,03) | –2,18 (0,01) | –2,09 (0,20) | –2,01 (0,04) | –1,97 | |
| Lipasa/kg | 13312,7 | 13003,2 (517,3) | 12310,8 (5097,3) | 12292,5 (1783,3) | 10294,8 (225,9) | 10135,1 | ||
| Paciente 4 | ||||||||
| Peso, z-score | –3,31 | –0,72 (0,84) | 0,43 (0,15) | 0,6 | ||||
| IMC, z-score | –3,0 | 0,25 (0,91) | 1,38 (0,39) | 1,7 | ||||
| Talla, z-score | –1,74 | –1,62 (0,09) | –1,20 (0,1) | –1,20 | ||||
| Lipasa/kg | 4889,97 | 3618,31 (457,1) | 3252,03 | |||||
IMC: índice de masa corporal.
Datos expresados como frecuencias absolutas o media (DE).
La significación estadística se calculó con respecto al año previo a iniciarse el tratamiento:
También se observaron mejorías en el peso corporal que se mantuvieron constantes durante el seguimiento. El z-score del peso al final del seguimiento mejoró 1,53 puntos respecto al basal y 0,50 puntos respecto al año previo al tratamiento en los pacientes 1-3. La mejoría en el z-score de la talla fue mucho más modesta, con un aumento al final del seguimiento de 0,41 puntos respecto al basal, y de 0,01 puntos con respecto al año previo en los pacientes 1-3.
La dosis de lipasa por kilogramo de peso corporal se redujo significativamente y de manera gradual en los 4 pacientes (tabla 3). Cuando analizamos conjuntamente las dosis de los pacientes 1-3, encontramos una reducción del 39,5% al final del seguimiento en comparación con el momento inicial. Asimismo, la dosis total de enzimas pancreáticas se redujo en 2 pacientes.
Antes de iniciarse el tratamiento con ivacaftor, la concentración de cloro en sudor era ≥ 90 mEq/l en todos los pacientes. Este valor había disminuido significativamente cuando se hizo el primer control a las 6 semanas. En los 3 pacientes que habían sido tratados con ivacaftor durante 2 o más años, la última determinación reveló valores de menos de 40 mEq/l (tabla 4). La reducción media al final del seguimiento fue de –58 mEq/l.
El número de aislamientos de P. aeruginosa de muestras de secreciones respiratorias fue bajo en general, y disminuyó ligeramente con respecto al año previo a la iniciación de ivacaftor en los pacientes 1-3 (ninguno tuvo una infección crónica). El número medio de aislamientos de P. aeruginosa fue de 0,67 por paciente/año durante el año previo al tratamiento (pacientes 1-3) y de 0,27 por paciente/año durante el tratamiento. El número de exacerbaciones respiratorias que requirieron antibioterapia también disminuyó en los pacientes 1-3 con respecto al año previo, tanto para la antibioterapia oral (3 vs. 1,7 ciclos por paciente/año) como para la intravenosa (uno vs. 0,5 ciclos por paciente/año).
Se observó mejoría radiológica en 3 pacientes. En el paciente 1, la TC mostró una mejoría significativa, aunque la comparación se realizó al finalizarse el tratamiento para la infección por M. abscessus y la ABPA. Según el informe del radiólogo, la radiografía del paciente 2 mostró resolución del engrosamiento peribronquial en la base del pulmón izquierdo en comparación con la radiografía previa. La paciente 4 presentaba bronquiectasias significativas al diagnóstico, que mejoraron considerablemente durante el tratamiento.
El único efecto adverso que se observó en el estudio fue una elevación leve y transitoria en los niveles séricos de transaminasas en el paciente 1 (AST, 43 UI/ml; ALT, 42 UI/ml). No se observaron problemas de adherencia.
DiscusiónEn este estudio de la evolución en vida real de 4 pacientes con FQ y genotipo F508del/G551D, el uso de ivacaftor se asoció a mejorías en la función pulmonar, el estado nutricional, la dosis de enzimas pancreáticas, el cloro en sudor, el número de aislamientos de P. aeruginosa y el uso de antibióticos. Aunque estudios previos sobre el uso de ivacaftor ya habían reportado mejorías en muchos de estos parámetros, los estudios con datos en la vida real ofrecen un valor añadido de efectividad. La practica clínica difiere significativamente de los protocolos de ensayos clínicos que además excluyen a muchos pacientes por no cumplir los criterios de inclusión. Así, 3 de los 4 pacientes en el presente estudio no están representados en los ensayos clínicos. El paciente 1 fue tratado con inhibidores del citocromo P450 3A durante 9 meses, lo que era motivo de exclusión en los ensayos clínicos de ivacaftor8. En el caso de la paciente 3, de 6 años de edad, no se dispuso de datos espirométricos fiables hasta los 6 meses de tratamiento. La paciente 4 recibió un diagnóstico tardío y comenzó tratamiento con ivacaftor a la vez que iniciaba el tratamiento multidisciplinar de la fibrosis quística.
En el presente estudio se analizaron todos los datos de la función pulmonar y antropometría registrados durante el tratamiento con ivacaftor y también durante el año previo a su iniciación. En los ensayos clínicos, el protocolo requiere una evaluación basal de la función pulmonar, cuyos resultados se comparan con los obtenidos tras un período preestablecido, normalmente a intervalos de 8-12 semanas. Sin embargo, los pacientes con FQ experimentan fluctuaciones frecuentes en la función pulmonar y el peso corporal debido a las exacerbaciones respiratorias y complicaciones diversas. En este sentido, consideramos que la inclusión de todos los datos recogidos durante el período de estudio añade valor en lo concerniente a la efectividad real de ivacaftor. Además, la comparación con valores del año previo puede incrementar aún más la precisión del análisis, ya que es posible que el estado del paciente al inicio del tratamiento no refleje su situación en los meses previos.
La mejoría en el FEV1% con respecto al valor basal (25,72 puntos porcentuales) fue mayor que la observada en estudios previos (10,6 y 12,5 puntos a las 24 semanas y 10,5 y 10 puntos a las 48 semanas8,9). Tres de nuestros pacientes tenían un FEV1% basal ≤70,3%, mientras que la mayoría de los pacientes en los estudios ENVISION y PERSIST tenían valores basales de FEV1% > 70%. En el estudio ENVISION los pacientes con mayor gravedad, expresada por un menor cociente FEV1/FVC (≤ 0,748) o FEV1% basal (50-80%), fueron también los que mostraron mayor efecto del tratamiento, con una mejoría del FEV1% de alrededor de 20 puntos8. Además, el mayor incremento en el FEV1% en nuestro estudio se registró en la paciente 4 (49,5 puntos), en la que se inició el programa de manejo multidisciplinar (incluyendo antibioterapia intravenosa) cuando comenzó el tratamiento con ivacaftor, por lo que parte de la mejoría observada en este caso podría deberse al manejo general de la FQ. No obstante, la mejoría observada en su TC superó las expectativas. Cuando comparamos los resultados de los pacientes 1 y 2 con el valor medio del año previo a la iniciación de ivacaftor, encontramos un aumento de 18,85 puntos porcentuales en el FEV1%, lo que concuerda más con los resultados de los ensayos clínicos. La mejoría obtenida con el ivacaftor podría alterar el deterioro progresivo de la función pulmonar característico de la historia natural de la FQ10.
La mejoría en los mesoflujos también fue mayor que la descrita en los ensayos clínicos, probablemente por las razones ya mencionadas en relación con el FEV1, mientras que la mejoría en la FVC fue modesta. El incremento en el cociente FEV1/FVC observado en el paciente 1 probablemente se debió a la mejoría de la obstrucción bronquial tras el tratamiento de la ABPA.
El estado nutricional, evaluado por medio del z-score del IMC, mejoró rápidamente y de manera sostenida en todos los pacientes durante el tratamiento. La mejoría global de 1,6 puntos se debe en parte a la mejoría de 4,7 puntos en la paciente 4, a la que también contribuyó el manejo multidisciplinar de la FQ y el inicio de la terapia con enzimas pancreáticas; al excluir a esta paciente del análisis, la mejoría global fue de 0,57 puntos con respecto al z-score basal y de 0,50 puntos con respecto al año previo. Estos hallazgos fueron similares a los del estudio ENVISION a las 48 semanas de tratamiento (en comparación con el grupo de control)8. Los cambios de peso siguieron un patrón similar al de los cambios del IMC. Sin embargo, el incremento en el z-score de la talla fue muy modesto, aunque es posible que se hubieran registrado diferencias mayores si el tratamiento hubiera durado más o se hubiera iniciado a edades más tempranas.
La dosis de lipasa ajustada por peso se redujo progresivamente en todos los pacientes durante el tratamiento, aunque el ajuste se basó en datos clínicos sin monitorización exhaustiva de la función pancreática. La mejoría observada podría haber sido sesgada por la ganancia de peso, aunque en 2 pacientes también hubo una reducción significativa en la dosis total. Es posible que este efecto esté asociado a la normalización del pH gastrointestinal resultante del tratamiento con ivacaftor11 o al aumento en la permeabilidad de los conductos pancreáticos. Cabe mencionar que se observó una mejoría significativa en la paciente 4 a pesar del inicio tardío del tratamiento, lo que sugiere la posibilidad de que los cambios observados en la función pancreática no sean completamente irreversibles.
La comparación de los datos del seguimiento con los del año previo mostró que los aislamientos de P. aeruginosa fueron menos frecuentes durante el tratamiento, lo que probablemente se deba a la mejoría en el aclaramiento mucociliar producida por el ivacaftor11,12. También se redujo la necesidad de antibioterapia oral e intravenosa, un hallazgo importante, pues las exacerbaciones tienen un impacto significativo en la calidad de vida13 y se asocian a un deterioro de la función pulmonar que en ocasiones no retorna a los valores previos14.
Otros estudios han descrito efectos adicionales del ivacaftor en la sinusitis, la secreción de insulina, la esteatosis hepática y la enfermedad pulmonar grave15–20. El ivacaftor también se ha mostrado eficaz en el tratamiento de otras mutaciones de clase III y de pacientes de 18 años de edad o mayores con la mutación de clase IV Arg117His-CFTR21–23.
Se observó mejoría radiológica en 3 pacientes durante el tratamiento. En un paciente se resolvió la infección por M. abscessus con remisión de ABPA recurrente, lo que pudo haber contribuido a la mejoría radiológica. El ivacaftor reduce la inflamación de la vía aérea y aumenta el aclaramiento mucociliar, por lo que los cambios en pruebas de imagen podrían utilizarse como marcadores objetivos para verificar la respuesta al tratamiento de cada paciente24–26.
El ivacaftor fue bien tolerado y no se asociaron efectos adversos a su uso. Los estudios postautorización son esenciales para garantizar la seguridad de los fármacos y detectar los efectos adversos que pueden surgir a largo plazo en situaciones clínicas diversas y con el uso concomitante de otros fármacos con posibles interacciones. Recientemente se confirmó la seguridad de ivacaftor en niños de 2 a 5 años, aunque la elevación de los niveles de transaminasas fue un hallazgo frecuente27.
La muestra de nuestro estudio solo incluyó 4 pacientes, y uno recibió únicamente 12 meses de tratamiento. Además, es posible que la mejoría observada en la función pulmonar y otras variables no se debiera exclusivamente al tratamiento con ivacaftor, sino también al inicio del manejo multidisciplinar de la FQ (paciente 4) o a la resolución de una infección por M. abscessus asociada a ABPA (paciente 1). En cualquier caso, ambos pacientes siguieron mejorando a lo largo del seguimiento. El objetivo de nuestro estudio no era obtener medidas específicas de mejora, que ya se han descrito extensamente en estudios previos, sino proporcionar datos sobre la efectividad y la seguridad de ivacaftor en situaciones clínicas diferentes y complejas que se dan en la vida real, como las infecciones concomitantes, el uso de fármacos que podrían interaccionar con ivacaftor y pacientes inestables. Además, para el análisis comparativo con el año previo se excluyó al paciente 4-.
La mutación G551D afecta solamente al 5% de los pacientes en el Reino Unido. Esta limitación reduce la posibilidad de incluir un mayor número de pacientes procedentes de una sola unidad de FQ y sería recomendable realizar estudios multicéntricos que valoren las situaciones en la vida real.
En conclusión, llevamos a cabo un estudio de la evolución en vida real de 4 niños con FQ y la mutación G551D en quienes el tratamiento con ivacaftor se asoció a mejoras significativas en la función pulmonar, el estado nutricional, las dosis de lipasa, el cloro en sudor, el aislamiento de P. aeruginosa y el uso de antibióticos. Por añadidura, se confirmó la efectividad y seguridad del ivacaftor en situaciones clínicas que no se tienen en consideración en ensayos clínicos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.