La ecografía a pie de cama (EPC) se ha convertido en los últimos años en una herramienta imprescindible para la práctica clínica. La EPC debe entenderse como una extensión de la exploración física habitual que, sin sustituirla, la complementa y la enriquece. La EPC permite al clínico responder preguntas concretas sobre el diagnóstico, entender mejor la fisiopatología, orientar el tratamiento o realizar procedimientos invasivos con mayor seguridad. A pesar de su integración en muchos centros y en las diferentes subespecialidades pediátricas, no disponemos de recomendaciones específicas que establezcan los objetivos formativos en las distintas áreas de capacitación, la metodología de entrenamiento o la certificación de competencias en pediatría. Estos elementos son imprescindibles para que la EPC pueda implementarse en la práctica diaria con garantías de eficiencia y seguridad.
Este artículo aborda las principales aplicaciones de la EPC en pediatría mediante una revisión no sistemática por parte de expertos en diferentes áreas de la práctica clínica en España. Además, se discute acerca de la falta de planes formativos a nivel estatal, contando con la aportación de la experiencia de Estados Unidos.
En vista de la situación actual de la EPC, en nuestra opinión es urgente que se establezcan recomendaciones basadas en la evidencia para el entrenamiento en EPC que sirvan como base para el desarrollo de planes formativos y la integración de la EPC en el programa formativo de la especialidad.
Point-of-care ultrasound (POCUS) has become an essential tool for clinical practice in recent years. It should be considered as an extension of the standard physical examination, which complements and enriches it without substituting it. POCUS enables the physician to answer specific clinical questions about the diagnosis, to understand better the pathophysiological context, to orientate the treatment, and to perform invasive procedures more safely. Despite its current use in many centres, and in most paediatric sub-specialties, there are currently no specific recommendations addressing educational aims in the different training areas, as well as methodology practice and the certification process in paediatrics. These ingredients are essential for POCUS implementation in daily practice, with a quality guarantee in terms of efficiency and safety.
Several POCUS experts in different paediatric medicine environments performed a non-systematic review addressing the main paediatric POCUS applications in paediatrics. The lack of educational programs in POCUS in Spain is also discussed, and the experience in the United States of America in this topic is provided.
Considering the current situation of POCUS in paediatrics, we strongly believe that it is urgent to establish evidence-based recommendations for POCUS training that should be the base to develop educational programs and to include POCUS in the paediatric residency training.
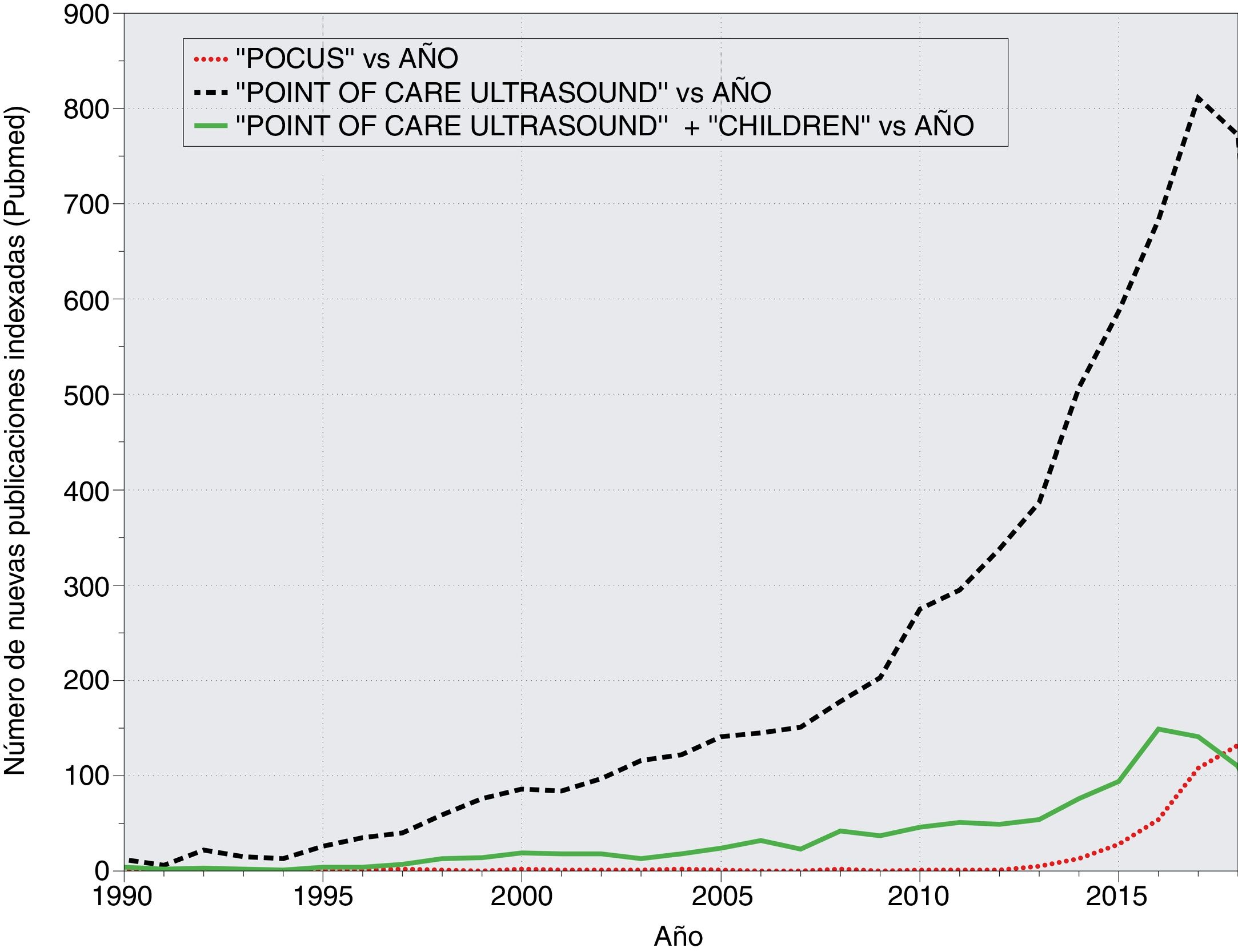
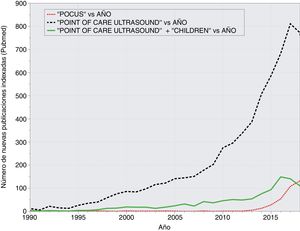
Desde su introducción en la práctica médica a mitad del sigloXX, la ecografía constituye una valiosa herramienta que permite la visualización de diversas estructuras anatómicas de manera no invasiva. Su principal ventaja con respecto a otras técnicas de imagen es que no emplea radiación ionizante. Además, se realiza de forma rápida y a pie de cama (evita desplazar a los pacientes) y puede repetirse de forma seriada, permitiendo estimar la eficacia de las intervenciones terapéuticas por el médico responsable, sin depender de otros profesionales. Aunque su uso ha estado vinculado principalmente a los especialistas en radiodiagnóstico, desde hace décadas es una técnica indispensable para otras especialidades médicas y quirúrgicas como la cardiología o la ginecología y obstetricia, entre otras1. El empleo de la ecografía por médicos no especialistas en radiodiagnóstico como complemento a la exploración física se ha definido como ecografía clínica, ecografía en el punto de cuidado o ecografía a pie de cama (EPC)1. Aunque su uso no está exento de controversias y particularidades2,3, parece una herramienta clínica ya implantada (fig. 1) que ha obligado a diversas sociedades científicas a adoptar posiciones claras al respecto4,5.
Tanto el amplio campo de subespecialidades pediátricas existentes, como las características anatómicas y fisiopatológicas de los pacientes pediátricos (claramente diferenciadas de los adultos), hacen que el uso de la EPC en pediatría tenga ciertas particularidades con respecto a su implantación en otras especialidades médicas.
En la actualidad, el programa formativo de la especialidad de Pediatría y sus áreas específicas en España está regulado por el Ministerio de Sanidad6. Dicho programa señala que el especialista en pediatría debe estar capacitado para realizar e interpretar los procedimientos diagnósticos inherentes al ejercicio de la pediatría clínica, incluyendo el ecocardiograma o algunas técnicas invasivas como la cateterización venosa central, cuya realización precisa el uso de la ecografía7. A pesar de esto, el aprendizaje de la EPC aún no se encuentra definido de manera específica en el mencionado programa, ni tampoco en el Libro Blanco de las Especialidades Pediátricas, salvo en el caso de la reumatología pediátrica8.
A lo largo de la última década las sociedades científicas pediátricas en nuestro país han visto cómo en su seno se han desarrollado grupos de trabajo cuyos objetivos han estado dirigidos a la difusión, a la enseñanza y a la investigación sobre el uso de la EPC9,10.
El objetivo de este trabajo es ofrecer una visión sobre el uso de la EPC que recoja los puntos de vista de diferentes áreas de la práctica pediátrica, teniendo en cuenta las diferentes aplicaciones de la técnica y las necesidades y recursos formativos existentes.
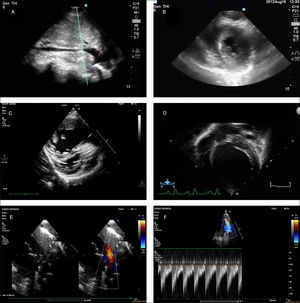
Ecografía cardiaca dirigidaLa ecografía cardiaca dirigida (ECD), o «focused cardiac ultrasound» (FoCUS), es el término aceptado para designar la ecocardiografía realizada por el clínico a pie de cama para la evaluación del paciente con signos o síntomas de compromiso circulatorio11. A diferencia de la ecocardiografía estándar realizada por el cardiólogo, en la ECD no se persigue realizar un diagnóstico anatómico o funcional completo. En la ECD, mediante una exploración simplificada pero sistemática (fig. 2), el clínico pretende responder a preguntas clave sobre la fisiología del paciente con inestabilidad hemodinámica (¿por qué está el paciente hipotenso?, ¿podría beneficiarse de la administración de líquidos?, ¿es preferible iniciar soporte inotrópico?) o realizar diagnósticos críticos como un taponamiento. La sistemática de la ECD incluye la ventana subcostal (eje largo y vena cava inferior), la ventana apical y la ventana paraesternal en eje largo y eje corto. Los elementos fundamentales en la ECD son la valoración del pericardio, la valoración del tamaño relativo de las cavidades, la estimación de la función sistólica y del estado de volemia. En el paciente en shock se ha demostrado que la ECD permite identificar el mecanismo predominante (cardiogénico, obstructivo o hipovolémico/distributivo) cambiando el manejo, reduciendo la demora en el tratamiento y mejorando el pronóstico12 (tabla 1). Asimismo, la valoración de estos patrones puede servir para identificar causas reversibles de parada cardiorrespiratoria con ritmo no desfibrilable, teniendo además la presencia o ausencia de actividad contráctil organizada un importante valor pronóstico sobre la recuperación de la circulación espontánea13. Las guías de práctica clínica y las sociedades científicas establecen que la formación en ECD debe formar parte del entrenamiento básico de especialidades como los cuidados intensivos, la anestesiología o la medicina de emergencias, estableciendo pautas sobre cómo debería realizarse el entrenamiento11,14,15. Aunque existe mucha variabilidad en cuanto a la metodología, la mayoría de las iniciativas promueven un aprendizaje basado en la evaluación de competencias, la práctica individual supervisada en pacientes reales con revisión de imágenes y la utilidad de las herramientas de tipo e-learning11. Las guías internacionales apoyan la utilidad de la EPC en pediatría y recogen recomendaciones sobre la práctica clínica11,14. El entrenamiento en ECD es ya una realidad en formación de determinadas subespecialidades pediátricas, como los cuidados intensivos y la neonatología16. Sin embargo, no existe a día de hoy un consenso que establezca cómo deberían formarse los pediatras en ECD, más allá de iniciativas individuales17. Por tanto, es necesario un esfuerzo conjunto para establecer un estándar formativo en ECD para las subespecialidades pediátricas implicadas.
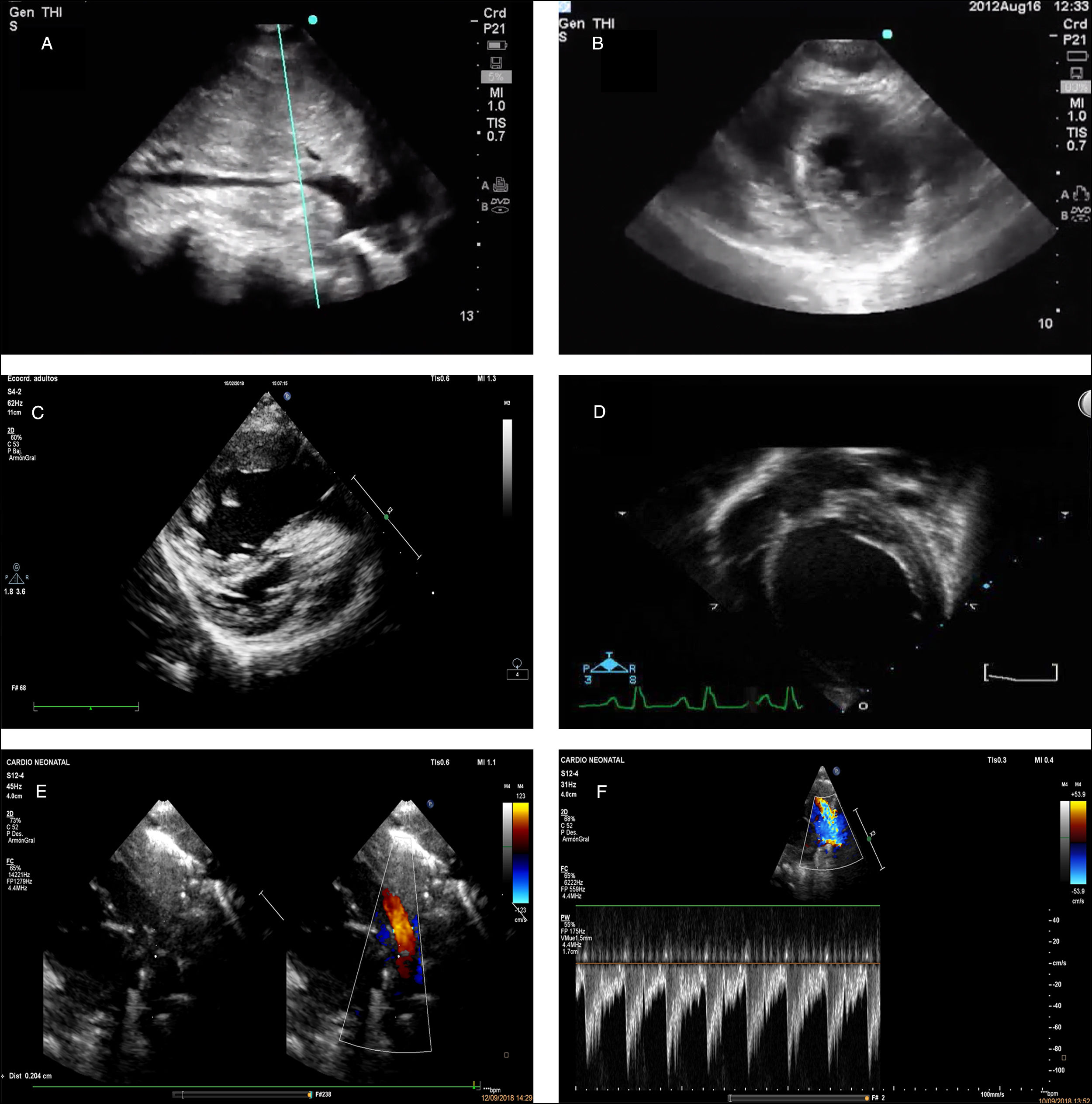
Imágenes de ecocardiografía a pie de cama correspondientes a diversas situaciones clínicas. A)Colapso inspiratorio de la vena cava inferior en un plano subcostal. Signo indicativo de hipovolemia en contexto clínico compatible. B)Colapso sistólico del ventrículo izquierdo en un plano paraesternal (eje corto). Signo indicativo de hipovolemia en contexto clínico compatible. C)Imagen compatible con ventrículo derecho dilatado y rectificación septal. Sugestivo de hipertensión pulmonar. D)Imagen de dilatación del ventrículo izquierdo en el contexto de pacientes con cuadro de inestabilidad hemodinámica, sugestiva de disfunción ventricular grave. E)Ductus arterioso persistente grande en prematuro. F)Imagen doppler a nivel de la arteria pulmonar izquierda con aumento de la velocidad del flujo telediastólico sugestivo de hiperaflujo pulmonar y ductus hemodinámicamente significativo.
Resumen de las principales potenciales aplicaciones de ecografía a pie de cama en cuidados intensivos pediátricos, destacando el nivel de entrenamiento precisado y los principales hallazgos ecográficos
| Contexto clínico | Aplicación y nivel de entrenamiento | Hallazgos ecográficos |
|---|---|---|
| PCR12,13 | Actividad cardiaca global (A) | • Pseudoasistolia-AESP: actividad contráctil organizada• Asistolia-AESP verdadera: ausencia de actividad contráctil organizada (cardiac standstill) |
| Valoración hemodinámica11,14,15 | Estimación de la volemia (B)• Tamaño cavidades• Tamaño y colapso respiratorio de vena cava inferior | Shock hipovolémico/distributivo• Cavidades pequeñas «vacías» con tendencia al colapso sistólico (por aumento compensador de la contractilidad)• Vena cava inferior pequeña con tendencia al colapso inspiratorio |
| Estimación de la función sistólica del VI (B)• Tamaño del VI• Estimación visual de la función• Vena cava inferior | Shock cardiogénico• Dilatación del VI (no siempre)• Estimación visual de la función del VI (eye-balling): escasa movilidad sistólica global, escasa excursión de la valva mitral hacia el septo en diástole, escaso/nulo engrosamiento de las paredes del VI en sístole• VCI dilatada con escasa variación respiratoria | |
| Tamaño y presión del VD (B)• Tamaño relativo de los ventrículos• Curvatura septal | Shock obstructivo con fallo/dilatación del VD• Dilatación del VD (relación VD:VI >0,6 en niños mayores y >1 en niños pequeños)• Inversión de la curvatura septal hacia la izquierda (aumento de la presión derecha) | |
| Pericardio (B)• Presencia de derrame• Compresión del corazón | Shock obstructivo con «taponamiento»• Presencia de derrame pericárdico y colapso diastólico o compresión de cavidades derechas• VI «vacío» e hipercontráctil | |
| Evaluación respiratoria1,21,24,26,29 | Derrame pleural (B) | Identificación y cuantificación de colección en espacio pleural |
| Consolidaciones parenquimatosas (B) | Hepatización del parénquima, desaparición de los signos de aireación pulmonar | |
| Aireación pulmonar y/o agua pulmonar extravascular (A) | Líneas B y consolidación/atelectasia (número, extensión y distribución) | |
| Detección de la presencia de neumotórax (B) | • Ausencia de deslizamiento pleural• Punto pulmón• Ausencia de pulso pulmón y líneas B | |
| Movilidad diafragmática (A) | • Excursión del diafragma (cualitativa y modoM)• Cambio porcentual del grosor inspiratorio del diafragma | |
| Evaluación neurológica4,26 | Desviación de la línea media (A) | Medición de distancia a tercer ventrículo desde ambas corticales desde ventana transtemporal (en situación normal deben ser aproximadamente iguales) |
| Doppler transcraneal (A) | Valoración del flujo sanguíneo cerebral: determinación de velocidades en vasos del polígono de Willis. Cálculo de IP e IR | |
| Evaluación pupilar (A) | Evaluación del tamaño y de la respuesta pupilar a la luz | |
| Vaina del nervio óptico (A) | Aumento del diámetro en HTIC | |
| Evaluación abdominal (politrauma) | Protocolo E-FAST30 (B) | • Detección de hemoperitoneo• Detección de hemopericardio• Detección de hemo-neumotórax |
| Realización de técnicas ecoguiadas/ecoasistidas | Acceso vascular1,7,9,26 (B) | Canalización ecoguiada de arterias, venas centrales y venas periféricas |
| Intubación traqueal (A) | Valoración de columna de gas traqueal/esofágica, deslizamiento pleural y posición de tubo endotraqueal (protocolo TRUE) | |
| Colocación de drenajes31 (A) | Técnica ecoguiada o ecoasistida (toracocentesis, paracentesis y pericardiocentesis) | |
| Control sonda vesical (B) | Volumen vesical, permeabilidad de la sonda y control de la posición e hinchado del balón de la sonda |
(A): nivel de entrenamiento avanzado; (B): nivel de entrenamiento básico.
AESP: actividad eléctrica sin pulso; E-FAST: evaluación extendida mediante ecografía enfocada al trauma; IP: índice de pulsatilidad; IR: índice de resistencia; PCR: parada cardiorrespiratoria; VCI: vena cava inferior; VD: ventrículo derecho; VI: ventrículo izquierdo.
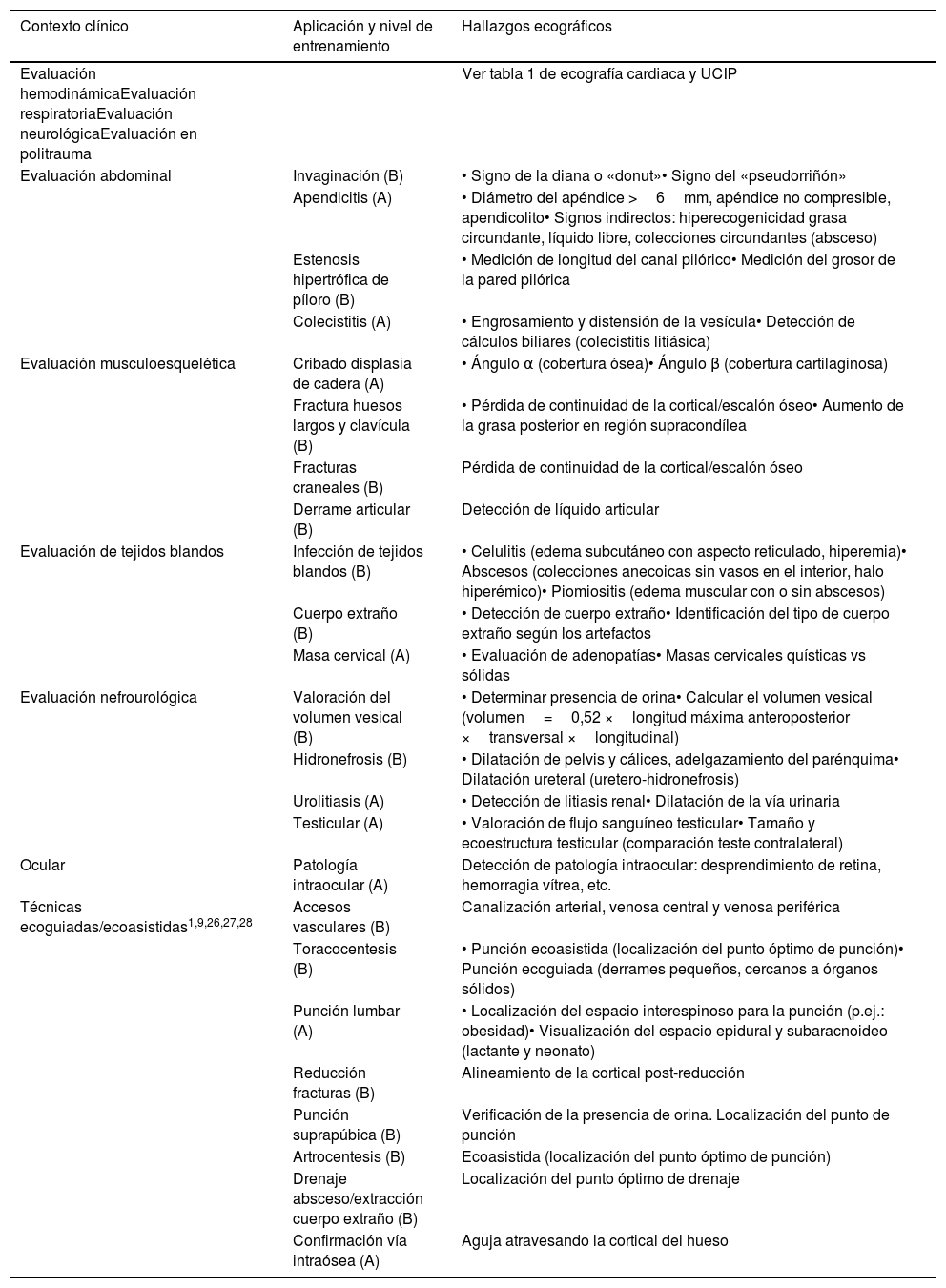
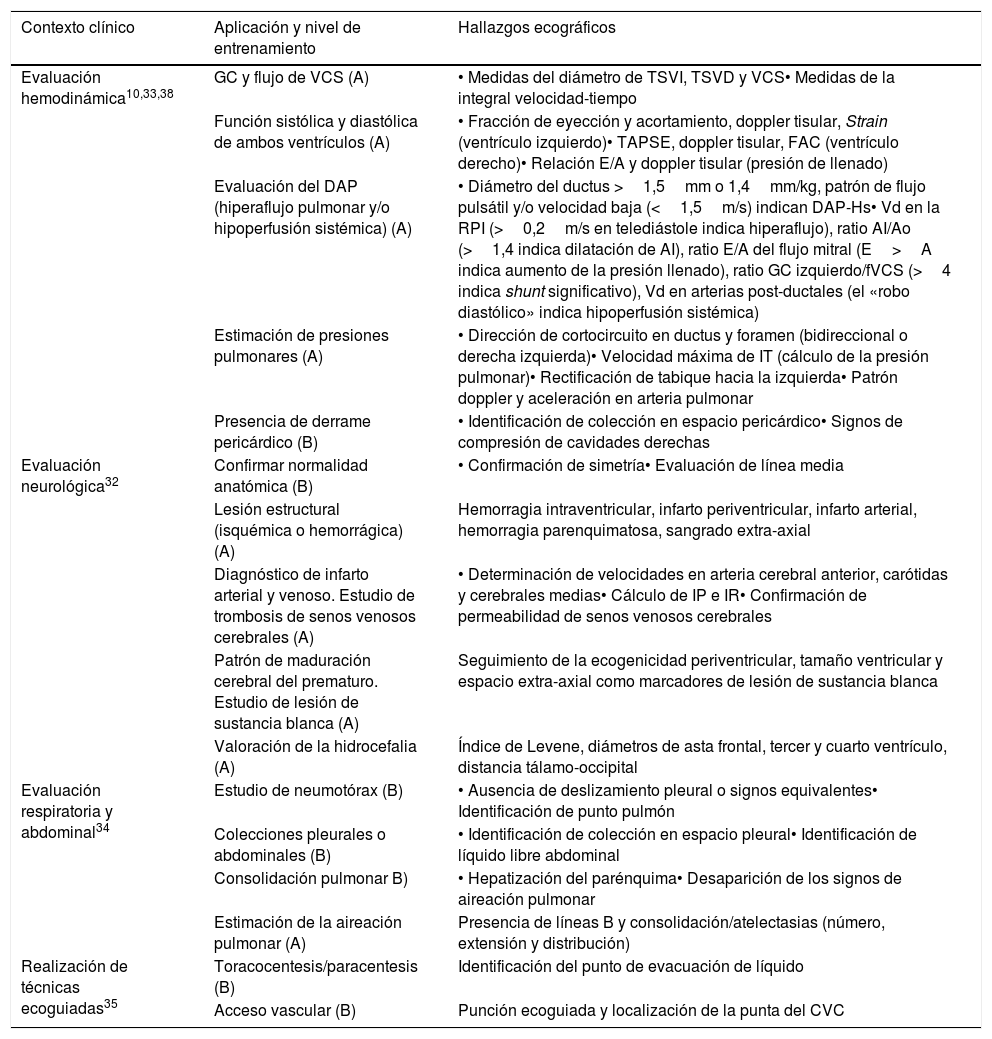
Pese a su incorporación más tardía, el uso de la EPC en atención primaria (AP) está experimentando un gran crecimiento en los últimos años18. El uso de la EPC se ha incorporado a la práctica diaria en el adulto en muchos centros de salud en España19. La EPC tiene también un gran potencial para el pediatra de AP. Sin embargo, su incorporación es aún muy escasa, probablemente en relación con la falta de formación, el mantenimiento de la capacitación, la escasez de equipos, la presión asistencial, la percepción de intrusismo profesional y los potenciales conflictos medicolegales. No obstante, existen iniciativas, como el grupo de trabajo en Ecografía Clínica de la AEPAP, que buscan extender su uso promoviendo la formación y la difusión entre los pediatras de AP20. En este ámbito es clave insistir en que la EPC ha de responder a preguntas clínicas concretas y no pretender una evaluación anatómica completa, escogiendo las patologías más prevalentes en las que la EPC haya demostrado mayor eficiencia que la exploración física aislada19. Sirva de ejemplo paradigmático el diagnóstico de la neumonía adquirida en la comunidad21. Otros ejemplos donde la EPC podría mejorar la atención son el diagnóstico de infecciones de partes blandas (celulitis vs absceso), la detección de derrame articular o el cribado de displasia de cadera en el lactante (tabla 2). Hay que señalar que la implantación de la EPC en pediatría de AP debe acompañarse de una planificación adecuada, no solo desde el punto de vista de costes materiales, sino también con una adecuación de los tiempos de consulta que permita su uso.
Resumen de las principales potenciales aplicaciones de la ecografía a pie de cama en urgencias de pediatría, atención primaria y unidades de hospitalización, destacando el nivel de entrenamiento precisado y los principales hallazgos ecográficos
| Contexto clínico | Aplicación y nivel de entrenamiento | Hallazgos ecográficos |
|---|---|---|
| Evaluación hemodinámicaEvaluación respiratoriaEvaluación neurológicaEvaluación en politrauma | Ver tabla 1 de ecografía cardiaca y UCIP | |
| Evaluación abdominal | Invaginación (B) | • Signo de la diana o «donut»• Signo del «pseudorriñón» |
| Apendicitis (A) | • Diámetro del apéndice >6mm, apéndice no compresible, apendicolito• Signos indirectos: hiperecogenicidad grasa circundante, líquido libre, colecciones circundantes (absceso) | |
| Estenosis hipertrófica de píloro (B) | • Medición de longitud del canal pilórico• Medición del grosor de la pared pilórica | |
| Colecistitis (A) | • Engrosamiento y distensión de la vesícula• Detección de cálculos biliares (colecistitis litiásica) | |
| Evaluación musculoesquelética | Cribado displasia de cadera (A) | • Ángulo α (cobertura ósea)• Ángulo β (cobertura cartilaginosa) |
| Fractura huesos largos y clavícula (B) | • Pérdida de continuidad de la cortical/escalón óseo• Aumento de la grasa posterior en región supracondílea | |
| Fracturas craneales (B) | Pérdida de continuidad de la cortical/escalón óseo | |
| Derrame articular (B) | Detección de líquido articular | |
| Evaluación de tejidos blandos | Infección de tejidos blandos (B) | • Celulitis (edema subcutáneo con aspecto reticulado, hiperemia)• Abscesos (colecciones anecoicas sin vasos en el interior, halo hiperémico)• Piomiositis (edema muscular con o sin abscesos) |
| Cuerpo extraño (B) | • Detección de cuerpo extraño• Identificación del tipo de cuerpo extraño según los artefactos | |
| Masa cervical (A) | • Evaluación de adenopatías• Masas cervicales quísticas vs sólidas | |
| Evaluación nefrourológica | Valoración del volumen vesical (B) | • Determinar presencia de orina• Calcular el volumen vesical (volumen=0,52 ×longitud máxima anteroposterior ×transversal ×longitudinal) |
| Hidronefrosis (B) | • Dilatación de pelvis y cálices, adelgazamiento del parénquima• Dilatación ureteral (uretero-hidronefrosis) | |
| Urolitiasis (A) | • Detección de litiasis renal• Dilatación de la vía urinaria | |
| Testicular (A) | • Valoración de flujo sanguíneo testicular• Tamaño y ecoestructura testicular (comparación teste contralateral) | |
| Ocular | Patología intraocular (A) | Detección de patología intraocular: desprendimiento de retina, hemorragia vítrea, etc. |
| Técnicas ecoguiadas/ecoasistidas1,9,26,27,28 | Accesos vasculares (B) | Canalización arterial, venosa central y venosa periférica |
| Toracocentesis (B) | • Punción ecoasistida (localización del punto óptimo de punción)• Punción ecoguiada (derrames pequeños, cercanos a órganos sólidos) | |
| Punción lumbar (A) | • Localización del espacio interespinoso para la punción (p.ej.: obesidad)• Visualización del espacio epidural y subaracnoideo (lactante y neonato) | |
| Reducción fracturas (B) | Alineamiento de la cortical post-reducción | |
| Punción suprapúbica (B) | Verificación de la presencia de orina. Localización del punto de punción | |
| Artrocentesis (B) | Ecoasistida (localización del punto óptimo de punción) | |
| Drenaje absceso/extracción cuerpo extraño (B) | Localización del punto óptimo de drenaje | |
| Confirmación vía intraósea (A) | Aguja atravesando la cortical del hueso | |
(A): nivel de entrenamiento avanzado; (B): nivel de entrenamiento básico.
La incorporación de la EPC en pediatría hospitalaria ha surgido en las últimas décadas, con especial impacto en los servicios de urgencias pediátricos (SUP)22. La inclusión de la EPC dentro del currículum del pediatra de urgencias23 y el posicionamiento de la Academia Americana de Pediatría a favor de su uso en dicho ámbito5 han favorecido la consolidación de la EPC como técnica indispensable en el SUP. Respecto a otros ámbitos, se ha descrito su uso en hospitalización y otras especialidades.
Dentro de las aplicaciones de la EPC en el ámbito hospitalario (tabla 2), las que poseen más evidencia son la evaluación mediante ecografía enfocada al trauma (focused abdominal sonography for trauma [FAST]), la detección de neumonía, la detección de fracturas, la valoración de tejidos blandos (celulitis/absceso) y la realización de técnicas como el acceso vascular, la reducción de fracturas, la punción lumbar y la punción suprapúbica5,24. También se ha estudiado el uso de la EPC en otras entidades, aunque la evidencia existente es aún escasa (patología abdominal, bronquiolitis, cuerpo extraño, derrame articular y masa cervical). No obstante, en referencia a la introducción de la EPC, cada centro debe decidir qué aplicaciones resultarán más beneficiosas, no solo en base a la evidencia, sino también en función de las necesidades y de los recursos de que se dispone.
Existe una amplia oferta formativa en EPC mediante cursos, libros y material en línea25. Sin embargo, la falta de programas formativos intrahospitalarios a nivel estatal dificulta la adquisición de competencia práctica, siendo esta muy dependiente de la disponibilidad de ecógrafo y de personal experto. En ese sentido, las líneas de futuro deben focalizarse en la consolidación de los programas formativos hospitalarios en EPC para favorecer una formación más completa y estandarizada.
Ecografía en el punto de cuidado en cuidados intensivos pediátricosEl uso de EPC en las unidades de cuidados intensivos pediátricas (UCIP) está creciendo de forma notable en los últimos años7,26. Diversos autores sostienen que su uso en UCIP mejora la valoración clínica, modifica el tratamiento hasta en un 40% de los pacientes27 y aumenta la seguridad en los procedimientos invasivos28. La medicina crítica de adultos cuenta ya con documentos de consenso de sociedades próximas para la formación de ecografía4,14, con algunas recomendaciones específicas para pacientes pediátricos14.
Las principales aplicaciones de EPC en UCIP (tabla 1) incluyen:
Ecografía cardiaca dirigida (ECD). Ya descrita en la sección de ecocardiografía (fig. 2).
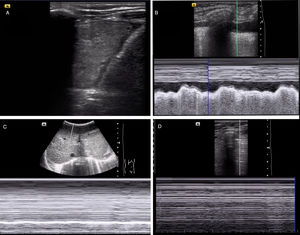
Ecografía pulmonar. Permite descartar/diagnosticar neumotórax, detectar condensaciones parenquimatosas y derrame pleural (fig. 3). También útil para detectar parálisis/paresia diafragmática y para la posición de tubo endotraqueal.
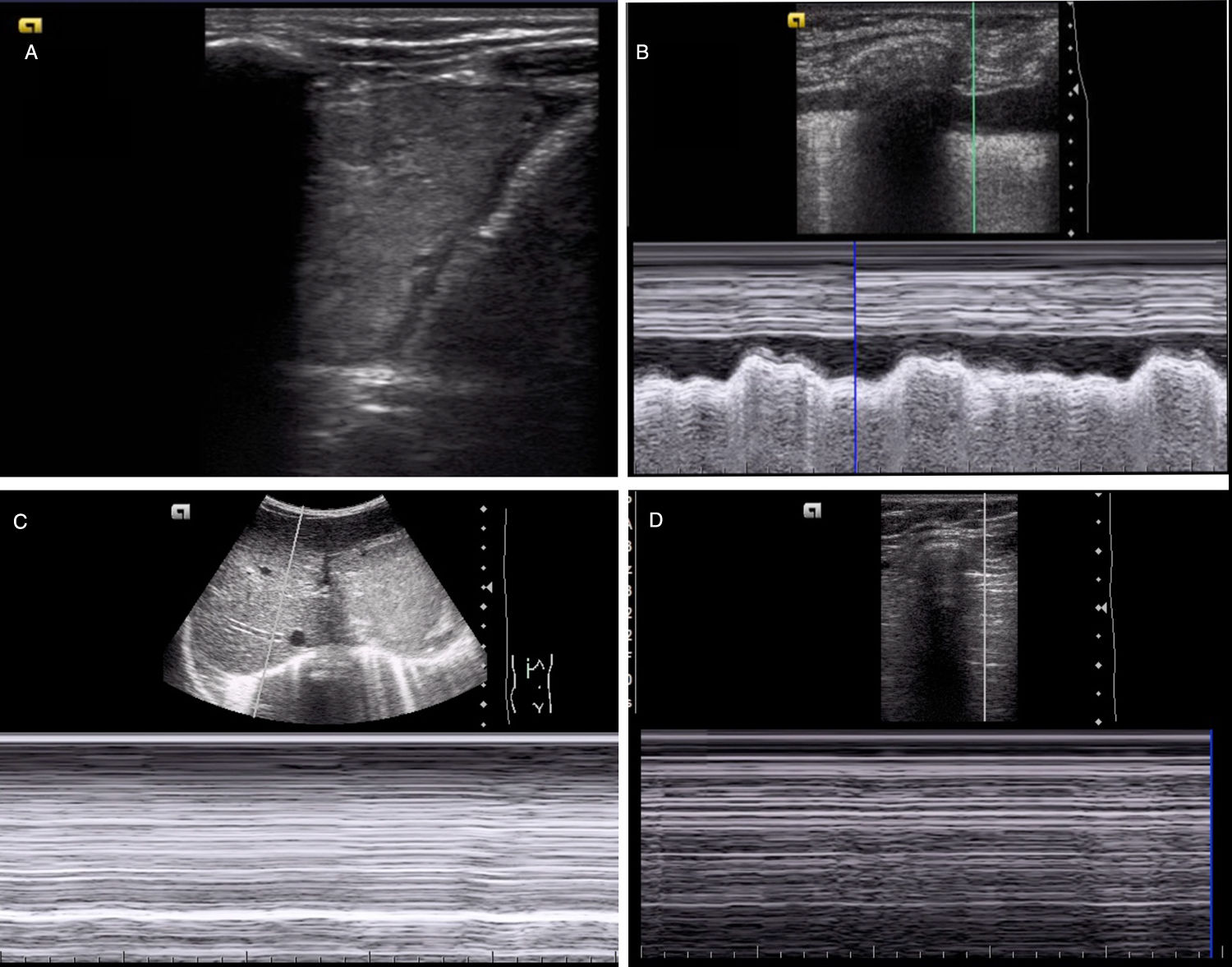
Diagnóstico de diferentes patologías respiratorias mediante ecografía a pie de cama. A)Consolidación del parénquima pulmonar con derrame pleural asociado. B)Identificación de derrame pleural empleando el modoM (signo del sinusoide). C)Evaluación de la motilidad diafragmática empleando el modoM con ausencia de excursión diafragmática (compatible con paresia diagragmática). D)Ausencia de deslizamiento pleural mediante modoM sugestiva de neumotórax (signo de la estratosfera o código de barras).
Neuroecografía1. Estimación y repercusión de la presión intracraneal mediante doppler transcraneal, diámetro de la vaina del nervio óptico; también útil para valorar la desviación de la línea media en caso de lesiones ocupantes de espacio.
Abdomen. Fundamentalmente detección de líquido libre en el protocolo FAST30; también es útil para el control de la sonda vesical y el estado de la vejiga en caso de anuria.
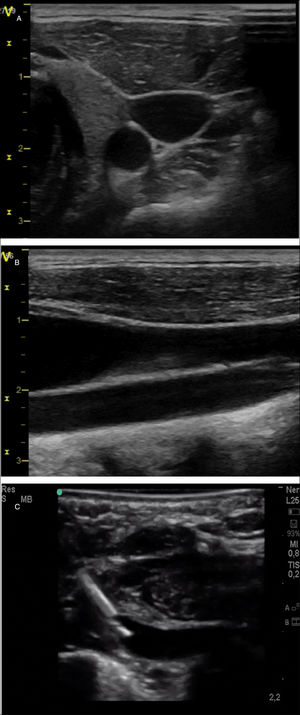
Procedimientos ecoguiados. Canalización de vías9 (fig. 4), paracentesis, pericardiocentesis, toracocentesis/tubo de tórax31.
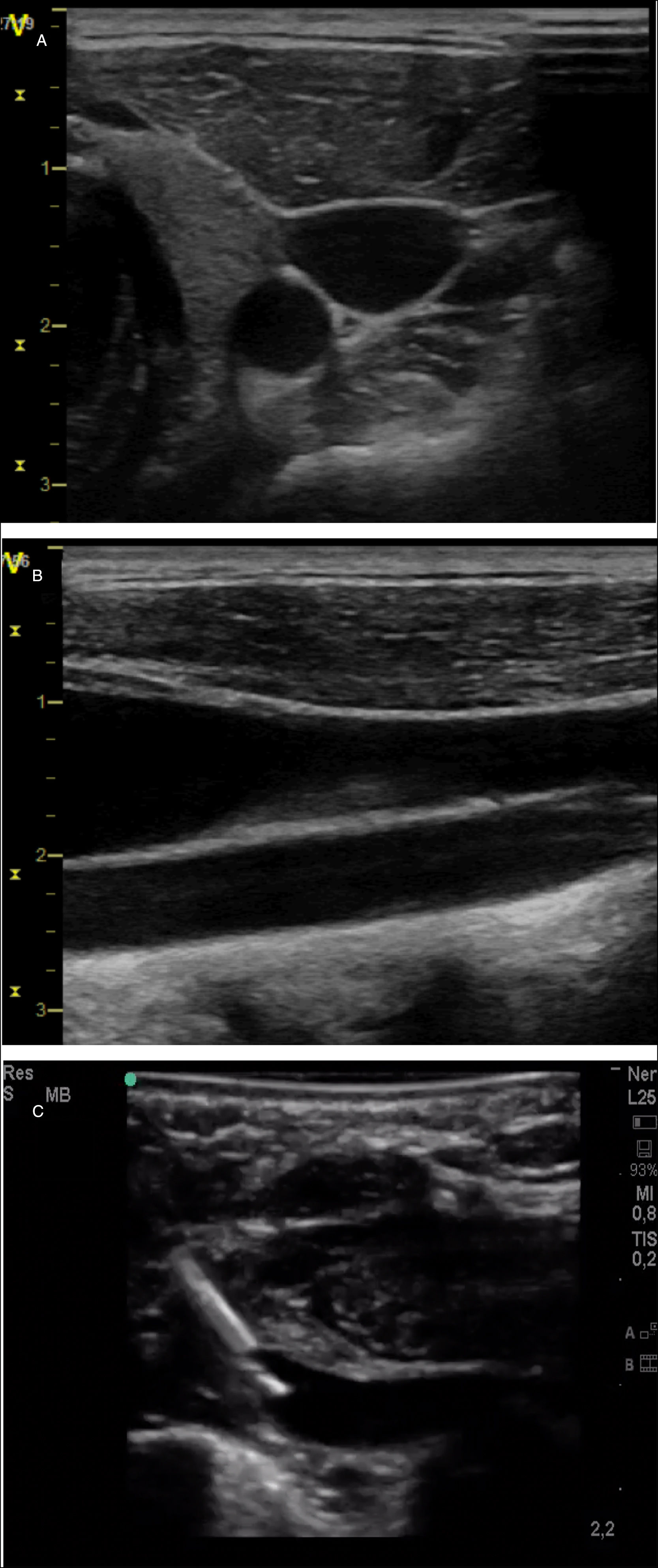
Exploración vascular cervical con ecografía a pie de cama. A)Corte transversal de los vasos identificando la arteria carótida como estructura hipoecoica redondeada y la vena yugular como estructura hipoecoica ovalada algo más superficial. B)Corte longitudinal de los vasos; se identifican la vena yugular a nivel más superficial y la arteria carótida a nivel profundo. C)Imagen de una canalización de la vena subclavia en un paciente neonato mediante abordaje longitudinal en plano.
Un punto clave en el uso de la ecografía en UCIP es la formación, de la que no se ha establecido hasta la fecha un programa unificado. Conlon et al.17 proponen una formación teórico-práctica de 16h seguida de al menos 25 exploraciones correctas en las aplicaciones no relacionadas con procedimientos (valoración hemodinámica, pulmonar y abdominal) para estimar la competencia en esas técnicas, de forma similar a lo sugerido por el American College of Emergency Physicians15. Sin embargo, en nuestra experiencia y según algunos autores4, el número de estudios supervisados varía significativamente de una persona a otra, por lo que es muy difícil sugerir una cifra mínima de estudios adecuada.
El documento de consenso para la formación en ecografía en medicina intensiva de adultos en España sugiere diferentes niveles formativos y detalla los diferentes requerimientos para las principales aplicaciones de EPC en ese ámbito. El nivel básico comprende: ecografía pleuropulmonar, accesos vasculares, ecografía abdominal, ecografía dúplex transcraneal y ECD4.
Se impone en definitiva diseñar un currículo longitudinal de etapas formativas, uso de simuladores, número de ecografías y examen de certificación y re-certificación en manejo global y/o en sus diversos apartados, siendo así mismo necesario establecer sistemas de acreditación para los «formadores»4,31. Para ello deberán elaborarse guías y recomendaciones por parte del grupo de trabajo de la Sociedad Española de Cuidados Intensivos Pediátricos.
Ecografía en el punto de cuidado en neonatosActualmente la EPC es una técnica diagnóstica imprescindible en las unidades de neonatología donde las ventajas ya señaladas de esta tecnología permiten que pueda ser aplicada en pacientes tan vulnerables como los recién nacidos (RN).
Se emplea fundamentalmente para la evaluación cerebral (USC), cardíaca, abdominal, torácica y para la realización de procedimientos ecoguiados (tabla 3).
Resumen de las principales potenciales aplicaciones de ecografía a pie de cama en neonatología, destacando el nivel de entrenamiento precisado y los principales hallazgos ecográficos
| Contexto clínico | Aplicación y nivel de entrenamiento | Hallazgos ecográficos |
|---|---|---|
| Evaluación hemodinámica10,33,38 | GC y flujo de VCS (A) | • Medidas del diámetro de TSVI, TSVD y VCS• Medidas de la integral velocidad-tiempo |
| Función sistólica y diastólica de ambos ventrículos (A) | • Fracción de eyección y acortamiento, doppler tisular, Strain (ventrículo izquierdo)• TAPSE, doppler tisular, FAC (ventrículo derecho)• Relación E/A y doppler tisular (presión de llenado) | |
| Evaluación del DAP (hiperaflujo pulmonar y/o hipoperfusión sistémica) (A) | • Diámetro del ductus >1,5mm o 1,4mm/kg, patrón de flujo pulsátil y/o velocidad baja (<1,5m/s) indican DAP-Hs• Vd en la RPI (>0,2m/s en telediástole indica hiperaflujo), ratio AI/Ao (>1,4 indica dilatación de AI), ratio E/A del flujo mitral (E>A indica aumento de la presión llenado), ratio GC izquierdo/fVCS (>4 indica shunt significativo), Vd en arterias post-ductales (el «robo diastólico» indica hipoperfusión sistémica) | |
| Estimación de presiones pulmonares (A) | • Dirección de cortocircuito en ductus y foramen (bidireccional o derecha izquierda)• Velocidad máxima de IT (cálculo de la presión pulmonar)• Rectificación de tabique hacia la izquierda• Patrón doppler y aceleración en arteria pulmonar | |
| Presencia de derrame pericárdico (B) | • Identificación de colección en espacio pericárdico• Signos de compresión de cavidades derechas | |
| Evaluación neurológica32 | Confirmar normalidad anatómica (B) | • Confirmación de simetría• Evaluación de línea media |
| Lesión estructural (isquémica o hemorrágica) (A) | Hemorragia intraventricular, infarto periventricular, infarto arterial, hemorragia parenquimatosa, sangrado extra-axial | |
| Diagnóstico de infarto arterial y venoso. Estudio de trombosis de senos venosos cerebrales (A) | • Determinación de velocidades en arteria cerebral anterior, carótidas y cerebrales medias• Cálculo de IP e IR• Confirmación de permeabilidad de senos venosos cerebrales | |
| Patrón de maduración cerebral del prematuro. Estudio de lesión de sustancia blanca (A) | Seguimiento de la ecogenicidad periventricular, tamaño ventricular y espacio extra-axial como marcadores de lesión de sustancia blanca | |
| Valoración de la hidrocefalia (A) | Índice de Levene, diámetros de asta frontal, tercer y cuarto ventrículo, distancia tálamo-occipital | |
| Evaluación respiratoria y abdominal34 | Estudio de neumotórax (B) | • Ausencia de deslizamiento pleural o signos equivalentes• Identificación de punto pulmón |
| Colecciones pleurales o abdominales (B) | • Identificación de colección en espacio pleural• Identificación de líquido libre abdominal | |
| Consolidación pulmonar B) | • Hepatización del parénquima• Desaparición de los signos de aireación pulmonar | |
| Estimación de la aireación pulmonar (A) | Presencia de líneas B y consolidación/atelectasias (número, extensión y distribución) | |
| Realización de técnicas ecoguiadas35 | Toracocentesis/paracentesis (B) | Identificación del punto de evacuación de líquido |
| Acceso vascular (B) | Punción ecoguiada y localización de la punta del CVC |
(A): nivel de entrenamiento avanzado; (B): nivel de entrenamiento básico;
AI: aurícula izquierda; Ao: aorta; CVC: catéter venoso central; DAP: ductus arterioso persistente; DAP-Hs: ductus arterioso persistente hemodinámicamente significativo; E/A: ondas de llenado diastólico temprano (E) y auricular (A); FAC: cambio en fracción de acortamiento por área; fVCS, flujo en vena cava superior; GC: gasto cardíaco; IP: índice de pulsatilidad; IR: índice de resistencia; IT: insuficiencia tricúspide; LCR: líquido cefalorraquídeo; RPI: rama pulmonar izquierda; TAPSE: excursión sistólica del anillo tricúspide; TSVD: tracto de salida del ventrículo derecho; TSVI: tracto de salida del ventrículo izquierdo; VCS: vena cava superior; Vd: velocidad diastólica.
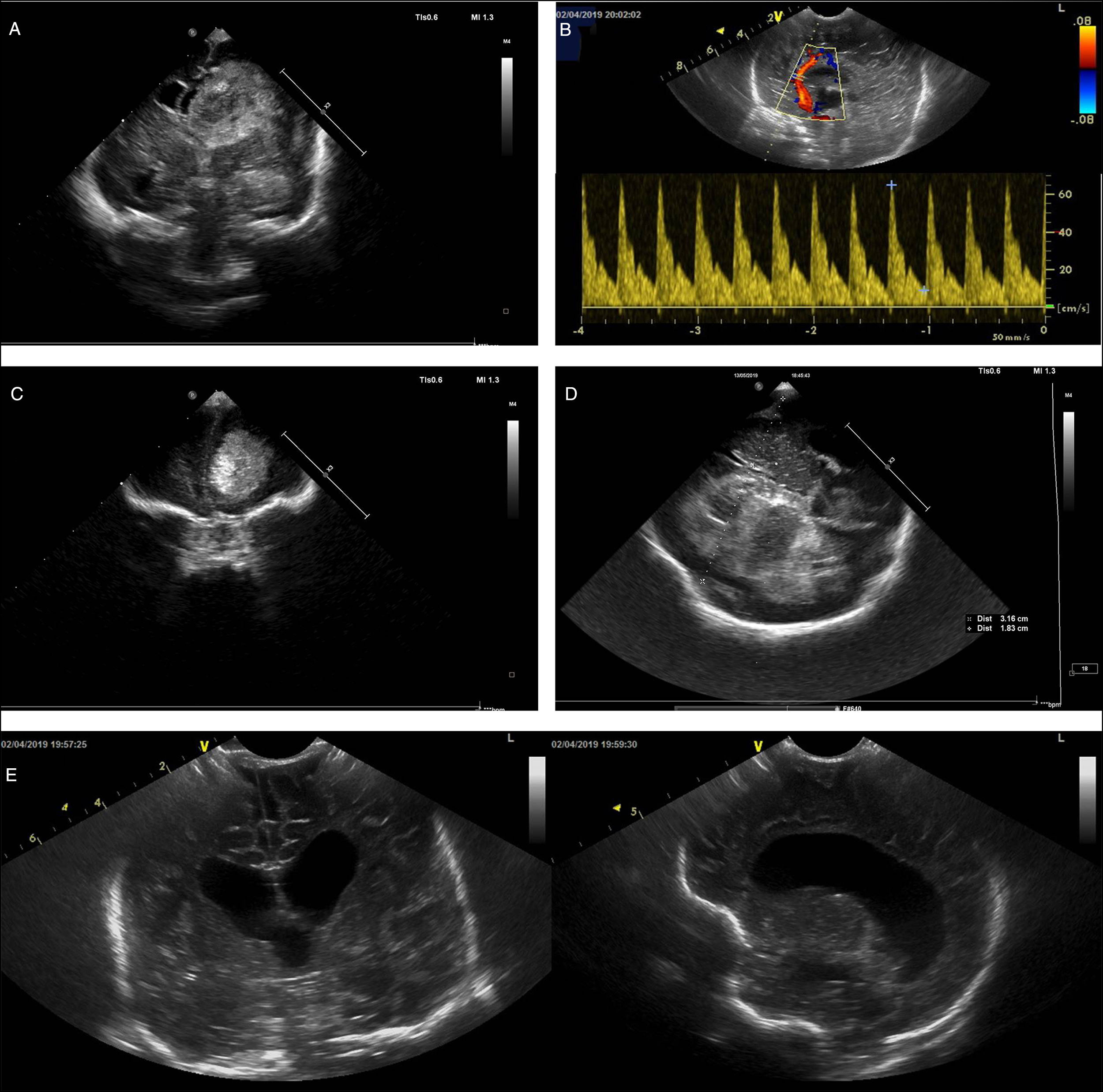
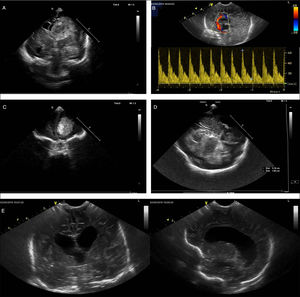
USC-doppler (fig. 5). Permite detectar la existencia de lesiones cerebrales a través de distintas ventanas acústicas (fontanela anterior, posterior, mastoides y temporal), ofreciendo información con fines tanto diagnósticos como pronósticos. Los estudios seriados permiten estudiar la maduración cerebral del RN prematuro para determinar si esta es adecuada, y es esencial para determinar la causa que ha producido la lesión estructural32.
Exploraciones cerebrales realizadas en neonatos mediante ecografía a pie de cama. A)Corte coronal en que se observa imagen hiperecoica compatible con hemorragia intraventricular con desplazamiento de la línea media. B)Estudio doppler de la arteria pericallosa en paciente con hidrocefalia descompensada que muestra aumento de la resistencia (índice de pulsatilidad de 1,94) compatible con aumento de la presión intracraneal. C)Corte coronal que muestra una lesión hiperecogénica en la región frontal. D)Ecografía realizada a través de ventana transtemporal en la que se observa una lesión hiperecogénica compatible con hemorragia que desplaza la línea media. E)Cortes coronal (izquierda) y sagital (derecha) de un paciente neonato con meningitis en el que se observa dilatación ventricular.
Ecocardiografía. La ecocardiografía evalúa el corazón estructural y funcionalmente. La ecocardiografía funcional es capaz de cuantificar los rápidos cambios hemodinámicos en el RN, así como estudiar la respuesta al tratamiento (fig. 2). En los últimos 20años se ha extendido en las unidades neonatales el concepto de «ecografía realizada por el neonatólogo» (NPE)33, que señala que el neonatólogo es el profesional indicado para evaluar hemodinámicamente un corazón estructuralmente normal (sin evidencia de cardiopatía congénita, excluido el foramen oval y el ductus arterioso).
Ecografía torácica. Evalúa la presencia de neumotórax, derrame pleural, consolidación o atelectasias pulmonares29,34.
Ecografía abdominal. Permite estudiar malformaciones de las vísceras abdominales, ascitis, evaluación hemodinámica esplácnica, así como la correcta posición de la sonda vesical.
Canalización y localización de catéteres intravasculares. Útil para reducir el riesgo de complicaciones durante la canalización de accesos vasculares centrales, incluso en RN de muy bajo peso y para la verificación de la correcta posición del catéter35.
Formación en ecografía en el punto de cuidado en pediatría en Estados UnidosEn Estados Unidos la ecografía pediátrica en la práctica clínica se ha restringido tradicionalmente al ámbito de las subespecialidades de radiología y cardiología. Tras el reconocimiento por parte de los médicos de urgencias de adultos de la importancia de integrar la EPC en su práctica clínica, en los años noventa las sociedades que los representan apoyaron su uso en el ámbito clínico, a lo que siguió, en 2001, la publicación de las primeras guías prácticas15. Actualmente la formación en ecografía diagnóstica e intervencionista es una materia troncal que ha de incluirse en todos los programas de residencia y de especialización de posgrado (fellowship) en medicina intensiva del adulto36.
En Estados Unidos los especialistas pediátricos han seguido el ejemplo de sus colegas de medicina adulta. En 2015, la American Academy of Pediatrics (Academia Americana de Pediatría) apoyó la expansión del ámbito de práctica de la ecografía para incluir en él a los pediatras de urgencias5. Recientemente, la Society of Critical Care Medicine (Sociedad de Medicina Intensiva) ratificó una guía para el uso de la EPC, que incluía un espectro limitado de aplicaciones diagnósticas y de procedimientos en la edad pediátrica. Las aplicaciones, la formación y los procesos de acreditación relevantes a la UCIP se han descrito previamente17. Por añadidura, una encuesta de programas de formación en UCIP acreditados en Estados Unidos por el Consejo de Acreditación para la Educación Médica de Posgrado realizada en 2017 reveló que el 64% de los programas incluían la práctica de la EPC diagnóstica, y el 98% proporcionaban acceso a equipos de ecografía37. En 2011, la American Society of Echocardiography (Sociedad Americana de Ecocardiografía [ASE]), en colaboración con otras sociedades europeas, publicó una guía práctica y recomendaciones para la formación en ecografía dirigida en neonatología38. Estas guías han sido criticadas por ser demasiado prescriptivas e imponer requerimientos de formación inviables para los especialistas en neonatología39. Más recientemente, la ASE ha reconocido los beneficios clínicos de la «ecocardiografía dirigida», definida como «un complemento a la exploración física con objeto de detectar signos ecográficos específicos», si bien la aplicación de estas recomendaciones se circunscribe a la población adulta.
Los profesionales que practican la EPC dentro de las distintas especialidades pediátricas continúan esforzándose en estandarizar los currículos formativos, ofrecer formación, desarrollar competencias, estructurar el aseguramiento de calidad y establecer vías formales para la acreditación institucional. Estos elementos estructurales han conseguido promover los programas de EPC dentro de la medicina de urgencias del adulto15, pero aún no se han establecido en las especialidades pediátricas17. La preocupación por posibles problemas medicolegales se ha identificado con frecuencia como una de las barreras que impiden la implantación de la EPC en la práctica clínica en Estados Unidos, a pesar de que la literatura médica, tanto de adultos como pediátrica, sugiere que no realizar ecografías cuando dicha tecnología se encuentra disponible conlleva un riesgo mayor de problemas medicolegales para los clínicos3. En 2012, un sondeo efectuado en facultades de medicina estadounidenses encontró que el 62% de las instituciones participantes incluían la formación en ecografía en el currículo médico40. Así, en poco tiempo una generación de estudiantes de medicina con formación previa en ecografía comenzará a integrarse en la profesión pediátrica. Con la llegada de la próxima generación de pediatras clínicos, la integración de los conocimientos clínicos y la experiencia en tecnología de EPC supondrá un reto apasionante en la práctica clínica pediátrica en Estados Unidos.
Discusión y conclusionesEste trabajo pretende ofrecer un punto de vista multidisciplinar sobre la utilización de la EPC en diferentes ámbitos de la pediatría. Para ello hemos contado con la participación en la elaboración de este manuscrito de pediatras con papeles especialmente reseñables en la difusión e implantación de la EPC en nuestro país (y en Estados Unidos) procedentes de diferentes áreas de la pediatría7,9,10,17. Hay que señalar que, aunque en el trabajo se incluyen numerosas citas bibliográficas relativas a la evidencia científica existente que apoya el uso de la EPC en pediatría, no se ha realizado un procedimiento de revisión sistemática y evaluación de la evidencia científica existente para las aplicaciones propuestas, especialmente en cuanto a su clasificación como aplicaciones básicas o avanzadas.
La aplicación de la EPC, que únicamente es orientativa, una técnica no invasiva, segura, repetible y con utilidad clínica en manos expertas, ya está bien implantada en distintos ámbitos de la pediatría en algunos países, entre los que se encuentra España5,7. Algunas guías internacionales establecen recomendaciones pediátricas para la ecografía pulmonar en el paciente crítico o la ECD11,29. Sin embargo, a excepción del ámbito de urgencias pediátricas en Estados Unidos5,23, no hay guías clínicas que establezcan las aplicaciones básicas de EPC específicas para pediatría, ni que determinen el modo de realizar y acreditar el aprendizaje de esta técnica. Creemos que este es un punto clave en la adecuada implantación de la EPC, ya que, al igual que otras técnicas, su uso debe ir acompañado de un adecuado conocimiento de la técnica y sus limitaciones, y debe emplearse siempre en el contexto clínico de cada paciente. El no cumplimiento de las anteriores premisas podría conllevar una toma incorrecta de decisiones terapéuticas, con posible repercusión sobre los pacientes1.
Es importante destacar que la EPC debe servir para complementar la valoración clínica habitual y responder a cuestiones concretas de importancia en el manejo del paciente, sin pretender sustituir una evaluación ecográfica más completa por parte del cardiólogo o radiólogo cuando estas son necesarias.
Algunos autores han descrito que varias aplicaciones ecográficas presentan una curva de aprendizaje relativamente rápida, requiriendo un pequeño número de exploraciones adicionales tras una formación teórico-práctica previa17,37. Además, la EPC cuenta con la ventaja de que varias de sus aplicaciones son comunes en distintas subespecialidades, como es el caso de la ecografía pulmonar.
Con todo lo expuesto, resulta oportuno proponer la definición de unas aplicaciones mínimas de EPC a incluir en el currículo formativo del médico interno residente en pediatría y sus áreas específicas, así como en las diferentes subespecialidades pediátricas. Además, deben establecerse criterios que permitan mantener unos conocimientos actualizados en EPC, como por ejemplo un número de estudios determinados al año.
Parece necesario también proponer el posicionamiento en relación con el uso de la EPC por parte de las diferentes sociedades científicas pediátricas en España y en Europa, con el fin de dar soporte al desarrollo de programas formativos específicos que favorezcan una mayor y mejor implantación.
Finalmente, consideramos necesario continuar generando evidencia científica en relación con el uso de la EPC en las distintas áreas de la pediatría, que sirva como base para establecer recomendaciones de uso claras y programas de formación adecuados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.