Introducción
Esta Conferencia de Consenso (CC) forma parte del proyecto de investigación titulado "Estudio de la Variabilidad e Idoneidad del Manejo Diagnóstico y Terapéutico de las Infecciones del Tracto Urinario en la Infancia". Este proyecto tiene por objetivo describir la variabilidad y la idoneidad del tratamiento diagnóstico y terapéutico de la infección urinaria en la infancia en una muestra de casos pediátricos de infección del tracto urinario (ITU) identificados en los servicios de hospitalización pediátrica, urgencias, consultas y microbiología de nueve hospitales españoles. Como parte del estudio se ha realizado una conferencia de consenso para establecer los patrones de referencia de idoneidad, que se presentan en este documento.
Métodos
El grupo investigador ha realizado una revisión en profundidad de la evidencia existente sobre el diagnóstico y tratamiento de las ITU (fundamentalmente ensayos clínicos y revisiones sistemáticas; en su defecto, estudios observacionales y guías de práctica clínica), procedentes de la bibliografía internacional (MEDLINE, EMBASE, Tripdatabase, Cochrane Library) y nacional (Índice Médico Español), así como de la situación epidemiológica en España de las bacterias patógenas urinarias y de sus patrones de sensibilidad1. Producto de ello son varios documentos, que resumen la información más importante de2-8:
Métodos para la recogida de muestras de orina para urocultivo y perfil urinario.
Utilidad de los distintos parámetros del perfil urinario en el diagnóstico de ITU en niños.
Criterios de ingreso hospitalario.
Perfil etiológico de las ITU en la infancia y patrón de sensibilidad de los uropatógenos.
Tratamiento antibiótico recomendado en episodios de ITU.
Indicaciones de profilaxis antibiótica.
Pruebas diagnósticas de imagen recomendadas en ITU (ecografía, cistouretrografía miccional seriada [CUMS], gammagrafía renal DMSA, etc.), cronograma de realización recomendado.
Cada uno de los documentos tiene un apartado fundamental, titulado "bases para la toma de decisiones". En el mismo se revisan los criterios de evaluación necesarios para una posterior selección "bien informada" de los procedimientos que se deben recomendar en un contexto que podríamos llamar de "guías de buena práctica clínica". En nuestra opinión, los criterios que hay que considerar están situados en cinco niveles distintos:
Evidencia existente sobre eficacia y seguridad de los tratamientos de ITU.
Etiología de las infecciones urinarias en España. Información disponible en series españolas de casos pediátricos.
Epidemiología de las resistencias de los patógenos urinarios en España.
Evidencia sobre la validez e impacto clínico de las pruebas diagnósticas empleadas en el diagnóstico de la infección urinaria, sus factores predisponentes y sus complicaciones.
Valoración de los efectos adversos y coste económico de los procedimientos recomendados.
Para aquellos procedimientos en los que sea adecuado se establecerán las siguientes categorías en las recomendaciones:
1.Primera elección.
2.Uso alternativo.
3.Uso inapropiado o no recomendado.
Consideramos que nuestras recomendaciones deben basarse en una evaluación rigurosa de los resultados y por ello, ser explícitas acerca de cada argumentación que conduzca a una determinada recomendación. En esta línea metodológica, las recomendaciones de la CC se deben realizar clasificando su "robustez" en función de una jerarquización de la evidencia científica, que se debe aplicar cuando se evalúen los datos disponibles de eficacia, seguridad, efectividad y validez (tabla 1):
1.Recomendación basada en una evidencia científica bien demostrada (nivel de evidencia I; recomendación grado A).
2.Recomendación sugerida por una evidencia científica (nivel de evidencia II; recomendación grado B).
3.Recomendación basada en experiencia clínica y opinión de expertos (niveles de evidencia III y IV; recomendación grado C).
Se consideró oportuno denominar esta reunión "conferencia de consenso" porque tiene componentes esenciales del modelo de los National Institutes of Health de CC, a saber:
1.Un panel multidisciplinar no gubernamental.
2.Un grupo investigador que revisa y presenta los datos de la literatura tras su revisión con profundidad, con una metodología explícita y, en nuestro caso, incorpora además un sistema de jerarquización de la evidencia científica.
3.Unas preguntas específicas al panel.
4.Una elaboración de un documento de consenso que es esencialmente de "recomendaciones para la buena práctica clínica".
Para la formación del panel de expertos se han tenido en cuenta tres criterios:
1.Ser profesionales con amplia experiencia y prestigio en el ámbito de su especialidad.
2.Proporcionar un carácter multidisciplinar al panel.
3.Procurar una representación nacional equilibrada.
Se ha incorporado al panel a expertos de cada una de las siguientes áreas: nefrología pediátrica, pediatría de atención primaria, urgencias pediátricas, infectología pediátrica, cirugía y urología pediátricas, microbiología y farmacología clínica.
Métodos para la recogida de muestras de orina para urocultivo y perfil urinario
¿Cuál debe ser la técnica de recogida de orina de primera elección en el niño mayor?
En el niño mayor continente se recomienda recoger orina limpia de la mitad del chorro miccional. Este método presenta unos indicadores de validez aceptables en relación con la punción suprapúbica, pero su utilización implica la asunción de cierto riesgo de error, aunque no justificaría el empleo de técnicas más invasivas. Debe esmerarse la limpieza de los genitales externos; en los varones, la orina debe recogerse con el prepucio retirado todo lo que sea posible.
El nivel de evidencia está basado en metaanálisis de estudios de pruebas diagnósticas con limitaciones (nivel II) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Cuál debe ser la técnica de recogida de orina de primera elección en el lactante?
En el lactante y el niño incontinente debe emplearse una técnica de recogida estéril: cateterismo vesical o punción suprapúbica. En niños de bajo riesgo en los que no se requiere un diagnóstico o tratamiento inmediato, estaría justificado el empleo de técnicas no estériles, como la bolsa adhesiva perineal, insistiendo en la trascendencia de la realización de un procedimiento de recogida riguroso. En estos casos sólo sería fiable un resultado negativo; el resultado positivo debería confirmarse con una técnica más válida. El cateterismo vesical sería la técnica que considerar como primera opción (aunque no excluye cierto riesgo de contaminación), salvo en varones menores de 1 mes o niños con fimosis importante, en quienes se recomienda la punción suprapúbica.
El nivel de evidencia está basado en estudios de pruebas diagnósticas con limitaciones, estudios observacionales en los que se ha estimado el riesgo de contaminación y el bajo valor predictivo positivo de los urocultivos recogidos mediante bolsa perineal (nivel III), y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Deben establecerse diferencias en función del sexo del paciente?
No deberían establecerse diferencias en la técnica de recogida de orina en función del sexo.
El nivel de evidencia está basado en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Deben establecerse diferencias en función de la verosimilitud del diagnóstico?
Ejemplo: lactante febril sin foco y con análisis de orina patológico (nitritos, piuria).
Deben establecerse diferencias en la técnica de recogida de orina en función de la verosimilitud del diagnóstico. En el lactante febril sin foco y con análisis de orina patológico debe emplearse una técnica estéril de recogida de orina.
El nivel de evidencia está basado en estudios observacionales, en los que se han estimado el alto riesgo de contaminación y el escaso valor predictivo positivo del urocultivo recogido con técnicas no estériles (nivel III), ya que pueden comprometer el diagnóstico e interferir en el tratamiento posterior del paciente; también se ha considerado la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Cuál es la técnica de recogida de primera elección en el paciente que requiere el inicio inmediato de antibioterapia?
Debe emplearse de entrada una técnica estéril (véase la respuesta a la segunda pregunta).
En el niño con micción voluntaria podría recogerse orina limpia de la mitad del chorro miccional, salvo en los casos en que esto no sea posible.
El nivel de evidencia está basado en estudios de pruebas diagnósticas con limitaciones, estudios observacionales en los que se han estimado el riesgo de contaminación y el bajo valor predictivo positivo de los urocultivos recogidos mediante bolsa perineal (nivel III) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Deben establecerse diferencias entre atención primaria y hospitalaria?
No debería haber diferencias en la técnica de recogida de orina en función del medio asistencial (atención primaria u hospital). No obstante, el panel de expertos reconoce que la disponibilidad de medios no es la misma en todos los lugares, por lo que este hecho puede condicionar la elección de la técnica de recogida de orina.
El nivel de evidencia está basado en la opinión de expertos IV.
Grado de recomendación propuesto: C.
Si obtenemos un urocultivo positivo con una técnica de recogida de orina no estéril, ¿debemos confirmarlo con alguna técnica más válida? ¿es suficiente con la repetición de la misma muestra?
Un urocultivo recogido con bolsa adhesiva perineal que resulte positivo debe ser confirmado con una técnica más válida (véase la respuesta a la segunda pregunta).
El nivel de evidencia está basado en estudios observacionales, en los que se han estimado el alto riesgo de contaminación y el escaso valor predictivo positivo del urocultivo recogido con técnicas no estériles (nivel III), y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Debe cambiar el tratamiento del paciente en función del grado de validez de la técnica de recogida de orina empleada en el diagnóstico?
La validez del diagnóstico debe influir en el tratamiento del paciente con ITU. La verosimilitud del diagnóstico puede influir en la actuación inmediata (tratamiento) y posterior del paciente (pruebas de imagen solicitadas), dado que influye en la probabilidad preprueba, no sólo del propio diagnóstico de ITU, sino, además, de los posibles diagnósticos asociados.
El nivel de evidencia está basado en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
Utilidad de los distintos parámetros del perfil urinario en el diagnóstico de ITU en niños
¿Existe algún parámetro urinario o combinación de parámetros que en alguna circunstancia permita establecer el diagnóstico de ITU, sin recurrir al urocultivo?
Es opinión consensuada mayoritaria que el diagnóstico de ITU siempre debe basarse en el resultado del urocultivo. Es preciso tener en cuenta que existirán pacientes con alto riesgo y verosimilitud de tener una ITU en los cuales el urocultivo podría resultar negativo.
Sin embargo, algún miembro del panel considera que en el paciente mayor de 3 años el hallazgo simultáneo de nitritos y leucocitos en una tira de orina o bien de piuria y bacteriuria en un examen microscópico permitiría asumir el diagnóstico de ITU sin recurrir a urocultivo (salvo que se considere necesario para conocer la sensibilidad del microorganismo implicado).
El nivel de evidencia está basado en las limitaciones de los parámetros del análisis urinario (nivel I) y en la importancia de la información microbiológica para el tratamiento diagnóstico y terapéutico de la ITU en la infancia (nivel II).
Grado de recomendación propuesto: A.
En el lactante febril ¿qué parámetros o combinación de parámetros sugieren el diagnóstico de ITU y aconsejan el inicio de tratamiento empírico?
La interpretación del análisis de orina está condicionada por la calidad de la técnica de recogida utilizada. La presencia en la orina de nitritos o bacteriuria implica un alto riesgo de ITU y justificaría el inicio de tratamiento en el lactante febril, después de la recogida de un urocultivo mediante técnica adecuada. La presencia de leucocitos en orina implica un riesgo medio-bajo de ITU. No obstante, el panel de expertos opina que la leucocituria, en orinas recogidas con técnica válida, justificaría el inicio de tratamiento empírico en el lactante febril. Por otra parte, la ausencia de nitritos, bacteriuria o leucocitos no permite descartar la existencia de ITU.
No obstante, algún miembro del panel considera que, en niños mayores de 3 años, la ausencia simultánea de nitritos y leucocitos en la tira reactiva (o de piuria y bacteriuria en el examen microscópico) permitiría descartar una ITU.
El nivel de evidencia está basado en metaanálisis de numerosos estudios de pruebas diagnósticas con algunas limitaciones metodológicas (nivel I-II) y en la opinión de expertos (grado IV).
Grado de recomendación propuesto: B.
¿Debe condicionar el resultado del análisis de orina la técnica de recogida de orina para cultivo?
El resultado del análisis de orina debe condicionar la técnica de recogida de orina para cultivo, ya que un análisis patológico incrementa la probabilidad preprueba de ITU. En el lactante febril sin foco y con análisis de orina patológico debe emplearse una técnica estéril de recogida de orina (véase la respuesta a la cuarta pregunta del apartado de recogida de orina).
El nivel de evidencia está basado en el alto riesgo de contaminación y el escaso valor predictivo positivo del urocultivo recogido con técnicas no estériles (nivel III), que pueden comprometer el diagnóstico e interferir en el tratamiento posterior del paciente, y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
En presencia de alteraciones en la tira reactiva, ¿es necesario recurrir al examen microscópico de la orina?
En presencia de alteraciones en la tira reactiva urinaria no es necesario recurrir al examen microscópico. No obstante, podría resultar útil la realización de un examen microscópico de orina no centrifugada con tinción de Gram en el tratamiento de la ITU del lactante (identificación de bacteriuria y microorganismos grampositivos), salvo que la tira muestre previamente la presencia de nitritos (poco frecuente dado el escaso tiempo de retención urinaria a esta edad). En ningún caso debe olvidarse enviar muestra para urocultivo.
El nivel de evidencia está basado en metaanálisis de estudios de pruebas diagnósticas con algunas limitaciones metodológicas (nivel I-II) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Debe influir el resultado del análisis de orina en el tipo de tratamiento y seguimiento que reciban los pacientes con ITU?
La verosimilitud del diagnóstico puede influir en la actuación inmediata (tratamiento) y posterior del paciente (pruebas de imagen solicitadas), puesto que influye en la probabilidad preprueba, no sólo del propio diagnóstico de ITU, sino además de los posibles diagnósticos asociados.
El nivel de evidencia está basado en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
Criterios de ingreso hospitalario.
¿Cuáles son los criterios de ingreso hospitalario en un niño con ITU? ¿Deben basarse en la sospecha de pielonefritis? ¿Qué criterios clínicos aconsejan la hospitalización?
La sospecha de pielonefritis no debe considerarse un criterio absoluto de ingreso hospitalario. Se consideran criterios generales que indican el ingreso hospitalario en pacientes con ITU (la presencia de alguno de los siguientes):
Edad inferior a 3 meses.
Afectación del estado general (signos de deshidratación, decaimiento o disminución de la respuesta a estímulos, palidez, piel moteada, etc.).
Intolerancia de la medicación o alimentación oral.
Sospecha de mal control del tratamiento en el entorno familiar
Antecedentes de inmunodeficiencia, uropatía o nefropatía grave (reflujo de alto grado, o alteración de la función renal).
El nivel de evidencia está basado en un metaanálisis de ensayos clínicos con alguna limitación (nivel I), estudios observacionales de series de ITU que permiten estimar bajo riesgo de sepsis urinaria (nivel III) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Pueden establecerse límites de edad para aconsejar el ingreso hospitalario de niños con ITU? ¿Deben estos límites tener en cuenta la presencia de fiebre o de signos de pielonefritis?
Se recomienda ingresar a los niños con ITU menores de 3 meses. La presencia de fiebre o signos de pielonefritis no establece puntos de corte de edad a partir de la cual deban ser ingresados o no los niños con ITU.
El nivel de evidencia está basado en estudios observacionales de series de ITU que permiten estimar bajo riesgo de sepsis urinaria (nivel III) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Debe considerarse la concentración plasmática de procalcitonina o de otros parámetros en la elección de la vía de administración de antibióticos y, en consecuencia, en la decisión de ingreso hospitalario?
La decisión de ingresar o no un niño con ITU no debe sustentarse, de forma exclusiva, en los resultados de los parámetros analíticos asociados a la existencia de pielonefritis. No obstante, deben ser tenidos en cuenta a la hora de valorar la posible repercusión sistémica de la ITU, la alteración de la función renal, el inicio inmediato de antibioterapia, el tipo de tratamiento y el seguimiento posterior.
El nivel de evidencia está basado en metaanálisis de estudios de pruebas diagnósticas con algunas limitaciones (nivel II) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Pueden ser tratados con antibiótico oral en su domicilio los niños con buen estado general y sospecha de pielonefritis aguda? ¿Debe modificarse este criterio en función de la edad?
Pueden tratarse inicialmente con antibiótico oral en su domicilio los niños con buen estado general y sospecha de pielonefritis aguda, salvo los menores de 3 meses o los que presenten factores de riesgo asociados, que aconsejen el ingreso hospitalario. Si la evolución es favorable se evitará el ingreso de muchos niños que actualmente se tratan hospitalariamente.
El nivel de evidencia está basado en un metaanálisis de ensayos clínicos con alguna limitación (nivel I), estudios observacionales de series de ITU que permiten estimar bajo riesgo de sepsis urinaria (nivel III) y opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
Tratamiento antibiótico recomendado en episodios de ITU
¿Debe diferenciarse el tratamiento de la ITU en la infancia en función del nivel de riesgo del paciente? ¿Podemos seleccionar el tipo de tratamiento en función de la clínica del paciente, su edad o la necesidad de hospitalización?
Debe diferenciarse el tratamiento de la ITU en la infancia en función del nivel de riesgo del paciente, considerando la siguiente información:
Necesidad de ingreso hospitalario (véase el apartado previo).
Antecedentes de riesgo: malformaciones de vías urinarias, inmunodeficiencias, ITU o episodios febriles repetidos.
ITU con afectación sistémica o signos-síntomas de pielonefritis: fiebre elevada, dolor lumbar o abdominal, vómitos, irritabilidad, rechazo de la alimentación o frialdad.
La necesidad de ingreso hospitalario, más que la existencia o no de pielonefritis, va a condicionar la utilización de tratamiento intravenoso, al menos durante los primeros días. Sin embargo, la sospecha de pielonefritis sí que va a influir en la elección del antibiótico y la duración del tratamiento. Los antecedentes de riesgo deberán ser valorados individualmente, junto a la clínica del paciente, para considerar el ingreso y tipo de tratamiento. Por otra parte, la elección de tratamiento en los pacientes con sospecha de pielonefritis y reflujo vesicoureteral de alto grado (III-V) tendrá que ser individualizada.
El nivel de evidencia está basado en un metaanálisis de ensayos clínicos con alguna limitación (nivel I) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Qué antibióticos deben ser considerados como de primera elección y alternativos en la ITU en la infancia? ¿Debe diferenciarse en función del nivel de riesgo?
Tratamiento intravenoso empírico:
Se consideran tratamientos de primera elección gentamicina o tobramicina, en dosis única diaria, asociadas en los menores de 1 mes a ampicilina (salvo que la tinción de Gram no observe cocos grampositivos). A las 48-72 h se reconsiderará el tratamiento en función de la evolución, y especialmente de los resultados del urocultivo y antibiograma. Puede optarse por un cambio de grupo de antibiótico si lo aconseja el antibiograma. En los niños con nefropatía instaurada los aminoglucósidos serán sustituidos por cefotaxima o ceftriaxona.
Se consideran tratamientos alternativos cefotaxima o ceftriaxona, asociados a ampicilina en menores de 1 mes. Se consideran también alternativas válidas amoxicilina-ácido clavulánico o cefuroxima intravenosas, salvo en aquellas áreas con resistencia de Escherichia coli a estos antimicrobianos por encima del 10-20 %. Para algún miembro del panel, la jerarquización aminoglucósidos (primera elección)-cefalosporinas (alternativas) podría ser cuestionada si se considera la mayor toxicidad de los aminoglucósidos.
Otros antibióticos deberán ser reservados a circunstancias especiales en las que haya información microbiológica que haga aconsejable una elección antibiótica específica (amikacina, fluoroquinolonas, ceftazidima, carbapenémicos).
Tratamiento oral empírico:
En aquellas ITU en que no pueda descartarse una infección de vías altas (pielonefritis) se considera tratamiento de primera elección una cefalosporina de tercera generación oral.
Se consideran tratamientos alternativos en estas ITU: amoxicilina-ácido clavulánico y las cefalosporinas de segunda generación oral.
En los niños mayores (> 2 años) con clínica de cistitis serían tratamientos de primera elección amoxicilina-ácido clavulánico, nitrofurantoína (niños mayores que tomen tabletas), fosfomicina y fosfomicina-trometamol.
Se considerarán tratamientos alternativos en cistitis las cefalosporinas orales de primera, segunda y tercera generaciones.
El uso de fluoroquinolonas queda reservado a su empleo en circunstancias seleccionadas y guiado por antibiograma.
El nivel de evidencia está basado en ensayos clínicos con alguna limitación (nivel I), en información epidemiológica sobre la etiología de las ITU y la sensibilidad de los uropatógenos en la infancia (nivel II), además de en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: A para los tratamientos de primera elección grado B para el resto.
¿Cuál es la vía de administración de antibióticos (inicial y de continuación) más apropiada? ¿Debe diferenciarse en función del nivel de riesgo?
En los pacientes de alto riesgo que requieren ingreso hospitalario se recomienda emplear la vía intravenosa, al menos como tratamiento inicial (durante 2-3 días) o según la evolución. Puede emplearse tratamiento oral para el tratamiento de las ITU en general, tanto pielonefritis como cistitis.
La elección de la vía de tratamiento inicial en los pacientes con sospecha de pielonefritis y reflujo vesicoureteral de grados III-V tendrá que ser individualizada.
La utilización de pautas de antibioterapia parenteral ambulatoria (uno o más días) con una dosis diaria de ceftriaxona, gentamicina o tobramicina, seguida de antibioterapia oral, podría ser una alternativa al tratamiento oral.
El nivel de evidencia está basado en un metaanálisis de ensayos clínicos con alguna limitación (nivel I) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Cuál es la pauta de administración de antibióticos (número de dosis/día) más apropiada? ¿Debe diferenciarse en función del nivel de riesgo?
Los aminoglucósidos se administrarán en dosis única diaria. No hay información que permita recomendar la utilización de dosis más espaciadas de las habitualmente recomendadas con otros grupos de antibióticos.
El nivel de evidencia está basado en metaanálisis de ensayos clínicos con alguna limitación (nivel I), en estudios de farmacocinética-farmacodinámica (nivel III) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: A.
¿Cuál es la duración de la antibioterapia más apropiada? ¿Debe diferenciarse en función del nivel de riesgo?
Las pautas cortas de tratamiento antibiótico (3-5 días) sólo se recomiendan para el tratamiento de las ITU de bajo riesgo o cistitis. La duración del tratamiento de las ITU de alto riesgo o pielonefritis será superior a 7 días (7-14 días).
En el niño menor de 2 años es recomendable realizar tratamientos prolongados, aunque pensemos que pueda tener una ITU de bajo riesgo (difíciles de diagnosticar pues suelen tener fiebre asociada) ya que tienen mucho mayor riesgo de cicatriz si la ITU no evoluciona bien (opinión de experto).
No existe información que permita diferenciar la eficacia de pautas de 7-10 días con las de mayor duración.
No se recomienda la repetición del urocultivo en el curso del tratamiento para valorar la respuesta o duración del mismo, salvo en los casos en los que la evolución sea desfavorable.
El nivel de evidencia está basado en metaanálisis de ensayos clínicos con alguna limitación (nivel I), en estudios de farmacocinética-farmacodinámica (nivel III) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: A.
Indicaciones de profilaxis antibiótica
¿Está indicada la profilaxis con antibióticos en niños con tracto urinario normal tras un primer episodio de infección urinaria?
No se recomienda la profilaxis con antibióticos de forma sistemática en niños con tracto urinario normal tras un primer episodio de infección urinaria.
La profilaxis no se recomienda pero no puede considerarse inapropiada, en tanto que no sepamos si existe reflujo de alto grado. Podría usarse hasta la realización de ecografía o CUMS, siempre que estas pruebas no se demoraran más de un mes.
El nivel de evidencia está basado en metaanálisis de ensayos clínicos con importantes limitaciones y un ensayo clínico posterior (nivel I), así como en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
¿Está indicada la profilaxis con antibióticos en niños con reflujo vesicoureteral tras un primer episodio de infección urinaria?
En pacientes con reflujos vesicoureterales grados I-III, no se recomienda la profilaxis antibiótica. No obstante, dado que sólo se ha evaluado en un trabajo y con período de seguimiento corto, no se puede considerar inadecuada la profilaxis, al menos en reflujos de grado II-III.
A pesar de la ausencia de información suficientemente válida que lo apoye, se recomienda la utilización de profilaxis antibiótica en los casos de reflujo grados IV-V, al menos durante un año, continuando en función de la existencia de recaídas de ITU y la evolución del reflujo.
El nivel de evidencia está basado en un ensayo clínico de pequeño tamaño y corto período de seguimiento (nivel I) para los reflujos de grado I-III y en la opinión de expertos (nivel IV) para los reflujos IV-V.
Grado de recomendación propuesto: B para la profilaxis en reflujos grado I-III; grado C para los reflujos grado IV-V.
¿Está indicada la profilaxis con antibióticos en niños con cicatrices renales en ausencia de reflujo vesicoureteral tras un primer episodio de infección urinaria?
No está indicada la profilaxis antibiótica en niños con cicatrices renales en ausencia de reflujo vesicoureteral tras un primer episodio de infección urinaria.
El nivel de evidencia está basado en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
¿Está indicada la profilaxis con antibióticos en niños con infecciones del tracto urinario recurrentes?
No hay información en la que sustentar las recomendaciones sobre la utilidad de la profilaxis en pacientes con ITU recurrentes. Se recomienda valorar individualmente su indicación. Considerar el diagnóstico y tratamiento de disfunción vesical en estos pacientes.
El nivel de evidencia está basado en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: C.
Si está indicada la profilaxis, ¿qué antibiótico utilizar y durante cuánto tiempo? ¿Qué antibióticos serían de primera elección y cuáles alternativos?
Se consideran antibióticos apropiados para profilaxis la nitrofurantoína (en niños mayores que tomen tabletas), fosfomicina, trimetoprim y cotrimoxazol (trimetoprim-sulfametoxazol).
En menores de un mes, podría emplearse amoxicilina o amoxicilina-ácido clavulánico.
Serían antibióticos de primera elección nitrofurantoína y trimetoprim, salvo en el neonato, que sería amoxicilina.
Amoxicilina, amoxicilina-ácido clavulánico, o cefalosporinas orales de primera, segunda o tercera generaciones sólo se deben usar en situaciones excepcionales, pues implican un alto riesgo de desarrollo de resistencias bacterianas. No obstante, no podemos considerarlos medicamentos inapropiados, ya que pueden necesitarse cuando otros preparados han fallado o no son tolerados.
El nivel de evidencia está basado en ensayos clínicos con algunas limitaciones (nivel I), en información epidemiológica sobre la etiología y sensibilidad de los uropatógenos en la infancia (nivel II) y en la opinión de expertos (nivel IV).
Grado de recomendación propuesto: B.
Pruebas diagnósticas de imagen recomendadas en ITU (ecografía, CUMS, gammagrafía renal DMSA, etc.); cronograma de realización recomendado
Las siguientes preguntas son contestadas en conjunto:
• ¿Está indicada la realización de ecografía renal después de una primera ITU? ¿Debe realizarse en la fase aguda o se puede hacer de forma diferida? ¿Existe algún criterio clínico que permita precisar estas recomendaciones (edad, fiebre, sexo, lugar de asistencia, analítica o evolución)?
• ¿Debe realizarse cistografía de forma habitual después de una primera ITU? ¿Debe realizarse CUMS o puede sustituirse por pruebas alternativas (ecocistografía, cistografía isotópica indirecta)? ¿En qué momento debe efectuarse? ¿Existe algún criterio clínico que permita precisar estas recomendaciones (edad, fiebre, sexo, lugar de asistencia, analítica o evolución)?
• ¿Debe recomendarse la realización de gammagrafía DMSA en la fase aguda de una ITU? ¿Existe algún criterio clínico que permita precisar estas recomendaciones (edad, fiebre, sexo, lugar de asistencia, analítica o evolución)?
• ¿Debe realizarse gammagrafía DMSA diferida después de una primera ITU? ¿En qué momento debe efectuarse? ¿Existe algún criterio clínico que permita precisar estas recomendaciones (edad, fiebre, sexo, lugar de asistencia, analítica o evolución)?
• Ante la existencia de ITU recurrentes, ¿debe indicarse alguna prueba previamente no realizada o está justificada la repetición de otras ya disponibles?
• En los niños mayores con clínica de cistitis ¿está indicada la realización de alguna prueba de imagen?
• ¿Debe hacerse alguna recomendación concreta en cuanto a otras pruebas de imagen?
Considerando, por un lado, la información disponible sobre la limitada validez de la ecografía para el diagnóstico de pielonefritis, reflujo vesicoureteral y daño renal, la escasa utilidad clínica de la DMSA en fase aguda, así como la inviabilidad de su empleo habitual y los inconvenientes de la CUMS y, por otro lado, la carencia de información sobre el impacto real que puedan tener en los pacientes los diagnósticos que estas pruebas nos ofrecen (pielonefritis, reflujo vesicoureteral y daño renal), el panel de expertos opina que debe cambiarse la actual estrategia de uso habitual de estas pruebas por otra en la que sólo se indiquen de forma individualizada, considerando el nivel de riesgo de cada paciente.
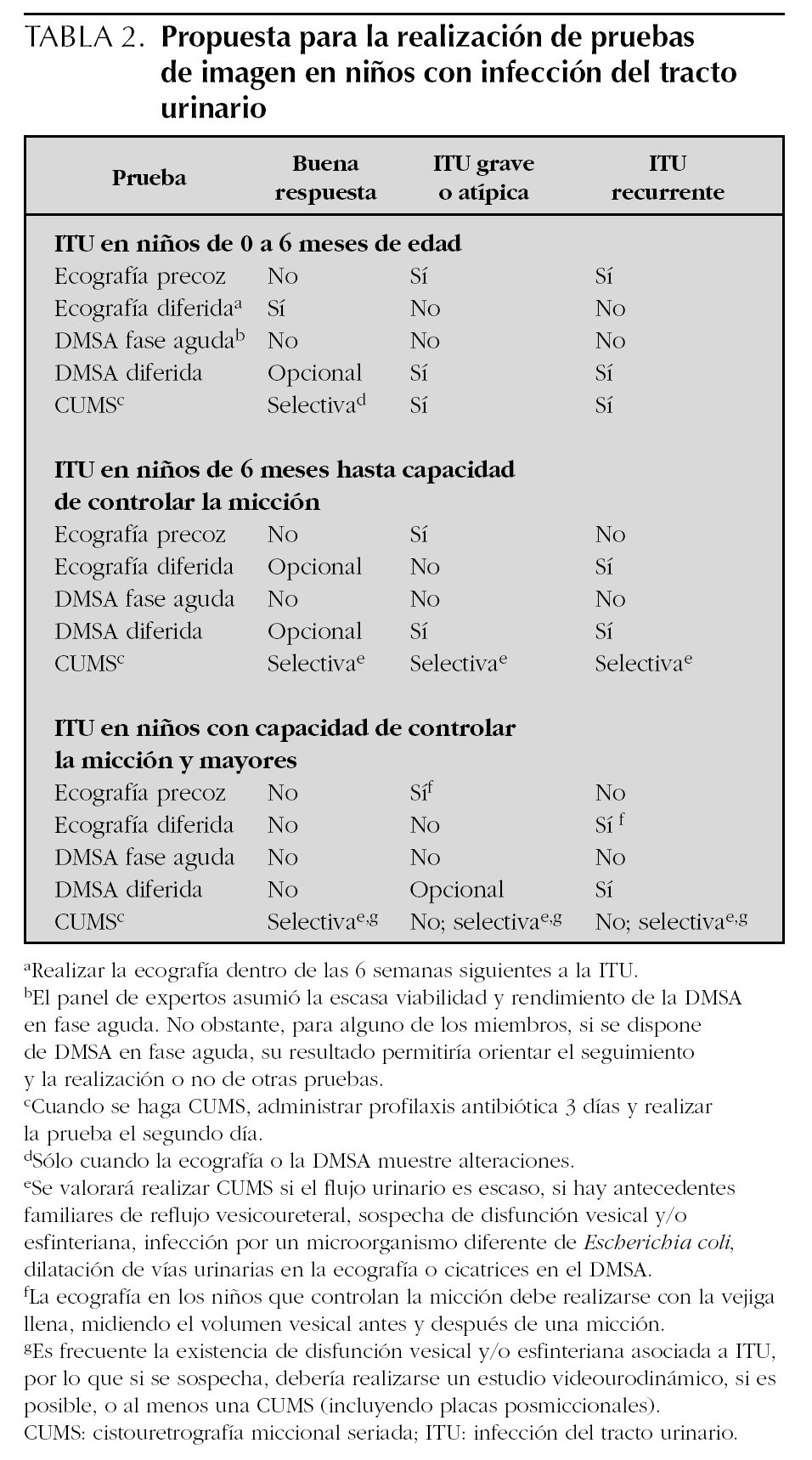
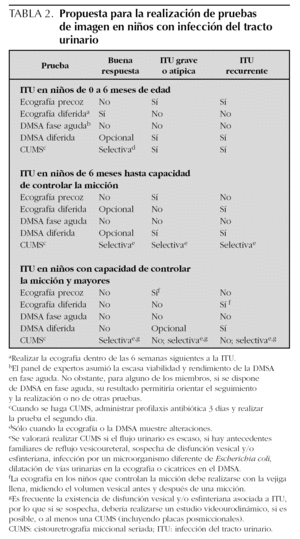
En ausencia de evidencia en la que sustentar estrategias concretas de diagnóstico aplicables a nuestro entorno, se ha valorado la categorización propuesta por el National Collaborating Centre for Women's and Children's Health9, comisionado por el National Institute for Health and Clinical Excellence (NICE) en 2006, pero incorporando indicaciones opcionales o selectivas, según el criterio del panel de expertos. Las recomendaciones se recogen en la tabla 2.
Esta propuesta diferencia las recomendaciones en función de la edad del paciente, la capacidad del niño para controlar la micción, la existencia de ITU recurrentes o la existencia de ITU graves o atípicas. Se considera ITU atípica la que cursa con persistencia de fiebre a las 48 h de tratamiento adecuado, con flujo urinario escaso (elevación de creatinina o baja capacidad de concentración urinaria) o que es debida a un microorganismo diferente de E. coli. Se considera ITU recurrente cuando hay dos o más episodios de ITU con síntomas o signos, o tres o más ITU sin síntomas o signos.
El nivel de evidencia está basado en metaanálisis de estudios de pruebas diagnósticas con algunas limitaciones (nivel II) y en la opinión de expertos (nivel IV). No existe evidencia suficiente en la que sustentar la estimación del impacto clínico de los diagnósticos que ofrecen estas pruebas diagnósticas.
Grado de recomendación propuesto: C.
Miembros del Panel de Expertos de la Conferencia de Consenso
S. Málaga Guerrero (Nefrología Pediátrica, Oviedo); J. Ignacio Alós (Microbiología, Madrid); J. Benito Fernández (Urgencias Pediátricas, Bilbao); I. Danés Carreras (Farmacología Clínica, Barcelona); J. Escribano Subías (Nefrología Pediátrica, Reus, Tarragona); C. Loris Pablo (Nefrología Pediátrica, Zaragoza); C. Miguélez Lago (Urología-Cirugía Pediátrica, Málaga); J. Ruiz Canela (Pediatría de Atención Primaria, Sevilla); y J. Ruiz Contreras (Infectología Pediátrica, Madrid).
Miembros del Grupo Investigador del Proyecto "Estudio de la Variabilidad e Idoneidad del Manejo Diagnóstico y Terapéutico de las Infecciones del Tracto Urinario en la Infancia"
C. Ochoa Sangrador (Hospital Virgen de la Concha, Zamora); C. Pérez Méndez y G. Solís Sánchez (Hospital de Cabueñes, Gijón, Asturias); J.C. Molina Cabañero y J. Lara Herguedas (Hospital del Niño Jesús, Madrid); F. Conde Redondo, R. Bachiller Luque, J.M.ª Eiros Bouza, V. Matías del Pozo y B. Nogueira González (Hospital Clínico Universitario, Valladolid); M.ªC. Urueña Leal, J.M. Andrés de Llano, P. Rostami y J.F. Sáenz Martín (Complejo Asistencial de Palencia); E. Formigo Rodríguez, M. Cueto Baelo y M.ªC. González Novoa (Hospital Xeral-Cies, Vigo, Pontevedra); N. Silva Higuero y H. González García (Hospital de Medina del Campo, Valladolid); J. González de Dios (Hospital de Torrevieja, Alicante); M. Brezmes Raposo (Hospital La Fe, Valencia); M.ªM. Urán Moreno y J.M. Gea Ros (Hospital Universitario San Juan, Alicante); M.ªV. Barajas Sánchez, M.ªF. Brezmes Valdivieso y M.ªA. Fernández Testa (Hospital Virgen de la Concha, Zamora).
Financiado parcialmente por una beca de la Gerencia Regional de Salud de la Junta de Castilla y León (año 2006).
Correspondencia: Dr. C. Ochoa Sangrador.
Unidad de Investigación. Hospital Virgen de la Concha.
Avda. Requejo, 35. 49029 Zamora. España.
Correo electrónico: cochoas@meditex.es
Recibido en mayo de 2007.
Aceptado para su publicación en junio de 2007.