Los fármacos inhibidores del factor de necrosis tumoral alfa se usan cada vez más frecuentemente en la práctica clínica diaria. Han mostrado su efectividad en el tratamiento de trastornos de base inflamatoria mediada por el sistema inmunitario, principalmente enfermedades reumáticas, pero también en la enfermedad inflamatoria intestinal y en la psoriasis.
En los últimos años se han descrito diversos efectos secundarios, entre los cuales se encuentra el desarrollo, que resulta paradójico, de psoriasis o exantemas psoriasiformes.
Desde finales de los noventa, la extensión de estos fármacos a la edad pediátrica es un hecho, y es necesario que los pediatras conozcamos los fenómenos adversos que pueden producir.
Describimos aquí un caso de psoriasis invertida secundaria al tratamiento con infliximab y adalimumab en un paciente de 13 años con enfermedad de Crohn. Hasta donde llegamos a conocer, se trata del primer caso comunicado en edad pediátrica, así como el primer caso desencadenado por adalimumab en la enfermedad inflamatoria intestinal.
Anti-TNF drugs are used increasingly in several diseases with immune-mediated inflammation, not only in rheumatological conditions, but also in inflammatory bowel disease and psoriasis.
Different side effects have been described over the last few years, including the development of psoriasis or psoriasiform exanthemas.
These drugs began to be used in paediatrics during the 90's, therefore paediatricians need to be aware of the adverse effects that may occur.
We describe here a flexural psoriasis induced by both infliximab and adalimumab in a paediatric patient with Crohn's Disease. To the best of our knowledge, this is the first reported paediatric case of psoriasis triggered by an anti-TNF drug, as well as the first case of psoriasis induced by adalimumab in patients with inflammatory bowel disease.
Actualmente hay en el mercado 3 fármacos inhibidores del factor de necrosis tumoral alfa (TNFα), 2 anticuerpos monoclonales, infliximab y adalimumab, y un inhibidor competitivo de la unión del TNF a sus receptores de superficie, etanercept. Estos fármacos anti-TNF están siendo utilizados en múltiples trastornos de base inflamatoria mediada inmunológicamente, sobre todo enfermedades reumatológicas. En los últimos años, infliximab se ha usado con éxito en el tratamiento de la enfermedad de Crohn (EC) resistente a los corticoides en niños1,2, y más recientemente se han publicado estudios esperanzadores acerca del uso de adalimumab en la enfermedad inflamatoria intestinal (EII), tanto en niños como en adultos3,4.
Aunque en general son fármacos bien tolerados, la extensión de su uso conllevó la descripción de diversos efectos secundarios5, como el riesgo de infecciones potencialmente graves, neuritis óptica, anemia aplásica, etc., y múltiples efectos cutáneos adversos, eccemas, síndromes lupus-like, eritema y edema local, lesiones malignas, vasculitis e incluso psoriasis.
Dado que estos fármacos han demostrado su efectividad en el tratamiento de la psoriasis vulgar y la artritis psoriásica6–8, resulta paradójico que se los haya relacionado con el desarrollo de lesiones psoriasiformes, muchas de ellas con componente pustular. Desde el año 2003 se han publicado diversos casos que describen la aparición de psoriasis en pacientes tratados con anti-TNF. Mediante una búsqueda con la herramienta MEDLINE encontramos un total de 38 artículos que describen a más de 100 pacientes5,8–13. Ahora bien, si la búsqueda se restringe a los que presentaban EC de base, el número se reduce a 14 casos en sólo 8 artículos, todos ellos en pacientes adultos y en relación con infliximab14–20.
Presentamos el primer caso pediátrico de psoriasis desencadenada por un anti-TNF, así como el primer caso publicado de psoriasis producida por adalimumab en pacientes con EII.
Observación clínicaPaciente de 13 años de edad, diagnosticado de EC a los 7 años. Entre los antecedentes familiares destaca psoriasis y EC en rama materna. Tratado con corticoides sistémicos y azatioprina, a pesar de lo cual persiste la afección ileocólica con importante afección perianal, además de anemia microcítica y estancamiento ponderal.
Se inicia tratamiento con infliximab en junio de 2006; después de la tercera dosis aparecen lesiones cutáneas eritemato-descamativas, pruriginosas, que afectan predominantemente a las áreas flexurales: axilas, fosa cubital anterior, hueco poplíteo, región inguinal, además de tórax y cuero cabelludo.
Dichas lesiones eran clínicamente características de psoriasis invertida, y desaparecieron en pocas semanas al cesar el tratamiento con infliximab. El mal control de la enfermedad, en situación de corticorresistencia, nos llevó a iniciar adalimumab en marzo de 2007. Tras la séptima dosis, desarrolló un intenso brote de psoriasis invertida. Las lesiones se resolvieron parcialmente con el uso de corticoides tópicos, mientras se continuó el tratamiento con adalimumab.
DiscusiónLa psoriasis es una enfermedad inflamatoria crónica de la piel, en la cual la producción de citocinas mediada por las células T conlleva una proliferación de queratinocitos y un aumento de la angiogénesis tisular. A pesar de que el TNFα es una molécula esencial en la cascada inflamatoria que desencadena la psoriasis, recientemente se ha relacionado su inhibición farmacológica con la inducción de psoriasis.
Dado que los primeros casos se han descrito en pacientes con trastornos reumatológicos, principalmente artritis reumatoidea, se planteó la posibilidad de que estos casos fuesen realmente artritis psoriásicas no diagnosticadas, cuyas manifestaciones articulares habrían precedido a las cutáneas9,21. O bien que se tratase de una simple casualidad, dado que la psoriasis ha demostrado ser algo más frecuente en pacientes con trastornos reumatológicos de base13. El número creciente de publicaciones al respecto en los últimos años, así como la relación temporal con la administración del fármaco y su aparición con distintos anti-TNF, ha llevado a estudiar el desarrollo de psoriasis como un posible efecto de clase de este grupo farmacológico.
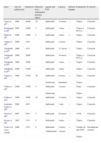
En la tabla 1 se esquematizan los casos publicados de psoriasis desencadenada por anti-TNF en pacientes que recibían el fármaco por una EC. Como se puede observar, hay un claro predominio del sexo femenino y la edad es variable. Sólo en uno de los casos constan antecedentes familiares de psoriasis. El período de latencia desde la introducción del fármaco varió desde las 4 semanas a los 5 años. En la mayoría de los casos no fue necesaria la suspensión del anti-TNF para conseguir la resolución de las lesiones, que evolucionaron favorablemente con el uso de corticosteroides tópicos.
Casos publicados de psoriasis inducida por un inhibidor del factor de necrosis tumoral (TNF) en pacientes con enfermedad de Crohn
| Autor | Año de publicación | Edad/sexo | Duración de la enfermedad primaria (años) | Agente anti-TNF | Latencia | Historia familiar | Tratamiento | Evolución |
| Verea et al15 | 2004 | 46/M | 20 | Infliximab | 12 meses | − | Tópico | Curación |
| Peramiquel et al16 | 2005 | 29/M | 3 | Infliximab | 3 años | − | Tópico y PUVA | Curación |
| Pirard et al17 | 2006 | 19/M | 5 | Infliximab | 3 años | + | Tópico | Curación |
| Adams et al19 | 2006 | 19/V | Infliximab | 2 meses | Tópico | Curación | ||
| Takahashi et al18 | 2006 | 21/V | Infliximab | 1,5 meses | − | Tópico | Curación | |
| Takahashi et al18 | 2006 | 29/M | Infliximab | 10 meses | − | Tópico y PUVA | Curación | |
| Takahashi et al18 | 2006 | 30/M | Infliximab | 5 años | − | Tópico | Curación | |
| Takahashi et al18 | 2006 | 42/M | Infliximab | 4 años | Tópico | Curación | ||
| Cohen et al14 | 2006 | 53/M | 20 | Infliximab | 6 meses | + | Tópico | Curación |
| Etanercept | Inmediato | Tópico | ||||||
| Cohen et al14 | 2006 | 32/M | 4 | Infliximab | 2 meses | − | Nada | Curación |
| Etanercept | Tópico | |||||||
| Cohen et al14 | 2006 | 56/M | 28 | Infliximab | 11 meses | − | Tópico | Curación |
| González-López et al25 | 2006 | 39/V | Infliximab | 1 año | − | Tópico | Curación | |
| Severs et al24 | 2007 | 38/V | 3 | Infliximab | 42 meses | − | UVB | Curación |
| Severs et al24 | 2007 | 21/V | 6 | Infliximab | 4 años | − | Tópico | Curación |
| Ávila et al (caso actual) | 2008 | 13/V | 6 | Infliximab | 2 meses | + | Cambio de anti-TNF | Parcialmente resuelto |
| Adalimumab | 3 meses | |||||||
| Tópico |
M: mujer; V: varón.
Todos los casos implicaban al infliximab como agente desencadenante, y en dos de ellos además aparecieron las lesiones cutáneas con el uso de etanercept.
No hemos encontrado ningún caso publicado de pacientes pediátricos, y ninguno en relación con adalimumab en pacientes con EII.
La fisiopatología subyacente a este proceso permanece todavía sin aclarar, aunque todo parece indicar que el interferón alfa (IFNα) tiene un papel esencial.
El TNFα regula la producción de IFNα, de hecho, la neutralización del TNF aumenta la producción de IFNα por parte de las células dendríticas plasmocitoides (PDC) y aumenta la expresión de receptores de citocinas, como CXCR3 en las células T circulantes, promoviendo la migración hacia la piel de estas células autorreactivas9,10,13,22. En modelos animales se ha demostrado que la aparición de PDC e IFNα en la piel es el primer paso en el desarrollo de psoriasis23. Recientemente se ha demostrado el incremento de IFNα en la vasculatura de la lesión psoriásica, así como infiltrados linfocíticos perivasculares13,21.
Según estos hallazgos, se ha propuesto que la inhibición del TNF produciría una expresión tisular aberrante de IFNα en individuos predispuestos. El retraso entre la introducción del anti-TNF y la aparición de las lesiones cutáneas indica que éste sería sólo uno de los factores a tener en cuenta13,21.
De una revisión profunda del tema podemos extraer una serie de conclusiones. Primero, la aparición de psoriasis es un probable efecto de clase de los fármacos anti-TNF, ya que se ha descrito con los tres fármacos, así como en la mayoría de las enfermedades en que es común su uso. Segundo, la aparición de este efecto secundario parece ser más frecuente en las mujeres y en la edad media de la vida. Tercero, en la mayoría de los casos no hay antecedentes familiares ni personales de psoriasis. Cuarto, no siempre es necesaria la suspensión del anti-TNF ni su cambio a otro fármaco del grupo, ya que en muchas ocasiones se controla con tratamientos tópicos. Quinto, hay gran variabilidad en cuanto a la latencia entre la introducción del fármaco y la aparición de psoriasis, fenómeno que permanece todavía inexplicado. Sexto, se necesitan nuevos estudios y publicación de nuevos casos para elucidar la fisiopatología subyacente, en la que la sobreexpresión de IFNα parece tener un papel importante. Séptimo, creemos que es necesario que los pediatras generales y gastroenterólogos, en particular, conozcan estos efectos secundarios, dado el uso cada vez más frecuente de estos tratamientos en la edad pediátrica.