Introducción
La fiebre sin focalidad (FSF) es uno de los motivos de consulta más frecuente en los servicios de urgencias pediátricos (SUP)1.
Se define FSF como el registro de temperatura rectal superior a 38 °C, en un niño en el que tras haber efectuado una historia clínica y una exploración física cuidadosa, no se evidencia la causa de la fiebre (no cuadro catarral, clínica respiratoria ni proceso diarreico)2. En la mayoría de los casos, la FSF está causada por infecciones virales, pero en ocasiones puede presentarse en forma de bacteriemia oculta y ésta puede conducir a complicaciones graves como meningitis. El riesgo de bacteriemia oculta es mayor en los lactantes de 3 a 36 meses de edad, siendo Streptococcus pneumoniae la causa más frecuente de bacteriemia en este grupo de edad3-5.
La vacuna neumocócica conjugada heptavalente (VCN-7), está indicada en la inmunización activa contra las enfermedades invasivas (incluyendo bacteriemia, sepsis, meningitis, neumonía bacteriémica) causadas por los serotipos 4, 6B, 9V, 14, 18C, 19F y 23F de S. pneumoniae en niños desde 2 meses hasta 2 años de edad6.
La introducción de la VCN-7 ha disminuido la incidencia de infecciones invasivas neumocócicas (meningitis) y bacteriemia en niños que han recibido VCN-77-10. Por ello, muchos autores defienden que las estrategias diagnóstico-terapéuticas del pediatra de urgencias deberían modificarse ante un lactante con FSF que haya recibido VCN-7. En este caso serían necesarias menos pruebas diagnósticas y se podrían adoptar estrategias terapéuticas más conservadoras8,11.
Este trabajo tiene como objetivo conocer el impacto de la VCN-7 en el manejo del lactante con FSF en los SUP, con relación al porcentaje de vacunación de la población asistida.
Pacientes y métodos
Subestudio 1
Estudio prospectivo multicéntrico realizado durante el mes de febrero de 2005 en 14 SUP, donde se recogieron datos sobre el estado de VCN-7 de lactantes con FSF de 3 a 36 meses. Se incluyeron niños de esa edad, con FSF, temperatura igual o superior a 38 °C y duración de la fiebre inferior a 72 h. Se recogieron los siguientes datos para cada paciente: edad, sexo, temperatura máxima (axilar y/o rectal) registrada en su domicilio y/o en el SUP, si el niño había sido o no vacunado con la vacuna neumocócica y, en caso afirmativo, el número de dosis recibidas y la edad a las que las recibió. Se estimó el porcentaje VCN-7 en los lactantes con FSF que consultaron en cada uno de los 14 SUP.
Subestudio 2
Se realizó una encuesta a los pediatras de los 14 SUP participantes en el estudio, sobre el manejo concreto que se haría de 2 casos clínicos hipotéticos de FSF (tabla 1). Caso 1: una niña de 7 meses, y caso 2: una niña de 20 meses de edad, en tres situaciones: niña sin vacunar; que ha recibido 1 o 2 dosis de la VCN-7; o que ha recibido 3 dosis de la vacuna. Esta encuesta se hizo siguiendo parcialmente la metodología de un estudio publicado previamente12. En el estudio previo, se envían cuestionarios preguntando sobre el manejo del lactante con FSF (en 2 casos clínicos: lactante de 7 y 20 meses) teniendo en cuenta el estado de VCN-7. Se envían 15.000 cuestionarios, 7.500 a pediatras de atención primaria y 7.500 a pediatras de urgencias, cada uno de estos grupos se subdivide en 2 grupos, "educacional" (reciben información sobre la eficacia del estudio del grupo permanente de Kaiser) y grupo "no educacional" (no reciben dicha información); se incluye el grupo educacional para determinar si la familiaridad con los resultados del estudio permanente de Kaiser afecta al manejo y toma de decisiones.
En la encuesta realizada en nuestro estudio, se recogieron datos sobre los siguientes aspectos: la frecuencia de realización de pruebas diagnósticas (hemograma, hemocultivo, velocidad de sedimentación globular [VSG], proteína C reactiva [PCR], procalcitonina [PCT], análisis de orina, urocultivo, cultivo de líquido cefalorraquídeo, radiografía de tórax y detección del antígeno del neumococo en la orina), la frecuencia de ingreso hospitalario, la administración de antibióticos y alta domiciliaria, teniendo en cuenta el estado de VCN-7.
El programa estadístico utilizado fue el SPSS para Windows, versión 10.0. Para describir los resultados se utilizó las frecuencias relativas para las variables categóricas. Las variables categóricas se compararon entre grupos por medio del test de la chi cuadrado o el test exacto de Fisher en función del número de categorías y de las frecuencias esperadas en las diferentes celdas de la tabla de contingencia. El nivel de significación estadística se escogió como p < 0,05.
Centros participantes
Participaron, en total, los SUP de los 14 hospitales siguientes: Hospital de Sant Joan de Déu (Barcelona); Hospital de Cruces (Vizcaya); Complejo Hospitalario Carlos Haya (Málaga); Hospital Universitario Reina Sofía (Córdoba); Corporació Sanitaria Parc Taulí (Sabadell); Hospital Donostia (Guipúzcoa); Complejo Hospitalario Universitario La Paz (Madrid); Hospital de Basurto (Vizcaya); Hospital Virgen del Camino (Pamplona); Complejo Hospitalario Virgen del Rocío (Sevilla); Hospital General Universitario Gregorio Marañón (Madrid); Hospital Los Arcos (Murcia); Complejo Hospitalario Universitario de Santiago (A Coruña) y Hospital Comarcal de Vilafranca del Penedés (Barcelona).
Resultados
Subestudio 1
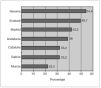
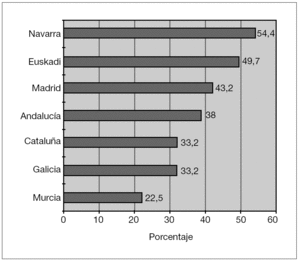
Durante el mes de febrero de 2005 se recogieron en los 14 hospitales que participaron en el estudio, datos de 1.357 lactantes de 3 a 36 meses de edad. Su edad media fue 14,58 ± 8,53 meses, siendo 665 (50 %) niños y 665 (50 %) niñas. Un total de 568 niños (41,86 %) habían recibido alguna dosis de VCN-7, con un promedio de 2,3 dosis ± 0,95 dosis por niño (tabla 2). El porcentaje de niños que habían recibido alguna dosis de VCN-7, fue diferente, según el área geográfica española a la que pertenecía el hospital (fig. 1). Para el análisis estadístico, se establecieron 2 grupos, en el primero (grupo A) se incluyeron hospitales en los cuales el porcentaje de niños vacunados fue superior o igual al 40 % (media: 49,1 %; rango: 43,2-54,4 %), 613 niños, formado por 6 hospitales (Hospital de Cruces, Hospital de Basurto, Hospital de Donostia, Hospital Virgen del Camino, Hospital La Paz, Hospital Gregorio Marañón) pertenecientes a 3 Comunidades Autónomas Españolas (País Vasco, Navarra y Madrid) y un segundo grupo (grupo B), en el que se incluyeron hospitales en los cuales el porcentaje de niños vacunados fue inferior al 40 % (media: 29,8 %; rango: 22,5-38 %), 744 niños, formado por 8 hospitales (Hospital de Sant Joan de Déu, Hospital Parc Taulí, Hospital de Vilafranca, Hospital Reina Sofía, Hospital Virgen del Rocío, Hospital Carlos Haya, Hospital de Santiago, Hospital Los Arcos) pertenecientes a 4 Comunidades Autónomas Españolas (Cataluña, Andalucía, Galicia y Murcia).
Figura 1. Porcentaje de vacunación en las distintas Comunidades Autónomas participantes en el estudio.
Subestudio 2
Se consiguieron reunir un total de 235 cuestionarios, sobre los 2 casos clínicos planteados, 104 cuestionarios correspondientes al grupo A (porcentaje de vacunación superior o igual al 40 %) y 131 correspondientes al grupo B (porcentaje de vacunación inferior al 40 %).
Caso clínico 1
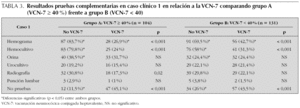
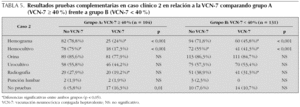
Los resultados de la encuesta, en ambos grupos de hospitales, sobre la indicación de pruebas complementarias en el lactante de 7 meses de edad con FSF se muestran en la tabla 3. Observamos que en ambos grupos de hospitales la indicación de practicar hemograma y hemocultivo disminuyó de forma significativa, en el supuesto de que el lactante hubiese recibido VCN-7, aunque este descenso fue más acusado y, estadísticamente significativo, en el grupo A con relación al grupo B (56,7 % frente a 26,7 % y 55,8 % frente a 26,7 %, respectivamente). Del mismo modo, la decisión de no practicar prueba alguna, se incrementó de forma significativa en el caso de que el lactante hubiese recibido VCN-7 en ambos grupos y nuevamente este incremento fue más acusado y, estadísticamente significativo en el grupo A (33,6 % frente a 17,5 %). En el grupo A, la intención de practicar radiografía de tórax en el lactante no vacunado fue significativamente mayor (p = 0,02). No existieron diferencias significativas en el resto de pruebas solicitadas (orina/urocultivo y punción lumbar) teniendo en cuenta el estado de vacunación, en ninguno de los grupos establecidos.
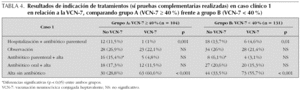
Los resultados de la encuesta, en ambos grupos de hospitales, sobre el tratamiento en este lactante de 7 meses con FSF, en el que se hubieran practicado exámenes complementarios, se muestran en la tabla 4. La indicación de administrar una dosis de ceftriaxona y seguimiento ambulatorio en el niño no vacunado, fue significativamente mayor en el grupo A (15,4 % grupo A frente a 6,1 % grupo B), no existiendo diferencias en el resto de indicaciones de tratamiento. Al igual que los pediatras en el grupo A se inclinaron por una postura menos intervencionista en el lactante vacunado, también son más agresivos en su estrategia de tratamiento en el niño no vacunado, pudiendo reflejar este hecho una mayor adhesión a los protocolos en aquellas áreas con mayor porcentaje de VCN-7.
En ambos grupos de hospitales la indicación de hospitalización y administración de antibioterapia parenteral, descendió de forma significativa, en el niño que había recibido VCN-7, incrementándose de forma significativa la indicación de seguimiento ambulatorio sin antibióticos.
Caso clínico 2
Los resultados de la encuesta sobre la indicación de pruebas complementarias en el lactante de 20 meses de edad con FSF se muestran en la tabla 5. En ambos grupos de hospitales la indicación de hemograma y hemocultivo disminuyó de forma significativa en el supuesto de que el lactante hubiese recibido VCN-7, aunque este descenso fue más acusado en las encuestas del grupo A (54,8 % frente a 26 % y 57,7 % frente a 13,7 %, respectivamente). Por otro lado, la indicación de hemocultivo en el niño no vacunado fue significativamente más alta en el grupo A frente a grupo B (75 % frente a 55 %) y también fue significativamente menor la indicación de radiografía de tórax en el niño vacunado en el grupo A frente a grupo B (19,2 % frente a 31,3 %). Al igual que en el caso 1, no existieron diferencias significativas según el estado de VCN-7 en el resto de pruebas solicitadas (orina/urocultivo y punción lumbar), en ninguno de los grupos establecidos. La decisión de no practicar prueba alguna, se incrementó de forma significativa en el caso de que el lactante hubiese recibido VCN-7, únicamente en el grupo A.
Los resultados de la encuesta, en ambos grupos de hospitales, sobre el tratamiento en el lactante de 20 meses con FSF en el que se hubieran practicado exámenes complementarios, se muestran en la tabla 6. La indicación de administrar una dosis de ceftriaxona y seguimiento ambulatorio del niño no vacunado, fue significativamente mayor en el grupo A (grupo A 26 % frente a 6,1 % grupo B) y menor, también en este grupo, la indicación de alta sin antibióticos (grupo A 11,5 % frente a 25,1 % grupo B). En ambos grupos de hospitales la indicación de hospitalización y administración de antibioterapia parenteral descendió de forma significativa, en el niño que había recibido VCN-7, incrementándose la indicación de seguimiento ambulatorio sin antibióticos. En el grupo A la opción que incluía hospitalización con antibiótico parenteral en el lactante que había recibido VCN-7 fue escogida significativamente menos que en el grupo B (1,9 % frente a 9,9 %). No existiendo diferencias significativas entre ambos grupos en el resto de indicaciones de tratamiento. Por otro lado, también en el grupo A, descendió de forma significativa, la indicación de administrar ceftriaxona y seguimiento ambulatorio, en el niño vacunado (13,5 % VCN-7 frente a 26 % no VCN-7; p = 0,02).
Discusión
El presente estudio demuestra que el estado vacunal frente al neumococo puede influir en la toma de decisiones ante el lactante con fiebre sin focalidad, por parte de los pediatras de urgencias de diferentes hospitales españoles. Si los resultados de esta encuesta reflejaran la práctica clínica en el manejo del lactante con FSF, en caso de que el niño hubiera recibido VCN-7 completa se produciría un descenso significativo del número de pruebas diagnósticas, siendo este descenso más notable en aquellos hospitales con mayor porcentaje de niños vacunados (mayor o igual al 40 %). También, en caso de que el niño hubiera recibido VCN-7 completa se produciría un descenso en el número de hospitalizaciones con antibióticos parenterales.
Se trata de la primera encuesta realizada en España, sobre el manejo del lactante con fiebre, desde la introducción de la VCN-7. Para ello, se utilizó una encuesta en la que se plantearon 2 casos clínicos, 2 lactantes de 7 y 20 meses de edad con FSF, idénticos a los utilizados por Gabriel et al12, en un estudio previo, con pediatras de atención primaria y urgencias en Estados Unidos. Los resultados de nuestro estudio sugieren que los pediatras de urgencias españoles encuestados, muestran un manejo mucho menos intervencionista, en aquellos lactantes con fiebre que hayan recibido VCN-7 completa. La intención de practicar hemograma y hemocultivo en los lactantes no vacunados, en ambos casos clínicos fue similar a la mostrada en el grupo de pediatras de urgencias del estudio de Gabriel et al12, alrededor del 75 %. Sin embargo, es llamativo que en nuestro estudio, en el supuesto de que los lactantes hubiesen recibido VCN-7, la intención de practicar estas pruebas por parte del pediatra, disminuyó de manera mucho más significativa, en una proporción casi tres veces mayor, siendo el descenso más notable en las áreas geográficas en las cuales el porcentaje de VCN-7 fue igual o mayor al 40 %. Probablemente, el tiempo transcurrido entre ambos estudios, 2 años, haya sido crucial en el conocimiento y convencimiento, por parte de los pediatras de urgencias, de los grandes beneficios comunicados por la introducción de esta vacuna. Efectivamente, numerosos estudios publicados en los últimos años7,9,10,13, han incidido en la reducción de la enfermedad invasiva neumocócica en los niños vacunados, e indirectamente en la población general, debido a la disminución de la circulación de los serotipos de neumococo incluidos en la vacuna14.
Sin embargo, existen grandes diferencias en el manejo global del lactante con fiebre sin focalidad, entre los diferentes hospitales participantes en el presente estudio. Las diferencias no sólo se reflejan en su práctica habitual, sino también en la respuestas que sus pediatras muestran en la encuesta de los supuestos clínicos, especialmente cuando se les plantea cuál sería su actuación en el caso de que el lactante hubiese recibido VCN-7 completa. Pensamos que se trata de una muestra más de las diferentes posturas que existen por parte de los pediatras de urgencias, en cuanto a cuál es la estrategia más coste-efectiva en el manejo del lactante con fiebre. Las dos corrientes, la de pediatras menos intervencionistas que optarían por la no práctica de pruebas complementarias y una actitud conservadora y la de los pediatras más intervencionistas que optarían por el intento de reducir riesgos con la práctica de pruebas complementarias y tratamientos más agresivos15,16, podrían estar representados de alguna manera en nuestra muestra. Sin embargo, aquellos pediatras que se inclinaron por una postura menos intervencionista en el lactante no vacunado, modificaron en menor cuantía su estrategia de diagnóstico y tratamiento en el niño vacunado. Podría especularse que este colectivo reflejaría más fidedignamente la postura actual en Europa ante el manejo del lactante febril, en general menos intervencionista y con menor adherencia a protocolos y por otra parte menos proclive a trasladar al entorno europeo, los mismos resultados de la vacunación neumocócica en Estados Unidos y Canadá17,18.
En España la vacuna neumocócica conjugada heptavalente fue comercializada en el año 2001, pero hasta la fecha no ha sido incluida en el calendario oficial de vacunas del sistema sanitario público, salvo en la Comunidad Autónoma de Madrid, en donde esta incluida en el calendario de vacunas desde noviembre de 2006. La Asociación Española de Pediatría19 sí la recomienda, aconsejando a los pediatras seguir una política activa, indicando esta vacuna, en los niños menores de 2 años de edad. La base de esta discrepancia se encuentra probablemente, en la falta de estudios en España y Europa en general, sobre la incidencia de enfermedad neumocócica invasiva y a la ausencia, en la vacuna heptavalente actual, de algunos de los serotipos más prevalentes en este entorno. Esto ha provocado que la introducción de esta vacuna haya sido muy irregular y haya dependido de factores como el grado de información de los pediatras, la influencia de las autoridades sanitarias locales, el poder adquisitivo de las familias, etc. Este hecho queda reflejado indirectamente en nuestro estudio, identificándose áreas geográficas con porcentajes muy diferentes de VCN-7, dibujándose un escenario epidemiológico único que parece traducirse incluso, en diferencias en la actitud que el pediatra de urgencias puede tomar sobre el lactante con fiebre que haya recibido VCN-7.
El hecho que los resultados se basen en una encuesta con casos clínicos hipotéticos puede constituir una limitación en nuestro estudio, ya que en ocasiones las repuestas en una encuesta pueden no adaptarse de forma fiel a la práctica clínica habitual. Por otro lado, el hecho de que el porcentaje de vacunación se estime sobre una muestra y no en toda la población, nos da una cifra aproximada pero no exacta del porcentaje de población vacunada.
Creemos que en el lactante con FSF, con vacunación previa frente al neumococo, se produciría una disminución significativa en el número de pruebas diagnósticas, la estancia del paciente en el SUP, la tasa de hospitalización y tratamiento antibiótico. La reducción en el número de pruebas diagnósticas sería más notable en aquellas áreas con porcentajes superiores de vacunación neumocócica.
Correspondencia: Dra. S. Capapé Zache.
Urgencias de Pediatría. Hospital de Cruces.
Pl. de Cruces, s/n. 48903 Baracaldo. Bilbao. España.
Correo electrónico: sacapape@hcru.osakidetza.net
Recibido en noviembre de 2006.
Aceptado para su publicación en marzo de 2007.