El efecto de la implantación de la prescripción electrónica asistida en la seguridad de los pacientes pediátricos ha sido poco estudiado. El objetivo de este estudio es comparar los errores de medicación antes y después de su implantación en un hospital terciario.
Material y métodosEstudio cuasiexperimental comparativo de los errores de medicación detectados antes y después de la implantación de la prescripción electrónica. Se analizaron todas las líneas de tratamiento y se recogió el punto de la cadena donde ocurrió el error, el tipo de error y su causa. Se realizó un estudio Delphi sobre la importancia de cada error en el que participaron médicos, enfermeros y farmacéuticos.
ResultadosSe incluyeron 166 pacientes (83 en cada etapa). Se detectó algún error en el 92% de los pacientes en la etapa preimplantacional (2,8±2,1 errores/paciente) y en el 7,2% en la etapa postimplantacional (0,1±0,4 errores/paciente). La prescripción electrónica asistida supuso una reducción absoluta del riesgo de error de un 40% (intervalo de confianza del 95%=35,6-44,4%). Los lapsus/despistes fueron la principal causa de error en ambos grupos. En la etapa preimplantacional se consideraron graves el 9,5% de los errores, y en la etapa postimplantacional todos fueron leves o moderados.
ConclusionesLa implantación de la prescripción electrónica con sistemas de ayuda a la prescripción, validación y administración de medicamentos reduce de forma significativa los errores de medicación y elimina los errores graves.
There have been very few studies on the effect of assisted electronic prescription on paediatric patient safety. The objective of this study is to compare medication errors that occurred before and after its introduction in a tertiary hospital.
Material and methodsA quasi-experimental comparative study of medication errors detected before and after assisted electronic prescription introduction. All treatment lines were analysed in order to detect the point in the chain where the medication error occurred, as well as its type and cause. A Delphi study was conducted on the importance of each medication error involving doctors, nurses, and pharmacists.
ResultsThe study included 166 patients (83 at each stage). At least one medication error was detected in 92% in the pre-introduction phase patients (2.8±2.1 errors/patient) and 7.2% of post-introduction phase patients (0.1±0.4 errors/patient). The assisted electronic prescription led to an absolute risk reduction of 40% (95% confidence interval=35.6-44.4%). The main cause of error was lapses and carelessness in both stages. Medication errors were considered serious in 9.5% of cases in the pre-introduction phase, while all of them were mild or moderate in the post-introduction phase.
ConclusionsThe assisted electronic prescription implementation with prescription, validation and medication administration assistance systems significantly reduces medication errors and eliminates serious errors.
El National Coordinating Council for Medication Error Reporting and Prevention (NCC MERP) define los errores de medicación (EM) como «Cualquier incidente prevenible que pueda causar daño al paciente o dé lugar a una utilización inapropiada de los medicamentos, cuando éstos están bajo el control de los profesionales sanitarios o del paciente o consumidor. Estos incidentes pueden estar relacionados con la práctica profesional, con los procedimientos o con los sistemas, incluyendo fallos en la prescripción, comunicación, etiquetado, envasado, denominación, preparación, dispensación, distribución, administración, educación, seguimiento y utilización»1.
El Estudio Nacional sobre los Efectos Adversos ligados a la Hospitalización (Estudio ENEAS), impulsado por el Ministerio de Sanidad y Consumo en el año 2005, puso de manifiesto que un 37,4% de los efectos adversos estaban directamente relacionados con la medicación, y un 34,8% de los mismos eran prevenibles2. Las características de la población pediátrica (constante desarrollo, particularidades farmacocinéticas y farmacodinámicas, déficit de medicamentos disponibles que requieren cálculos de dosis y reajustes de dosis según peso y superficie corporal), y el uso de fármacos en condiciones diferentes a las recogidas en la ficha técnica no respaldadas por ensayos clínicos, la convierten en un colectivo con alto riesgo de sufrir EM, 3 veces mayor que en adultos3–5.
La implantación de la prescripción electrónica con sistemas de soporte se encuentra en las recomendaciones de distintas organizaciones, sociedades y grupos de expertos para aumentar la seguridad en el uso de medicamentos (Instituto para el Uso Seguro de los Medicamentos [ISMP], American Society of Health-System Pharmacists [ASHP])6. Diversos trabajos publicados avalan la capacidad de la prescripción electrónica asistida (PEA) para reducir la incidencia de los EM, aunque con gran variabilidad en los resultados (20-80%)7–10, y es uno de los objetivos recogidos en el documento «Estrategia de seguridad del paciente del Sistema Nacional de Salud, 2015-2020» para promover un uso seguro de los medicamentos11.
El efecto de la implantación de la PEA en pacientes pediátricos ha sido poco estudiado. Este estudio se diseñó con el objetivo de evaluar el efecto de la implantación de la PEA sobre la prevalencia de los EM en el área pediátrica de un hospital de tercer nivel.
Material y métodosSe realizó un estudio cuasiexperimental, en el que se analizaron las prescripciones médicas y registros de medicación, durante las etapas que precedieron (de forma retrospectiva) y siguieron (de forma prospectiva) a la implantación de la PEA en el área pediátrica.
Se eligió el mismo período del año (noviembre-diciembre) de 2015 y 2018 para que el tipo de patología y medicación empleada fuese similar. Se incluyeron en el estudio todos aquellos pacientes con edad comprendida entre 2 meses y 15 años ingresados en una planta de hospitalización durante al menos 24 horas y con tratamiento farmacológico activo (se excluyeron los ingresos en la unidad de cuidados intensivos por disponer de un programa propio de prescripción).
Se analizaron todas las líneas de tratamiento de cada uno de los pacientes y se recogió, en una base de datos (Microsoft Access® 2019), el punto de la cadena donde ocurrió el error, el tipo de error y su causa. Las variables analizadas se muestran en la tabla 1.
Variables analizadas al considerar cada error de medicación, tanto en la prescripción manual como en la prescripción electrónica asistida
| Origen del EM |
| Prescripción, transcripción o validación |
| Tipos de EM |
| Errores de identificación del paciente |
| Omisión de la fecha o firma del médico prescriptor; firma del médico ilegible; omisión en la hoja de prescripción o transcripción del número de historia clínica o nombre completo del paciente |
| Errores del medicamento |
| Medicamento contraindicado por presentar el paciente historia de alergias |
| Errores en la frecuencia/hora de administración |
| Frecuencia mayor o menor de la correcta, omitida, ambigua y/o confusa |
| Errores en la dosis |
| Dosis mayor de la correcta, menor de la correcta, omitida o ilegible, ambigua o confusa |
| Errores en la duración del tratamiento |
| Duración mayor de la correcta, menor de la correcta, cálculo erróneo de las fechas de administración |
| Errores en la vía o modo de administración |
| Vía de administración errónea, omitida o ilegible en la hoja de tratamiento |
| Forma farmacéutica no adecuada |
| Duplicidad |
| Interacciones |
| Problema de salud insuficientemente tratado consecuencia de un error de la identificación del tratamiento |
| Selección de un principio activo incorrecto por confusión, selección de una especialidad o un medicamento inadecuado, omisión de la transcripción del tratamiento o medicación ilegible o confusa en la hoja de prescripción y/o enfermería |
| Causas del EM |
| Falta de conocimientos o formación sobre el medicamento |
| Falta de conocimientos o información sobre el paciente |
| Errores en el manejo de la tecnología |
| Lapsus/despiste |
EM: error de medicación; PEA: prescripción electrónica asistida; PM: prescripción manual.
La primera etapa se correspondió con la fase de prescripción manual (PM) y registro de administración de enfermería en papel. En esta etapa se realizó una revisión retrospectiva manual de la historia clínica en papel, tanto de la orden de prescripción médica como de la hoja de transcripción de enfermería. Se recogieron los errores, las deficiencias, las discrepancias y las oportunidades de mejora en relación con el tratamiento del paciente.
En la segunda etapa, tras la implantación de la PEA y el registro electrónico de administración, se recogieron los datos de forma prospectiva participando el farmacéutico en la validación de las prescripciones médicas.
Se realizó un análisis de la eficacia comparando el número de EM en la etapa preimplantacional frente a la etapa postimplantacional. Los EM se basaron en los criterios taxonómicos del NCC MERP y su adaptación y posterior actualización por parte del grupo de trabajo Ruiz-Jarabo 200012.
Posteriormente, se graduó la importancia de los EM detectados a través de un método de consulta Delphi en el que participó un grupo de expertos constituido por 3 médicos, 3 enfermeros y 3 farmacéuticos. Los participantes fueron seleccionados considerando su nivel de conocimiento y experiencia en el campo de la pediatría. El objetivo de la herramienta Delphi fue llegar a un acuerdo entre todos los participantes en la categorización de la gravedad de los diferentes errores detectados en cada una de las etapas. Cada error fue catalogado como leve, moderado o grave. Se realizaron diferentes rondas de consulta, en las que fueron públicas las graduaciones y justificaciones del resto de miembros, hasta finalmente alcanzar un consenso para determinar la gravedad de cada uno de los errores13.
Con base en la tasa de reducción de errores recogida en estudios previos, se calculó que un tamaño muestral de 83 pacientes en cada etapa del estudio nos permitiría estimar como significativa una diferencia en la prevalencia de EM igual o superior al 20%, con una seguridad del 95% y un poder estadístico del 80%, asumiendo un 10% de posibles pérdidas. Considerando una media de 17 altas por semana, se estimó una duración de 5 semanas para la recogida de datos en cada una de las etapas.
Se realizó un análisis descriptivo de todas las variables recogidas en el marco del estudio, antes y después de la implantación de la PEA. Las variables numéricas se expresaron como media±desviación típica y rango intercuartílico, y las variables cualitativas como frecuencias y porcentajes.
Se realizó un análisis de la eficacia comparando el porcentaje de EM en el momento del estudio de PM, y a los tres años de la implantación de la PEA, mediante el test de Chi-Cuadrado o el test exacto de Fisher para datos independientes. Se determinó la reducción absoluta y relativa del riesgo de errores entre los 2 períodos y sus intervalos de confianza (IC). En la comparación de datos cuantitativos entre 2 grupos se utilizó la prueba t de Student para datos independientes como prueba paramétrica y el test de la U de Mann-Whitney como prueba no paramétrica, dependiendo de la distribución de los datos.
Para estudiar la asociación de la implantación de la PEA con la disminución en las tasas de errores, se utilizó un modelo de regresión logística multivariante para ajustar las posibles variables de confusión.
Todas las pruebas estadísticas se consideraron bilaterales, y como valores significativos, aquellos cuya p<0,05. El análisis estadístico se realizó con el programa estadístico SPSS, v. 23.0.
El estudio se llevó a cabo con respecto a los principios enunciados en la declaración de Helsinki y a las normas de buena práctica clínica. Previamente al inicio del estudio se obtuvo la aprobación del Comité de Ética de Investigación de referencia.
ResultadosSe incluyeron un total de 166 pacientes (83 en cada una de las etapas). En la etapa preimplantacional solamente se consideraron en el análisis 75 de los 83 pacientes inicialmente incluidos, debido a que la historia clínica en papel de 8 de ellos estaba incompleta. Las características basales de los pacientes se reflejan en la tabla 2.
Análisis descriptivo de los pacientes en los 2 grupos del estudio
| Variable | Período preimplantacional (75 pacientes) | Período postimplantacional (83 pacientes) | p |
|---|---|---|---|
| Edad (años), mediana (rango intercuartílico) | 5,2 (0-15) | 5,7 (0-15) | - |
| Sexo, n (%) | |||
| Varón | 60 (80) | 50 (60,2) | 0,044 |
| Mujer | 15 (20) | 33 (39,8) | |
| Tipo paciente, n (%) | |||
| Médico | 35 (46,7) | 36 (43,4) | 0,678 |
| Quirúrgico | 40 (53,3) | 47 (56,6) | 0,678 |
| Estancia, n (%) | |||
| <7 días | 64 (85,3) | 71 (85,5) | 0,970 |
| ≥7 días | 11 (14,7) | 12 (14,5) | 0,970 |
| Días de ingreso, media ± desviación típica | 4,8±5,6 | 4,8±3,7 | - |
Se analizaron en total 1.017 líneas de tratamiento: 510 líneas de 75 pacientes en la etapa preimplantacional y 507 líneas de 83 pacientes en la etapa postimplantacional. El número medio de líneas de prescripción por paciente en la parte preimplantacional fue de 6,8±4,6 (rango intercuartílico=1-30), y en la parte postimplantacional fue de 6,1±3,5 (rango intercuartílico=1-18).
Se detectó algún error en el 92,0% de los pacientes en la etapa preimplantacional y en el 7,2% en la etapa postimplantacional. En la etapa preimplantacional se detectó un EM en 212 líneas de prescripción correspondientes a 69 pacientes, siendo el número medio de errores de 2,8±2,1 (rango intercuartílico=0-12). Tras la implantación de la PEA se detectó un EM en 8 líneas de prescripción correspondientes a 6 pacientes, siendo el número medio de errores de 0,1±0,4 (rango intercuartílico=0-3). La diferencia en el número de errores por paciente entre los grupos es estadísticamente significativa (p<0,001). La diferencia en el número de líneas con error (41,6% frente a 1,6%) también es estadísticamente significativa (p<0,001). La distribución y características de los EM se recogen en la tabla 3.
Distribución y características de los errores de medicación en los 2 grupos
| Variable | Período preimplantacional | Período postimplantacional | p |
|---|---|---|---|
| Líneas de tratamiento revisadas, n | 510 | 507 | - |
| Líneas de tratamiento por paciente, media ± desviación típica (RIC) | 6,8±4,6 (1-30) | 6,1±3,5 (1-18) | - |
| Líneas con error, n (%) | 212 (41,6) | 8 (1,6) | <0,001 |
| Pacientes con algún EM, n (%) | 69 (92) | 6 (7,2) | <0,001 |
| EM por paciente, media ± desviación típica (RIC) | 2,8±2,1 (0-12) | 0,1±0,4 (0-3) | <0,001 |
| Origen del EM, n (%) | |||
| Prescripción médica | 125 (59) | 4 (50) | 0,721 |
| Transcripción | 87 (41) | 0 (0) | 0,023 |
| Validación farmacéutica | 0 (0) | 4 (50) | <0,001 |
| Tipos de EM, n (%) | |||
| Errores de identificación | 68 (32,1) | 0 (0) | 0,054 |
| Otros errores | 144 (67,9) | 8 (100) | 0,054 |
| Causa del EM, n (%) | |||
| Información insuficiente del fármaco | 14 (6,6) | 3 (37,5) | 0,012 |
| Información insuficiente del paciente | 1 (0,5) | 0 (0) | 0,003 |
| Uso deficiente de la tecnología | 0 (0) | 1 (12,5) | 0,036 |
| Lapsus/descuido | 197 (92,9) | 4 (50) | 0,003 |
La implantación de la prescripción electrónica asistida supuso una reducción relativa del riesgo de errores de medicación de un 96,2% (intervalo de confianza del 95%=92,4-98,1%) y una reducción absoluta del riesgo de errores de medicación de un 40% (intervalo de confianza del 95%=35,6-44,4%).
EM: error de medicación; RIC: rango intercuartílico.
Atendiendo al origen del error, en la etapa preimplantacional, 125 (59,0%) EM ocurrieron en el momento de la prescripción y 87 (41,0%) en el proceso de transcripción a la hoja de enfermería. En la etapa postimplantacional, 4 (50,0%) EM ocurrieron durante la prescripción y 4 (50,0%) durante la validación farmacoterapéutica.
Las características de los EM detectados en ambos grupos se recogen en la tabla 4. En la PM los errores más frecuentes fueron los errores de identificación del paciente (68/212), seguidos de los errores de frecuencia u hora de administración (44/212) y de los errores de identificación del tratamiento (44/212). Con la PEA se observaron un total de 8 errores: 5/8 fueron errores de identificación del tratamiento (prescripción y/o validación de medicación confusa), 2/8 fueron errores en la dosis (sobredosificación) y 1/8 ocurrió tras la selección de una forma farmacéutica no adecuada a la dosis prescrita.
Detalle en la distribución de los errores de medicación en los 2 grupos considerando los tipos de errores
| Tipo de EM | Período preimplantacional(212 errores)n (%) | Período postimplantacional(8 errores)n (%) |
|---|---|---|
| Errores de identificación del paciente | 68 (32,1) | 0 (0) |
| Omisión de fecha | 15 (7,1) | 0 (0) |
| Omisión de firma | 19 (9) | 0 (0) |
| Firma ilegible | 34 (16) | 0 (0) |
| Omisión NHC | 0 (0) | 0 (0) |
| Omisión nombre del paciente | 0 (0) | 0 (0) |
| Errores del medicamento | 3 (1,4) | 0 (0) |
| Errores frecuencia/hora de administración | 44 (20,7) | 0 (0) |
| Mayor | 6 (2,8) | 0 (0) |
| Menor | 6 (2,8) | 0 (0) |
| Frecuencia omitida | 12 (5,7) | 0 (0) |
| Pauta confusa | 20 (9,4) | 0 (0) |
| Errores en la dosis | 28 (13,2) | 2 (25) |
| Sobredosificación | 7 (3,3) | 2 (25) |
| Infradosificación | 1 (0,5) | 0 (0) |
| Omisión de dosis | 6 (2,8) | 0 (0) |
| Dosis confusa | 14 (6,6) | 0 (0) |
| Errores en la duración del tratamiento | 3 (1,4) | 0 (0) |
| Mayor | 2 (0,9) | 0 (0) |
| Menor | 1 (0,5) | 0 (0) |
| Error en el cálculo de la fecha de administración | 0 (0) | 0 (0) |
| Errores en la vía o modo de administración | 21 (9,9) | 0 (0) |
| Errónea | 3 (1,4) | 0 (0) |
| Ilegible | 18 (8,5) | 0 (0) |
| Forma farmacéutica no adecuada | 0 (0) | 1 (12,5) |
| Duplicidad | 1 (0,5) | 0 (0) |
| Interacciones | 0 (0) | 0 (0) |
| Error en la identificación del tratamiento | 44 (20,8) | 5 (62,5) |
| Principio activo incorrecto | 8 (3,8) | 0 (0) |
| Especialidad inadecuada | 3 (1,4) | 0 (0) |
| Medicamento no sustituible | 0 (0) | 0 (0) |
| Omisión de la transcripción | 26 (12,3) | 0 (0) |
| Medicación confusa | 7 (3,3) | 5 (62,5) |
EM: error de medicación; NHC: número de historia clínica.
Como causa de error se posicionaron como más prevalentes, en ambos grupos, los lapsus/despistes (92,9% en la PM y 50,0% en la PEA), seguidos de la falta de información sobre el fármaco (6,6% en la PM y 37,5% en la PEA).
Considerando los errores detectados en los 2 períodos, la implantación de la PEA supuso la eliminación de los siguientes tipos de EM: los errores en la identificación del paciente, la duración, la posología, la vía o modo de administración, la omisión de la dosis, así como los errores derivados de contraindicaciones en el paciente o duplicidades. De manera global, la implantación de la PEA supuso una reducción relativa del riesgo de EM de un 96,2% (IC 95%=92,4-98,1%) y una reducción absoluta del riesgo de EM de un 40,0% (IC 95%=35,6-44,4%).
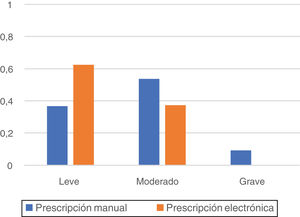
La graduación de los errores detectados tras la aplicación del método Delphi al personal sanitario implicado se recoge en la figura 1. En la etapa preimplantacional se consideraron graves el 9,5% de los errores, moderados el 53,7% y leves el 36,8%; mientras que en la etapa postimplantacional, todos los errores se consideraron leves (62,5%) o moderados (37,5%).
DiscusiónEl presente estudio pone de manifiesto que la implantación de la PEA en un área pediátrica consigue una reducción absoluta del riesgo de error de un 40% y la eliminación de los errores considerados graves por el personal sanitario implicado. La inclusión de información de fácil acceso para todo el personal sanitario sobre dosis ajustada a peso y edad, pautas de prescripción frecuentes, dosis máximas, interacciones, alergias, protocolos consensuados y recomendaciones de administración y conservación de medicamentos se traduce en una mejora en la seguridad y calidad del proceso asistencial. Además, al eliminarse el proceso de transcripción por parte del personal de enfermería, se minimiza una posible fuente de error.
La clasificación de los EM es muy variable entre los diferentes estudios y, probablemente, sea uno de los motivos por los cuales la literatura muestra resultados tan diferentes y difícilmente comparables. La disminución de los EM tras la implantación de la PEA en los distintos estudios en población pediátrica varía entre un 30-70%10,14–16. En nuestro estudio fue seleccionada la clasificación de NCC MERP y su adaptación por parte del grupo de trabajo Ruiz-Jarabo 2000 para la estandarización de los EM, adaptándola a nuestro marco de actuación al omitir alguna de las subcategorías relativas a la información sobre el error, ya que la única fuente de información era aquello registrado en la historia clínica en papel y en la electrónica12.
Un hallazgo común a la mayoría de los trabajos en los que se valora la implantación de la PEA es que los errores de dosificación son los que se evitan con mayor frecuencia, reduciéndose en un porcentaje que varía entre el 1-15,6%16–18. Nosotros no observamos esta reducción, quizás por los pocos errores detectados en la etapa postimplantacional. En nuestro estudio los errores de identificación del paciente fueron los que se redujeron en mayor medida (32,1% en la PM y ninguno en la PEA). Los errores más prevalentes detectados durante la etapa de PM son aquellos relacionados con la falta de información del paciente o su médico en la hoja de prescripción médica, la dosificación, la vía de administración o las prescripciones ilegibles. Nuestros resultados son coincidentes en proporciones similares con otros estudios donde se describen como errores más prevalentes los errores de dosificación, los defectos en la identificación de la vía de administración y la ausencia de un intervalo de dosificación19.
Con la implantación de la PEA, en nuestro estudio, hay errores que desaparecen (identificación del paciente, identificación y firma del médico prescriptor, fecha de la prescripción, omisión de la transcripción a la hoja de enfermería, dosis o pauta ilegible o confusa, omisión de la vía de administración, prescripción de un principio activo incorrecto o especialidad inadecuada) aunque no se eliminan la totalidad de los EM. De hecho, recogimos en el período postimplantacional un total de 8 errores. Diferentes estudios han puesto de manifiesto nuevos tipos de errores derivados de la PEA previamente inexistentes, como la duplicidad de los tratamientos, la selección incorrecta de la medicación de un cuadro desplegable, la selección incorrecta de la dosis por error tipográfico o la selección de un protocolo predefinido que no es apropiado para el paciente17,20. En nuestro estudio la validación farmacéutica de las prescripciones médicas fue clave para evitar que este tipo de EM alcanzasen al paciente.
La principal causa de error, tanto en la etapa preimplantacional como en la postimplantacional, fueron los lapsus/despistes. En nuestro estudio no hemos analizado sus posibles causas, pero experiencias similares ponen de manifiesto que factores como la fatiga laboral, la falta de formación, el estrés o el cansancio son factores determinantes en la incidencia de EM21. El uso deficiente de la tecnología no se manifiesta como una causa de error aparente en la etapa de PEA en nuestro estudio, a diferencia de otros trabajos donde se determinó que esta causa era la responsable del 19% de los errores20. Una posible explicación puede ser que la recogida de datos se realizó 3 años después de la implantación de la PEA, lo que permitió al personal sanitario la familiarización con la tecnología en la práctica clínica diaria tras varias sesiones formativas presenciales e instrucciones accesibles en la intranet del hospital.
Considerando la importancia atribuida por el personal sanitario a los errores detectados, destaca la ausencia de errores considerados graves en la etapa de PEA y la mayor prevalencia de errores clasificados como leves al comparar la etapa de PEA con la de PM.
LimitacionesNuestro estudio presenta algunas limitaciones. La más relevante es la ausencia de una forma universal de clasificar los EM. Otra limitación es que la primera parte del estudio (etapa preimplantacional) se hizo revisando las historias clínicas de forma retrospectiva, por lo que hay errores que no han sido posible analizar adecuadamente (prescripción de una forma farmacéutica incorrecta/inexistente). Además, en esta primera etapa no podemos saber si todos los errores detectados alcanzaron o no al paciente. En la etapa postimplantacional se recogieron los errores detectados de forma prospectiva, siendo muchos de ellos subsanados antes de llegar al paciente gracias a la validación farmacéutica.
Con el fin de minimizar el sesgo de selección, los pacientes se reclutaron en el mismo período del año, para evitar que los datos no fuesen comparables a los de otra etapa donde prevaleciesen otras patologías con diferentes tratamientos. No obstante, a pesar de analizar las mismas unidades de hospitalización, no tenemos la seguridad de que los médicos y enfermeros implicados fuesen los mismos en los 2 períodos de estudio.
ConclusionesLa población pediátrica tiene mayor riesgo, respecto a un paciente adulto, de sufrir un EM. Se trata, además, de un grupo de pacientes especialmente vulnerable ante un error por la inmadurez de su función renal, hepática e inmunológica. La implantación de la prescripción electrónica, con sistemas de ayuda a la prescripción, validación y administración de medicamentos, ha demostrado reducir de forma significativa los EM y ha permitido eliminar la totalidad de aquellos considerados graves por el personal sanitario. La incorporación de la validación farmacéutica en la PEA permite, además, identificar y resolver los EM antes de que alcancen al paciente, mostrándose como una actividad que aumenta la calidad y seguridad en el uso de medicamentos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.