El metilfenidato (MTF) es un psicoestimulante que aumenta frecuencia cardiaca (FC) y presión arterial (PA), lo cual a largo plazo podría modificar la geometría del ventrículo izquierdo (VI) y alterar sus propiedades funcionales, principalmente la diastólica.
Material y métodosEstudio prospectivo, longitudinal y comparativo tipo caso-caso en niños y adolescentes sanos diagnosticados de trastorno por déficit de atención e hiperactividad (TDAH) tratados con MTF durante 3 años. Se valoró pre y postratamiento PAS/PAD, geometría ventricular, función sistólica y diastólica.
ResultadosIncluimos a 112 pacientes, completando 73. El 75,3% varones, entre 4-15 años (9±2,6), con índice de masa corporal de 18,27±3,75 y una dosis media de MTF de 0,9±0,17mg/kg/día. Objetivamos aumento de PAS/PAD de 3,7±9mmHg (p = 0,004) y 2±11,5mmHg, respectivamente. No tuvimos ningún evento cardiovascular grave, cambios estructurales ni variación en los parámetros de función sistólica estudiados. Sin embargo, encontramos un aumento discreto, pero progresivo y significativo del tiempo de relajación isovolumétrica del VI (p = 0,046) y del tiempo de desaceleración (p = 0,016) indicativos de alteración en la relajación. No observamos variación en los parámetros relacionados con la distensibilidad ni con las presiones diastólicas tempranas y ningún paciente cumplió criterios de disfunción diastólica.
ConclusionesEl incremento de PAS/PAD y las alteraciones de la relajación del VI objetivadas podrían ser un indicador precoz de una posible disfunción diastólica y riesgo cardiovascular a largo plazo.
Although methylphenidate (MPH) used for treatment of Attention deficit hyperactivity disorder (ADHD) are considered safe in healthy children and adolescents in the short and medium term, there is a widespread concern about long-term cardiovascular safety.
Material and methodsInterventional, prospective, longitudinal and comparative study with a crossover design to evaluate the cardiovascular impact of the treatment with MPH in healthy children and adolescents diagnosed with ADHD. A protocol for the cardiovascular evaluation was established at a basal point, after the first and the second year of the beginning with treatment based on the monitoring of Blood pressure (BP) and echocardiographic follow-up of the systolic and diastolic functions, and structural cardiac properties.
Results73 patients completed the study, with an average age of 9+/- 2.6 years, 75.3% were male and the majority were thin (64.4%). We found an increase in Systolic and Diastolic BP of 3.7±9mmHg (P).004) and 2±11,5mmHg respectively. There were no severe cardiovascular events. We didn’t find any echocardiographic alterations namely on the structural properties or parameters of systolic function. Regarding diastolic function, a significant increase in the isovolumic relaxation time (IVRT) (P=.046) and deceleration time (P=.016) was observed. However, no significant alterations in the parameters related to distensibility of the LV neither in the early diastolic pressure were found.
ConclusionFurther studies are needed to evaluate the impact of psychostimulants as a modifiable long-term Cardiovascular Risk Factor.
El trastorno por déficit de atención e hiperactividad (TDAH) es el trastorno del neurodesarrollo más frecuente en la infancia con una prevalencia que oscila entre el 5 y el 8% según las características socioculturales de la población analizada, las fuentes de información consultadas o los criterios diagnósticos utilizados1-3.
En la última década, hemos experimentado un importante incremento de la prescripción de psicoestimulantes en países occidentales4-6 y se prevé que el porcentaje de pacientes potencialmente expuestos sea cada vez mayor, debido a su extensión a otras indicaciones7,8 y al incremento en usos ilícitos como mejorar el rendimiento cognitivo en personas sanas («píldoras inteligentes»)9.
Aunque la evidencia clínica apoya la idea de que el riesgo cardiovascular a corto y medio plazo en niños, adolescentes y adultos sanos es bajo10,11, tras una publicación en 200612 acerca del posible riesgo de eventos cardiovasculares graves (infartos de miocardio, muerte súbita, etc.), aunque no demostrado, existe una preocupación generalizada sobre su seguridad cardiovascular a largo plazo13-16.
Se ha descrito un aumento de la frecuencia cardiaca (FC) y presión arterial (PA) entre 5-10 latidos por minuto y 4-5mmHg de media, respectivamente16,17, existiendo un subconjunto de niños y adolescentes (alrededor del 5-15%) que pueden experimentar incrementos mayores, o incluso referir algún tipo de queja durante el tratamiento17. Aunque algunos autores consideran estos efectos cardiovasculares irrelevantes, debemos tener en cuenta que pequeños aumentos de la PA pueden modificar progresivamente la geometría del ventrículo izquierdo (VI) y alterar sus propiedades funcionales. En este contexto, la disfunción diastólica ha sido el tipo de daño cardiaco más frecuentemente documentado18.
Teniendo en cuenta que desconocemos si existe una relación entre la dosis o el tiempo de exposición a psicoestimulantes con la aparición efectos adversos cardiovasculares, y que el metilfenidato (MTF) y la lisdexanfetamina (LDX) son agentes simpaticomiméticos cuya influencia sobre la FC y la PA es una característica intrínseca a su actividad farmacológica, creemos que su seguridad cardiovascular no está bien establecida.
Los objetivos del estudio fueron:
- 1.
Valorar si la influencia de los psicoestimulantes sobre el tono simpático y la poscarga repercuten a medio plazo sobre las propiedades funcionales (sistólicas o diastólicas) o estructurales del VI.
- 2.
Valorar la utilidad de la exploración ecocardiográfica seriada para este propósito en niños y adolescentes sanos con TDAH, tratados con psicoestimulantes.
- 3.
Determinar la necesidad de protocolizar un seguimiento cardiovascular a medio plazo en este grupo de pacientes.
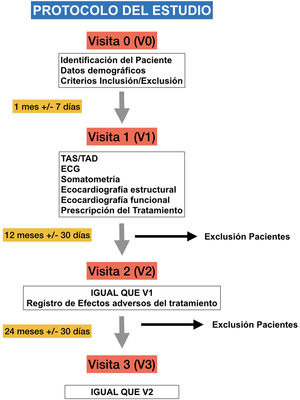
Estudio de intervención prospectivo, longitudinal y comparativo tipo case-crossover para evaluar la repercusión cardiovascular del tratamiento con psicoestimulantes (MTF o LDX) a dosis terapéuticas habituales en la práctica clínica (0,8-1,5mg/kg/día), en niños y adolescentes diagnosticados de TDAH según los criterios del Manual de diagnóstico y estadística de los trastornos mentales en su versión iv revisada y v (DEM-IV-TR y DSM-V) y tratados por primera vez («pacientes naïve»), en la consulta de Neuropediatría de un Hospital de nivel ii situado al sur de la Comunidad de Madrid (España).
La inclusión de pacientes se realizó durante el periodo comprendido desde enero del 2011 hasta junio del 2014, completando el seguimiento todos los pacientes en julio del 2017.
Criterios de exclusiónPatología cardiaca conocida que contraindicara el uso de psicoestimulantes o pudiera sesgar los resultados del estudio: cardiopatía congénita, isquémica, historia de muerte súbita, síncopes, palpitaciones en reposo, intolerancia al ejercicio, arritmias cardiacas…
Factores de riesgo cardiovascular que pudieran alterar la función diastólica:
- 1.
Hipertensión arterial (HTA) conocida19: definida por una PAS/PAD > P95 para la edad, sexo y talla correspondientes y según las tablas de población americana de la Task Force20 y las europeas de Wühl y Stergiou21-23 para la monitorización ambulatoria de la PA de 24h y la medida de la PA domiciliaria respectivamente.
- 2.
Comorbilidades médicas que afecten a la función diastólica como la diabetes mellitus (DM) tipo 124 e insuficiencia renal crónica25,26.
- 3.
Obesidad: definida a partir del índice de masa corporal (IMC) > 30.
- –
Abandono del tratamiento antes de completar el estudio.
- –
Mala adherencia al tratamiento o «vacaciones terapéuticas».
- –
Tratamiento con cualquier otro fármaco.
- –
Rechazo del tratamiento con psicoestimulantes o prescripción de no estimulantes como la atomoxetina.
Fueron realizadas en la consulta, siempre por el mismo facultativo, siguiendo las recomendaciones de la Sociedad Europea de Cardiología y la Sociedad Europea de Hipertensión27,28. Se utilizaron un dispositivo oscilométrico y un manguito de esfigmógrafo según la anchura y la longitud del brazo y se tomaron 3medidas a lo largo de la consulta obteniendo el valor definitivo promediando los datos obtenidos.
Estudio ecocardiográficoFueron realizados siempre por el mismo facultativo experto en cardiología infantil, en posición supina lateral izquierda, con el mismo equipo (Esaote MyLab™25Gold, Esaote España S.A.), una sonda de 3 o 5MHz (transductor multifrecuencia) según la edad del paciente y siguiendo las recomendaciones de la American Society of Echocardiography29. El cable de electrocardiograma se conectó al ecógrafo para definir y medir el tiempo de los eventos del ciclo cardiaco.
- 1.
Ecocardiografía estructural: morfología de las cámaras cardiacas, válvulas y grandes vasos desde múltiples accesos.
- 2.
Geometría ventricular izquierda: por ecocardiografía en modo M en eje paraesternal largo, medimos el espesor de la pared posterior (PP) del VI, del septum interventricular (SIV) y el diámetro diastólico del VI (DdVI). La masa ventricular izquierda fue calculada según la formula Devereux30 y se normalizó según la superficie corporal.
- 3.
Función sistólicas: determinamos la fracción de eyección (FE) y acortamiento (FA) del VI así como el desplazamiento sistólico del anillo tricuspídeo (TAPSE).
- 4.
Función diastólica: las velocidades de flujo mitral se obtuvieron en la vista apical de 4cámaras. Se determinaron las mediciones de la velocidad temprana de entrada diastólica (E), velocidad durante la contracción auricular activa (A) y la relación (E/A) mediante Doppler pulsado, así como el tiempo de desaceleración (TD) de la onda E por DTI. Usando índices de velocidad de tejido pulsado, los volúmenes de muestra se colocaron en los lados laterales de los anillos mitral y tricúspide y la base del tabique interventricular. Se midieron también las velocidades sistólica máxima, diastólica temprana y tardía (E’ y A’, respectivamente) y se calculó la relación E/E’. El tiempo de relajación isovolumétrica (TRIV) se midió en las paredes laterales del VI. Para reducir la variabilidad intraobservador se realizaron 3mediciones diferentes para cada índice y se tomó el promedio.
En este estudio, la disfunción diastólica del VI se definió como relación E/E’ > 8 o la relación E/A < 1,0.
Se consideraron valores normales del TRIV y TD: 50 ± 9ms y 142 ± 19 ms, respectivamente29,31.
EstadísticaTodos los análisis estadísticos y gráficos fueron realizados con el programa estadístico SPSS en su versión 23 (IBM SPSS Statistics Versión 23). El nivel de significación (p) para todos los análisis se consideró a partir de un valor de la p < 0,05.
Las variables cualitativas se resumieron con su distribución de frecuencias absolutas y relativas. Las variables cuantitativas con la media y desviación estándar. La comparación de los parámetros de estudio en el tiempo se analizó realizando un análisis de la varianza (ANOVA) de medidas repetidas introduciendo los diferentes momentos como factor intrasujeto. Para las comparaciones entre los 3momentos se aplicó el método de corrección de Bonferroni para comparaciones múltiples.
Con el objetivo de evaluar el efecto de la dosis del fármaco en la evolución de los parámetros en el tiempo, se realizó un ANOVA de medidas repetidas de un factor introduciendo el tiempo como factor intrasujeto y la dosis (variable dicotomizada en 2grupos según fuera > 0,9mg/kg/día o < 0,9mg/kg/día) como factor intragrupo.
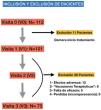
Se evaluó el cambio en la evolución de los parámetros en el tiempo entre la visita basal y la visita 3 mediante la interacción de los factores tiempo y dosis (fig. 1).
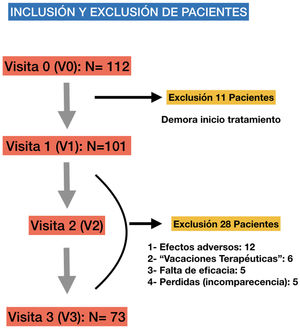
ResultadosIncluimos a un total de 112 pacientes, de los cuales 39 (34,8%) fueron saliendo en distintos momentos y por distintas causas (fig. 2), completando el estudio 73 pacientes con edades comprendidas entre los 4 y 15 años, edad media de 9±2,6 años) en el momento de la inclusión (V1), el 75,3% varones (n = 55) y delgados en su mayoría (64,4%) con un IMC medio de 18,27±3,75. Respecto al diagnóstico de TDAH, el subtipo más frecuentemente incluido fue el inatento (56%) y el 66% presentó alguna comorbilidad neuropsicológica siendo la más frecuente los trastornos del aprendizaje (40%) seguidos de trastornos de conducta (18%), del sueño (4%) y la discapacidad cognitiva leve (4%). Respecto al tratamiento, el MTF fue el estimulante más utilizado (92%) y el MTF de liberación osmótica sostenida (Metilfenidato OROS, Concerta, Janssen-Cilag, S.A., España) la fórmula farmacéutica más frecuentemente prescrita (58%). No hubo diferencias entre la dosificación de ambos estimulantes (MTF y LDX) y cuya dosis varió entre 0,5-1,36 mg/kg/día con una dosis media de 0,90,17mg/kg/día. Las características demográficas de nuestra población se detallan en la tabla 1.
Características demográficas de la muestra. Pacientes incluidos
| Pacientes incluidos | 112 |
| Abandonos (%) | 34,8 |
| N.° final | 73 |
| Edad, años (media ± DE) | 9±2,6 |
| Varones (%) | 75,3 |
| IMC (media ± DE) | 18,27±3,75 |
| Subtipo TDAH (%) | Inatento 56Combinado 43Hiperactivo 2 |
| Comorbilidad neuropsicológica (%) | 66T. aprendizaje 40T. conducta 18T. sueño 4Discapacidad cognitiva leve 4 |
| Psicoestimulante (%) | Metilfenidato 92 |
| Dosis (mg/kg/día), media ± DE | 0,9±0,17 |
| Nivel sociocultural (%) | Elemental 20,6Medio 40,3Superior 39,1 |
IMC: índice de masa corporal; MTF: metilfenidato; TDAH: trastorno por déficit de atención e hiperactividad.
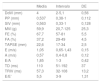
Respecto al estado cardiovascular al inicio del estudio, todos los pacientes tuvieron unas cifras de PAS/PAD normales con relación al sexo, la edad y la somatometría, con unos valores medios de 104±8,3mmHg y de 62,7±8,3mmHg, respectivamente. No encontramos alteraciones en ninguno de los parámetros estudiados (DdVI, PP, SIV, masa del VI) para describir la geometría ventricular izquierda y la masa ventricular calculada según la fórmula Devereux y agrupada según la superficie corporal fue normal. Tampoco encontramos alteraciones en parámetros de función sistólica de VI o VD (valores medios de FE 67,7±5,5, FA 37,2±4,5 y un TAPSE 22,64±2,48) y una función diastólica normal (relación media E/É 5,5 y E/A 1,85) (tabla 2).
Estado cardiovascular al inicio del estudio
| Media | Intervalo | DE | |
|---|---|---|---|
| DdVI (mm) | 4 | 2-5,1 | 0,56 |
| PP (mm) | 0,537 | 0,38-1 | 0,112 |
| SIV (mm) | 0,563 | 0,33-1 | 0,128 |
| MVI (g) | 59,9 | 20,7-125 | 25,3 |
| FE (%) | 67,7 | 57-81 | 5,5 |
| FA (%) | 37,2 | 29-49 | 4,5 |
| TAPSE (mm) | 22,6 | 17-34 | 2,5 |
| E (m/s) | 1,05 | 0,65-1,43 | 0,15 |
| A (m/s) | 0,57 | 0,4-0,8 | 0,12 |
| E/A | 1,85 | 1-3 | 0,42 |
| TD (ms) | 110 | 51-192 | 37 |
| TRIV (ms) | 57,3 | 32-108 | 13,2 |
| E/E’ | 5,5 | 3-9 | 1,31 |
A (onda): velocidad durante la contracción auricular activa; DE: desviación estándar; DdVI: diámetro diastólico del ventrículo izquierdo; E (onda): velocidad temprana de entrada diastólica; E/A: relación onda E/A; E/E’: relación onda E/E’; FA: fracción de acortamiento; FE: fracción de eyección; MVI: masa del ventrículo izquierdo; PP: pared posterior; SIV: septo interventricular; TAPSE (tricuspid annular plane systolic excursion) desplazamiento sistólico del anillo tricuspídeo; TD: tiempo de desaceleración; TRIV: tiempo de relajación isovolumétrica del VI.
Se objetivó un incremento significativo entre V1 y V3 de la PAS de 3,7±9mmHg (p = 0,004) y de la PAD de 2±11,5mmHg, en este caso sin significación estadística, que fue independiente de la dosis (alta: > 0,9mg/kg/día vs. baja: < 0,9) y el tipo de estimulante (MTF vs. LDX).
Desde el punto de vista estructural, la geometría y la masa ventricular se mantuvieron estables al final del estudio. Los parámetros relacionados con función sistólica de ambos ventrículos (FE 70,3±5,1, FA 39,9±4,6 y un TAPSE 22,2±2,95) no experimentaron cambios significativos a lo largo de los 3controles. Respecto a la función diastólica, se objetivó un aumento discreto pero progresivo y significativo del TRIV desde 57,3±13,2 en V1 hasta 62,4±14,6 en V3 (p = 0,046) y del porcentaje pacientes con el TRIV alargado (31%) al final del estudio. Sin embargo, no encontramos alteración significativa de los parámetros relacionados con la distensibilidad del VI ni con las presiones diastólicas tempranas y ningún paciente cumplió criterios estrictos de disfunción diastólica. Aunque se encontraron variaciones significativas en el TD (p = 0,016), estas no fueron clínicamente relevantes, el tamaño de la onda E se mantuvo por encima de la onda A con una relación entre ambas (E/A) por encima de 1 durante todo el seguimiento, y tampoco se objetivaron variaciones significativas en la relación E/E’ (tabla 3).
Evolución del estado cardiovascular durante el estudio
| V1 | V2 | V3 | p(V1-V3) | |
|---|---|---|---|---|
| DdVI (mm) | 4±0,56 | 4,3±0,56 | 4,7±0,58 | 0,246 |
| PP (mm) | 0,537±0,112 | 0,54±0,09 | 0,545±0,1 | 1,00 |
| SIV (mm) | 0,563±0,128 | 0,561±0,1 | 5,5±0,1 | 1,00 |
| MVI (g) | 59,9±25,3 | 61±26,4 | 61,96±25,7 | 0,61 |
| TAPSE (mm) | 22,6±2,48 | 22±3,4 | 22,2±2,95 | 0,68 |
| FE (%) | 67,7±5,5 | 68,9±4,6 | 70,3±5,1 | 0,02 |
| FA (%) | 37,2±4,5 | 38,9±4,5 | 39,9±4,6 | 0,01 |
| E (m/s) | 1,05±0,15 | 1,01±0,16 | 1,03±0,16 | 1,00 |
| A (m/s) | 0,57±0,12 | 0,57 ± 0,12 | 0,59 ± 0,13 | 0,95 |
| E/A | 1,85 ± 0,42 | 1,78 ± 0,52 | 1,74 ± 0,38 | 0,167 |
| TD (ms) | 110 ± 37 | 99 ± 24,9 | 96,3 ± 25,7 | 0,016 |
| TRIV (ms) | 57,3 ±13,2 | 58,.99 ± 17,1 | 62,4 ± 14,6 | 0,046 |
| E/E’ | 5,5 ± 1,31 | 5,4 ± 1,16 | 5,23 ± 1 | 0,276 |
A (onda): velocidad durante la contracción auricular activa; DdVI: diámetro diastólico del ventrículo izquierdo; E (onda): velocidad temprana de entrada diastólica; E/A: relación onda E/A; E/E’: relación onda E/E’; FA: fracción de acortamiento; FE: fracción de eyección; MVI: masa del ventrículo izquierdo; PP: pared posterior; SIV: septo interventricular; TAPSE (tricuspid annular plane systolic excursion) desplazamiento sistólico del anillo tricuspídeo; TD: tiempo de desaceleración; TRIV: tiempo de relajación isovolumétrica del VI.
En negrita se resaltan los datos estadísticamente significativos (p< 0,05).
Datos de V1, V2 y V3: media ± DE.
El MTF es un psicoestimulante disponible en la Unión Europea (UE) desde la década de los 50; sin embargo, y a pesar de que su prescripción en los países occidentales se ha disparado en la última década4-6, el perfil de efectos adversos a largo plazo no está completamente caracterizado.
Tras una revisión del Comité de Medicamentos de Uso Humano de la Comisión Europea realizada en enero de 200932, se establecieron unas recomendaciones para estandarizar su prescripción, la información acerca de su seguridad en todos los estados miembros de la UE y se indicó la necesidad de realizar más estudios que investigaran, entre otras cosas, los efectos cardiovasculares a largo plazo en adultos que han tomado o están tomando MTF32.
Estudios realizados con estimulantes de abuso como la metanfetamina indican una posible cardiotoxicidad relacionada con el desequilibrio que se genera entre el incremento de las necesidades de O2 que produce el aumento de la FC y la PA, y su baja disponibilidad a nivel cardiaco33,34, que conlleva la vasoconstricción que asocia. Además, niveles excesivos de catecolaminas pueden causar necrosis del músculo cardiaco, fibrosis o hipertrofia34,35.
Aunque no existe evidencia de que los estimulantes prescritos en el TDAH condicionen un incremento del riesgo cardiovascular en jóvenes sanos36, si partimos de la base de que el MTF y la LDX, por su mecanismo de acción, tienen un efecto similar a los estimulantes de abuso37, parece razonable al menos plantear estudios que evalúen las posibles consecuencias cardiovasculares a largo plazo.
Nuestro estudio, a diferencia de otros12-17, es el primero en valorar de forma prospectiva y a medio plazo (36 meses) posibles alteraciones precoces de las propiedades estructurales o funcionales del corazón mediante estudio ecocardiográfico seriados, en niños y adolescentes con TDAH que inician tratamiento con psicoestimulantes.
Establecimos un protocolo de seguimiento y de evaluación ecocardiográfica similar al de estudios parecidos realizados en diversas enfermedades crónicas de pacientes pediátricos19,24-26, pero con unos criterios de exclusión muy estrictos que minimizaran las posibles variables de confusión o modificadoras del efecto como la obesidad, HTA previa al tratamiento, cardiopatía, etc.
Obtuvimos un muestra considerable24-26, pero con algunas particularidades desde el punto de vista epidemiológico1-5, como el predominio del TDAH inatento (56%) sobre el combinado y de los trastornos del aprendizaje sobre los trastornos de conducta (40% vs. 18%) como comorbilidad más frecuente. Su explicación se basa en que, debido al predominio de los síntomas conductuales de tipo externalizante, los TDAH combinados mostraron mayor «urgencia terapéutica» y 11 paciente incluidos en V0 rehusaron acudir a V1 y fueron excluidos del estudio. Aunque es una muestra homogénea respecto al nivel socioeconómico y cultural, la sintomatología y las disfunciones producidas por el trastorno, estas variantes epidemiológicas podrían alejar la muestra de ser representativa de la práctica clínica habitual y poder extrapolar los resultados sobre la seguridad cardiovascular a toda la población.
Otro aspecto epidemiológico importante por su posible influencia en la seguridad cardiovascular a largo plazo, es que. desde el punto de somatométrico, la mayoría de los pacientes (64,4%) fueron delgados según el IMC (< 18,49) y al igual que lo descrito en otros estudios realizados a nivel nacional38, de forma global, se produjo un descenso de 0,5±2,2 puntos en el IMC a expensas principalmente de una ligera pérdida de peso.
La importancia del dato radica en que el exceso de peso aumenta el riesgo cardiovascular de manera independiente a otros FRCV en hombres y especialmente en mujeres. Además, favorece la presencia de otros FRCV como la HTA, DM o la dislipidemia (especialmente hipertrigliceridemia, niveles bajos de HDL y aumento de LDL), la aparición de hipertrofia ventricular, y aumenta los niveles de marcadores de inflamación sistémica39,40. Teniendo en cuenta que la obesidad en la edad pediátrica se asocia a su persistencia en la edad adulta, el hecho de que en nuestra muestra no haya ningún paciente obeso ni sus FRCV asociados puede reforzar los resultados obtenidos.
Respecto a la evolución cardiovascular, aunque como era de esperar16,17 encontramos un incremento progresivo de la PAS/PAD y las mediciones se realizaron siguiendo las recomendaciones establecidas22,27,28, pensamos que deben ser interpretados con cautela.
A diferencia del resto, y partiendo de una hipótesis aún no demostrada41, el aumento de PAS/PAD fue independiente del tipo y la dosis (alta vs. baja) de estimulante.
Puesto que no hubo ningún evento cardiovascular grave, y no encontramos alteraciones ecocardiográficas estructurales ni funcionales suficientes como para hablar de disfunción sistólica o diastólica en los 3años de seguimiento, podríamos concluir que ambos psicoestimulantes son seguros desde el punto de vista cardiovascular.
Sin embargo, teniendo en cuenta que los cambios que producen los psicoestimulantes en la PA no se traducen automáticamente en un efecto cardiovascular clínicamente relevante, pensamos que los datos obtenidos indicativos de estadios precoces de alteraciones de la relajación son relevantes y abren la puerta a nuevas investigaciones aleatorizadas, con grupo control, mayor tamaño muestral y a más largo plazo que confirmen los resultados obtenidos.
Desde el punto de vista fisiopatológico, nuestros resultados sugieren que el aumento de la PA, aunque no sea clínicamente significativo, podría condicionar un remodelado miocárdico que no demuestra alteraciones en la valoración ecocardiográfica 2D, pero sí en el Doppler.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
El presente estudio fue presentado en el 66.° Congreso de la AEP, celebrado en Zaragoza del 7 al 9 de junio del 2018, y fue premiado dentro de las mejores comunicaciones orales.