Se presenta el Documento de Consenso sobre etiopatogenia y diagnóstico de la osteomielitis aguda y la artritis séptica no complicadas elaborado por la Sociedad Española de Infectología Pediátrica, la Sociedad Española de Reumatología Pediátrica y la Sociedad Española de Ortopedia Pediátrica.
En este documento se revisan la etiopatogenia y la fisiopatología de la infección osteoarticular aguda en niños, considerada como aquella no complicada, de origen comunitario, que presenta una evolución inferior a 14 días, así como la aproximación clínico-diagnóstica a estas entidades, basándonos en las mejores evidencias científicas disponibles. En función de dichas evidencias, se aportan una serie de recomendaciones para la práctica clínica.
This is a Consensus Document of the Sociedad Española de Infectología Pediátrica, Sociedad Española de Reumatología Pediátrica and Sociedad Española de Ortopedia Pediátrica on the aetiology and diagnosis of uncomplicated acute osteomyelitis and septic arthritis.
A review is presented of the aetiopathogenesis and pathophysiology of acute osteoarticular infection defined as a process with less than 14 days of symptomatology, uncomplicated, and community-acquired. The diagnostic approach to these conditions is summarised based on the best available scientific knowledge. Based on this evidence, a number of recommendations for clinical practice are provided.
La infección osteoarticular (IOA) presenta una especial importancia debido a que el sistema músculo-esquelético en el niño está en constante crecimiento. Así, una infección que afecte al cartílago de crecimiento o la epífisis puede producir una alteración en el desarrollo del hueso, con las correspondientes secuelas. Las 3 sociedades participantes, la Sociedad Española de Infectología Pediátrica (SEIP), la Sociedad Española de Reumatología Pediátrica (SERPE) y la Sociedad Española de Ortopedia Infantil (SEOP), consideramos muy importante la existencia de un documento de consenso que recoja la información científica publicada sobre la IOA no complicada en pediatría. En este documento incluimos tanto la osteomielitis aguda (OmA) como la artritis séptica (AS), revisándose, fundamentalmente, las infecciones comunitarias de causa hematógena y evolución clínica aguda (< 14 días). Además, se desarrolla un conjunto de recomendaciones, con nivel de evidencia y grado de recomendación (tabla 1)1.
Nivel de evidencia y fuerza de recomendación utilizadas en este consenso
| Categoría | Definición |
|---|---|
| Fuerza de la recomendación | |
| A | Buena evidencia |
| B | Moderada evidencia |
| C | Pobre evidencia |
| Calidad de la evidencia | |
| I | Estudios clínicos adecuadamente aleatorizados |
| II | Estudios clínicos bien diseñados pero no aleatorizadosEstudios de cohortesEstudios de casos y controlesOtros: múltiples series o consecuencia de resultados contundentes de experimentos no controlados |
| III | Opinión de expertos basada en experiencia clínicaEstudios descriptivosRecomendaciones de comités de expertos |
Modificado de Khan et al.1.
Este consenso no pretende reemplazar el juicio clínico o establecer un protocolo para todos los niños con este tipo de infecciones y, probablemente, no representa el único abordaje adecuado para la IOA en el niño.
En otro documento posterior se abordará el tratamiento de las IOA.
EpidemiologiaLas IOA son más frecuentes en la infancia, con una prevalencia en países desarrollados de 22 casos/100.000 niños2. El 50% de los casos se produce en < 5 años y, al menos, el 25% en < 2 años3. Se estima una incidencia anual de 4 casos/100.000 niños de AS4 y de 2-13 casos/100.000 niños para la OmA5,6, siendo, esta última, hasta 2 veces más frecuente. En el caso de osteomielitis neonatal, se describen de 1-3 casos/1.000 ingresos en cuidados intensivos7. La relación varón:mujer es de 1,2:3,7 veces7.
Se ha descrito un aumento del número de casos de OmA de hasta 2,8 veces en los últimos 20 años, manteniéndose constante el de AS5,6, lo que podría deberse a la mejora de las técnicas diagnósticas. Existe una serie de factores predisponentes que favorecen el desarrollo de una IOA y que se detallan en la tabla 2, aunque la mayoría de las IOA se producen en niños sin enfermedad de base.
Factores predisponentes que favorecen el desarrollo de una infección osteoarticular
| Inmunodeficiencias primarias, como la enfermedad granulomatosa crónica, el síndrome de Wiskott-Aldrich o el síndrome de Chediak-Higashi |
| Infección por el virus de la inmunodeficiencia humana |
| Hemoglobinopatías, sobre todo, drepanocitosis |
| Sepsis |
| Traumatismos con bacteriemia (responsables del 30% de casos de OmA) |
| Varicela |
| Cirugía (articular, intestinal y urinaria) |
| Heridas penetrantes, infecciones cutáneas o presencia de cuerpos extraños |
| Hemodiálisis |
| Diabetes |
| Durante el periodo neonatal |
| Prematuridad |
| Infecciones cutáneas |
| Canalización umbilical o catéteres venosos centrales |
| Infecciones previas, especialmente cuando asocian bacteriemia (o fungemia) |
| En ocasiones, se han desarrollado OmA tras la punción con lanceta del talón |
La OmA suele ser unifocal, afectando, generalmente, a las metáfisis de huesos largos, especialmente fémur (30%), tibia (22%) y húmero (12%)7,8, siendo menos frecuente la afectación del calcáneo o la pelvis. La OmA pélvica se describe entre el 1 y el 11% y suele afectar a niños mayores8,9. Las infecciones multifocales son más frecuentes en recién nacidos (RN) (hasta un 40%), niños con inmunodeficiencia o en aquellos con enfermedad causada por Staphylococcus aureus (S. aureus) resistente a meticilina (SARM)9,10.
En el caso de las AS, más del 90% son monoarticulares3, siendo las articulaciones de miembros inferiores las más frecuentemente afectadas (70% de los casos): especialmente rodilla (35-40%), cadera (25-30%), tobillo (13-15%), codo (10%) y hombro (5%)3,4,11.
A nivel de la columna, la IOA puede ocasionar discitis, más frecuentes en zona lumbar7,12,13 y en niños < 5 años, dado que el disco intervertebral se vasculariza desde la vértebra adyacente (vascularización que desaparece posteriormente)7,8,12. La discitis descrita en adolescentes podría representar más una necrosis avascular que una verdadera infección. Las vértebras se afectan en el 1-2% de los casos, especialmente en niños > 8 años.
Hasta en un 30% de niños (sobre todo neonatos [70% de los casos] y < 18 meses) coexisten OmA y AS (osteoartritis), especialmente en hombro y cadera por la existencia de metáfisis intraarticular7,8,12.
EtiologíaBacterias más frecuentesEl microorganismo más frecuente en todas las edades es S. aureus. En RN y hasta los 3 meses de edad, también son patógenos importantes Streptococcus agalactiae y las enterobacterias (especialmente Escherichia coli). Entre los 3 meses y los 2-5 años, los agentes etiológicos más frecuentes son S. aureus y Kingella kingae, mientras que a partir de esa edad la gran mayoría de infecciones son producidas por S. aureus y, en menor medida, por Streptococcus pyogenes14 (tabla 3). En caso de artritis en adolescentes sexualmente activos, habría que pensar en Neisseria gonorrhoeae11. Las bacterias asociadas a distintos factores de riesgo se detallan en la tabla 3.
Etiología más frecuente de la infección osteoarticular en función de la edad y de los factores de riesgo asociados
| Edad | Bacterias |
|---|---|
| < 3 mesesa | Staphylococcus aureusStreptococcus agalactiaeEnterobacterias (especialmente Escherichia coli) |
| 3 meses-5 añosb | S. aureusKingella kingaeS. pyogenes |
| > 5 añosc | S. aureusS. pyogenes |
| Situación de riesgo | Bacterias |
|---|---|
| Herida punzante en el pie con calzado deportivo | Pseudomonas aeruginosa |
| Varicela y heridas | S. pyogenes |
| Drepanocitosis | Salmonella enteritidis |
| Déficit de complemento | Neisseria meningitidisd |
| Recién nacido con patologías complejas, inmunodeficiencias, pacientes con prótesis o material de osteosíntesis | Staphylococcus plasmocoagulasa negativos; S. epidermidis, S. hominis, S. saprophyticus, S. haemolyticus, S. lugdunensis. Candida spp., así como otros cocos y bacilos grampositivos y bacilos gramnegativos |
| Agammaglobulinemia | Mycomplasma pneumoniae |
| Enfermedad granulomatosa crónica | S. aureus, Serratia marcescens y Aspergillus fumigatus, entre otros |
| Pacientes procedentes de países con alta endemia de tuberculosis, inmunodeficiencias que afectan al eje gamma interferón-interleucina 12 y tratamientos con inmunomoduladores biológicos que interfieren con la producción de interferón | Mycobacterium tuberculosis |
Otros microorganismos ocasionalmente asociados a infección osteoarticular en recién nacidos son: N. gonorrhoeae, Staphylococcus plasmocoagulasa negativo o Candida.
La mayoría de los casos de AS se producen a partir de la siembra hematógena de organismos en la sinovial. Las endotoxinas bacterianas en el espacio articular inducen liberación de citocinas, migración leucocitaria y destrucción de la matriz del cartílago articular11. En el caso de la cadera y del hombro, a este efecto hay que unir la lesión producida por el colapso vascular debido al aumento de la presión intraarticular por acúmulo de pus.
La infección también puede llegar desde focos contiguos, especialmente osteomielitis en lactantes13. Finalmente, las articulaciones pueden infectarse a partir de heridas penetrantes, artroscopias o inyección intraarticular de medicamentos, las 2 últimas, excepcionalmente15.
Osteomielitis agudaLa forma más frecuente de infección es la vía hematógena. Menos frecuentes son las OmA producidas a partir de fracturas abiertas, heridas punzantes, mordeduras de animales o infecciones contiguas como sinusitis, infecciones dentarias o mastoiditis.
A partir de una bacteriemia, se produce la infección de la metáfisis de huesos largos por su rico aporte vascular: el lento flujo sanguíneo a través de sus asas capilares y la existencia de poros en el endotelio permiten el paso de microorganismos. Las bacterias proliferan, formándose grandes colonias que obstruyen las luces capilares, dificultando la fagocitosis y la penetración de antibióticos. A partir de los focos de infección metafisaria, se desarrolla infección en la médula ósea y el hueso cortical. La existencia de vasos transepifisarios en los RN y lactantes pequeños proporciona una conexión vascular entre la metáfisis y la epífisis, favoreciendo la aparición de osteoartritis en estas edades. La atrofia de los capilares metafisarios a los 18 meses hace que, a partir de esta edad, la afectación articular sea excepcional, excepto en el caso de metáfisis intracapsulares, como la cadera o el hombro13.
S. aureus, patógeno más frecuente de las IOA, posee numerosas proteínas de superficie responsables de la adherencia a los tejidos del huésped. Una vez lograda la adherencia, la capacidad de formar biofilms o variantes de colonias pequeñas favorece la persistencia de la infección. Además, es capaz de producir proteínas que inhiben la quimiotaxis, leucocidinas (leucocidina de Panton-Valentine o PVL en inglés) que destruyen los leucocitos y modulinas con capacidad lítica de los osteoblastos16,17.
Manifestaciones clínicasSíntomas generalesEl inicio de los síntomas de una IOA aguda será de un periodo < 14 días. Por encima de este tiempo se considera infección subaguda o crónica. Esta duración es arbitraria, aunque generalmente aceptada, y otros criterios radiológicos, clínicoa o anatomopatológicoas pueden ser importantes para definir mejor esta infección.
Los síntomas iniciales en la IOA pueden ser inespecíficos, como irritabilidad, malestar general, disminución del apetito o de la actividad. La fiebre no siempre está presente en el momento de la consulta, sobre todo en RN y lactantes pequeños6,9, objetivándose en un 62-72% de los casos18, y siendo más frecuente en la AS11,19.
Síntomas localesLo más significativo es el dolor localizado y la disminución de la movilidad o impotencia funcional, presentes en el 56-95% y el 50-92% de las ocasiones, respectivamente6,20, con la adopción de una postura antiálgica. Cuando la infección se sitúa en los miembros inferiores o el eje axial (espondilodiscitis, sacroilitis), aparece cojera o rechazo de la deambulación. Otros síntomas locales dependerán de la localización:
- –
En la OmA, además de dolor, puede existir tumefacción, calor e, incluso, eritema si la infección ha progresado hasta el espacio subperióstico y el tejido celular subcutáneo6.
- –
En las AS superficiales, como la rodilla, hay dolor, tumefacción y calor, casi siempre sin eritema. Sin embargo, cuando la AS es profunda, como en la cadera, no hay tumefacción, calor o rubor9, y la sospecha clínica se establece por el dolor referido en ingle, muslo o rodilla ipsolaterales, junto con una limitación dolorosa de la movilidad de la articulación, especialmente con la rotación interna: el niño suele presentar una actitud antiálgica de la cadera, manteniéndola en flexión, rotación externa y abducción.
- –
Los pacientes con espondilodiscitis y sacroilitis evitan la deambulación y la sedestación, y mantienen la típica postura de trípode. Hace falta un alto índice de sospecha para el diagnóstico de la IOA en estas localizaciones9.
La forma más benigna y frecuente cursa sin síntomas de enfermedad sistémica ni fiebre, siendo la irritabilidad, la falta de apetito y la seudoparálisis del miembro afectado, junto con dolor a la movilización, el cuadro típico8. Existe un cuadro grave que asocia bacteriemia y signos típicos de sepsis, siendo más característico en el RN pretérmino8,21. También puede observarse OmA secundaria a cefalohematoma o a la monitorización12.
DrepanocitosisEstos niños tienen un elevado riesgo de presentar OmA y AS debido a oclusiones microvasculares11,22. La presentación clínica de la OmA es similar a la de una crisis vaso-oclusiva y el diagnóstico diferencial puede ser muy difícil. Los episodios infecciosos parecen cursar con fiebre más elevada, dolor más persistente y en una única localización23.
Exploración físicaLa exploración física es clave para establecer la sospecha diagnóstica y valorar la evolución posterior del cuadro clínico. Consta de:
- –
Exploración general minuciosa, comenzando por el lado contralateral.
- –
Observación de la actitud espontánea.
- –
Evaluación del sistema músculo-esquelético, que puede realizarse con el pGALS (pediatric Gait, Arms, Legs, Spine), un instrumento validado y fácil de utilizar. De forma simplificada se muestra en la tabla 424,25.
Tabla 4.The pGALS (pediatric Gait, Arms, Legs, Spine), examen para la detección de síntomas músculo-esqueléticos
Preguntas ¿Tiene el niño dolor o rigidez (entumecimiento tras el reposo) en sus articulaciones, músculos o espalda? ¿Tiene dificultad para vestirse sin ayuda? (si antes lo hacía) ¿Tiene dificultad para subir o bajar escaleras? (si antes lo hacía) Maniobras de detección ¿Qué valora? Observar al paciente de pie y tumbado Actitud espontánea. Exantema. Dismetría. Tumefacción articular. Desviación en valgo/varo. Atrofia muscular. Pies planos Miembros superiores «Mantén las manos extendidas delante de ti» Flexión anterior de hombrosExtensión de codos, carpos y dedos «Pon las palmas hacia arriba y cierra las manos en un puño» Supinación de codosFlexión de las articulaciones de los dedos «Haz pinza con el índice y el pulgar» Destreza manual «Toca las yemas de los dedos con el pulgar de la misma mano» Destreza manual «Mantén juntas las palmas de las manos a la altura de los codos» Extensión de las articulaciones de dedos y carpos «Levanta los brazos, estíralos todo lo que puedas» Extensión de codos y muñecasAbducción de hombros «Pon las manos detrás del cuello» Abducción y rotación externa de hombrosFlexión de codos Hay dolor al apretar los nudillos Articulaciones metacarpofalángicas Miembros inferiores Realizar signo de peloteo rotuliano Tumefacción de rodillas «Extiende y flexiona las rodillas» Flexión y extensión de rodillas Realizar movimientos pasivos de caderas(Flexión pasiva de 90° de las rodillas y rotación interna de la cadera en decúbito prono, es la maniobra más sensible en la exploración de la cadera) Rotación, abducción y flexión de caderas Realizar movimientos pasivos de tobillos Movilidad de articulaciones tibioastragalina y subastragalina Columna y temporomandibulares «Abre mucho la boca»’ Articulaciones temporomandibulares y desviación de la apertura bucal «Mira al techo» Extensión de la columna cervical «Intenta tocar el hombro con la oreja» Flexión lateral de la columna cervical «De pie y con las rodillas extendidas, intenta tocar el suelo» Flexión de la columna toraco-lumbarEscoliosis Deambulación Observar la marcha espontánea«Camina de puntillas»«Camina de talones» Cojera o rechazo de la deambulación Modificado Goff et al.24.
- –
Comparación del lugar afectado con el contralateral sano, para distinguir diferencias de actitud, tamaño, temperatura y color.
- –
Valoración de la deambulación.
Para la exploración de la zona sacroilíaca puede ser de utilidad la maniobra tipo Fabere (http://www.aeped.es/sites/default/files/documentos/cojera.pdf).
Conviene destacar que: 1) en la OmA es típico el dolor a la presión a punta de dedo; 2) las maniobras exploratorias para el diagnóstico de la sacroilitis, tipo Fabere, no son útiles en niños pequeños porque no colaboran bien, y 3) el eritema de la piel suprayacente a una articulación indica afectación de tejidos blandos, no correspondiéndose, en la mayoría de los casos, con una verdadera artritis.
Diagnóstico de la infección osteoarticularDiagnóstico analítico y microbiológicoLa sospecha clínica, la anamnesis y la exploración física son el primer paso hacia el diagnóstico. El resto de las pruebas nos ayudarán a confirmarlo.
- –
Hemograma y reactantes de fase aguda: el aumento de la velocidad de sedimentación globular (VSG), de la proteína C reactiva (PCR) y de otros reactantes de fase aguda es frecuente, aunque inespecífico. Estos valores no suelen estar muy elevados, salvo en etapas evolucionadas. La combinación de PCR y VSG es de gran utilidad para la valoración inicial, siendo improbable la existencia de una IOA si no se elevan los primeros días del ingreso26. La leucocitosis es poco frecuente19.
- –
Hemocultivo: debe recogerse siempre para intentar la identificación del microorganismo responsable, aunque su rentabilidad es < 50%27.
- –
Análisis del líquido articular: la artrocentesis o punción del espacio articular para la extracción de líquido sinovial debería realizarse ante toda sospecha de AS, previo al inicio del tratamiento antibiótico. Así, el análisis citobioquímico del líquido sinovial, aunque inespecífico, nos puede ofrecer una aproximación diagnóstica (tabla 5)15. Generalmente, un recuento > 50.000 células/mm3 con predominio de polimorfonucleares es más indicativo de etiología infecciosa, como lo es una disminución de la glucosa (< 50% de la plasmática).
La identificación del patógeno responsable es el gold standard del diagnóstico de la AS, aunque solo se logra en un 20-80% de los casos6,28. Es ideal enviar, lo antes posible, todo el líquido o material obtenido en un tubo estéril (evitar torundas) para que sea procesado para tinción de Gram y cultivo. La recogida del líquido articular en frasco de hemocultivo aumenta la rentabilidad del aislamiento, en especial ante la sospecha de K. kingae (posiblemente el agente más frecuente cuando los cultivos son negativos)7,29. La técnica de reacción en cadena de polimerasa (RCP) permite identificar esta y otras bacterias con mal crecimiento en cultivo o en infecciones previamente tratadas con antibiótico6,14,30-32.
No se han encontrado, hasta la fecha, unas características biológicas y clínicas de las AS que permitan predecir el patógeno involucrado33,34, salvo la menor edad, menor repercusión clínica y de marcadores inflamatorios de los niños con infección por Kingella19,32,34.
Para el diagnóstico de la artritis tuberculosa conviene recoger una muestra adicional para tinción de Ziehl-Neelsen, cultivo y RCP, pudiendo requerir una biopsia sinovial para el diagnóstico35.
- –
Punción ósea: algunos autores no la consideran necesaria previamente a la instauración del tratamiento antibiótico empírico en la OmA, reservándola para los casos con mala evolución, presencia de abscesos u osteomielitis crónicas6,19. Sin embargo, algunos centros la realizan habitualmente sin complicaciones, con/sin ecografía, permitiendo la identificación del microorganismo hasta en un 40-60% de los casos7.
- –
Prueba de la tuberculina (o pruebas inmumológicas de diagnóstico): debería solicitarse ante la sospecha de tuberculosis osteoarticular, aunque suele cursar de una forma más subaguda o crónica.
El diagnóstico de otras causas infecciosas menos frecuentes podría requerir la realización de otras pruebas específicas (RCP, serologías, etc.).
Pruebas de imagen- –
Radiografía (Rx) simple. La Rx simple continúa teniendo un papel relevante ante la sospecha de una IOA, siendo útil para descartar otras patologías, como fracturas o tumores. En la OmA suele ser normal en los primeros 10-14 días, alcanzando una sensibilidad y especificidad de hasta el 82 y el 92%, respectivamente, a las 2-3 semanas del comienzo del cuadro clínico. Son imágenes características la osteólisis, la osteopenia y la elevación o engrosamiento perióstico36. En la osteomielitis vertebral o espondilodiscitis puede observarse una disminución del espacio intervertebral o erosiones vertebrales en la Rx lateral7. En el caso de la AS, puede objetivarse un aumento del espacio articular y de partes blandas en la fase aguda.
- –
Ecografía. Técnica de gran utilidad en la AS, por ser barata, de fácil acceso y por su elevada sensibilidad. Detecta derrame articular en el 95% de los casos, aunque las características ecográficas no son patognomónicas de infección. Es especialmente importante en el diagnóstico de AS de cadera y hombro dada la dificultad del diagnóstico clínico6,11, y puede ser de gran ayuda para guiar la realización de artrocentesis. La técnica Doppler puede documentar un aumento del flujo vascular, aunque su ausencia no descarta una AS.
- –
En las OmA, es útil para poner de manifiesto abscesos subperiósticos o de partes blandas, pero su normalidad no excluye esta infección6,7,37. Igualmente, puede ser utilidad para la punción ósea guiada. En fases precoces, la presencia de Doppler positivo a nivel óseo orienta hacia la presencia de OmA.
- –
Tomografía computarizada (TC). Aunque no detecta cambios específicos de forma precoz, puede objetivar edema de partes blandas y abscesos profundos extraóseos, pudiendo facilitar la punción-drenaje. Puede resultar útil para el diagnóstico de localizaciones pélvicas o de formas subagudas/crónicas de infección, pudiendo detectar secuestros óseos7. En la actualidad, no suele realizarse por su excesiva radiación.
- –
Resonancia magnética. Es, probablemente, la mejor prueba de imagen para el diagnóstico de OmA, y resulta de gran utilidad en el estudio de lesiones del esqueleto axial y de la pelvis7,12. Si conocemos la localización de la lesión, tiene una alta sensibilidad (97%) y especificidad (92%)7. No obstante, puede presentar dificultad para diferenciar otras lesiones que cursan con edema tisular, como tumores, fracturas, infartos o cambios tras contusión, aunque en la práctica clínica no suele existir este problema diagnóstico. Su coste, la necesidad de sedación en niños pequeños y la menor disponibilidad hacen que, con frecuencia, su uso quede restringido a casos con evolución tórpida o complicada. Sus principales indicaciones, serían: confirmación de osteomielitis, sospecha de complicaciones (absceso/secuestro), osteomielitis vertebral o pélvica, ecografía o gammagrafía no concluyentes de IOA y AS con falta de respuesta al tratamiento antibiótico.
- –
Gammagrafía ósea. A pesar de su escasa especificidad, es una técnica muy sensible para localizar osteomielitis, sacroilitis o espondilodiscitis, así como para descartar multifocalidad. Se ha encontrado una sensibilidad menor en lactantes pequeños o neonatos, y en bacterias muy virulentas como SARM de la comunidad (AC)7,38. Por su facilidad y rapidez, se prefiere como isótopo el tecnecio-99, pero puede dar falsos positivos en otras enfermedades con hiperactividad osteoclástica como fracturas, tumores, infartos óseos o lesiones posquirúrgicas37,39. El galio-67 o los leucocitos marcados se consideran más específicos de cuadro infeccioso activo, pero son técnicas más complejas, requiriendo hasta 48 h para obtener las imágenes39.
- –
Otras técnicas. La TC por emisión de fotón único o la gammagrafía de médula con sulfuro coloidal podrían, en un futuro, tener indicaciones en esta patología.
Aunque, en la mayoría de las situaciones, el diagnóstico de OmA debería confirmarse con una prueba de imagen más allá de la Rx simple, en formas clínicas leves, con buena respuesta al tratamiento, estas podrían no ser necesarias.
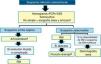
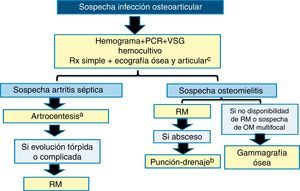
En la figura 1 se muestra un algoritmo para el diagnóstico de la IOA.
Algoritmo diagnóstico de la infección osteoarticular.
a En la artritis séptica de cadera y hombro debe considerarse la realización de descompresión articular lo antes posible (véase el texto).
b La punción-drenaje se podrá realizar guiada por ecografía o tomografía computarizada.
c La ecografía es muy útil para la orientación diagnóstica inicial de la artritis séptica, pero no tanto de la osteomielitis (véase el texto).
En la tabla 6 se muestran las patologías más relevantes a diferenciar con la AS monoarticular, así como características específicas importantes25. La infección de piel y partes blandas o la bursitis de rodilla también deben ser consideradas. En raras ocasiones, la AS será poliarticular, precisando diferenciarla de enfermedades reumatológicas, como lupus eritematoso sistémico, fiebre reumática o artritis idiopática juvenil, así como de artritis reactivas de algunas infecciones11 (tabla 7).
Diagnóstico diferencial de monoartritis
| Edad(años) | Sexo | Líquido sinovial | Datos clave | |||
|---|---|---|---|---|---|---|
| Aspecto | Recuento (células/mm3) | Cultivo o RCP | ||||
| Artritis séptica | < 5 | V | Turbio, purulento | > 50.000 | (+) | Inmovilidad por dolor, afectación del estado general, comienzo agudo |
| Artritis vírica | Amarillo, transparente | < 10.000 | (–) | Generalmente, poliarticularExantema, leucopenia Serología (+) | ||
| Artritis postinfecciosaa | Amarillo, turbio | > 10.000 | (–) | Generalmente, poliarticularAntecedente de faringitis o diarrea | ||
| AIJ (oligoarticular) | < 6 | M | Amarillo, turbio | > 10.000 | (–) | Artritis persistente. ANA (+) |
| AIJ. ArE | > 6 | V | Amarillo, turbio | > 10.000 | (–) | Artritis persistente y/o entesitisHLA B27 (+) |
| Trastorno de coagulación | Hemático | (–) | Hematomas en lugares poco habituales | |||
| Artritis tuberculosa | Amarillo, turbio | 10-20.000 | (+) | Mantoux (+). Rx tórax +/–. Ambiente epidemiológico | ||
| Sinovitis villonodular | Hemático | (–) | Proliferación benigna de sinovialbDiagnóstico por biopsia | |||
| Hemangioma sinovial | Hemático | (–) | Proliferación benigna de vasos sinoviales. Diagnóstico por RM | |||
| Artritis traumática | > 10 | Amarillo o hemático | < 2.000 | (–) | Traumatismo/aumento actividad | |
| Sinovitis transitoria cadera | 3-9 | V | Artrocentesis no indicada | El cuadro clínico permite sospecharlaPuede existir antecedente de infección viral autolimitadaResolución en 5-7 díasPoco frecuente en < 3 años | ||
| Enfermedad de Perthes | 3-9 | V | Artrocentesis no indicada | El cuadro clínico permite sospecharlaAntecedente de episodios de cojeraPrueba de imagen compatible | ||
AIJ: artritis idiopática juvenil; ANA: anticuerpos antinucleares; ArE: artritis relacionada con entesitis; M: mujer; RM: resonancia magnética; RCP: reacción de la polimerasa en cadena; V: varón.
Resumen de recomendaciones y evidencia
| – La OmA y la AS son más frecuentes en menores de 5 años (AI) |
| – El 70% de los casos afecta a los miembros inferiores, generalmente en una única localización (AI) |
| – El microorganismo más frecuentemente aislado en todas las edades es S. aureus (AI). En RN y hasta los 3 meses de edad, son también patógenos importantes S. agalactiae y las enterobacterias (sobre todo E. coli) (AI) |
| – K. kingae es frecuente, sobre todo, en niños entre 3 meses y 5 años de edad, donde es la segunda causa etiológica (AI) |
| – La AS por Salmonella puede ocurrir, rara vez, en niños sanos, pero es más característica de niños inmunodeprimidos y, especialmente, con hemoglobinopatías, como drepanocitosis. La duración del tratamiento debería ser, al menos, de 4-6 semanas (BIII) |
| – La fiebre o febrícula pueden no estar presentes en el momento de la consulta. El síntoma más significativo es el dolor, responsable de la inmovilidad del lugar afectado (AII) |
| – El diagnóstico de las IOA es fundamentalmente clínico, siendo clave el examen físico, apoyándose en los marcadores de inflamación y de imagen y el análisis del líquido sinovial en las AS (AII) |
| – El examen citobioquímico del líquido articular es importante para el diagnóstico de AS, aunque tampoco es específico (BIII) |
| – El diagnóstico definitivo se establece cuando los cultivos (líquido articular, sangre, material óseo) o la RCP son positivos (AI). En el caso de que las pruebas microbiólogicas fueran negativas, el diagnóstico es solo de presunción |
| – En la AS siempre debería realizarse artrocentesis para el diagnóstico y la descompresión del espacio articular (AI). En caso de AS evolucionadas o material más organizado, podría requerir apertura quirúrgica para el drenaje y la obtención de muestras (BII) |
| – Aunque es una práctica habitual en algunos centros que puede ayudar al abordaje de la OmA al aumentar la rentabilidad diagnóstica, la obtención de una muestra ósea para el diagnóstico microbiológico previo al inicio de antibioterapia no es imprescindible para el abordaje de la OmA hematógena no complicada (AII); no obstante, debería valorarse ante la falta de respuesta a la antibioterapia a las 48-72 h del inicio de la misma (BII) y en la OmA no hematógena |
| – Se debe realizar una Rx simple inicial de la zona supuestamente afectada por su disponibilidad, bajo coste y la posibilidad de detectar otras patologías subyacentes o cambios crónicos en controles evolutivos (AII) |
| – La ecografía es la técnica más útil en la valoración inicial de la AS por su elevada sensibilidad para la detección de aumento de líquido articular, aunque las características del derrame articular no son específicas (AII) |
| – Si sospechamos una OmA, la radiología es negativa y no se localiza clínicamente la lesión, se debería realizar una gammagrafía ósea (AII), especialmente ante sospecha de afectación del esqueleto axial y huesos pequeños |
| – La RM constituye la prueba de imagen más específica en las IOA, especialmente en la OmA (AI), pudiendo ser muy útil para descartar o confirmar IOA en caso de dudas en el diagnóstico. En el caso de AS no suele ser necesaria. En las OmA, aunque no tiene por qué realizarse en todas las situaciones, puede ser de mucha utilidad, especialmente en caso de afectación de esqueleto axial, evolución tórpida o sospecha de complicaciones (AII) |
El diagnóstico diferencial se plantea con: 1) celulitis e infecciones de partes blandas, especialmente miositis (a veces asociadas a OmA); 2) fracturas y otras lesiones traumáticas; 3) osteocondrosis, que suelen cursar con signos inflamatorios locales, sin aumento de reactantes de fase aguda y con imagen radiológica típica; 4) tumores benignos (osteoma osteoide, osteoblastoma); 5) tumores malignos, como el sarcoma de Ewing (afectación de partes blandas, fiebre y afectación del estado general), el neuroblastoma (metástasis en hueso) y el osteosarcoma; 6) osteítis inflamatorias asépticas, como la osteomielitis crónica recurrente multifocal (OCRM); 7) histiocitosis de células de Langerhans, que puede cursar clínica y radiológicamente de forma indistinguible de la osteomielitis; 8) enfermedad linfoproliferativa, cuya sintomatología de dolor e inflamación podría confundirse con una OmA8,12, y 9) osteonecrosis por crisis vasooclusivas en la enfermedad de células falciformes8,22. En los infrecuentes casos de localización múltiple (S. aureus, Bartonella, Coxiella), es necesario realizar diagnóstico diferencial con OCRM.
La biopsia ósea y el estudio histológico deberían realizarse cuando el diagnóstico sea dudoso, precisando el procesamiento para cultivo y determinación de RCP de microorganismos menos frecuentes, como hongos y micobacterias. En la tabla 7 se exponen las recomendaciones más relevantes de este consenso con el grado de evidencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses en relación con lo expresado en este documento.
Al Grupo de Infecciones Osteoarticulares de la SERPE.