Introducción
La función principal de la respiración es proporcionar oxígeno a las células del organismo y eliminar el exceso de anhídrido carbónico (CO2). Para ello se emplean dos sistemas: uno transporta el aire, y el otro, la sangre. Su finalidad es el intercambio de gases entre el aire y las células de los tejidos.
El sistema respiratorio utiliza una bomba aérea que transporta el aire exterior hasta las unidades funcionales pulmonares (conductos alveolares y alvéolos). El aparato circulatorio utiliza una bomba, el corazón, que moviliza la sangre a la periferia (células) y los capilares alveolares. El sistema respiratorio consta de una vía aérea de conducción (sin prácticamente intercambio de gases) y los alvéolos, donde se realiza un intercambio rápido de grandes cantidades de oxígeno (O2) y de CO2 (fig. 1).
Figura 1. Unidad funcional pulmonar. Esquema de intercambio de gases entre el compartimento aéreo y el compartimento vascular.
Para llevar a cabo esta función es necesario que la ventilación pulmonar aumente la presión parcial alveolar de oxígeno (PAO2), a un nivel mucho mayor que la que existe en la sangre venosa (PvO2) capilar que llega a los alvéolos, para que esta sangre, destinada a las células, esté cargada de oxígeno. También es necesario disminuir la presión parcial de CO2 de los alvéolos (PACO2) a cifras menores a las de la sangre venosa que llega a los alvéolos, para disminuir la cantidad total de CO2. Así, los gases difunden entre los alvéolos y la sangre capilar, y entre los tejidos y su sangre capilar, alcanzando una homeostasis correcta para el metabolismo adecuado.
Mecánica ventilatoria
El aire fluye de una zona de presión mayor a una zona de presión menor. Cuando la presión gaseosa en los alvéolos es igual a la presión atmosférica (PB), no se produce corriente de aire. Para que haya inspiración es necesario que disminuya la presión alveolar (PA) en frente a la PB. Para que haya espiración, la PA debe ser mayor a la PB.
Hay dos formas de producir la diferencia de presión necesaria para que penetre aire a los pulmones: que la PA sea inferior a la PB o que la PB sea superior a la PA. La respiración normal se lleva a cabo por contracción activa de los músculos respiratorios: el tórax se agranda, disminuyendo la presión intratorácica; se distienden los pulmones, los bronquios, los conductos alveolares y los alvéolos, y disminuye así la PA. El aire, a presión atmosférica, penetra en las vías aéreas.
En la inspiración existe una participación muscular activa. Entre los músculos inspiratorios básicos destacan el diafragma y los músculos intercostales externos; otros como el esternocleidomastoideo y los escalenos también participan en la inspiración de modo accesorio (fig. 2). En la espiración normal la participación muscular es más pasiva que en la inspiración, y destaca la función que desempeñan los músculos intercostales internos y el diafragma. En situaciones de ventilación máxima o de obstrucción de la vía de conducción aérea, la participación de los músculos intercostales internos y los abdominales (oblicuo mayor del abdomen, recto, oblicuo menor y transverso del abdomen) en la espiración es muy activa.
Figura 2. Estructura anatómica de la caja torácica.
Sin embargo, los músculos respiratorios no tienen un ritmo contráctil propio. Se contraen sólo si reciben impulsos nerviosos procedentes de los centros respiratorios del troncoencéfalo, aunque estos impulsos también pueden proceder de la corteza cerebral y de la medula, como respuesta en este caso a aferentes sensitivos periféricos (pH, PO2 y PCO2 arteriales; pH y PO2 tisulares). Es decir, existe un control automático de la respiración, pero a diferencia de otras actividades automáticas involuntarias, la respiración también tiene un control voluntario. Y ambos sistemas de control de la respiración, automático y voluntario, están estrechamente relacionados.
Volúmenes y capacidades pulmonares
La fuerza de los músculos respiratorios se determina a partir de las presiones respiratorias estáticas máximas; es decir, la máxima presión que se genera durante una maniobra inspiratoria o espiratoria forzada. La medición de las presiones respiratorias estáticas resulta útil en los pacientes, fundamentalmente en aquellos con enfermedad neuromuscular. Mayor interés tiene los volúmenes y las capacidades pulmonares (fig. 3) que se definen a continuación:
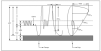
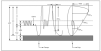
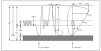
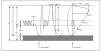
Figura 3. Diagrama de volúmenes y flujos respiratorios. *No determinado por espirometría.
1. Volúmenes pulmonares:
a)El volumen corriente (VC) en una respiración normal es el volumen de aire que entra en los pulmones durante la inspiración y sale de ellos durante la espiración.
b)El volumen de reserva espiratorio (VRE) es el máximo volumen que puede exhalarse después de una espiración normal.
c)El volumen de reserva inspiratorio (VRI), que es el volumen máximo de gas que puede inhalarse a partir de una inspiración normal.
d)El volumen residual (VR), que es el volumen de aire que queda en los pulmones después de una espiración máxima.
2. Capacidades pulmonares:
a)La capacidad vital (CV) es el máximo volumen de aire que puede exhalarse después de una inspiración máxima.
b)El volumen de aire que queda dentro de los pulmones al final de la espiración, durante una respiración normal, se denomina capacidad residual funcional (CRF).
c)La capacidad inspiratoria (CI) es el volumen máximo de aire que puede ser inhalado, partiendo de la CRF.
d)La capacidad pulmonar total (CPT) es el volumen de aire contenido en los pulmones después de una inspiración máxima.
La mayoría de las variables señaladas pueden medirse mediante espirometría convencional. Sin embargo, para medir la CPT, el VR y la CRF, se necesitan otras técnicas (pletismografía corporal).
La espirometría mide el volumen de aire exhalado durante una maniobra espiratoria máxima. Comienza desde la CPT y termina al alcanzar el VR. En espiración es habitual determinar los siguientes parámetros:
1. FVC: capacidad vital forzada.
2. FEV1: volumen espiratorio máximo en el primer segundo.
3. Relación FEV1/FVC.
4. FEM: flujo espiratorio máximo o máximo flujo espirado.
5. FEF25-75: flujo espirado forzado entre el 25 y el 75 % de la FVC.
La pletismografía mide el volumen de gas torácico (TGV) y, además, permite medir las resistencias de las vías respiratorias (sRaw, sGaw).
Cuando existe una obstrucción en la vía de conducción aérea, extratorácica o intratorácica, se producen modificaciones en los volúmenes y en las capacidades pulmonares de mayor o menor magnitud, según el grado de obstrucción. Cuando hay procesos restrictivos (no obstructivos), también se modifican los volúmenes y las capacidades pulmonares. Sin establecer criterios universales, desde el punto de vista docente, cabe señalar que un proceso obstructivo se caracteriza por limitar el flujo durante la espiración, es decir, por disminuir el flujo espiratorio produciendo:
1. Disminución del FEV1, con FVC en rangos normales.
2. Disminución de la relación FEV1/FVC (inferior al 75 %).
3. Aumento del VR, al quedar atrapado aire al final de la espiración.
4. Incremento de la relación VR/CPT.
5. Aumento de las resistencias de las vías respiratorias (sRaw).
Estos cambios, cuando se estudia la función pulmonar en situación basal, proporcionan una visión estática del problema. Las variables que definen los cambios pueden encontrarse en límites normales en relación con los valores teóricos poblacionales, o expresar limitaciones ligadas a la propia técnica de la medida que requiere con frecuencia una importante colaboración por parte del niño. De ahí que sea necesario contrastar estos resultados con los obtenidos tras la administración de fármacos broncodilatadores.
Reversibilidad de la obstrucción
La obstrucción bronquial se caracteriza:
1. Por la disminución de los flujos aéreos intrapulmonares.
2. Por el aumento de los volúmenes intrapulmonares.
La cuestión, desde el punto de vista funcional pulmonar, consiste en determinar cuánto deben disminuir los flujos o cuánto tienen que aumentar los volúmenes para considerar que existe obstrucción bronquial. Los valores de normalidad, cuanto existen, sólo son una referencia aproximada, y no existen valores de normalidad en niños para todas las variables de función pulmonar.
Por ello, la respuesta a la pregunta viene dada bajo otra formulación: se mide la función pulmonar basal, se administra medicación broncodilatadora y vuelve a medirse la función pulmonar; si se produce una mejoría evidente, podría afirmarse que existe una limitación del flujo aéreo intrapulmonar, reversible total o parcialmente con broncodilatadores, es decir, que existe una obstrucción bronquial.
El test de broncodilatación se realiza habitualmente midiendo una variable de función pulmonar que sea reproducible (escasa variabilidad intraindividual e interindividual). En espirometría forzada se utiliza el FEV1. En pletismografía, la sGaw o conductancia específica de las vías respiratorias (la recíproca de la resistencia específica de las vías respiratorias). La metodología consiste en realizar la función pulmonar basal. A continuación se administran 400 mg de salbutamol con aerosol dosificador presurizado con cámara espaciadora y 10-15 min después se repite la determinación de la función pulmonar.
El test de broncodilatación se considera positivo si se dan las siguientes circunstancias:
1. El índice de broncodilatación respecto al teórico es igual o superior al 9 % ([FEV1 pos-FEV1 pre/FEV1 teórico] * 100).
2. El índice porcentual de la sGaw es igual o superior a 35 % ([sGaw post-sGaw pre/sGaw pre] * 100).
Test de provocación específicos e inespecíficos
La respuesta bronquial se evalúa mediante diferentes estímulos que provocan broncoconstricción1. Se clasifican en estímulos directos e indirectos: los directos provocan broncoconstricción actuando directamente sobre los receptores específicos del músculo liso; los indirectos inducen broncoconstricción a través de la activación completa de la vía metabólica, como los mastocitos y sus mediadores, los reflejos neurogénicos, etc. También hay que tener en cuenta que, conceptualmente, los estímulos "específicos" (alergenos) pertenecen al grupo de los indirectos2.
Métodos directos
Los estímulos directos son aquellos que actúan directamente sobre los efectores postsinápticos: musculatura lisa y microcirculación de la vía respiratoria (histamina, derivados de la acetilcolina, bradicinina, leucotrienos C y D4). Los más habituales son los farmacológicos, realizados con histamina, metacolina y carbacol. Los métodos empleados por la mayoría de los autores que trabajan en hiperreactividad bronquial3 son los dos siguientes:
1. Inhalación de cantidades conocidas de las sustancias dispensadas a través de un dosímetro activado por la inspiración.
2. Inhalación de concentraciones conocidas de la sustancia inhalada durante un tiempo predeterminado en el transcurso de una respiración corriente.
Los resultados se expresan como dosis (PD20) o como concentración (PC20) que provocan un descenso del FEV1 del 20 % o más respecto al basal. También se estudia la pendiente de la curva dosis-respuesta o reactividad y el efecto máximo o plateau4.
Métodos indirectos
Los estímulos indirectos son aquellos que actúan sobre la musculatura lisa y la microcirculación de la vía respiratoria, a través de la estimulación local de las células que liberan determinados mediadores bioquímicos (ejercicio físico, hiperventilación isocápnica de aire seco o frío, inhalación de soluciones hiperosmolares o hipoosmolares, inhalación de metabisulfito o adenosina-5-monofosfato). El aire frío inhalado y el test de ejercicio (tapiz rodante, bicicleta, carrera libre) son los de uso más habituales en investigación y diagnóstico clínico, fundamentalmente este último.
En la clínica práctica, el incremento de la respuesta bronquial o hiperreactividad bronquial (HRB) se mide mediante la prueba de ejercicio (estímulo indirecto) o por la respuesta a la metacolina (estímulo directo). Se considera que cuando la sintomatología y los resultados espirométricos son dudosos, una hiperrespuesta positiva es diagnóstica de asma.
La HRB no es sinónimo de broncoconstricción propiamente dicha. La broncoconstricción que se produce puede ser debida a que hay un umbral de excitabilidad particularmente bajo, un acortamiento excesivo de la fibra muscular, un aumento de la contractibilidad o una hipertrofia o hiperplasia del músculo liso.
En resumen, el término HRB expresa una respuesta bronquial excesiva a estímulos que no producen obstrucción bronquial excepto en cantidades considerables5.
Interpretación de la exploración funcional respiratoria
Teóricamente, los métodos de estudio de la función pulmonar producen mediciones objetivas6: por mediciones se entienden las observaciones que describen los fenómenos en términos que pueden analizarse estadísticamente; por objetivas, se indica que su valor no depende de la interpretación del observador.
Para que una medida de función pulmonar sea válida, se requiere que la medida sea precisa y que la medida sea exacta: precisión significa que la medición produce siempre el mismo valor cada vez que se realiza; exactitud es el grado en el cual esta variable representa lo que se intenta medir.
Precisión
La precisión y los conceptos que incluye, como la fiabilidad o repetibilidad y la consistencia, están amenazados por los errores al azar. Los errores aleatorios que afectan la precisión disminuyéndola pueden provenir de la variabilidad del observador, de la variabilidad de los sujetos medidos (variabilidad biológica) y de la variabilidad de los instrumentos de medida. Para cuantificar la precisión se utilizan términos estadísticos, siendo los más habituales la desviación estándar (DE) y el coeficiente de variación. La precisión también se evalúa por la consistencia de los resultados a través de distintos métodos:
1. Consistencia test-retest (concordancia entre mediciones del mismo sujeto).
2. Consistencia interna (concordancia entre dos variables que miden el mismo fenómeno).
3. Consistencia interobservador e intraobservador (concordancia entre las observaciones realizadas por dos observadores a los mismos sujetos).
Para aumentar la precisión de una medición en función pulmonar se han diseñado distintas estrategias:
1. Estandarizar el método de medida (que debe constar en el manual de operaciones, donde se especifica cómo debe hacerse la medición).
2. Entrenar y certificar a los observadores.
3. Puesta a punto de los instrumentos empleados.
4. Automatizar al máximo la medición.
5. Repetir las mediciones.
Las dos primeras estrategias deben emplearse siempre en el estudio de la función pulmonar. La última es un recurso que se utiliza únicamente cuando las otras estrategias han fallado o no son posibles.
Exactitud
La exactitud de una variable (FEV1, sGaw, etc.) expresa el grado que realmente representa lo que se intenta medir. La exactitud es función del error sistemático o sesgo que actúa disminuyendo la exactitud y puede proceder de:
1. Sesgo del observador (distorsión contante, consciente o inconsciente, de las mediciones que realiza ese observador).
2. Sesgo del sujeto (distorsión constante de la medida debida al sujeto observado).
3. Sesgo del instrumento (error mecánico o electrónico del instrumento, por ejemplo, hardware, software, etc.).
La exactitud puede cuantificarse comparando los resultados con los obtenidos mediante el "patrón oro". Se expresa como la relación entre la diferencia media y el valor real.
Las estrategias para aumentar la exactitud son las siguientes:
1. Mediciones sin conocimiento del sujeto.
2. Mediciones ciegas.
3. Calibración del instrumental de medida de la función pulmonar.
Para finalizar, cabe recordar que el sistema de medida de la función pulmonar tiene que ser lo suficientemente sensible para detectar diferencia en aquellos aspectos de la patología respiratoria que el investigador considere de importancia (p. ej., obstrucción del flujo aéreo intrapulmonar en ausencia de síntomas clínicos); debe ser lo suficientemente específico, para que represente solamente la característica de interés; ha de ser apropiado al objetivo del estudio, y las medidas deben poseer una distribución adecuada de respuesta en la población de estudio (v. fig. 4).
Figura 4. Relaciones entre volúmenes respiratorios, flujos y tiempos. CI: capacidad inspiratoria; CPT: capacidad pulmonar total; CV: capacidad vital; FEV1: volumen espiratorio máximo en el primer segundo; FEM: flujo espiratorio máximo; TGV: volumen de gas torácico; VC: volumen corriente; VR: volumen residual; VRE: volumen de reserva espiratorio.
En conclusión, no parece tan fácil ni tan universal el estudio de la obstrucción bronquial en el niño. La estandarización de las técnicas y una rigurosa metodología contribuyen a realizar medidas próximas a la realidad funcional que tiene aplicabilidad clínica. Lo contrario sería irreal.
Alteraciones de la transferencia gaseosa
La transferencia o intercambio pulmonar de gases no es uniforme. Existen unidades funcionales pulmonares con diferentes ratios ventilación/perfusión (·VA/ ·Q) y, por tanto, diferentes valores de PAO2 y PACO2. De ahí que se consideren tres compartimentos pulmonares para el intercambio de gases: el ideal, donde existe un equilibrio perfecto entre la ventilación y la perfusión; uno sin ventilación pero con perfusión adecuada ( ·VA/ ·Q = 0, efecto shunt); y otro ventilado y no perfundido ( ·VA/ ·Q = , efecto espacio muerto).
En las enfermedades obstructivas de la vía respiratoria (bronquiolitis, asma) existen zonas pulmonares (unidades pulmonares funcionales) sin ventilación y bien perfundidas donde se produce un cortocircuito sanguíneo (mezcla venosa). Pero también existen unidades pulmonares funcionales bien ventiladas y no perfundidas, que se comportan, en términos de fisiología respiratoria, como espacio muerto. Cuanto mayor es la obstrucción al flujo aéreo intrapulmonar, más evidentes son los mecanismos que se ponen en marcha para conseguir una homeostasis adecuada: taquipnea, polipnea, disnea inspiratoria y espiratoria, tiraje subcostal e intercostal, aleteo nasal, quejido espiratorio, etc., hasta el extremo de que estos mecanismos de compensación hacen que en obstrucciones graves predomine un patrón "cuasi normal" de gases arteriales en cuanto al pH, pCO2, exceso de bases y bicarbonato actual, con ligera hipoxemia respirando oxígeno ambiente e hipoxemia manifiesta a concentraciones elevadas de oxígeno. Sólo en las fases finales, cuando el cuadro obstructivo está muy evolucionado, se aprecia un patrón característico de fallo ventilatorio agudo con hipoxemia.
*Nicolás Cobos Barroso - Unidad de Neumología Pediátrica y Fibrosis Quística. Hospital Universitario Materno-Infantil Vall d'Hebron. Barcelona. Amparo Escribano Montaner - Unidad de Neumología Infantil. Hospital Clínico Universitario. Universidad de Valencia. Gloria García Hernández - Sección de Neumología y Alergia Pediátricas. Hospital 12 de Octubre. Madrid. Eduardo González Pérez-Yarza - Unidad de Neumología Infantil. Hospital Donostia. Servicio Vasco de Salud-Osakidetza. San Sebastián. Santos Liñán Cortés- Unidad de Neumología Pediátrica y Fibrosis Quística. Hospital Universitario Materno-Infantil Vall d'Hebron. Barcelona. Martín Navarro Merino - Sección de Neumología Infantil. Hospital Universitario Virgen de la Macarena. Sevilla. Concepción Oliva Hernández - Unidad de Neumología. Departamento de Pediatría. Hospital Ntra. Sra. de la Candelaria. Santa Cruz de Tenerife. Javier Pérez Frías - Sección de Neumología Pediátrica. Hospital Materno-Infantil Carlos Haya. Málaga. Josep Sirvent Gómez - Unidad de Neumología Pediátrica. Hospital Juan Canalejo. A Coruña. José Ramón Villa Asensi - Sección de Neumología Infantil. Hospital Universitario Infantil del Niño Jesús. Madrid.