Se evalúa el protocolo de cribado de hipoacusia neonatal en un hospital comarcal.
PacientesAnálisis en 14.247 recién nacidos en la maternidad del centro desde el año 2002 al 2013 inclusive.
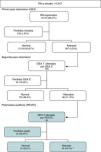
MétodosProtocolo con registro de otoemisiones bilaterales (registro inicial y repetición si falla, al mes de vida) y potenciales auditivos (confirmación).
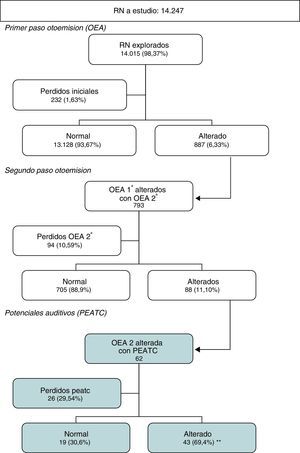
ResultadosSe realizó la prueba antes del alta a 14.015 neonatos (98,3% de la muestra) cumpliendo así los objetivos de cobertura del cribado. En el primer paso resultaron normales el 93,7%, lo que implica una adecuada tasa de paso y no obliga a excesivas repeticiones. La segunda determinación obtiene también buenos resultados, puesto que el 88,9% de los que acuden resultan normales, dejando solo un 0,63% del grupo inicial para valorar con potenciales. Un 10,6% no acude a la cita, lo que constituye el principal problema detectado. En los remitidos a potenciales esta pérdida es mayor, con un 29,5%, a pesar de que la rentabilidad en aquellos pacientes que se exploran con esta técnica es muy alta dado que el 69,4% de ellos presenta unos potenciales alterados. Esta cifra de alterados representa el 0,31% del total de recién nacidos estudiados, cifra similar a la incidencia de sordera congénita. Teniendo en cuenta las pérdidas en seguimiento referidas la incidencia real podría ser mayor.
ConclusionesEl programa es muy útil pero necesita un control estricto del seguimiento para evitar pérdidas de pacientes. Para ello es fundamental tener una base de datos dedicada y un coordinador del programa.
A critical analysis is performed on the results of a newborn hearing screening program in a regional hospital.
PatientsScreening results from 14,247 newborns in our maternity ward from 2002 to 2013.
MethodsTwo step recordings of bilateral otoacoustic emissions (initial and repeat, if failed, at about one month of life). Assessment by clinical brainstem responses.
ResultsThe first step was performed on 14,015 newborns (98.3% of the total) reaching the screening objective. The first step pass figures were 93.7%, which implies a good pass rate with a few patients to repeat.
The second step is also good because it has a pass rate of 88.9% of newborns examined (only 0.63% of initial group needed brainstem responses assessment), but 10.6% were lost to follow up, and that is a major problem.
In newborns, scheduled for brainstem responses, the loss to follow-up is worse, with a figure of 29.5%, despite the high accuracy of this test given that 69.4% of those assessed showed hearing loss. This figure represents a 0.31% of the initial group, and is a similar to that published for congenital hearing loss. Including patients that were lost to follow up this figure could be greater.
ConclusionNewborn hearing screening is useful but needs stronger control to avoid the follow up loss. In order to achieve this, it is crucial to have a good database and a screening coordinator.
Nadie duda de la importancia que la audición normal tiene para el desarrollo psicológico y social del niño, y en particular para la adquisición de esa cualidad exclusivamente humana que es el habla. De ahí la necesidad de determinar lo más pronto posible la existencia de alteraciones en la audición. Esto último no ha sido tarea fácil, especialmente en el recién nacido, del que se ha pensado, hasta hace poco, que no era apto para someterse a pruebas objetivas de audición, ni se podían corregir sus defectos auditivos cuando se descubrían.
El programa de cribado neonatal de hipoacusia en la Comunidad Valenciana se comenzó a instaurar en todos los hospitales públicos a partir de finales de 20011. Su finalidad es el diagnóstico precoz de esta patología congénita para permitir el inicio del tratamiento sobre los 6-12 meses de vida, lo que redundará en un mejor pronóstico final, existiendo numerosas publicaciones que así lo demuestran2-5, siendo pues injustificable que un niño presente retraso de desarrollo por un diagnóstico tardío y esto puede tener implicaciones legales6.
Hasta el momento, en España, existe escasa información disponible de los resultados de la fase inicial del cribado y no existe apenas información del final del proceso Es pues necesario saber cuántos de los niños estudiados en el programa de cribado presentan resultados alterados en la prueba de confirmación que obliga a remitirlos para control y/o tratamiento.
El objetivo del presente estudio es evaluar el proceso y el resultado del protocolo de cribado que se lleva a cabo en la maternidad de nuestro hospital, lo que permitirá conocer sus puntos fuertes y debilidades, así como la rentabilidad del programa.
Material y métodosMaterialCriterios de inclusión: todos los recién nacidos en la maternidad del Hospital Comarcal de Gandía (Valencia), desde el año 2002 al 2013 inclusive, con edad entre 24 y 72 h de vida.
Criterios de exclusión: neonatos en los que no se han podido realizar las otoemisiones con esa edad.
MétodosSe valoran y analizan los resultados de la primera determinación de otoemisiones acústicas evocadas (OEA). De ahí se extrae a los niños con resultados alterados en la primera prueba y se comprueba si han pasado a la segunda y su resultado. Posteriormente, se seleccionan los patológicos al segundo paso de otoemisiones, que son remitidos a potenciales auditivos (PEATC), para conocer el resultado de estos.
Protocolo de cribado: el protocolo se articula en 3 pasos. En el primero, a todos los recién nacidos se les realiza una determinación de OEA bilateral lo más cercana posible al alta en la maternidad (sobre las 48h), la realizan todas las enfermeras, durante todos los turnos, según disponibilidad y presión asistencial. Se realiza sin sedación, mientras el niño está tranquilo en una habitación de la misma sala o incluso en su cuna dentro de la habitación. Si sale normal es alta y si sale alterada se remite a consultas externas para repetirla sobre el mes de vida. Allí es repetida por una enfermera dedicada, si sale normal es alta y si sale alterada se remite al Servicio de Neurofisiología para realizar potenciales auditivos evocados con sedación, si estos son patológicos se remite al otorrinolaringólogo (ORL) para valoración y tratamiento, si procede.
TécnicasOtoemisiones acústicas evocadas (OEA): la técnica empleada es la recogida de OEA con ECHOCHECK OAE Screener® basado en el sistema ILO 88 (Otodynamics Ltd.), unido a la sonda ILO ECP® neonatal (Otodynamics Ltd.). Se trata de un equipo automatizado. Emplea un estímulo de tipo clic no lineal de 1ms de duración cuya intensidad es de 84±3 decibelios (dB) «sound pressure level» a una frecuencia de 80 ciclos/s. El resultado normal exige una respuesta espectral por encima del ruido ambiente con un nivel de señal/ruido mayor de 6dB. Solo se acepta como no patológico el resultado normal bilateral. Tras información y consentimiento verbal, se realiza la prueba en una habitación en la maternidad con escaso ruido de fondo y con la madre presente. Se suele aprovechar el horario posprandial para que el neonato esté tranquilo.
PEATC: los PEATC se realizan en el Servicio de Neurofisiología empleando en todos los pacientes un equipo mixto de electromiografía y potenciales evocados Modelo Viking IV-D de la marca Nicolet® (Natus Med. Inc.).
El paciente acude a la consulta privado de sueño en lo posible y se le administran 0,3ml por kilogramo de peso de una solución de hidrato de cloral (100 mg/ml) para inducir el sueño. Se le colocan los electrodos según el sistema internacional 10/20 y un estimulador tipo casco.
Se realiza una serie en cada oído con estímulo tipo clic alternante a 27,7Hz y a intensidades de 80, 60, 50, 40 y 30dB, con ruido de enmascaramiento contralateral a –30dB para cada serie. Siempre realizando 2 pruebas en cada nivel.
Los parámetros de adquisición fueron: filtro alto a 3 Khz, filtro bajo a 150Hz, filtro de red a 50Hz. Se promediaron 1.500 estímulos en cada test (2 por nivel).
Se midieron las latencias e interlatencias de las ondas i, iii y v en el nivel de 80dB, marcando la latencia de la onda v en el resto de niveles. Se consideró el umbral auditivo de cada oído como el nivel más bajo en el que se pudo medir la onda v.
El Servicio de Neurofisiología realiza la interpretación del estudio y su informe final. Se considera un umbral auditivo alterado cuando es superior a 30dB «hearing level».
Análisis de datos: los resultados se almacenan en una base de datos Access® (Microsoft Co.). El análisis se ha realizado en una hoja de cálculo Excel® (Microsoft Co.) y el paquete estadístico SPSS 20.0® (IBM Co.).
Variables de estudio- –
Resultado de la primera y la segunda determinaciones de otoemisiones (normal/alterado).
- –
Resultado de la determinación de potenciales auditivos (normal/alterado), y en los alterados, distribución del umbral en dB.
El grupo susceptible de estudio incluye a 14.247 neonatos.
Los resultados se exponen en las tablas 1–7 y la figura 1.
Pérdida de pacientes en proceso y seguimiento por años
| % | % | % | |
|---|---|---|---|
| Año | Fallos 1.ª OEA | Fallos 2.ª OEA | Fallos PEATC |
| 2002 | 0,1 | 28,1 | 0 |
| 2003 | 0,3 | 23 | 10 |
| 2004 | 0,2 | 23,1 | 0 |
| 2005 | 0,1 | 8,6 | 20 |
| 2006 | 0,2 | 15,7 | 20 |
| 2007 | 0,1 | 25,5 | 0 |
| 2008 | 0,1 | 5,1 | 17,6 |
| 2009 | 0 | 6,4 | 0 |
| 2010 | 0 | 8,4 | 23,1 |
| 2011 | 0 | 8,4 | 33,3 |
| 2012 | 0 | 6,6 | 54,5 |
| 2013 | 0 | 4,3 | 50 |
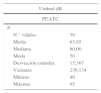
Distribución agrupada según umbral de pérdida auditiva de los niños con potenciales alterados (n=39)
| PEATC, dB | Frecuencia | Porcentaje explorados | Acumulado porcentaje |
|---|---|---|---|
| 40 | 3 | 7,7 | 7,7 |
| 50 | 12 | 30,8 | 38,5 |
| 60 | 7 | 17,9 | 56,4 |
| 70 | 4 | 10,3 | 66,7 |
| 80 | 10 | 25,6 | 92,3 |
| 85 | 1 | 2,6 | 94,9 |
| 90 | 1 | 2,6 | 97,4 |
| 95 | 1 | 2,6 | 100,0 |
| Total | 39 | 100,0 | |
La primera determinación (tablas 1 y 2) se realizó en la maternidad al 98,3% de niños, con un escaso 1,7% de niños que no se hacen la prueba allí por diversos motivos, como no estar adecuado el niño, avería de sonda/aparato, sobrecarga asistencial, etc., citándose a consulta externa (datos no incluidos).
La segunda determinación en consultas externas (tabla 3) debería haberse realizado a 887 niños pero acudieron a repetírsela 793. De este grupo, un 88,9% de ellas resultaron normales y un 11,1% alteradas (un 0,6% del grupo inicial), citándose estos a potenciales auditivos (n=88).
Un 0,1% global de recién nacidos iniciales no se hizo la prueba por no autorizarlo los padres, aunque los últimos años se ha realizado al 100% de neonatos (tabla 4) y en el análisis de las pérdidas en seguimiento se ha registrado un 10,6% de pérdidas en la segunda prueba, aunque por años se aprecia una tendencia descendente, siendo en los últimos solo del 4%.
De los citados a potenciales y explorados (tabla 5) resultaron alterados un 69,4% y normales el 30,6%, es decir, 2/3 son patológicos. Se determinó el umbral de los patológicos (tablas 6 y 7) en 39 casos, siendo lo más frecuente 50dB con un 30,8%, seguido de 80dB con un 25,6%. Las pérdidas en seguimiento de los potenciales por años oscilan mucho (tabla 4) y tienen un promedio del 29,5% (tabla 5).
DiscusiónLa hipoacusia cumple todos los requisitos para ser una enfermedad de cribado y actualmente existen métodos seguros para su diagnóstico. En nuestro protocolo empleamos las otoemisiones por ser el método más barato, rápido y fácil7,8, con adecuada sensibilidad y especificidad2,9.
El proceso está integrado en la labor diaria asistencial y, por tanto, es realizado por todo el personal de enfermería disponible en las salas. Existen estudios que demuestran que para llevarlo a cabo no se necesita personal especialmente dedicado10,11.
Resultados del proceso con otoemisionesLa cifra del 98,3% de cobertura (tabla 1) cumple perfectamente los objetivos del cribado que necesita incluir más del 95% de la población diana para ser válido9. De los niños explorados (tabla 2), un 93,7% resultaron normales en la primera determinación, lo que deja solo un 6,3% para recitar a una segunda prueba, siendo esta cifra más que aceptable y similar a los protocolos realizados con potenciales automáticos que registran porcentajes del 4%7. En cualquier caso, este volumen de repeticiones es fácilmente asumible por una o 2 personas en consulta externa que sean expertas. Estas sirven de filtro mucho mejor y así a PEATC/ORL se remiten menos niños.
La segunda determinación en consultas externas (tabla 3) presenta una cifra de alterados del 11,1% (un 0,6% del grupo inicial). Esta cifra es muy inferior al 4% del grupo inicial que recomienda la CODEPEH9 como índice de buen funcionamiento. Hay que recordar que la incidencia de hipoacusia en series muy amplias publicadas oscila entre el 0,2 y el 0,6%12-14.
De nuestros resultados, se puede deducir pues que gran parte de los neonatos remitidos inicialmente a consultas externas serán normales (el 89%). Esto está plenamente justificado por la mejora de la otoemisión con el paso del tiempo. Por eso, la repetición de la prueba tiene una alta rentabilidad incluso en intervalos cortos pero se maximiza a partir de los 21 días, lo que justifica que se repita la prueba sobre el mes15.
Se podría argumentar que, hipotéticamente, estos niños sanos que fallan la primera determinación se evitarían haciendo la prueba inicial a los 15-30 días de vida, cuando la respuesta es más intensa, pero este proceder aumenta el riesgo de pérdidas en seguimiento, que es uno de los problemas de los programas de cribado.
Las pérdidas en seguimiento, en este estudio, demuestran una tendencia anual descendente (tabla 4), siendo en los últimos años solo del 4% porque, tras sufrir 2 averías del aparato de OEA los años previos que provocaron pérdidas del 15 al 25%, se compró uno de recambio y porque se insiste más a los padres incluso por vía telefónica. Los primeros años sí que existían un 23% de pérdidas por inmadurez del programa. Estas cifras, aunque llamativas, no son extrañas en otros protocolos, como demuestra Akinpelu et al.15 en su revisión sobre 558 artículos de protocolos de cribado con otoemisiones que muestran cifras de pérdidas que oscilan entre el 0% (para estudios pequeños) y el 11% (en estudios más grandes). También Metzger- Müller et al.16 refieren unas pérdidas para la segunda prueba del 13% en Suiza, demostrando que es un problema global que se da también en países desarrollados. Las causas hay que buscarlas en varios frentes que implican déficits en las capacidades del sistema de salud y en los conocimientos del programa de los sanitarios del área, déficits de información y contacto con las familias y también de coordinación. Para disminuir este problema, es necesario que exista una buena base de datos para el seguimiento y un coordinador que se encargue de controlar todo el proceso.
Resultados de los potenciales auditivos solicitados (tablas 5-7)La cifra de alterados (69,4%) representa el 0,31% del total de recién nacidos incluidos en la muestra, siendo concordante con las publicadas en diversos estudios parecidos con un 0,36%17. Este resultado es similar a la incidencia de sordera real (0,1 a 0,6%) referida1, lo que demuestra una alta rentabilidad de la prueba (tabla 5) con 2/3 de los explorados finalmente patológicos, de los cuales un 56,4% presenta una sordera leve-moderada (< 60dB) y el resto son sorderas graves, siendo esta una alta incidencia.
Un problema serio de los potenciales es la negativa de los padres a hacer la prueba, con un 29,5% que no acuden a la cita (tabla 5). Aunque las cifras en porcentajes varían mucho por años (tabla 4), porque al ser pocos casos cada fallo pesa mucho, lo cierto es que se aprecia que ha ido en aumento y no se ha podido mejorar a pesar insistir en su importancia vía telefónica. En este aspecto, necesitaría revisión el hecho de sedarlos con hidrato de cloral por el miedo de los padres a tener complicaciones. Este problema también ha sido referido por otros estudios en zonas desarrolladas como Bélgica18, con cifras de pérdida del 42,6%, o EE. UU.19, con un 45,1%, y es un hecho dramático puesto que estos niños tienen un riesgo muy elevado de presentar sordera.
Acerca del protocolo realizadoHay varios trabajos de análisis de coste beneficio y todos concluyen que el cribado de cualquier forma es útil. Respecto a los protocolos, los estudios más recientes6 refieren un coste más eficiente para los protocolos basados en 2 pasos (OEA y después PEATC) en población normal. Hay otros estudios7,8 que prefieren PEATC para todos los pacientes sobre la base de una mejor tasa de paso pero esto depende mucho de la adecuada realización de las OEA; nuestras tasas de paso son muy similares a las que se consiguen con potenciales.
Un factor crucial para conseguir altas tasa de paso son las horas de vida del neonato15,20, siendo óptimo a partir de las 48h, afectándose más las OEA (más sensibles a patología del oído medio) que los PEATC10.
En poblaciones de alto riesgo sería más eficiente el estudio con un solo paso de PEATC, siguiendo las recomendaciones de la CODEPEH9. En nuestro hospital, los niños de riesgo se remiten siempre al ORL para control, aunque tengan resultados normales.
El coste del aparataje y consumibles de los PEATC es mucho más alto y también necesitan más tiempo que las OEA, entre el doble7,8 y 5 veces más10,20, cosa a tener muy en cuenta cuando se manejan grandes poblaciones.
Personal dedicado vs. no dedicadoEn nuestro estudio, todas las enfermeras del servicio hacen las otoemisiones en el momento más adecuado por nivel de ruido bajo y/o escasa presión asistencial. El hecho de no tener personal especialmente dedicado podría tener el problema de una cifra alta de referencia en primer paso por errores en la realización, pero en realidad se ve que es solo del 6%. Este enfoque permite que no haya pérdidas por festivos/bajas del personal9.
Otros factores a considerarA nivel práctico, es muy útil tener al menos 2 aparatos para asegurar la realización sin fallos ante averías.
También ha resultado muy útil la figura del coordinador del programa para analizar la marcha del programa y como figura de referencia para solventar problemas asociados, formar y apoyar a las enfermeras, recuperar pacientes y servir de retroalimentación positiva a todos los implicados19.
Asimismo es fundamental una amplia información previa a los padres que insista en la importancia de la prueba y su significado, y reduzca así la ansiedad que puede generar la prueba y un hipotético resultado alterado.
Limitaciones del estudioEl problema más importante que se ha constatado es la pérdida de los pacientes a lo largo de todo el proceso de cribado. Como ya se ha comentado, es un problema ya descrito en muchas otras publicaciones, incluso en países avanzados, como Suiza16, EE. UU.19 o Bélgica18, pero implica que, en nuestro estudio y con las cifras de alterados de cada paso descritas, se habrían perdido 15 pacientes patológicos en el primer paso, 10 pacientes patológicos en el segundo y hasta 18 niños patológicos en los potenciales, con una sordera para seguimiento por ORL.
Los niños perdidos en proceso son niños de riesgo que se deben minimizar al máximo y que podrían haber variado las cifras de incidencia referidas en este trabajo; son ellos el talón de Aquiles de estos programas, por lo que se necesitan estudios más amplios que incidan sobre estas poblaciones perdidas, que son muy difíciles de captar, para conocer la incidencia global real de sordera, que será previsiblemente más alta.
Lo esperanzador es que se ha observado que este porcentaje de pérdidas se reduce con la implantación del programa, De hecho, si se analizan los 3 últimos años del programa, la cobertura en maternidad sube al 100%, bajando también los que no acuden a consulta externa para repetir al 4%, cifras inferiores al 5% recomendado9.
Otras limitaciones del estudioAunque tanto las OEA como los PEATC tienen cifras de sensibilidad y especificidad parecidas y cercanas al 95-100%, hay que recordar que las OEA exploran el estado de la cóclea y no la vía auditiva. Son pues técnicas útiles pero no iguales, actuando de forma complementaria21,22.
La población de estudio se ha basado en pacientes de un hospital público y no incluye a pacientes procedentes de hospitales privados. Esto es una limitación, puesto que la incidencia de sordera podría no ser la misma dada la influencia que factores socioeconómicos y ambientales puede tener en esta patología como describen varios estudios23.
ConclusionesEl análisis demuestra que el primer paso cumple el objetivo del cribado con un 98,4% de neonatos explorados siendo la gran mayoría normales (94%).
El segundo paso, al mes, tiene un porcentaje de normalidad del 89%, lo que filtra muy bien (solo se remiten a potenciales un 0,6% del grupo inicial), pero un 10,6% no acude a la cita en consultas externas, pudiéndose perder algún niño sordo. En los remitidos a potenciales, esta pérdida es aún mayor con un 29,5%, que es una cifra inaceptable. La rentabilidad en aquellos que sí se exploran es muy alta, puesto que el 69% de ellos presenta unos potenciales alterados y debe ser seguido por ORL.
Esta cifra de alterados en potenciales representa el 0,31% del total de recién nacidos estudiados, cifra similar a la incidencia esperada de sordera.
Para reducir las pérdidas en seguimiento, que son el principal problema del programa, es fundamental establecer un registro informático de los neonatos explorados, así cómo crear la figura del coordinador y tener al menos 2 aparatos.
Con los datos presentados, se puede concluir que el programa es útil pero necesita mejorar los puntos débiles comentados.
FinanciaciónTrabajo financiado parcialmente con Beca Impulsa 2012, Fundación Bancaixa.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A toda la plantilla del Servicio de Pediatría, la Maternidad y Neurofisiología del Hospital Francesc de Borja, Gandía.