La neutropenia supone un descenso del número de neutrófilos totales por debajo de 1500/μl en mayores de un año o de 2.000/μl entre los 2 y los 12 meses. Se considera severa si es inferior a 500/μl y crónica si permanece más de 3 meses. Existen formas de neutropenia crónica mantenida o intermitente. Dentro de las intermitentes, se encuentra la neutropenia cíclica1.
La neutropenia cíclica es un trastorno hematológico raro, congénito y hereditario, generalmente autosómico dominante, aunque también existen mutaciones de novo. Su incidencia aproximada es de un caso por millón de habitantes2. La alteración genética más comúnmente asociada se encuentra en el gen de la elastasa del neutrófilo (ELA 2). Esta alteración se ha descrito en un 60% de los casos esporádicos y de herencia dominante de neutropenia congénita severa3,4. Suele comenzar en torno al año de vida con fiebre, aftas orales, gingivitis, faringitis y/o adenopatías cervicales, con una periodicidad variable entre 14 y 35 días, aunque hasta en un 90% de los casos aparece cada 21 días5,6. En adultos se ha descrito disminución del número e intensidad de episodios e incluso desaparición.
Una de las complicaciones más severas es la aparición de complicaciones infecciosas. Son más frecuentes en la neutropenia central y su riesgo se incrementa a medida que disminuye el número de neutrófilos. El riesgo se considera elevado ante recuentos inferiores a 200/μl y aumenta con la duración de la neutropenia. Las infecciones bacterianas más frecuentes son las secundarias a Staphylococcus aureus y Staphylococcus epidermidis, Streptococcus, enterococo, neumococo, Pseudomonas aeruginosa y a bacilos gramnegativos. El riesgo de infecciones fúngicas aumenta tras varias semanas de neutropenia1. Aunque la neutropenia cíclica se asocia con menos frecuencia a sepsis bacterianas, es esencial controlar el riesgo de infección mediante profilaxis antibiótica con trimetoprim-sulfametoxasol. El empleo de factor estimulante de colonias de granulocitos (G-CSF) también disminuye el riesgo de infecciones. Suele iniciarse el tratamiento entre 1-5μg/kg subcutáneos con diferentes pautas: uso diario, cada 3 o 21 días1,5,7,8. El G- CSF ha demostrado disminuir la duración de los episodios y el riesgo de infección bacteriana, y mejora la calidad de vida.
Se presenta el caso de un niño de 11 años que ingresó para estudio de aftas orales recurrentes. En los últimos 3 meses había presentado 3 episodios de aftosis sin fiebre, con neutropenia en uno de ellos. Presentó episodios de faringoamigdalitis, fiebre y aftosis con periodicidad variable a los 4-5 años de edad, que mejoraban tras antibioterapia. La madre describe episodios febriles con faringoamigdalitis y aftosis en su infancia hasta los 12 años.
Se observaron aftas orales en mucosa labial y oral, sin otras alteraciones en la exploración física.
Se realizaron los siguientes estudios: hemograma y frotis de sangre periférica confirmándose la neutropenia sin afectación de otras series (cifra máxima de neutrófilos 1500/μl, mínima 40/μl); bioquímica con perfil hepatorrenal, férrico, inmunoglobulinas, serología celíaca y autoinmunidad normales. Serologías para virus del herpes simple, virus de Epstein-Barr, citomegalovirus y parvovirus B19, y cultivo de frotis faríngeo negativos.
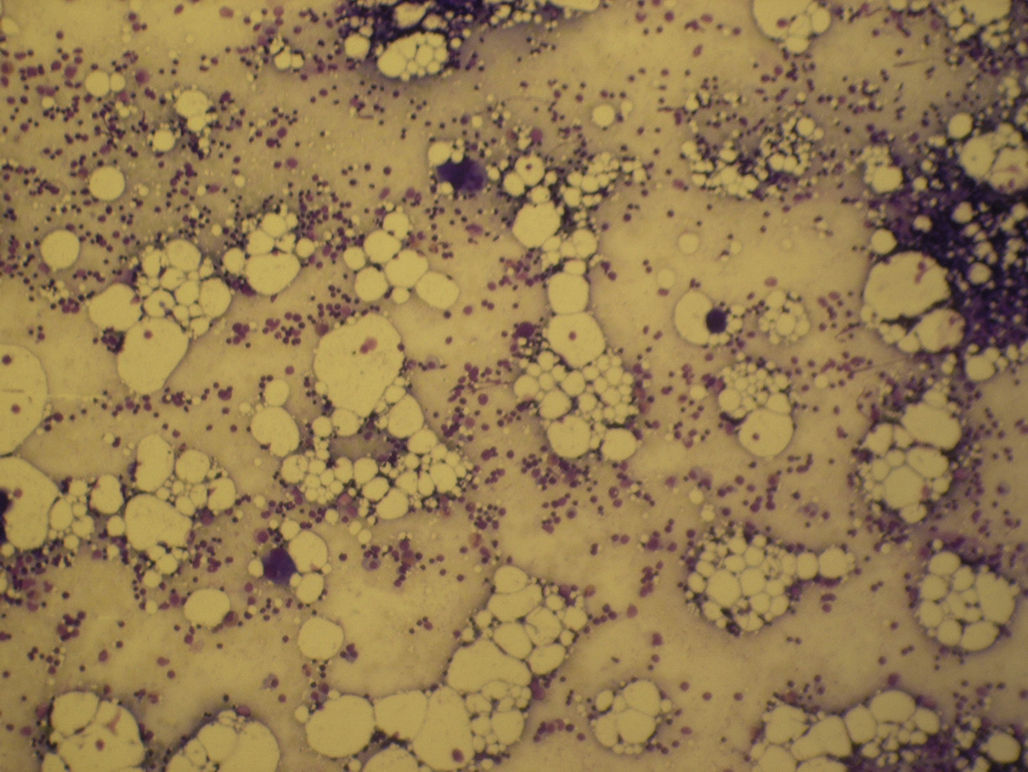
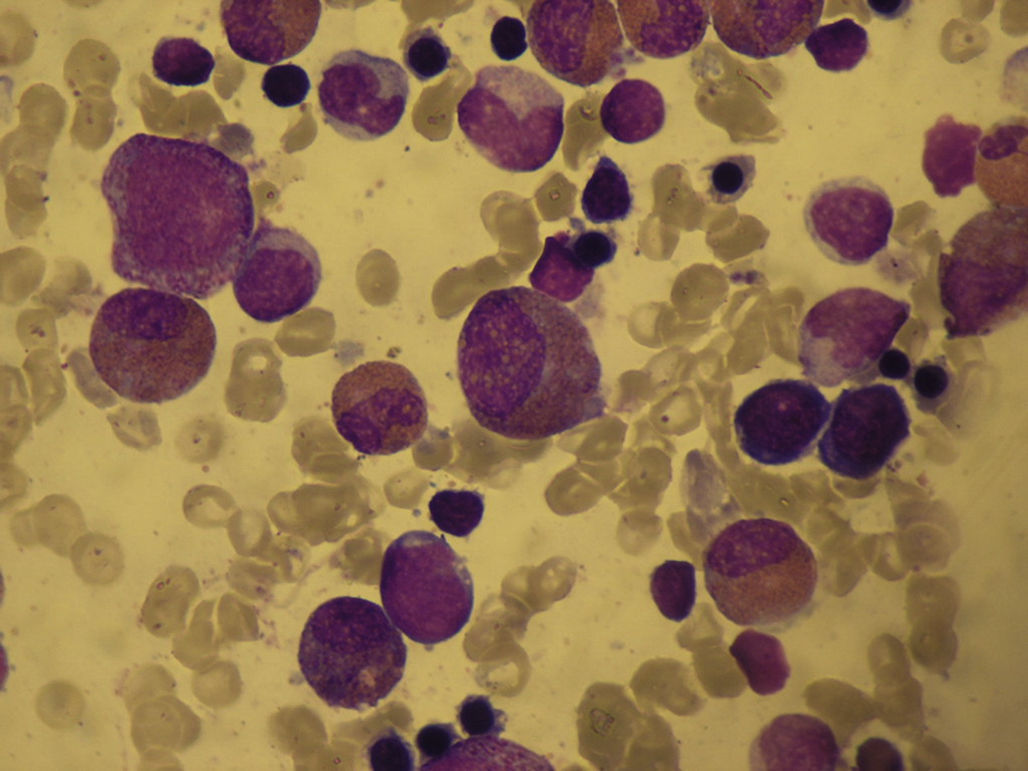
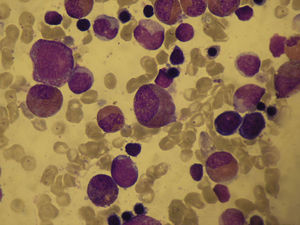
Ante la sospecha de neutropenia cíclica, se realizó punción de médula ósea, con disminución de la serie neutrofílica, predominio de formas inmaduras y escasa maduración posterior (figs. 1 y 2). No presentaba datos de síndrome mieloproliferativo. Se realizó estudio citogenético, sin alteraciones cromosómicas, y estudio genético, con resultado positivo para mutación en el gen de la proteína elastasa del neutrófilo. Ante este hallazgo, se derivó a la madre, debido a la clínica referida, al Servicio de Hematología. Se revisaron analíticas sanguíneas objetivando neutropenia (700-1.500). Se realizaron análisis de médula ósea, con datos de hipocelularidad neutrofílica y sin datos de síndrome mielodisplásico, y estudio genético con resultado positivo para el gen ELA 2.
Tras la confirmación diagnóstica, se inició tratamiento con G-CSF con pauta inicial a 4 μg/kg/día subcutáneo cada 3 días, con adecuada respuesta y sin objetivarse efectos adversos. Se asoció inicialmente profilaxis antibiótica con trimetoprim-sulfametoxazol. La evolución fue favorable, con episodios asintomáticos y menor descenso de neutrófilos.
La neutropenia cíclica es una forma de neutropenia congénita rara, de carácter hereditario. Es un diagnóstico que se debe tener en cuenta ante episodios de aftosis, faringitis, gingivitis, adenopatías cervicales y/o fiebre recurrente. Es importante una adecuada anamnesis, pues las manifestaciones clínicas descritas son frecuentes en la infancia y, en ocasiones, el no llevarla a cabo, puede conllevar un retraso en el diagnóstico y suponer un mayor riesgo de complicaciones. Por su carácter hereditario, se debe incidir en la historia familiar, pues permite, como en nuestro caso, filiar cuadros asintomáticos. El empleo de antibioterapia profiláctica y G-CSF ha mejorado el pronóstico de los pacientes con neutropenia cíclica.