El uso de medicamentos para aliviar los síntomas del «resfriado común» en los niños es muy frecuente. A la falta de evidencia científica que avale su utilidad se suma la potencial toxicidad, habiéndose descrito intoxicaciones graves e incluso letales. El objetivo de este estudio es describir las características clínico-epidemiológicas de los pacientes atendidos en un servicio de urgencias pediátricas por sospecha de intoxicación no intencionada por anticatarrales.
Material y métodosEstudio analítico-observacional de los pacientes con edad inferior a 18 años atendidos en un servicio de urgencias pediátricas por sospecha de intoxicación no intencionada por un medicamento anticatarral, entre julio-2012 y junio-2020. Se clasificó la gravedad según el Poisoning Severity Score (PSS): PSS-0=sin toxicidad; PSS-1=toxicidad leve; PSS-2=moderada; PSS-3=grave; PSS-4=letal. Si la intoxicación se produjo en el transcurso de un tratamiento con el medicamento, se determinó si la edad del paciente estaba incluida en las indicaciones terapéuticas según ficha técnica.
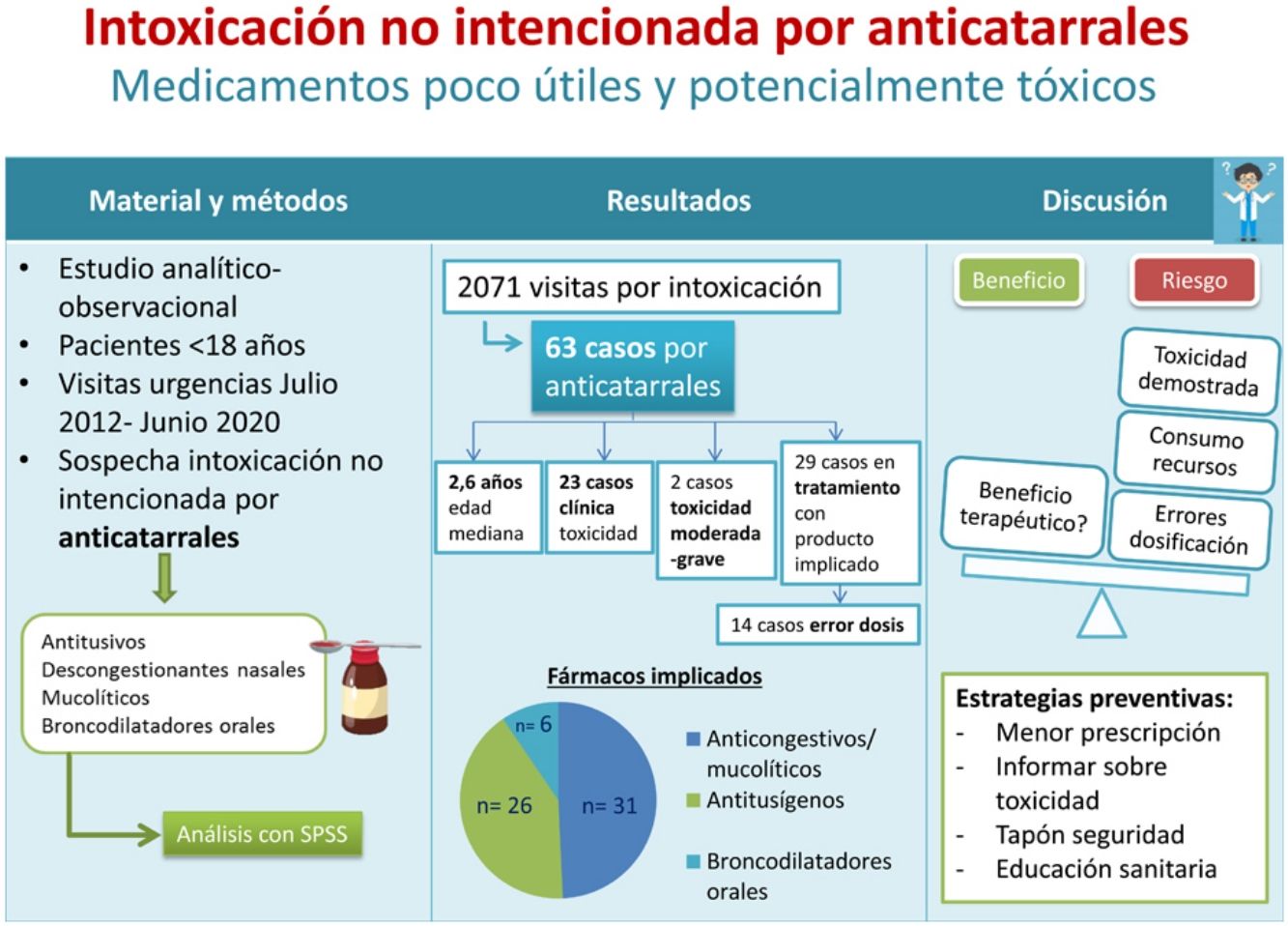
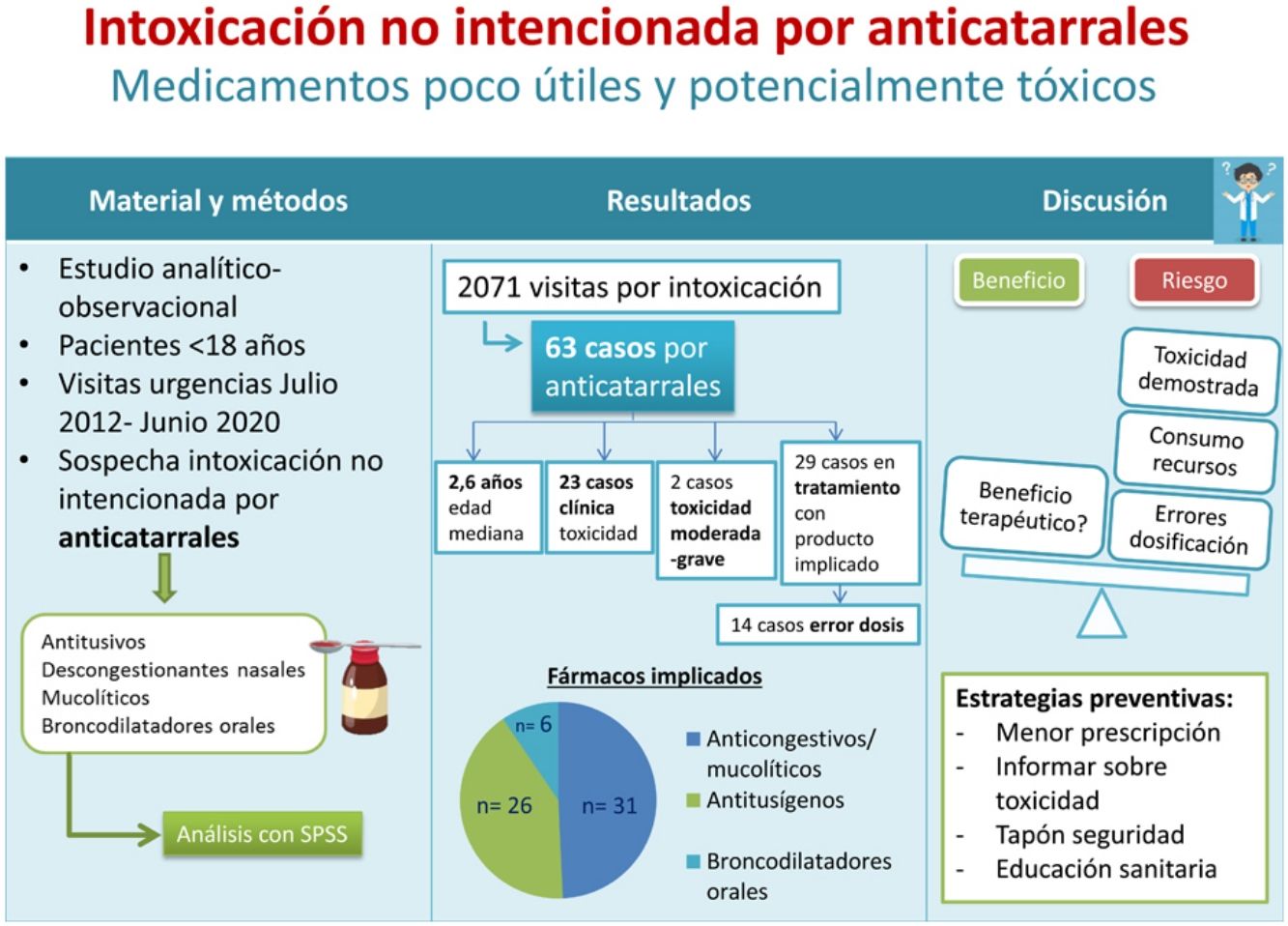
ResultadosSe recogieron 63 casos. Los medicamentos implicados fueron: anticongestivos y mucolíticos (31; 49,2%), antitusígenos (26; 41,2%), broncodilatadores orales (6; 9,5%). Se clasificaron según gravedad en: PSS-0=40 (63,5%), PSS-1=21 (33,3%), PSS-2=1 (1,6%) y PSS-3=1 (1,6%). En 29 pacientes (46%) existía antecedente de uso terapéutico; de estos, en 15 casos (51,7%) la edad del paciente era inferior a la recomendada en ficha técnica. En 14 pacientes (22,2%) la intoxicación se produjo por error en la dosis administrada por los cuidadores.
ConclusiónAunque la evidencia científica no recomienda medicamentos anticatarrales en niños, se siguen produciendo intoxicaciones no intencionadas por estos fármacos, en ocasiones moderadas o graves.
The use of medications to relieve the symptoms of the “common cold” in children is very frequent. In addition to the lack of scientific evidence supporting its usefulness, there is evidence of potential toxicity, and serious and even fatal cases of intoxication have been described. The objective was to describe the clinical and epidemiological characteristics of the patients treated in a paediatric emergency department for suspected unintentional intoxication by a cold medicine.
Material and methodsObservational and analytical study of patients aged less than 18 years managed in a paediatric emergency department for suspected unintentional poisoning by a cold medicine between July 2012 and June 2020. We classified severity according to the Poisoning Severity Score (PSS): PSS-0=no toxicity; PSS-1=mild toxicity; PSS-2=moderate; PSS-3=severe; PSS-4=lethal. If the intoxication occurred while the patient was in active treatment with the drug, we determined whether the patient's age was in the applicable range established in the therapeutic indications provided in the summary of product characteristics.
ResultsThe study included data for 63 cases. The drugs involved were decongestants and mucolytics (31; 49.2%), antitussives (26; 41.2%) and oral bronchodilators (6; 9.5%). The distribution by severity was 40 cases with PSS-0 (63.5%), 21 with PSS-1 (33.3%), 1 with PSS-2 (1.6%) and 1 with PSS-3 (1.6%). In 29 patients (46.0%) there was a history of therapeutic use; in 15 of these cases (51.7%) the age was lower than recommended in the summary of product characteristics. In 14 patients (22.2%) the intoxication was due to administration of the wrong dose by caregivers.
ConclusionAlthough scientific evidence does not support the use of cold medicines in children, unintentional intoxications by these drugs keep happening, in some cases causing moderate or severe symptoms.
El uso de medicamentos para aliviar los síntomas del «catarro» o «resfriado común» en los niños es muy frecuente e incluye fármacos antitusígenos, descongestivos nasales, expectorantes y antihistamínicos1,2. Además, existen en el mercado presentaciones que combinan más de un principio activo y, en nuestro país, son medicamentos que pueden obtenerse sin receta médica. Asimismo, frecuentemente se utilizan por debajo de la edad recomendada en ficha técnica1,2, lo cual puede aumentar el riesgo de intoxicación. A la falta de evidencia científica que avale la utilidad de estos fármacos3–7 se suma la potencial toxicidad, ya que se han descrito intoxicaciones graves e incluso letales8–21.
Se han publicado extensas series de casos de intoxicación por medicamentos para la tos y el catarro en niños, con aparición de clínica moderada, grave y mortal, así como numerosos reportes de casos aislados8–14. Además, los informes anuales de la American Association of Poison Control Centers’ National Poison Data System (NPDS) han registrado, entre los años 2000 y 2019, 9 casos de intoxicación mortal en niños menores de 8 años, en los que se consideró que la ingesta única de un fármaco antitusígeno o anticatarral fue indudable o probablemente responsable de la muerte15-21.
El objetivo de este estudio es describir las características clínico-epidemiológicas de los pacientes atendidos en un servicio de urgencias pediátricas (SUP) por sospecha de intoxicación no intencionada por tratamientos para el «resfriado común».
Material y métodosEstudio descriptivo observacional, realizado en el SUP de un hospital urbano materno-infantil de tercer nivel, que recibe de forma anual aproximadamente 110.000 visitas pediátricas. Se seleccionaron los pacientes menores de 18 años que consultaron en urgencias por sospecha de intoxicación no intencionada por un medicamento anticatarral entre julio de 2012 y junio de 2020. Se consideraron medicamentos anticatarrales los antitusivos, descongestionantes nasales, mucolíticos y broncodilatadores orales. No se incluyeron los casos de exposición a un antihistamínico como único principio activo.
Se identificaron como fármacos causantes de intoxicaciones graves en la infancia, por haberse reportado casos de toxicidad amenazante para la vida en menores de 8 años, los antitusígenos opiáceos, antihistamínicos, descongestivos simpaticomiméticos y las imidazolinas descongestivas22.
Para seleccionar los casos, se revisó la historia clínica de todos los pacientes cuyo motivo de consulta o diagnóstico final estaba relacionado con el contacto con tóxicos.
Se recogieron, mediante la revisión retrospectiva de las historias clínicas informatizadas de los pacientes, variables epidemiológicas, clínicas y de manejo. Se evaluó la toxicidad del episodio en base a la dosis ingerida y la presencia de clínica sugestiva de toxicidad. Se consideraron como dosis tóxicas las recogidas en TOXBASE (National Poison Information System)23. Se clasificó la gravedad de la intoxicación según el Poisoning Severity Score (PSS)24 en: PSS-0=ausencia de toxicidad; PSS-1=toxicidad leve; PSS-2=moderada; PSS-3=grave y PSS-4=letal. Para el estudio comparativo entre grupos farmacológicos, se agruparon los pacientes que ingirieron algún medicamento opiáceo, así como los que ingirieron algún antihistamínico.
Se consultó el informe clínico de urgencias y la historia clínica informatizada, buscando información que indicara que el paciente estaba realizando un tratamiento con el fármaco implicado en la consulta. Cuando la intoxicación se produjo en el transcurso de un tratamiento, se comprobó si la edad del paciente estaba incluida en las indicaciones terapéuticas según ficha técnica, disponible en el centro de información on-line de la Agencia Española de Medicamentos y Productos Sanitarios25.
El episodio de urgencias de la historia clínica informatizada del SUP dispone de una plantilla de anamnesis específica para el paciente con sospecha de intoxicación, favoreciendo la recogida de datos completa. Además, el sistema informático registra tanto las acciones realizadas como el momento de su realización.
Toda la información se almacenó y procesó en una base de datos relacional Microsoft Access (Microsoft Corporation, Redmond, EE. UU.). El análisis estadístico se realizó con el programa estadístico SPSS v25.0 para Windows. Los datos fueron expresados como mediana y rango intercuartílico para las variables cuantitativas, y como recuentos y porcentajes para las categóricas. Se aplicaron pruebas para el estudio de distribución de datos (Kolmogorov-Smirnov) y de comparación de datos cuantitativos (t de Student, U de Mann-Whitney) y cualitativos (Chi-cuadrado, tabla de contingencia, test exacto de Fisher). Se consideraron significativos los valores de p menores a 0,05.
El estudio fue aprobado por el Comité Ético de Investigación en Medicamentos del hospital donde se realizó el estudio, con referencia PIC-63-19.
ResultadosSe recogieron 63 casos de un total de 2171 consultas por sospecha de intoxicación (2,9%). De estos, 36 fueron varones (57,1%) con una edad mediana de 2,6 años (p25-75=1,8-3,6). En los 42 casos (66,6%) en los que se registró el lugar de la ingesta, este fue el domicilio habitual.
Los medicamentos implicados fueron: anticongestivos y mucolíticos (31; 49,2%), antitusígenos (26; 41,2%) y broncodilatadores orales (6; 9,5%). En 25 casos (39,6%), el preparado comercial implicado era un compuesto formado por varios principios activos. Treinta y cuatro pacientes (53,9%) ingirieron al menos un fármaco causante de intoxicaciones graves en la infancia, siendo un antitusivo opiáceo en 13 casos (20%) y un antihistamínico, combinado con otros principios activos, en 21 (33,3%).
En 30 casos (47,6%) la ingesta se consideró potencialmente tóxica por tratarse de una dosis tóxica o desconocida, o por la presencia de clínica de toxicidad.
Veintitrés pacientes (36,5%) presentaron algún tipo de clínica sugestiva de toxicidad. Se clasificaron según gravedad mediante el PSS con los siguientes resultados: PSS-0=40 (63,5%), PSS-1=21 (33,3%), PSS-2=1 (1,6%) y PSS-3=1 (1,6%).
Se realizó descontaminación digestiva en 29 pacientes (46%), en todos ellos mediante la administración de carbón activado y, en un caso, con realización previa de lavado gástrico. Se conocía el momento de la ingesta en 26 casos, con una mediana de tiempo transcurrido entre esta y la descontaminación de 82min (p25-75=62-116). Un paciente (1,6%) recibió antídoto (naloxona).
Dos pacientes (3,2%) requirieron ingreso hospitalario, ninguno en la unidad de cuidados intensivos pediátricos.
El caso de toxicidad grave se produjo en un varón de 2 años que presentó depresión neurológica y respiratoria tras la ingesta de una cantidad desconocida (máximo 15mg/kg) de dextrometorfano en jarabe. Precisó medidas de soporte y la administración de naloxona en bomba de infusión, con buena evolución posterior.
La tabla 1 muestra las características clínicas de los pacientes en función del producto anticatarral implicado.
Características clínicas y de manejo de los pacientes según el medicamento anticatarral implicado
| Cloperastina(N=13) | Clorfeniramina+fenilefrina+difenhidramina(N=18) | Codeína(N=2) | Dextrometorfano, solo o con pseudoefedrina(N=13) | Mepifilina(N=2) | Prometazinaa(N=3) | Sustancias de baja toxicidadb(N=6) | Terbutalinaa(N=6) | Total(N=63) | |
|---|---|---|---|---|---|---|---|---|---|
| Transporte sanitario | 0 | 2 (11,1) | 0 | 3 (23,1) | 0 | 1 (33,3) | 0 | 1(16,7) | 7 (11,1) |
| Tiempo ingesta-atención (horas)c | 1 (0,8-1,5) | 1,5 (1-2,2) | 2,7 (0,5 -5) | 3,8 (1-6) | 1 (-) | 2 (1,8-4,5) | 3,5 (1-4) | 10,7 (2– 18) | 1,5 (1-4) |
| Error de dosis | 2 (15,4) | 3 (16,7) | 0 | 4 (30,8) | 1 (50) | 2 (66,7) | 1 (16,7) | 1 (16,7) | 14 (22,2) |
| Ingesta de dosis superior a la tóxicad | 0 | 8 (44,4) | 0 | 10 (76,9) | 0 | 0 | 0 | 5 (83,3) | 23 (36,5) |
| Gravedad de la toxicidad | |||||||||
| PSS-0 | 13 (100) | 16 (88,9) | 2 (100) | 3 (23,1) | 0 | 2 (66,7) | 3 (50) | 1 (16,7) | 40 (63,5) |
| PSS-1 | 0 | 2 (11,1) | 0 | 8 (61,5) | 2(100) | 1 (33,3) | 3 (50) | 5 (83,3) | 21 (33,3) |
| PSS-2 | 0 | 0 | 0 | 1 (7,7) | 0 | 0 | 0 | 0 | 1 (1,6) |
| PSS-3 | 0 | 0 | 0 | 1 (7,7) | 0 | 0 | 0 | 0 | 1 (1,6) |
| Sintomatología | |||||||||
| Cardiovascular | 0 | 0 | 0 | 1 (7,7) | 0 | 0 | 0 | 1 (16,7) | 2 (3,2) |
| Digestiva | 0 | 1 (5,6) | 0 | 3 (23,1) | 1 (50) | 0 | 3 (50) | 2 (33,3) | 10 (15,9) |
| Neurológica | 0 | 1 (5,6) | 0 | 6 (46,1) | 1 (50) | 1 (33,3) | 0 | 2 (33,3) | 11 (17,5) |
| Otra | 0 | 0 | 0 | 2 (15,4) | 0 | 0 | 0 | 0 | 2 (3,2) |
| Descontaminación digestiva | 10 (76,9) | 11 (61,1) | 0 | 5 (38,5) | 1 (50) | 0 | 1 (16,7) | 1 (16,7) | 29 (46,0) |
| Administración de antídoto | 0 | 0 | 0 | 1 (7,7) | 0 | 0 | 0 | 0 | 1 (1,6) |
| Exploraciones complementarias | |||||||||
| Analítica sangre | 1 (7,6) | 2 (11,1) | 0 | 1 (7,7) | 1 (50) | 0 | 0 | 2 (33,3) | 7 (11,1) |
| ECG | 5 (38,5) | 15 (83,3) | 0 | 1 (7,7) | 0 | 0 | 0 | 6 (100) | 27 (42,9) |
| Estancia en el SUP en horas | 3,1 (2,4-3,3) | 3,2 (1,7-5) | 0,7 (0,6-0,8) | 1,9 (0,7-4,3) | 0,7 (-) | 0,9 (0,7-2,4) | 1,2 (0,9-2,2) | 2,6 (2,4-3,1) | 2,5 (0,9-3,7) |
| Ingreso hospitalario | 0 | 1(5,6) | 0 | 0 | 1 (50) | 0 | 0 | 0 | 2 (3,2) |
ECG: electrocardiograma; PSS: Poisoning Severity Score (PSS-0=sin toxicidad; PSS-1=toxicidad leve; PSS-2=toxicidad moderada; PSS-3=toxicidad grave); SUP: servicio de urgencias pediátricas.
Las variables cualitativas se expresan en número absoluto (porcentaje). Las variables cuantitativas se expresan en mediana (p25-75).
Al comparar los pacientes expuestos a medicamentos opiáceos (codeína y dextrometorfano; n=15) frente al resto, se objetivaron diferencias estadísticamente significativas en cuanto a la ingesta de dosis superiores a la tóxica (n=10; 66,7% vs. n=13; 27,1% con p=0,005) y a la presencia de sintomatología (n=10; 66,7% vs. n=12; 25% con p=0,003). Asimismo, se halló una tendencia a que el episodio fuera más grave (PSS 2-3=2; 13,3% vs. PSS 2-3=0 con p=0,054). Al comparar el grupo de pacientes que ingirieron algún antihistamínico (clorfeniramina+difenhidramina, mepifilina y prometazina; n=23) frente al resto, se detectaron diferencias estadísticamente significativas en cuanto a la realización de exploraciones complementarias (n=16; 69,6% vs. n=16; 40,0% con p=0,024) y, en concreto, de electrocardiograma (n=15; 65,2% vs. n=12; 30,0% con p=0,007). Por último, al comparar el grupo de pacientes que ingirieron terbutalina (n=6) frente al resto, se encontraron diferencias en cuanto a la mediana del tiempo transcurrido entre la ingesta y la consulta (10,75h vs. 1,5h; p=0,015), a que la dosis ingerida superara la dosis tóxica (n=5; 83,3% vs. n=18; 31,6% con p=0,021) y a la realización de electrocardiograma (n=6; 100% vs. n=21; 36,8% con p=0,004).
De la muestra global, en 29 casos (46,0%) se recogió el dato de que el paciente estaba realizando un tratamiento con el medicamento involucrado. En 15 de ellos (51,7%) la edad se encontraba por debajo de la recomendada en ficha técnica.
De los 29 pacientes en tratamiento, en 14 (48,3%) la sobreingesta se produjo por error en la dosis administrada por los cuidadores y en 15 (51,7%) por una ingesta no supervisada. En todos los casos en los que el paciente no se encontraba en tratamiento (n=34), el mecanismo fue la ingesta no supervisada.
Al comparar los pacientes en los que el mecanismo de la sobreingesta fue un error de medicación (n=14) frente a aquellos en los se produjo una ingesta no supervisada (n=49), se hallaron diferencias estadísticamente significativas en cuanto a la mediana de tiempo transcurrido desde la ingesta (4,5h vs. 1,5h; p=0,023) y en cuanto a la administración de algún tratamiento (n=4; 28,6% vs. n=29; 59,2% con p=0,043).
DiscusiónLos tratamientos para el «resfriado común» incluyen, con frecuencia, fármacos altamente tóxicos en la infancia22 y, en ocasiones, pueden producir intoxicaciones moderadas o graves.
Las características epidemiológicas de los pacientes incluidos en este estudio son similares a las descritas por el Grupo de Trabajo de Intoxicaciones de la Sociedad Española de Urgencias de pediatría (GTI-SEUP)26–28. Los datos más recientes, provenientes de los casos recogidos en el Observatorio Toxicológico de SEUP entre 2008 y 2017, muestran que la mayoría de ingestiones no intencionadas de medicamentos se producen en la edad preescolar (86,1% en menores de 6 años), en el domicilio (85,5%) y con un discreto predominio de los varones (53,5%)28. En cuanto a la aparición de clínica, fue más frecuente en los pacientes con ingesta de anticatarrales (36,5%, según los datos presentados) que en las ingestiones de medicamentos en general (25,7%)28.
Este estudio muestra que en más de la mitad de exposiciones a medicamentos anticatarrales estaban implicados fármacos altamente tóxicos en la infancia, en concreto opiáceos y antihistamínicos asociados a otros principios activos. Aunque la evolución fue buena en todos los casos, existen numerosas publicaciones que demuestran la gravedad que pueden conllevar estas intoxicaciones.
En una extensa revisión de casos llevada a cabo por Dart et al., se detectaron 99 casos mortales tras la ingesta de un producto anticatarral en menores de 6 años, siendo la pseudoefedrina, la difenhidramina y el dextrometorfano los principios activos más frecuentemente implicados8.
Los informes anuales de la American Association of Poison Control Centers’ NPDS publicados desde el año 2000 identificaron 5 casos mortales en menores de 6 años tras la ingesta de un medicamento anticatarral que contenía antihistamínicos (clorfeniramina en 3 de ellos). En todos los casos, el niño fue hallado en parada cardiorrespiratoria16–18,20.
En la serie presentada, el medicamento más frecuentemente implicado fue la combinación clorfeniramina-fenilefrina-difenhidramina, si bien solo apareció toxicidad en 2 casos y fue leve. La escasa gravedad de estos pacientes puede explicarse, parcialmente, por el hecho de que en menos de la mitad de los casos la dosis ingerida alcanzaba la dosis tóxica. Además, el tiempo transcurrido entre la ingesta y la consulta fue relativamente breve (mediana de 1,5h) y se practicó descontaminación digestiva en casi 2 tercios de los casos, lo que pudo intervenir en la limitada aparición de toxicidad.
El dextrometorfano, sin embargo, destacó por su toxicidad. Los pacientes que ingirieron opiáceos (siendo el dextrometorfano el fármaco implicado en casi todos ellos) alcanzaron con mayor frecuencia la dosis tóxica y presentaron más sintomatología que el resto. Además, el dextrometorfano fue responsable de los 2 casos moderado y grave. Estas diferencias pueden atribuirse, por un lado, a la toxicidad intrínseca de este fármaco y, por otro, a la existencia de preparados pediátricos, con características organolépticas agradables y cuya composición alcanza la dosis considerada altamente tóxica para un niño de 10kg de peso22.
De forma similar, y aunque el pequeño número de casos no permitió alcanzar la significación estadística, 5 de los 6 pacientes que ingirieron terbutalina superaron la dosis tóxica y presentaron sintomatología. Las características de las presentaciones comercializadas pueden, del mismo modo, estar relacionadas con estos resultados.
Por otro lado, la mayor realización de electrocardiograma en los pacientes que ingirieron terbutalina y antihistamínicos se relaciona con la conocida cardiotoxicidad de estos últimos y de los fármacos simpaticomiméticos29,30.
Un programa estadounidense que monitoriza la aparición de eventos adversos asociados a medicamentos anticatarrales en menores de 12 años (Pediatric Cough and Cold Safety Surveillance System) identificó, entre 2008 y 2014, 5342 casos9. Un estudio posterior extraído del mismo programa objetivó que, pese a los esfuerzos realizados en las últimas décadas para disminuir la incidencia de las intoxicaciones infantiles, la tasa de eventos adversos por millón de unidades de anticatarrales vendidos se mantuvo estable a lo largo del periodo 2009 a 2016 y que, incluso, se produjo un incremento en la necesidad de ingreso10.
Tanto la bibliografía expuesta como los resultados presentados demuestran que es necesario seguir trabajando en la prevención de las intoxicaciones en la infancia. Es preciso adecuar las presentaciones comercializadas, especialmente las dirigidas a la población pediátrica, tanto en cuanto a la cantidad de principio activo que contienen como, de manera imperativa, a la incorporación de tapón de seguridad.
Además, es significativo que, en casi la mitad de los casos de la muestra presentada, la sobreingesta se produjo mientras el niño estaba en tratamiento con un anticatarral, ya fuera por error de los cuidadores al administrarlo o por una acción del niño no supervisada. Este hecho obliga al pediatra a plantearse si merece la pena asumir el riesgo de prescribir un medicamento anticatarral, frente al posible beneficio terapéutico del mismo.
Los medicamentos anticatarrales, en general, no se recomiendan en las guías de práctica clínica pediátricas3,4. Diversas revisiones Cochrane han concluido que estos medicamentos deben evitarse en la infancia ya que no existe evidencia de su utilidad y son potencialmente peligrosos. Así lo indican De Sutter et al. en su revisión sobre antihistamínicos asociados a anticongestivos5, Gardiner et al. en la revisión sobre el uso de codeína y derivados6 y Smith et al. en un metaanálisis sobre el uso de medicamentos anticatarrales para el tratamiento de la tos aguda, tanto en niños como en adultos7. Aun así, son fármacos de muy fácil acceso debido a su dispensación sin receta médica e incluso son altamente prescritos por el colectivo médico2.
Es también destacable el hecho de que en más de la mitad de los casos en que el paciente estaba recibiendo un tratamiento con anticatarral, su edad se encontraba por debajo de la indicación en ficha técnica. Aunque debido a la falta de ensayos clínicos específicos en pediatría sea muy común el uso de medicamentos off-label31–33, su uso no siempre es el adecuado ni se registra de forma conveniente, como deja patente el reciente artículo de Piñeiro-Pérez et al.33. En el caso de los medicamentos anticatarrales es aún más difícil justificar su uso fuera de ficha técnica, dada la dudosa eficacia demostrada y el riesgo de intoxicación.
El error de dosis provocó casi una cuarta parte de los episodios, dando lugar a consultas más tardías (probablemente en relación con el momento en el que los cuidadores advierten el error) y con menor oportunidad para ser tratadas. En la muestra analizada no se detectaron intoxicaciones moderadas o graves por este mecanismo. Sin embargo, el Pediatric Cough and Cold Safety Surveillance System identificó, entre 2009 y 2016, 513 casos en los que se produjo algún evento adverso tras un error de administración de medicación anticatarral y, de ellos, el 25% precisó ingreso hospitalario y el 10% en una unidad de cuidados intensivos. Coincidiendo con los resultados presentados, el dextrometorfano y la difenhidramina fueron los fármacos más frecuentemente implicados en estos episodios34.
La principal limitación de este estudio viene dada por su diseño retrospectivo, con la pérdida de información que supone. La existencia de un formulario de anamnesis específica para el paciente intoxicado disminuye este riesgo, sin embargo, es posible que no se recogiera en la historia clínica el antecedente de estar utilizando el medicamento con fines terapéuticos, por lo que este puede ser un dato infravalorado. Tampoco pudo discernirse en qué casos el medicamento había sido prescrito por un facultativo o había sido adquirido sin receta médica.
Pese a estas limitaciones, este trabajo ha identificado algunos aspectos que favorecen la intoxicación por anticatarrales en pediatría. En primer lugar, la prescripción de fármacos potencialmente tóxicos y de escasa utilidad y, en segundo lugar, la frecuencia de errores en su administración, probablemente en relación con la ausencia de prescripción clara y por escrito. Otros factores probablemente implicados son la posibilidad de obtener dichos medicamentos sin receta médica, independientemente de la edad del niño y la insuficiente aplicación de las medidas de almacenaje responsable de medicamentos en el domicilio.
Como conclusión, este estudio pone en relieve que, pese a que la evidencia científica no recomienda el uso de medicamentos anticatarrales en niños, se siguen produciendo intoxicaciones no intencionadas por estos fármacos, en ocasiones moderadas o graves. Para reducir este riesgo, es fundamental desarrollar medidas que tengan como objetivo: 1- Disminuir la prescripción pediátrica de estos fármacos; 2- Si se dispensan sin receta médica, aportar información sobre el riesgo de intoxicación, así como el límite de edad según ficha técnica; 3- Promover la inclusión de tapón de seguridad en todas las presentaciones pediátricas y 4- Mejorar la educación sanitaria a las familias para disminuir el acceso no supervisado de los niños a los medicamentos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Presentación en congresos: Este trabajo en su forma preliminar se ha presentado previamente en la XXIV Reunión de la Sociedad Española de Urgencias de Pediatría, celebrada en Murcia en mayo de 2019 y en las XXIII Jornadas de Toxicología clínica celebradas en Valencia en noviembre de 2019.