Introducción
La hemorragia grave incontrolable es un acontecimiento poco frecuente en las unidades de cuidados intensivos pediátricos (UCIP), que puede poner en peligro la vida del paciente. Las causas que producen trastornos de coagulación con síntomas de sangrado en pacientes sin coagulopatía previa, son muy variables, pero el tratamiento médico está bastante estandarizado: transfusión de plasma fresco congelado, plaquetas, crioprecipitado, concentrado de hematíes y vitamina K. En algunas ocasiones la hemorragia no cede con este tratamiento y/o el paciente no tolera la administración de grandes volúmenes de líquidos. Existe bastante experiencia en la utilización del factor VII activado recombinante (FVIIaR), en pacientes hemofílicos con anticuerpos inhibidores del factor VIII o IX, en donde se ha demostrado su eficacia y buena tolerancia con escasez de efectos secundarios1,2. En los últimos años se han publicado experiencias aisladas de tratamiento con FVIIaR en hemorragias con coagulopatía, secundarias a enfermedades no hematológicas3-6, y han sido escasas las aportaciones pediátricas.
Observaciones clínicas
Caso 1
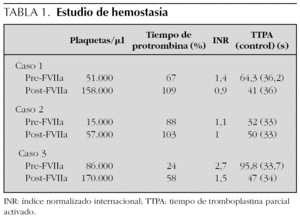
Varón de 18 meses de edad que ingresó en la UCIP por presentar shock séptico meningocócico grave, con coagulopatía, petequias y equimosis extensas que respetaban únicamente partes distales de extremidades e insuficiencia renal anúrica desde el inicio. La situación hemodinámica y la coagulopatía inicial se controlaron tras la administración de expansores, hemoderivados y fármacos vasomotores (dopamina y noradrenalina); se instauró ventilación mecánica y hemofiltración venovenosa continua. Al noveno día de evolución y con plaquetopenia (80.000 cél./μl) presentó hemorragia gástrica moderada y melenas. Se administraron plaquetas, omeprazol y perfusión de somatostatina. Al día 11 presentó un nuevo episodio de hemorragia gástrica grave con shock hipovolémico que no remonta con hemoderivados: plasma fresco congelado (25 ml/kg), plaquetas (1 U/4 kg) y concentrado de hematíes (15 ml/kg), vitamina K, otros expansores plasmáticos y fármacos presores. Ante la extrema gravedad del paciente (shock refractario e inicio de bradicardia) se decidió administrar FVIIaR (50 μg/kg), observándose el cese casi inmediato de la hemorragia, lo cual permitió la estabilización hemodinámica del paciente. El estudio de coagulación pretratamiento y postratamiento se representa en la tabla 1. La evolución posterior del paciente fue satisfactoria permitiendo el alta de UCIP a los 36 días del ingreso.
Caso 2
Varón de 4,5 años de edad con neurofibromatosis tipo I, diagnosticado de leucemia mielomonocítica crónica juvenil hacía 6 meses. Fue tratado con protocolo SHOP-LANL 2001 (arabinósido de citosina [ARA-C] y mitoxantrona). En espera de esplenectomía y posterior trasplante de médula ósea, presentó reagudización de la enfermedad de base y neumonía con insuficiencia respiratoria aguda que evolucionó a síndrome de dificultad respiratoria agudo (SDRA). Durante la estancia en UCIP presentó una gran hepatomegalia, deterioro hemodinámico con oliguria y trombopenia persistente a pesar del tratamiento sustitutivo con transfusiones repetidas de plaquetas. La situación hemodinámica se estabilizó y la alteración respiratoria evolucionó hacia fibrosis pulmonar. A la tercera semana se realizó nuevo ciclo de quimioterapia con idarubicina, ARA-C y etopósido (VP16). Tres semanas más tarde se realizó esplenectomía, presentando durante la intervención hemorragia incoercible que no se controló con la administración de plasma fresco, plaquetas y vitamina K, por lo que se administró una dosis de FVIIaR a 60 μg/kg lo cual permitió terminar la intervención. El estudio de hemostasia pretratamiento y postratamiento se representa en la tabla 1. La evolución es mala, presentando nueva recaída de la enfermedad de base, por lo que se decidió limitar el esfuerzo terapéutico; el paciente falleció a los 60 días de ingreso en la unidad (a los 7 días de realizar la esplenectomía).
Caso 3
Niña de 10 años de edad diagnosticada de atresia pulmonar con comunicación interventricular (CIV), e intervenida a los 3 años para realizar una fístula sistémica pulmonar y a los 4 años para cierre de CIV y colocación de homoinjerto desde ventrículo derecho a arteria pulmonar. Ingresó en UCIP tras realizar recambio del homoinjerto. La intervención quirúrgica fue prolongada, y precisó dos entradas en bomba con un tiempo total de circulación extracorpórea de 310 min, y complicada por presentar hemorragia muy abundante que precisó múltiples transfusiones de hemoderivados. A su llegada continuó sangrando por tubos de tórax a un ritmo de 10,7 ml/k/h en las primeras 4 h, a pesar de administrar plasma fresco congelado (20 ml/kg), plaquetas (6 U/kg), hematíes (30 ml/kg), fibrinógeno (3 g) y vitamina K, por lo que se administró FVIIaR a 35 μg/kg, dosis que se repitió a las 2 h con lo que disminuyó la hemorragia a 1,7 ml/kg/h en las siguientes 4 h. El estudio de coagulación pre y postratamiento se representa en la tabla 1. Se retiraron los tubos de tórax al séptimo día de postoperatorio y fue trasladada a planta a los 64 días del ingreso.
En los 3 casos se utilizó el FVIIaR, en situación clínica de extrema gravedad, con compromiso vital para el paciente, por lo que sólo fue posible solicitar el consentimiento informado en el caso 2. En la evolución posterior no se observaron complicaciones trombóticas ni de otro tipo atribuibles al fármaco.
Discusión
El FVIIa natural circula en pequeñas cantidades y no es biológicamente activo en el proceso de la coagulación hasta que se une al factor tisular (FT) que se libera en la zona de la lesión. El complejo FT/FVIIa inicia la cascada de la coagulación activando los factores IX y X cuyo resultado final es la activación de protrombina, con formación de trombina y del coágulo de fibrina insoluble6-8. El FT se ha localizado en numerosas superficies celulares incluyendo el sistema nervioso6. La administración de una dosis alta de FVIIaR produce un enorme incremento en la concentración de FVIIa comparado con la situación fisiológica, llevando a una mayor y más rápida producción de trombina9. Estudios in vitro han demostrado que los coágulos así formados tienen mayor resistencia a la degradación por enzimas fibrinolíticas10.
La experiencia adquirida con la utilización del FVIIaR en pacientes hemofílicos con inhibidores11 ha demostrado que es un fármaco eficaz y seguro, que no produce un estado de hipercoagulabilidad sistémica, a pesar de la mejoría en los tiempos de protrombina (TP) y de tromboplastina parcial activado (TTPA), limitando sus efectos al sitio donde se ha producido la lesión del vaso1,12. En menos del 1 % de pacientes se han encontrado complicaciones graves11,13: coagulación intravascular diseminada (CID), angina, taquicardia, ataxia, shock anafiláctico, insuficiencia renal aguda y anomalías de la función hepática; sólo se han referido complicaciones trombóticas en el 0,2 %13. Entre las complicaciones leves, también infrecuentes, destacan: reacciones cutáneas, fiebre, hipertensión arterial, cefalea, epistaxis y disminución del fibrinógeno11. El acortamiento del TP después de la administración del fármaco es causado por la presencia de FT en el sistema para realizar el test, y por lo tanto no refleja un estado de hipercoagulabilidad4.
Los pacientes hemofílicos con inhibidores constituyen el grupo más numeroso en los que se utiliza el FVIIaR1,2. Basados en estas experiencias se ha empleado en trastornos hemorrágicos14 secundarios a otras enfermedades hematológicas como la tromboastenia de Glanzmann15 o CID acompañante a leucosis3, y en otras coagulopatías de procesos no hematológicos como cirrosis e insuficiencia hepática16, postoperatorio de cirugía cardiovascular4,17, lesión cerebral aguda6 y politraumatizados5. La hemorragia relacionada con cirugía de cardiopatías congénitas es una complicación grave; en el año 2004 se ha publicado4 una serie (la mayor hasta la fecha) de 6 casos pediátricos con hemorragia que no respondía al tratamiento convencional y con buena respuesta al FVIIaR; un paciente tenía una fístula sistémico-pulmonar, otros dos conductos de Goretex® desde el ventrículo derecho hasta la arteria pulmonar y en tres se había realizado una cirugía de recambio arterial (Swich) con reimplantación de coronarias por d-transposición de grandes arterias (dTGA), sin que se produjeran efectos trombóticos en ninguno de ellos. En prematuros se ha estudiado18 el efecto de distintas dosis de FVIIaR sobre el TP y se ha utilizado de manera compasiva y con éxito en el tratamiento de dos recién nacidos con hemorragia aguda (hepaticoesplénica y pulmonar)19.
La dosis empleada ha sido muy variable y siempre tomando como referencia la utilizada en pacientes hemofílicos6,11, que es de 90 a 120 μg/kg. El rango varía entre 25-30 μg/kg como profilaxis de hemorragia3, 90 μg/kg en situaciones de coagulopatía secundaria a lesión cerebral6, hasta 180 μg/kg en el postoperatorio de cirugía cardíaca4. La dosis puede repetirse a las 2 h si la condición del paciente lo requiere.
El coste del fármaco constituye un aspecto limitante de su utilización. El precio varía de 591-630 1/mg dependiendo de la presentación, y el tratamiento de un niño de 10 kg de peso supondría un coste entre 567 y 1.134 1 según precisase una o dos dosis, contando con el aprovechamiento óptimo del vial. Beneficios añadidos serían la reducción de costes por menor utilización de productos sanguíneos y de pruebas analíticas y los derivados del mejor control clínico de los pacientes.
En resumen, con los datos actuales disponibles, el FVIIa no puede considerarse un tratamiento de uso sistemático para la hemorragia grave en pediatría, pero sí justifican un estudio más amplio, prospectivo para valorar su eficacia, eficiencia, dosis y seguridad, así como las indicaciones del mismo.