Las infecciones del tracto respiratorio inferior (ITRI) son la principal causa de hospitalización en niños, incluyendo bronquiolitis, neumonía adquirida en la comunidad, bronquitis y otras infecciones no especificadas. La mayoría son de origen vírico y no requieren tratamiento antibiótico1. Sin embargo, es frecuente el uso innecesario de antibióticos en estos pacientes2. Esta prescripción inadecuada podría deberse a circunstancias de la enfermedad, de los pacientes o de la asistencia sanitaria (gravedad, enfermedades coexistentes, disponibilidad de recursos), pero también puede deberse a hábitos clínicos asociados al uso excesivo de pruebas diagnósticas y de tratamientos3. El objetivo de este estudio fue medir la frecuencia de uso de antibióticos en niños hospitalizados por ITRI virales y explorar los factores relacionados con esta terapia antibiótica.
Se estudió una cohorte de niños (21días-14años), hospitalizados (enero de 2019-enero de 2023) desde urgencias en un hospital terciario, primariamente por ITRI, que no requirieron cuidados intensivos (podían haber recibido ventilación no invasiva) y con resultado positivo en una prueba de reacción en cadena de polimerasa (PCR) para virus respiratorios (influenza, virus respiratorio sincitial [VRS], adenovirus, bocavirus, coronavirus [NL63, 229E, OC43], enterovirus, parainfluenza, metapneumovirus, rinovirus y [desde 2020] SARS-CoV-2). Se excluyeron pacientes que solo dieron positivo en SARS-CoV-2, con enfermedades crónicas complejas, con diagnóstico concurrente de infección probablemente bacteriana, o con alguna prueba bacteriológica positiva en muestra biológica. En este hospital solo se dispone precozmente (24horas) de resultados de PCR para influenza, VRS y SARS-CoV-2. De las historias clínicas se recogieron datos de evolución clínica, pruebas diagnósticas y tratamiento.
Mediante chi cuadrado o pruebas Mann-Whitney se estudió la asociación de la antibioterapia con variables relacionadas con la gravedad clínica y el uso de métodos diagnósticos. Las variables significativas (p<0,05) en ese análisis se incluyeron en un modelo de regresión logística multivariante. Se realizó un análisis de sensibilidad, repitiendo el modelo multivariante en submuestras específicas.
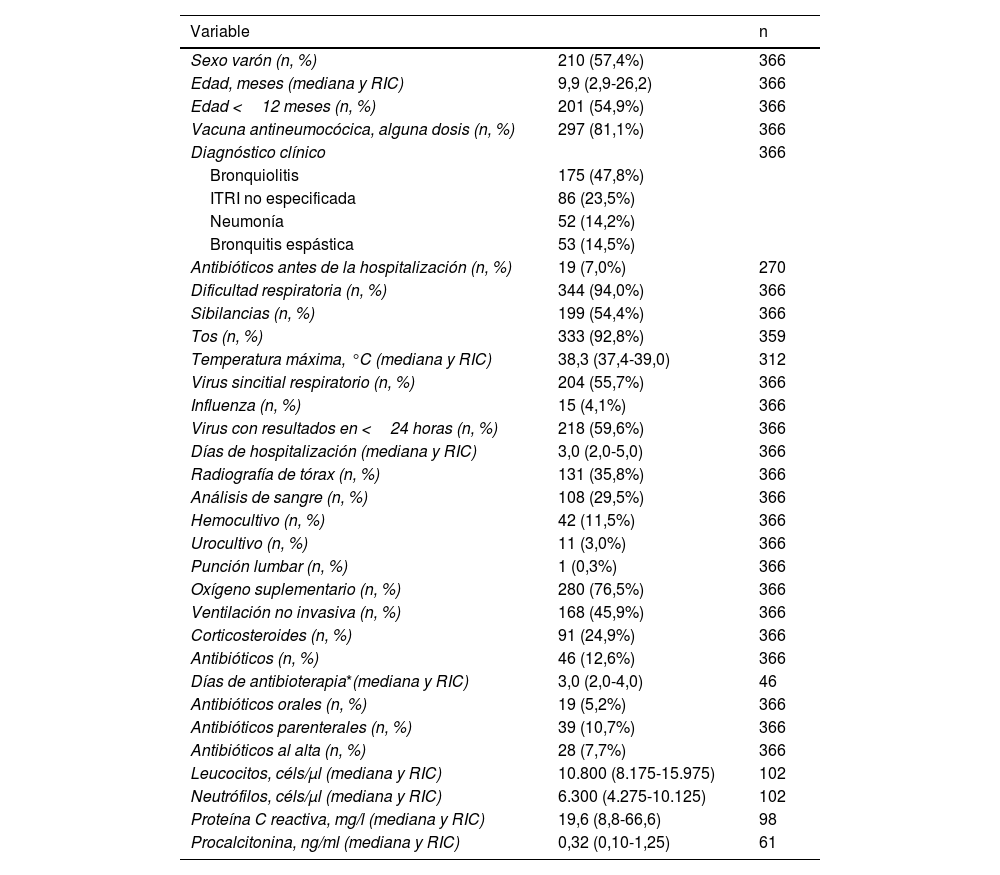
De 490 niños hospitalizados por ITRI, se excluyeron 109 por no identificarse ningún virus o solo SARS-CoV-2, 6 por necesitar cuidados intensivos, 2 por infecciones bacterianas asociadas y 7 por enfermedad crónica compleja, dejando una muestra final de 366 pacientes. Sus características se muestran en la tabla 1. Todos los pacientes tuvieron PCR positiva, sobre todo para VRS (41,7%) y rinovirus (21,0%).
Características de la muestra
| Variable | n | |
|---|---|---|
| Sexo varón (n, %) | 210 (57,4%) | 366 |
| Edad, meses (mediana y RIC) | 9,9 (2,9-26,2) | 366 |
| Edad <12 meses (n, %) | 201 (54,9%) | 366 |
| Vacuna antineumocócica, alguna dosis (n, %) | 297 (81,1%) | 366 |
| Diagnóstico clínico | 366 | |
| Bronquiolitis | 175 (47,8%) | |
| ITRI no especificada | 86 (23,5%) | |
| Neumonía | 52 (14,2%) | |
| Bronquitis espástica | 53 (14,5%) | |
| Antibióticos antes de la hospitalización (n, %) | 19 (7,0%) | 270 |
| Dificultad respiratoria (n, %) | 344 (94,0%) | 366 |
| Sibilancias (n, %) | 199 (54,4%) | 366 |
| Tos (n, %) | 333 (92,8%) | 359 |
| Temperatura máxima, °C (mediana y RIC) | 38,3 (37,4-39,0) | 312 |
| Virus sincitial respiratorio (n, %) | 204 (55,7%) | 366 |
| Influenza (n, %) | 15 (4,1%) | 366 |
| Virus con resultados en <24 horas (n, %) | 218 (59,6%) | 366 |
| Días de hospitalización (mediana y RIC) | 3,0 (2,0-5,0) | 366 |
| Radiografía de tórax (n, %) | 131 (35,8%) | 366 |
| Análisis de sangre (n, %) | 108 (29,5%) | 366 |
| Hemocultivo (n, %) | 42 (11,5%) | 366 |
| Urocultivo (n, %) | 11 (3,0%) | 366 |
| Punción lumbar (n, %) | 1 (0,3%) | 366 |
| Oxígeno suplementario (n, %) | 280 (76,5%) | 366 |
| Ventilación no invasiva (n, %) | 168 (45,9%) | 366 |
| Corticosteroides (n, %) | 91 (24,9%) | 366 |
| Antibióticos (n, %) | 46 (12,6%) | 366 |
| Días de antibioterapia*(mediana y RIC) | 3,0 (2,0-4,0) | 46 |
| Antibióticos orales (n, %) | 19 (5,2%) | 366 |
| Antibióticos parenterales (n, %) | 39 (10,7%) | 366 |
| Antibióticos al alta (n, %) | 28 (7,7%) | 366 |
| Leucocitos, céls/μl (mediana y RIC) | 10.800 (8.175-15.975) | 102 |
| Neutrófilos, céls/μl (mediana y RIC) | 6.300 (4.275-10.125) | 102 |
| Proteína C reactiva, mg/l (mediana y RIC) | 19,6 (8,8-66,6) | 98 |
| Procalcitonina, ng/ml (mediana y RIC) | 0,32 (0,10-1,25) | 61 |
ITRI: infección del tracto respiratorio inferior; RIC: rango intercuartil.
Recibieron antibióticos 46 pacientes (12,6%). La mayoría (69,6%) de los antibióticos fueron aminopenicilinas, pero el 23,9% recibieron una cefalosporina de tercera generación. Se administraron antibióticos al 4,0% de las bronquiolitis, al 5,7% de las bronquitis sibilantes, al 12,8% de ITRI no especificadas y al 48,1% de las neumonías. En 28 de esos 46 pacientes (60,9%) se continuó el tratamiento antibiótico tras el alta, siendo esto menos frecuente en las infecciones confirmadas precozmente (VRS e influenza): 45,8% vs 77,3%, p=0,038.
En análisis bivariante, las variables estadísticamente relacionadas con la antibioterapia fueron (material suplementario, tablas 1S y 2S): mayor edad, mayor temperatura, haber recibido alguna vacuna antineumocócica, no tener dificultad respiratoria, recibir antibióticos antes de la hospitalización, diagnóstico de neumonía y haberse realizado análisis de sangre, radiografía de tórax, urocultivo o hemocultivo. Entre los pacientes a quienes se realizó análisis de sangre, las cifras de neutrófilos, proteínaC reactiva y procalcitonina fueron mayores en los que recibieron antibióticos. Cuando se había hecho radiografía de tórax, la consolidación se asoció con mayor frecuencia de antibioterapia (75,0%) que en radiografías normales (11,1%) o con otros infiltrados (16,0%), p<0,001.
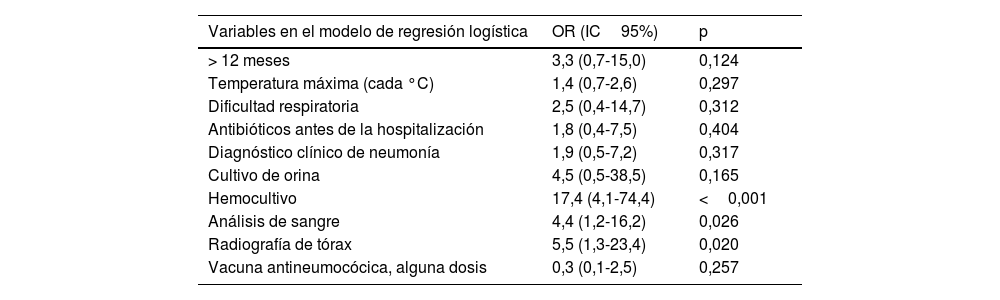
El análisis multivariante (tabla 2) identificó como únicas variables relacionadas con la antibioterapia la realización de radiografía de tórax, análisis de sangre y hemocultivo. El análisis de sensibilidad (material suplementario, tabla 3S) confirmó estos resultados. En otro modelo de regresión, los resultados de los estudios complementarios no mostraron asociación significativa con la antibioterapia (material suplementario, tabla 4S).
Análisis multivariante
| Variables en el modelo de regresión logística | OR (IC95%) | p |
|---|---|---|
| > 12 meses | 3,3 (0,7-15,0) | 0,124 |
| Temperatura máxima (cada °C) | 1,4 (0,7-2,6) | 0,297 |
| Dificultad respiratoria | 2,5 (0,4-14,7) | 0,312 |
| Antibióticos antes de la hospitalización | 1,8 (0,4-7,5) | 0,404 |
| Diagnóstico clínico de neumonía | 1,9 (0,5-7,2) | 0,317 |
| Cultivo de orina | 4,5 (0,5-38,5) | 0,165 |
| Hemocultivo | 17,4 (4,1-74,4) | <0,001 |
| Análisis de sangre | 4,4 (1,2-16,2) | 0,026 |
| Radiografía de tórax | 5,5 (1,3-23,4) | 0,020 |
| Vacuna antineumocócica, alguna dosis | 0,3 (0,1-2,5) | 0,257 |
IC 95%: intervalo de confianza al 95%; OR: odds ratio.
En conclusión, uno de cada ocho niños previamente sanos hospitalizados por una ITRI vírica y que no requirió cuidados intensivos recibió antibióticos. Aunque es una cifra inferior a la informada en otros estudios recientes4-6 (25-75%), hay que considerar que la muestra aquí estudiada está muy seleccionada, al excluir pacientes con alguna posible infección bacteriana asociada (p.ej., otitis media) y pacientes con condiciones de riesgo.
Los factores asociados a la antibioterapia no eran indicadores de gravedad (p.ej., necesidad de oxígeno o ventilación no invasiva, temperatura, síntomas respiratorios) ni circunstancias asistenciales (p.ej., antibióticos previos a la hospitalización, disponibilidad tardía de resultados de PCR víricos). A diferencia de otros estudios5, no se encontraron resultados analíticos o radiológicos relacionados independientemente con la antibioterapia. Los factores asociados al uso de antibióticos fueron decisiones como realizar radiografía de tórax, análisis de sangre o hemocultivo. Los resultados parecen indicar que la antibioterapia innecesaria es, sobre todo, parte de una práctica clínica que combina un exceso de pruebas diagnósticas y de tratamientos.