El malizumab es un anticuerpo monoclonal aprobado para mejorar el control del asma. Se administra como tratamiento adicional en pacientes con asma alérgica grave que presentan múltiples exacerbaciones asmáticas graves, a pesar de utilizar corticosteroides diarios inhalados a dosis altas, más un agonista beta-2 inhalado de larga duración. La dosis se calcula en función de la edad, el peso y los datos analíticos de IgE basal del paciente1.
Se presenta una niña boliviana de 10 años de edad que acude al servicio de urgencias por hematomas de repetición en el curso de 2-3 meses y, en las últimas 24 h, con 2 nuevas lesiones petequiales a nivel de ambos brazos sin antecedente traumático, afebril, sin otra clínica. Como antecedentes personales: dermatitis atópica y asma grave persistente mal controlada desde los 5 años, en tratamiento con budesonida/formoterol 160/4,5mcg (una inhalación cada 12 h), montelukast 5mg cada 24 h e inyección mensual de omalizumab de 150mg, tratamiento con el que lleva 10 meses a dosis iniciales de 300mg cada 15 días y, tras la mejoría, sin reagudizaciones y con alivio de los síntomas diarios, en descenso de las dosis de corticoides inhalados y omalizumab.
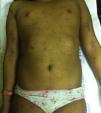
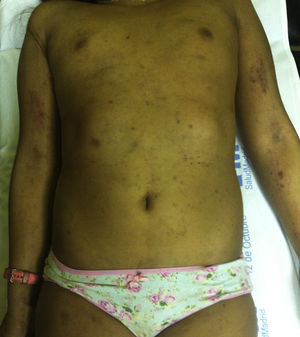
En la exploración: talla de 137cm (p75); peso de 44,4kg (p85). Dermatológicamente, se observa en extremidades superiores e inferiores lesiones petequiales agrupadas sobre fondo ictérico, de bordes mal definidos, confluentes, que coexisten con lesiones de rascado y hematoma. También en el tórax anterior (fig. 1).
Laboratorio: hemoglobina 12,8g/dl; plaquetas 7×103μl; VPM: 12 fl; leucocitos 5,2×103μl (neutrófilos 54,4%; linfocitos 28,3%; monocitos 7,2%; eosinófilos 9,5%; basófilos 0,6%). Coagulación: actividad de protrombina 76%; INR 1,23; TTPa 86,4 s.
Ante los hallazgos encontrados, se decide el ingreso para estudio y tratamiento. Se extraen serologías y se inician inmunoglobulinas a dosis de 0,8 UI/kg. La cifra de plaquetas asciende en 24 h a 45×103μl. Es dada de alta a los 3 días sin incidencias, con cifras de 57×103μl de plaquetas. Del estudio solo se obtiene una serología positiva (IgM e IgG) para parvovirus B19 con PCR negativa. Paralelamente, se suspende tratamiento con omalizumab.
Tras esto, inicia seguimiento en consulta por hematología con médula ósea normal y revisión quincenal. Actualmente en tratamiento con inmunoglobulinas según control analítico. En el momento de escribir esta carta, transcurridos 6 meses del primer ingreso, tiene recaída con 5×103μl plaquetas pendiente de diagnóstico hematológico definitivo.
Se define trombocitopenia inmune primaria al recuento plaquetario menor de 150×103μl cuando no existe causa tóxica o sistémica que lo justifique.
Las infecciones por B19 son mayoritariamente asintomáticas. Cuando lo son, se manifiesta bajo el cuadro conocido como quinta enfermedad o megaloeritema. Los parámetros hematológicos (hemoglobina, leucocitos, reticulocitos y trombocitos) disminuyen, aunque generalmente sin trascendencia clínica debido a que mayoritariamente afecta a precursores eritropoyéticos2. Excepcionalmente, en enfermos hematológicos conocidos, puede aparecer reticulocitopenia periférica, disminución de hemoglobina, neutropenia, trombocitopenia e, incluso, pancitopenia. El diagnóstico es principalmente serológico aunque se consigue mayor especificidad con las técnicas de ADN recombinante. Se han comunicado reacciones cruzadas con la rubéola, citomegalovirus, herpes simple, Epstein-Barr, sarampión y toxoplasma y también se han descrito falsos positivos en embarazadas sanas y en sueros con factor reumatoideo3.
En estudios preclínicos de omalizumab4 realizados en monos cinomolgos se observaron recuentos plaquetarios disminuidos, lo que motivó un aumento de las vigilancias. Posteriormente, en fase de poscomercialización, el análisis de casos y controles de pacientes con trombocitopenia y en tratamiento con omalizumab tuvieron un 3,4% de descenso en el recuento plaquetario respecto de los controles. La Agencia Europea del Medicamento ha puesto en abierto los resultados del EUDRAVIGILANCE, base de datos que recoge información nacional de los países de la Unión Europea y las notificaciones de los laboratorios farmacéuticos. Para omalizumab, hay 6.727 notificaciones. En 185 (2%), hay reacciones pertenecientes al sistema hematológico; relacionadas con plaquetas: púrpura trombocitopénica idiopática, 4; trombocitopenia, 13 y púrpura trombocitopénica, 3 casos. En la parte de alteraciones de laboratorio hay 9 casos de disminución del recuento.
La rica farmacopea de la que poco a poco nos hemos armado los clínicos es una herramienta esencial en la práctica diaria, sin embargo, no está exenta de riesgos. En algunas series está descrito que hasta un 8% de los diagnósticos de púrpura trombocitopénica ïnmune (PTI) correspondieron realmente a una causa farmacológica subyacente que no se consideró inicialmente5. El caso que presentamos puede, por tanto, corresponder a una de estas situaciones y debemos tener en cuenta la sospecha etiológica en previsión de la continuación del tratamiento posterior con omalizumab.