La monoterapia con lopinavir/ritonavir como estrategia de simplificación tiene el potencial de minimizar la toxicidad del tratamiento antirretroviral sin perder eficacia en casos seleccionados según estudios realizados en adultos; sin embargo, existen pocos datos en niños. Describimos una serie de 5 casos pediátricos tratados con este régimen durante una mediana de 112 semanas. Un niño con problemas de adhesión requirió intensificación de tratamiento por fallo virológico, presentando nuevamente carga viral indetectable. Ensayos clínicos aleatorizados controlados son necesarios para evaluar la eficacia de esta estrategia en niños y establecer las recomendaciones apropiadas.
Lopinavir/ritonavir monotherapy as a simplification strategy has the potential to minimize antiretroviral treatment toxicity without losing efficacy in selected cases, according to studies in adults, but little is known in paediatric patients. We report 5 children on this regimen for a median time of 112 weeks. One child with suboptimal adherence required intensification therapy to re-suppress viral load. Randomised controlled trials are needed to evaluate the efficacy of this strategy in children in order to make appropriate recommendations.
El tratamiento antirretroviral de gran actividad (TARGA) ha reducido de forma significativa la morbilidad y mortalidad de los niños infectados por el virus de la inmunodeficiencia humana (VIH) y es actualmente el estándar de tratamiento. Sin embargo, el tratamiento de por vida implica problemas de toxicidad, adherencia y resistencia a fármacos1.
Se han evaluado estrategias de simplificación de tratamiento para minimizar los efectos adversos y mejorar la adhesión, manteniendo al mismo tiempo la supresión virológica de forma efectiva a largo plazo. Lopinavir/ritonavir (LPV/r) ha sido estudiado en régimen de monoterapia en adultos en función de su alta potencia virológica, elevada barrera genética para el desarrollo de resistencias y capacidad de entrar en el sistema nervioso central1. Ensayos clínicos con LPV/r o darunavir/ritonavir en monoterapia tras un periodo de supresión virológica con el TARGA durante al menos 6 meses indican que su eficacia es similar a el TARGA a las 48 semanas (también a las 96 semanas en el caso de LPV/r), en pacientes sin mutaciones conocidas de resistencia a inhibidores de la proteasa1–3.
Existen pocos casos descritos de pacientes pediátricos en monoterapia con LPV/r como estrategia de simplificación4. Presentamos 5 casos con el fin de añadir más información sobre esta modalidad terapéutica en niños.
Material y métodosSe recogieron de forma retrospectiva datos demográficos y clínicos de niños infectados por VIH, seguidos desde el nacimiento en el Hospital del Mar de Barcelona, que iniciaron monoterapia con LPV/r (Kaletra®, Abbott Laboratories, Abbott Park, IL, USA) tras un periodo de supresión virológica con el TARGA. La carga viral de VIH-1 se midió con Amplicor HIV monitor Roche (rango 50–500.000 copias/ml). Se utilizó el software estadístico Medcalc (versión 11.1). La prueba de suma de rangos de Wilcoxon para variables continuas se utilizó para determinar cambios de células CD4 en el tiempo y significación estadística.
ResultadosDescribimos 5 niños infectados por el VIH por transmisión vertical que fueron simplificados a monoterapia con LPV/r (tabla 1).
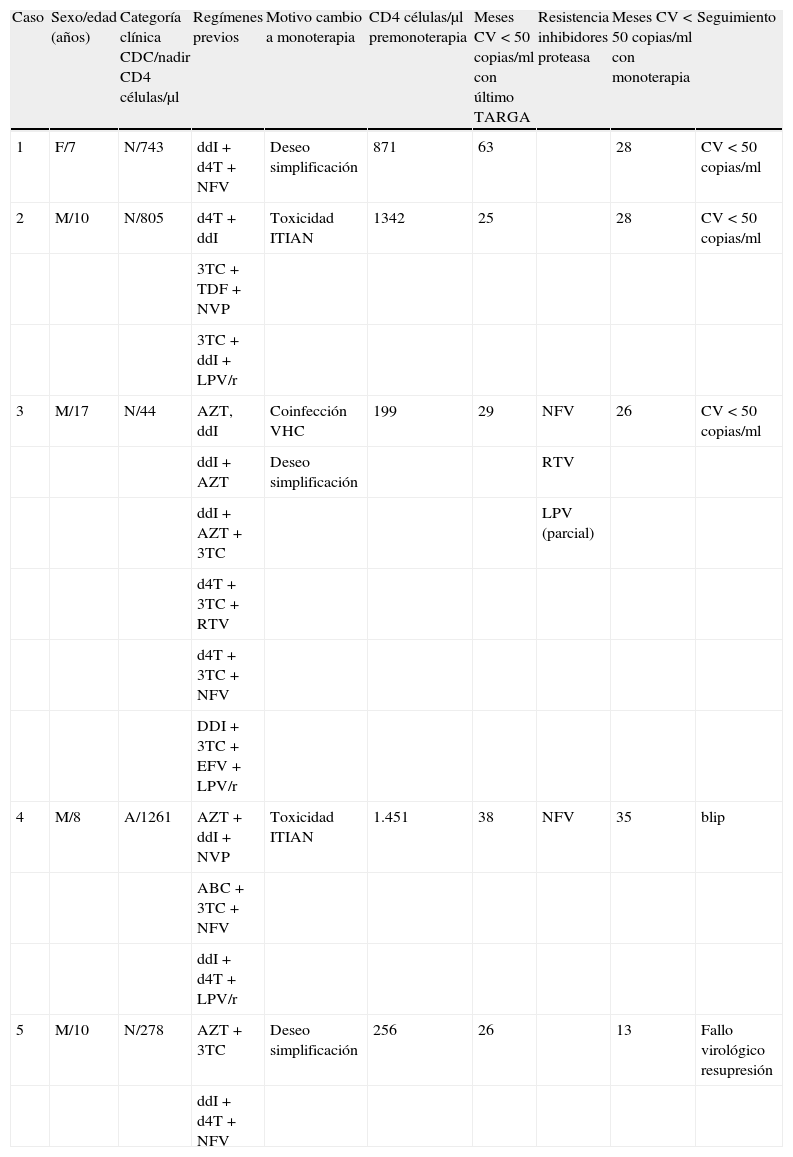
Características de los pacientes en monoterapia con LPV/r
| Caso | Sexo/edad (años) | Categoría clínica CDC/nadir CD4 células/μl | Regímenes previos | Motivo cambio a monoterapia | CD4 células/μl premonoterapia | Meses CV < 50 copias/ml con último TARGA | Resistencia inhibidores proteasa | Meses CV < 50 copias/ml con monoterapia | Seguimiento |
| 1 | F/7 | N/743 | ddI+d4T+NFV | Deseo simplificación | 871 | 63 | 28 | CV<50 copias/ml | |
| 2 | M/10 | N/805 | d4T+ddI | Toxicidad ITIAN | 1342 | 25 | 28 | CV<50 copias/ml | |
| 3TC+TDF+NVP | |||||||||
| 3TC+ddI+LPV/r | |||||||||
| 3 | M/17 | N/44 | AZT, ddI | Coinfección VHC | 199 | 29 | NFV | 26 | CV<50 copias/ml |
| ddI+AZT | Deseo simplificación | RTV | |||||||
| ddI+AZT+3TC | LPV (parcial) | ||||||||
| d4T+3TC+RTV | |||||||||
| d4T+3TC+NFV | |||||||||
| DDI+3TC+EFV+LPV/r | |||||||||
| 4 | M/8 | A/1261 | AZT+ddI+NVP | Toxicidad ITIAN | 1.451 | 38 | NFV | 35 | blip |
| ABC+3TC+NFV | |||||||||
| ddI+d4T+LPV/r | |||||||||
| 5 | M/10 | N/278 | AZT+3TC | Deseo simplificación | 256 | 26 | 13 | Fallo virológico resupresión | |
| ddI+d4T+NFV |
3TC: lamivudina; AZT: zidovudina; CV: carga viral; d4T: estavudina; ddl: didanosina; EFV: efavirenz; F: femenino; M: masculino; NFV: nelfinavir; NVP: nevirapina; RTV: ritonavir; TDF: tenofovir.
Todos los pacientes tuvieron carga viral indetectable basal y durante una mediana de 29 meses con el TARGA. El TARGA antes de monoterapia contenía 2 ITIAN y un inhibidor de la proteasa en todos los pacientes: LPV/r en 3 casos y nelfinavir en 2. Los niños habían recibido una mediana de 3 regímenes antirretrovirales en el pasado. Los pacientes 3 y 4 iniciaron monoterapia a pesar de la presencia de mutación en el gen de la proteasa debido al deseo expreso de simplificación y los efectos adversos de ITIAN, respectivamente. A pesar de tener una prueba genotípica que muestra resistencia, el TARGA que incluía LPV/r en el paciente 3 mantuvo supresión virológica durante 2 años y 5 meses antes de iniciar monoterapia.
La mediana de tiempo en monoterapia fue de 112 semanas. No hubo diferencias significativas en cuanto al último recuento de CD4 disponible en monoterapia respecto al basal (p=1). La carga viral fue indetectable en 3 pacientes durante todo el tiempo de seguimiento. El paciente 4 presentó un «blip» viral en la semana 27, pero las muestras posteriores presentaron carga viral indetectable. Sólo el paciente 5 tuvo un fallo virológico en la semana 73 (carga viral de 2.250 copias/ml), pero la introducción del tratamiento previo con ITIAN (zidovudina+lamivudina) condujo a la indetectabilidad en la semana 108. Se detectaron problemas de adhesión ante el fallo virológico; su madre descubrió al paciente escupiendo los comprimidos que previamente le había mostrado cómo se colocaba en la boca, el paciente confesó que lo hacía en numerosas ocasiones. Se habló con el paciente sobre la importancia de tomar el tratamiento a diario y la familia realiza un control exhaustivo de la toma de los fármacos.
No se identificaron signos clínicos de SIDA ni efectos adversos a fármacos que llevaran a la suspensión de LPV/r.
Aunque no fueron medidos de forma objetiva, los signos clínicos de lipoatrofia que presentaban dos de nuestros pacientes fueron menos evidentes a los 3 meses de iniciar monoterapia.
DiscusiónEl mayor ensayo clínico de monoterapia con LPV/r como estrategia de simplificación tras el TARGA en adultos (OK04) ha mostrado a las 96 semanas una eficacia similar al TARGA (77% pacientes en ambos grupos tenían una carga viral indetectable) y menos efectos adversos. Se requirió terapia de intensificación con 2 ITIAN en un 12% de los pacientes y un 83% alcanzó resupresión virológica5. En la mayoría de los estudios el factor de riesgo principal de fallo virológico es la adhesión subóptima, tal y como ocurrió en el paciente que precisó terapia de intensificación en nuestra serie de casos. Otro factor de riesgo identificado ha sido el nadir de células CD46,7. Un estudio ha mostrado menos lipoatrofia en pacientes en monoterapia con LPV/r (5% versus 34% pacientes con el TARGA y con ITIAN)8. Los signos clínicos de lipoatrofia que presentaban dos de nuestros pacientes fueron menos evidentes tras iniciar monoterapia.
No existe suficiente evidencia para recomendar de forma rutinaria el tratamiento de simplificación con inhibidores de la proteasa, la supresión virológica en reservorios (especialmente en el líquido cefalorraquídeo7,9) puede no ser adecuada y pueden aparecer mutaciones mayores de resistencia en caso de fallo virológico. Se considera una opción de tratamiento en pacientes adultos sin historia de fracaso previo a inhibidores de la proteasa, con carga viral indetectable al menos 6 meses con el TARGA y toxicidad a ITIAN/ITINAN, comorbilidad (enfermedad hepática, enfermedad renal) o interacciones medicamentosas potenciales1.
Nuestra limitada experiencia indica que 4/5 casos en monoterapia con LPV/r durante al menos 94 semanas mantuvieron supresión viral. A pesar de que 2 pacientes no eran buenos candidatos para monoterapia con LPV/r por presentar resistencia conocida a inhibidores de la proteasa, mantuvieron supresión viral durante 95 y 148 semanas. El primer estudio prospectivo no controlado en niños se está llevando a cabo y los resultados preliminares indican que el 85% de los pacientes tenía carga viral de < 50 copias/ml a las 24 semanas y no hubo mutaciones mayores de resistencia a inhibidores de la proteasa en casos de fallo virológico4. Es necesario esperar los resultados de ensayos clínicos como el PENTA 17 para establecer recomendaciones en niños en situaciones puntuales10.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.