El objetivo del estudio fue evaluar el rendimiento diagnóstico de la pregunta relacionada con la actividad física del cuestionario de control del asma de la Global Initiative for Asthma (GINA) para la detección de la broncoconstricción inducida por el ejercicio (BIE) en niños y adolescentes.
Materiales y métodosSe dividió a pacientes (de seis a 18 años de edad) con diagnóstico de asma en dos grupos de acuerdo con la clasificación de gravedad según el cuestionario GINA: asma leve/moderada (ALM) y asma grave refractaria (AGR). Se recogieron datos antropométricos, clínicos y funcionales (espirometría) y se realizó prueba de broncoprovocación con esfuerzo. Se utilizó la cuarta pregunta del cuestionario GINA, concerniente a los síntomas asociados con el esfuerzo físico, para evaluar el rendimiento diagnóstico de este instrumento.
ResultadosSe incluyeron a 40 pacientes (17 con ALM y 23 con AGR) con una edad media de 11,3 años y un z-score medio de FEV1 de -0,33, de los que 13 (32,5%) se clasificaron como casos de asma no controlada. De los pacientes con enfermedad no controlada, siete (53,8%) mostraron caídas en el FEV1 tras la prueba de esfuerzo. Se observó una mayor frecuencia de BIE en sujetos con z-score de FEV1 < -1,0 en comparación con aquellos con un z-score ≥ -1,0 (p = 0,05). No hubo diferencias significativas en la frecuencia de BIE con base en la gravedad o el control de la enfermedad. Tampoco se observó asociación entre la pregunta cuatro (GINA) y la BIE. El área bajo la curva de características operativas del receptor (receiver operating characteristic, ROC) evidenció que el poder discriminatorio del cuestionario GINA resulta insuficiente para detectar la BIE (p = 0,41), con una sensibilidad del 42,1% y una especificidad del 57,1%.
ConclusionesLa pregunta concerniente al ejercicio físico en el cuestionario GINA carece del poder diagnóstico necesario para detectar la BIE en niños y adolescentes asmáticos.
The aim of the study was to evaluate the diagnostic performance of the item concerning physical activity of the Global Initiative for Asthma (GINA) asthma control questionnaire for detection of exercise-induced bronchoconstriction (EIB) in children and adolescents.
Material and methodsWe divided participants (aged 6 to 18 years) with a diagnosis of asthma into two groups according to the GINA severity classification: mild/moderate asthma (MMA) and severe therapy-resistant asthma (STRA). We collected anthropometric, clinical and functional data (spirometry) and performed an EIB test. We used item 4 of the GINA questionnaire regarding exercise-induced symptoms to assess the diagnostic power of this instrument.
ResultsWe included 40 patients (17 with MMA and 23 with STRA) with a mean age of 11.3 years and a mean FEV1z-score of -0.33, of who 13 (32.5%) were classified as having uncontrolled asthma. Of the patients with uncontrolled asthma, 7 (53.8%) exhibited a decrease in the FEV1 after the EIB test. We found a higher frequency of EIB in participants with FEV1 z-score values of less than -1.0 compared to those with a z-score of -1.0 or greater (p = 0.05). There were no significant differences in the frequency of EIB based on disease severity and control. We also found no association of item 4 (GINA) with EIB. The area under the ROC curve demonstrated that the discriminative power of the GINA questionnaire for the detection of EIB is inadequate (p = 0.41), with sensitivity of 42.1% and specificity of 57.1%.
ConclusionsThe physical activity related question of GINA has insufficient diagnostic power to detect EIB in children and adolescents with asthma.
El asma es una enfermedad respiratoria crónica caracterizada por la obstrucción de las vías aéreas. En la población infantil, su prevalencia es alta y es una de las causas más importantes de hospitalización en todo el mundo. Su clínica se caracteriza por la presencia de sibilancias, disnea y tos seca, sobre todo por la noche, de madrugada o ambas1.
Numerosos mecanismos pueden desencadenar las exacerbaciones, entre los que se encuentran el ejercicio, la ansiedad y factores medioambientales. La broncoconstricción inducida por el ejercicio se define como el estrechamiento transitorio de la vía aérea que ocurre durante o después del mismo, evidenciado por una caída en el volumen espiratorio forzado en el primer segundo (FEV1) en combinación con signos y síntomas asmáticos. Entre el 40 y el 90% de los individuos con asma, aproximadamente, experimentan BIE2. La prueba de esfuerzo se considera el patrón de oro para la detección de BIE, ya que evalúa la hiperrespuesta bronquial. No obstante, este método requiere una cooperación considerable por parte del paciente y conlleva riesgos tales como el desarrollo de broncoespasmo grave o caídas en el tapiz rodante, especialmente en niños pequeños2.
En ese sentido, los cuestionarios podrían ofrecer un medio práctico, simple y factible para identificar la presencia de BIE. No obstante, los instrumentos disponibles actualmente3-8 parecen tener una sensibilidad y una especificidad de baja a moderada en niños y adolescentes asmáticos (del 13-71% y del 47-70,7%, respectivamente), lo que da lugar a falsos positivos o negativos en la detección de estos cambios. Por tanto, ninguno de los instrumentos disponibles hoy en día ha mostrado un rendimiento diagnóstico adecuado para la detección de BIE en la población pediátrica9. En un estudio llevado a cabo por Westergren et al.10 el uso del ítem «percepción actual de que el asma limita la actividad física» resultó insuficiente para detectar la BIE. De manera similar, un estudio reciente investigó el uso de un cuestionario desarrollado por la Global Initiative for Asthma (GINA) para predecir el diagnóstico de asma con base en los resultados de la prueba de provocación con metacolina11. De nuevo, los datos sugirieron una precisión diagnóstica de débil a moderada (sensibilidad del 70,2% y especificidad del 49,1%) para la pregunta relacionada con la actividad física en la escala de predicción clínica. En cualquier caso, el uso de este instrumento para monitorizar el control del asma está muy extendido en la práctica clínica. A nuestro conocer, ningún estudio previo ha analizado el uso de la cuarta pregunta del cuestionario GINA (limitación en la actividad debido al asma) para detectar la BIE mediante su comparación con los resultados de la prueba de esfuerzo.
De este modo, dado que el asma puede limitar la actividad física y que el cuestionario GINA es un instrumento sencillo y de uso muy extendido para monitorizar el control del asma, consideramos que la evaluación del rendimiento diagnóstico del ítem del cuestionario GINA que se refiere a los síntomas asociados a la actividad física en la detección de BIE en niños y adolescentes estaba justificada. Por lo tanto, el objetivo de nuestro estudio fue evaluar el rendimiento diagnóstico del ítem sobre la actividad física del cuestionario GINA para la detección de BIE en niños y adolescentes. Con este fin, se reclutaron pacientes con asma de leve a moderada (ALM) y con asma grave refractaria al tratamiento (AGR). También se analizó la asociación entre un resultado positivo en la prueba de esfuerzo y la gravedad del asma, el control de la enfermedad y la función pulmonar en nuestra muestra.
Pacientes y métodosEstudio transversal en niños y adolescentes de ambos sexos de seis a 18 años de edad con diagnóstico de asma seguidos en la clínica ambulatoria de pulmonología pediátrica de nuestro hospital entre marzo de 2016 y septiembre de 2018. Se excluyeron pacientes con anomalías osteoarticulares o musculoesqueléticas, incapaces de realizar la prueba de esfuerzo en el tapiz rodante o con manifestaciones sugestivas de infección de las vías aéreas.
El diagnóstico de asma y la clasificación de gravedad (leve/moderada o grave) se basaron en los criterios establecidos por la GINA12. Se dividió a los pacientes en dos grupos: el grupo de AGR y el grupo de ALM. Los criterios de inclusión en el grupo AGR fueron: asma con necesidad de los pasos cuarto a quinto de tratamiento de la GINA (budesonida ≥ 800 mg/día o equivalente asociado con el agonista β2 de acción prolongada; uso crónico de corticosteroides orales; omalizumab) o presencia de asma no controlada o asma que requiere ese nivel de tratamiento para su control. Se definió enfermedad no controlada como: 1) síntomas persistentes de asma o una puntuación superior a 20 en el cuestionario Asthma Control Test (ACT) (durante más de tres meses); 2) exacerbaciones agudas (con un mínimo de dos ingresos en la unidad de cuidados intensivos [UCI] o dos ciclos completos de corticosteroides orales en los últimos 12 meses); o 3) obstrucción no reversible del flujo aéreo a pesar de recibir corticoterapia. Los criterios para definir ALM fueron: episodios recurrentes de dificultad respiratoria, sibilancias, opresión torácica o función pulmonar alterada (FEV1 reducida y cociente FEV1/capacidad vital forzada [FVC], o aumento de al menos el 12% del FEV1 respecto al valor inicial obtenido tras la administración de un broncodilatador), tratamiento del primer al tercer pasos en la clasificación de la GINA, y un seguimiento en la clínica de al menos tres meses. También se utilizaron los cuatro ítems clínicos del cuestionario GINA para estratificar a los pacientes según el control de la enfermedad. Se dividieron a los pacientes en los siguientes grupos según la puntuación de control del asma: asma controlada (cuatro respuestas negativas); asma controlada parcialmente (una a dos respuestas negativas) y asma no controlada (tres a cuatro respuestas positivas).
Se calculó el tamaño muestral requerido para detectar una sensibilidad/especificidad del 80% del cuarto ítem del cuestionario GINA con una precisión de 0,10 asumiendo una prevalencia de BIE del 70%2. Se utilizó un nomograma para estimar la sensibilidad y especificidad de las pruebas diagnósticas13. Calculamos que sería necesaria una muestra de 40 pacientes. El estudio fue aprobado por el comité de ética de investigación local (protocolo número 47845415.4.0000.5336). Se obtuvo el consentimiento informado firmado por los padres o tutores legales y el asentimiento por escrito de los participantes.
Tras la inclusión en el estudio, los padres de los pacientes completaron el cuestionario GINA de control del asma. Se tomaron medidas antropométricas (peso y talla) y se realizó espirometría en cada paciente. La prueba de esfuerzo se realizó a continuación.
La evaluación antropométrica consistió en la obtención de dos medidas de talla y dos de peso. El peso se midió con el paciente de pie y descalzo y en ropa ligera con una báscula digital (G-Tech, Glass 1 FW, Río de Janeiro, Brasil) con precisión de 100 g. La talla se midió con un tallímetro portátil (AlturaExata, TBW, São Paulo, Brasil) con precisión de 1 mm con el paciente descalzo y de pie. Las medidas de peso y talla se utilizaron para calcular el índice de masa corporal (IMC = peso en kg/[talla en m]2), y a continuación se calculó el z-score del IMC para la edad14.
La espirometría se adhirió a los criterios de aceptabilidad y repetibilidad de la American Thoracic Society y la European Respiratory Society (ATS/ERS)15. Todas las maniobras se realizaron con un espirómetro KOKO (San Diego, California, EE. UU.). Los parámetros obtenidos mediante la espirometría fueron la FVC, el FEV1, el cociente FEV1/FVC y el flujo espiratorio forzado entre el 25 y 75% de la FVC (FEF25-75), expresados en litros (valor absoluto) y puntuaciones z calculadas mediante una ecuación de referencia internacional16.
Los cuestionarios GINA se emplean en todo el mundo para evaluar la gravedad y el control del asma. El control del asma se evalúa mediante cuatro ítems clínicos, de los que uno considera el asma en relación con la actividad física (las palabras exactas son «¿ha tenido el paciente alguna limitación en la actividad debido al asma?»)12. Se hizo esta pregunta a los padres o tutores legales en referencia a las cuatro semanas precedentes a la entrevista.
Las pruebas de esfuerzo se realizaron en un entorno seguro y tranquilo, a una temperatura de 20 a 24°C, aire seco con 10 mgH2O/L y una humedad relativa de aproximadamente el 60%. Todas las pruebas se adhirieron a las recomendaciones de la American Thoracic Society (ATS)17 y fueron supervisadas por fisioterapeutas y el médico a cargo del paciente, para garantizar la seguridad de los participantes. Se realizó espirometría en todos los casos antes de la prueba de esfuerzo (sin administración previa de broncodilatador), y la espirometría se repitió inmediatamente después de terminar la prueba de provocación y a los 5, 10, 15 y 30 minutos. La prueba de esfuerzo se llevó a cabo en un tapiz rodante KT-10400 (Imbramed, São Paulo, Brasil) con inclinación (15%) y velocidad ajustables. Se incrementó la velocidad hasta que el sujeto alcanzó una frecuencia cardíaca correspondiente al 80% del máximo establecido para su edad (220-edad en años)17. A partir de ese momento, el paciente tenía que continuar la carrera a esa intensidad durante cuatro seis minutos más, según su tolerancia. Se consideró el resultado positivo para BIE en caso de caída del FEV1 a los 30 minutos de finalizar el ejercicio de más del 15% con respecto a la medida inicial17. Solo se realizó la prueba en pacientes con valores iniciales del FEV1 superiores al 70% del valor teórico.
En el análisis estadístico, se evaluó la normalidad de la distribución por medio de la prueba de Kolmogorov-Smirnov. Las variables cuantitativas se presentan como media y desviación estándar o mediana y rango intercuartílico según su distribución, y las cualitativas como frecuencias absolutas y relativas. Se compararon las variables cuantitativas mediante la prueba t de Student para datos independientes y las cualitativas mediante la χ2 de Pearson. Se evaluó el rendimiento diagnóstico del ítem específico del cuestionario GINA para la detección de BIE por medio de una curva de las características operativas del receptor (curva ROC). El análisis estadístico se realizó con el software SPSS versión 17.0. Todas las pruebas fueron a dos colas, siendo considerados estadísticamente significativos los valores p ≤ 0,05.
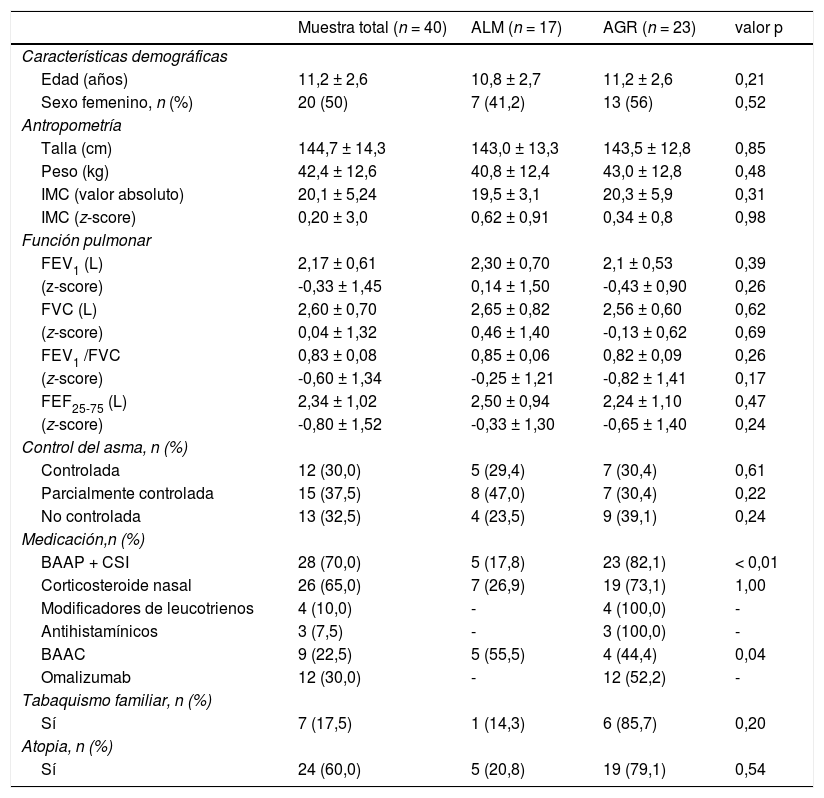
ResultadosSe invitó a participar a 45 pacientes, de los que finalmente se excluyeron cinco por no poder realizar la prueba de esfuerzo. Por lo tanto, la muestra total incluyó a 40 niños y adolescentes con asma, 17 con ALM y 23 con AGR. La edad media de la muestra total fue de 11,2 años. Veinte participantes (50%) eran varones, y el z-score medio del IMC fue de 0,20. Según la puntuación en el cuestionario GINA, 28 pacientes (70%) tenían asma no controlada o parcialmente controlada. El z-score medio del FEV1 fue -0,33, y el z-score medio del cociente FEV1/FVC-0,60. No hubo diferencias significativas entre grupos en los parámetros de función pulmonar. Tampoco se observaron diferencias significativas entre grupos en la comparación de características demográficas, el control del asma y otras variables de función pulmonar (tabla 1).
Características de los pacientes bajo estudio
| Muestra total (n = 40) | ALM (n = 17) | AGR (n = 23) | valor p | |
|---|---|---|---|---|
| Características demográficas | ||||
| Edad (años) | 11,2 ± 2,6 | 10,8 ± 2,7 | 11,2 ± 2,6 | 0,21 |
| Sexo femenino, n (%) | 20 (50) | 7 (41,2) | 13 (56) | 0,52 |
| Antropometría | ||||
| Talla (cm) | 144,7 ± 14,3 | 143,0 ± 13,3 | 143,5 ± 12,8 | 0,85 |
| Peso (kg) | 42,4 ± 12,6 | 40,8 ± 12,4 | 43,0 ± 12,8 | 0,48 |
| IMC (valor absoluto) | 20,1 ± 5,24 | 19,5 ± 3,1 | 20,3 ± 5,9 | 0,31 |
| IMC (z-score) | 0,20 ± 3,0 | 0,62 ± 0,91 | 0,34 ± 0,8 | 0,98 |
| Función pulmonar | ||||
| FEV1 (L) | 2,17 ± 0,61 | 2,30 ± 0,70 | 2,1 ± 0,53 | 0,39 |
| (z-score) | -0,33 ± 1,45 | 0,14 ± 1,50 | -0,43 ± 0,90 | 0,26 |
| FVC (L) | 2,60 ± 0,70 | 2,65 ± 0,82 | 2,56 ± 0,60 | 0,62 |
| (z-score) | 0,04 ± 1,32 | 0,46 ± 1,40 | -0,13 ± 0,62 | 0,69 |
| FEV1 /FVC | 0,83 ± 0,08 | 0,85 ± 0,06 | 0,82 ± 0,09 | 0,26 |
| (z-score) | -0,60 ± 1,34 | -0,25 ± 1,21 | -0,82 ± 1,41 | 0,17 |
| FEF25-75 (L) | 2,34 ± 1,02 | 2,50 ± 0,94 | 2,24 ± 1,10 | 0,47 |
| (z-score) | -0,80 ± 1,52 | -0,33 ± 1,30 | -0,65 ± 1,40 | 0,24 |
| Control del asma, n (%) | ||||
| Controlada | 12 (30,0) | 5 (29,4) | 7 (30,4) | 0,61 |
| Parcialmente controlada | 15 (37,5) | 8 (47,0) | 7 (30,4) | 0,22 |
| No controlada | 13 (32,5) | 4 (23,5) | 9 (39,1) | 0,24 |
| Medicación,n (%) | ||||
| BAAP + CSI | 28 (70,0) | 5 (17,8) | 23 (82,1) | < 0,01 |
| Corticosteroide nasal | 26 (65,0) | 7 (26,9) | 19 (73,1) | 1,00 |
| Modificadores de leucotrienos | 4 (10,0) | - | 4 (100,0) | - |
| Antihistamínicos | 3 (7,5) | - | 3 (100,0) | - |
| BAAC | 9 (22,5) | 5 (55,5) | 4 (44,4) | 0,04 |
| Omalizumab | 12 (30,0) | - | 12 (52,2) | - |
| Tabaquismo familiar, n (%) | ||||
| Sí | 7 (17,5) | 1 (14,3) | 6 (85,7) | 0,20 |
| Atopia, n (%) | ||||
| Sí | 24 (60,0) | 5 (20,8) | 19 (79,1) | 0,54 |
Datos presentados como media y desviación estándar, excepto el sexo y el control del asma (frecuencias relativas y absolutas).
AGR: asma grave refractaria; ALM: asma leve/moderada; BAAC: beta 2-agonistas de acción corta; BAAP: beta 2-agonistas de acción prolongada; CSI: corticosteroides inhalados; FEV1: volumen espiratorio forzado en el primer segundo; FEF25-75: flujo espiratorio forzado entre el 25 y el 75% de la capacidad vital; FVC: capacidad vital forzada; IMC: índice de masa corporal.
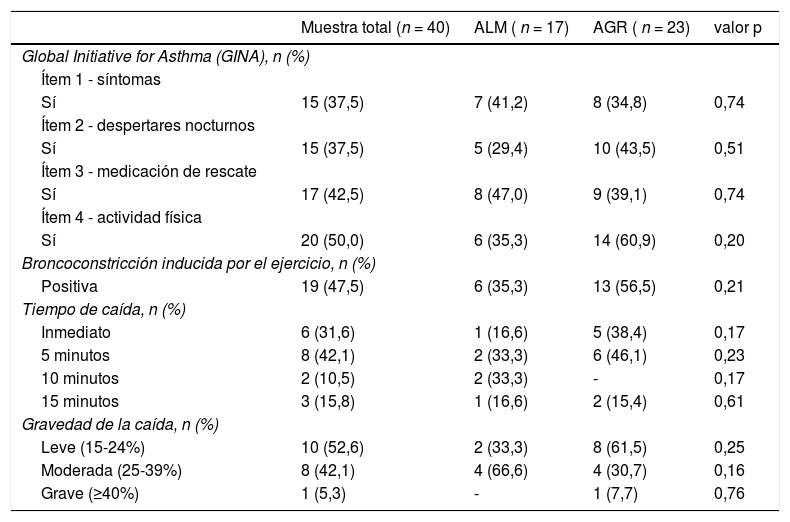
En cuanto al cuestionario GINA, el porcentaje de respuestas positivas osciló entre el 37,5 y el 50% en la primera pregunta (síntomas), la segunda (despertares nocturnos) y la tercera (tratamiento de rescate). Aunque la mayoría de los pacientes en el grupo de AGR (60,9%) respondieron afirmativamente a la cuarta pregunta (actividad física), no hubo diferencias significativas en comparación con el grupo de ALM (35,3%; p = 0,10). De los pacientes evaluados, 19 (47,5%) tuvieron caídas del FEV1 en la prueba de esfuerzo, 13 del grupo con AGR (56,5%) y seis del grupo con ALM (35,2%). La reducción se observó predominantemente a los cinco minutos, y en la mayoría de los casos fue una caída leve de la función pulmonar (del 15-24%). No se observaron diferencias entre grupos al comparar estas variables (tabla 2).
Resultados sobre el control del asma (cuestionario) y la broncoconstricción inducida por el ejercicio
| Muestra total (n = 40) | ALM ( n = 17) | AGR ( n = 23) | valor p | |
|---|---|---|---|---|
| Global Initiative for Asthma (GINA), n (%) | ||||
| Ítem 1 - síntomas | ||||
| Sí | 15 (37,5) | 7 (41,2) | 8 (34,8) | 0,74 |
| Ítem 2 - despertares nocturnos | ||||
| Sí | 15 (37,5) | 5 (29,4) | 10 (43,5) | 0,51 |
| Ítem 3 - medicación de rescate | ||||
| Sí | 17 (42,5) | 8 (47,0) | 9 (39,1) | 0,74 |
| Ítem 4 - actividad física | ||||
| Sí | 20 (50,0) | 6 (35,3) | 14 (60,9) | 0,20 |
| Broncoconstricción inducida por el ejercicio, n (%) | ||||
| Positiva | 19 (47,5) | 6 (35,3) | 13 (56,5) | 0,21 |
| Tiempo de caída, n (%) | ||||
| Inmediato | 6 (31,6) | 1 (16,6) | 5 (38,4) | 0,17 |
| 5 minutos | 8 (42,1) | 2 (33,3) | 6 (46,1) | 0,23 |
| 10 minutos | 2 (10,5) | 2 (33,3) | - | 0,17 |
| 15 minutos | 3 (15,8) | 1 (16,6) | 2 (15,4) | 0,61 |
| Gravedad de la caída, n (%) | ||||
| Leve (15-24%) | 10 (52,6) | 2 (33,3) | 8 (61,5) | 0,25 |
| Moderada (25-39%) | 8 (42,1) | 4 (66,6) | 4 (30,7) | 0,16 |
| Grave (≥40%) | 1 (5,3) | - | 1 (7,7) | 0,76 |
Datos presentados como valores absolutos medios y frecuencias relativas.
AGR: asma grave refractaria; ALM: asma leve/moderada.
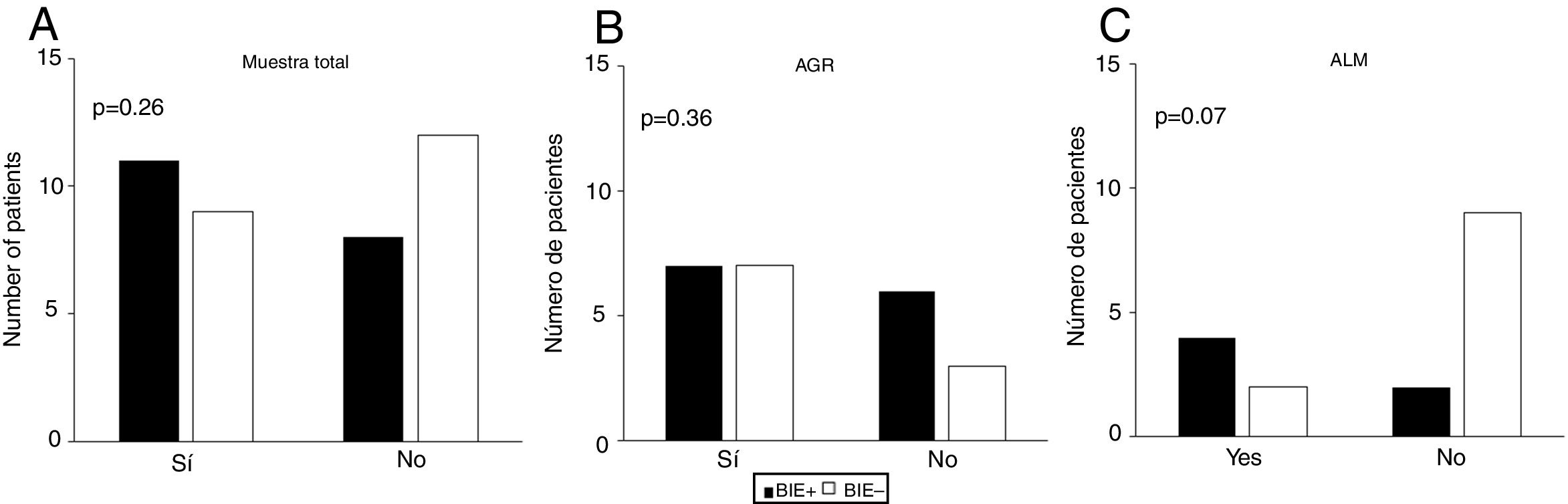
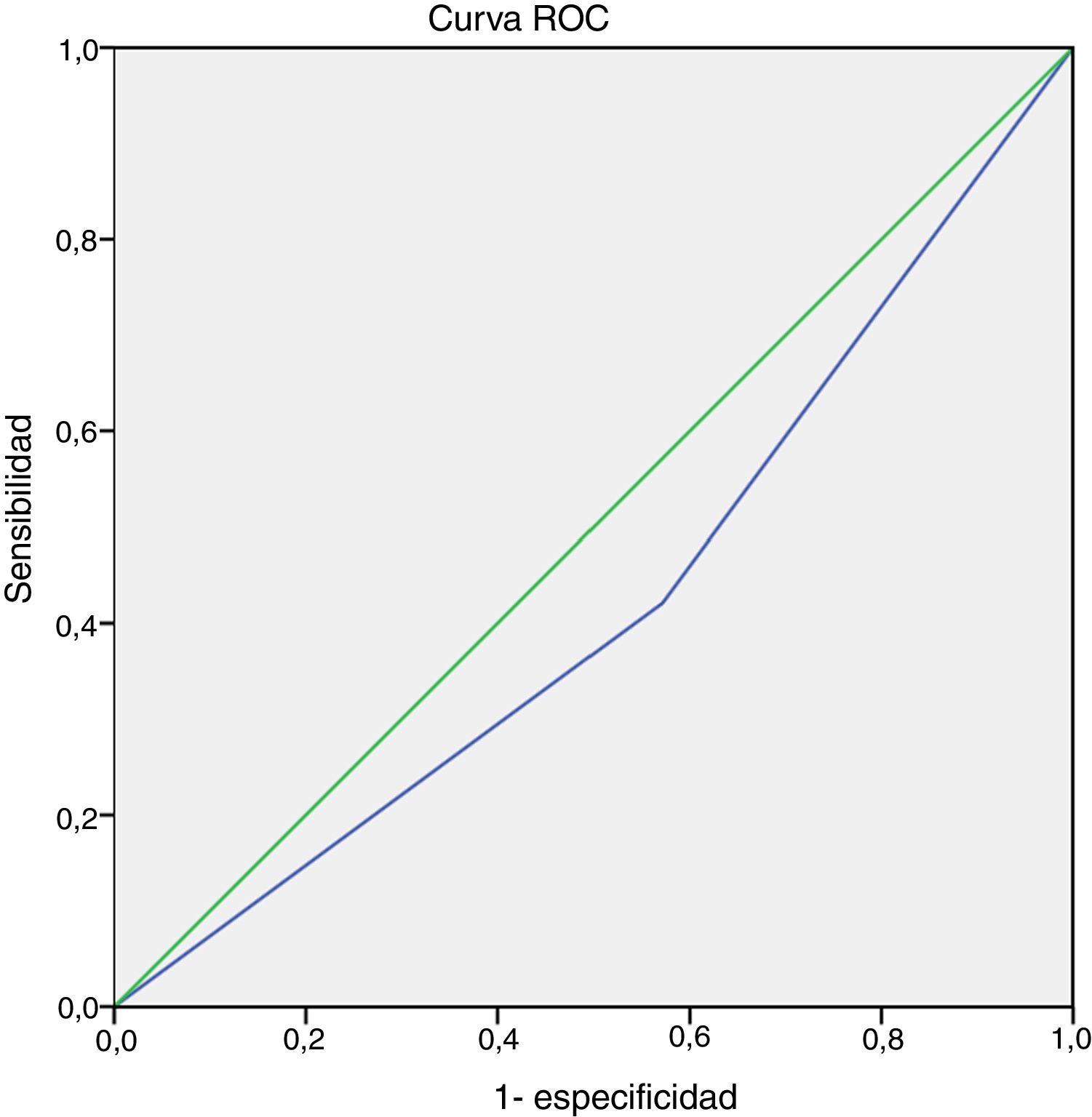
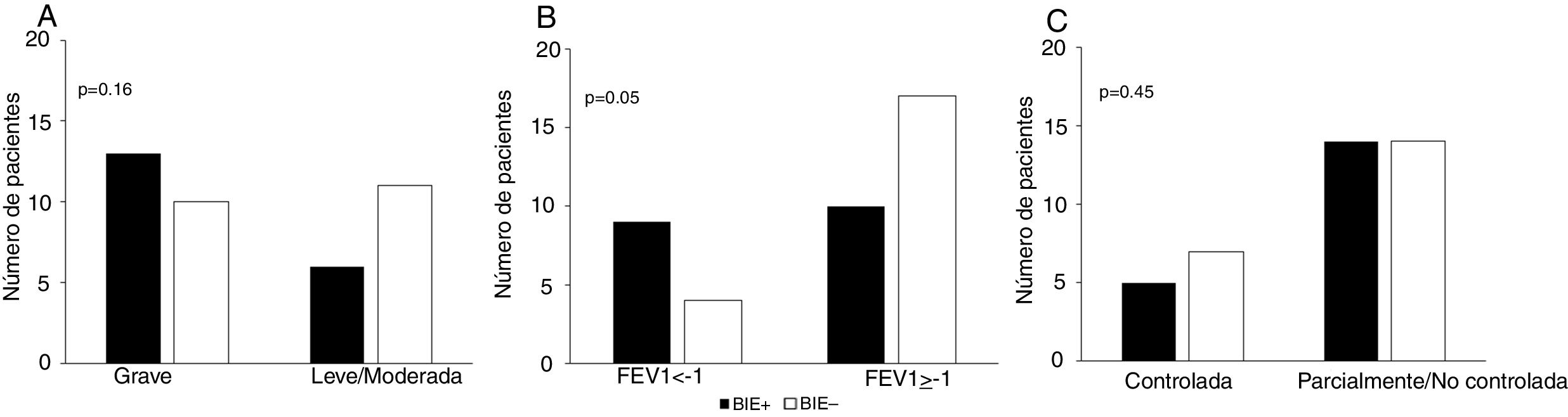
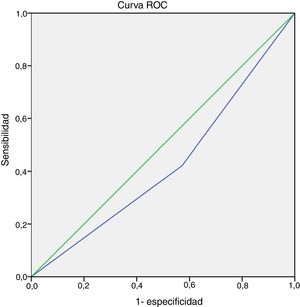
No se objetivó una asociación entre el cuarto ítem (actividad física) del cuestionario GINA y la BIE ni en la muestra total (p = 0,26) ni en los grupos de pacientes con ALM (p = 0,07) o con AGR (p = 0,36) (fig. 1). Además, la sensibilidad de este ítem para la detección de BIE en niños y adolescentes con asma en la muestra total (n = 40) fue del 42,10%, y la especificidad del 57,10% (intervalo de confianza [IC] del 95%, 0,24-0,60). El área bajo la curva ROC confirmó un poder predictivo bajo (fig. 2). Los resultados también fueron desfavorables cuando se analizaron los grupos con ALM y AGR por separado (datos no mostrados). La BIE fue más frecuente en participantes con valores bajos del FEV1 (z-score < -1,0) en comparación con aquellos con valores mayores (z-score ≥ -1,0) (p = 0,05). No obstante, no se observaron diferencias significativas en la frecuencia de BIE según la gravedad o el control del asma (fig. 3).
Asociación de la respuesta al cuarto ítem (actividad física) del cuestionario de la Global Initiative for Asthma (GINA) con la broncoconstricción inducida por el ejercicio (BIE) en A) la muestra total; B) el grupo con asma grave refractaria (AGR) y C) el grupo con asma leve/moderada (ALM). Los valores p corresponden a la prueba χ2.
Curva de las características operativas del receptor (curva ROC) del cuarto ítem (actividad física) del cuestionario de la Global Initiative for Asthma (GINA) para la identificación de pacientes con broncoconstricción inducida por el ejercicio (BIE). Área bajo la curva = 0,42 (IC 95%, 0,24-0,60; p = 0,416).
Los datos obtenidos demuestran que el rendimiento diagnóstico del cuarto ítem (referente a los síntomas asociados con actividad física) del cuestionario GINA para la detección de BIE en niños y adolescentes con ALM y AGR es insuficiente. Los datos de la curva ROC y su baja sensibilidad y especificidad evidencian las limitaciones de este instrumento.
Múltiples estudios han investigado los cuestionarios disponibles en la actualidad para diagnosticar la BIE en niños y adolescentes, pero han evidenciado una sensibilidad y especificidad de baja a moderada4,6,11,18,19. La mayoría de estos instrumentos evalúan los signos y síntomas más comunes del asma (tos, opresión torácica y disnea) durante y después del ejercicio en un intervalo de tiempo dado antes de hacerse la prueba (de 1-12 meses). Dicho esto, desde un punto de vista clínico, su poder discriminatorio parece insuficiente. Una baja forma física, la obesidad y comportamientos sedentarios son posibles factores de confusión en la interpretación de los síntomas de BIE en niños y adolescentes. Hasta donde conocemos, el presente estudio es el primero en evaluar el rendimiento diagnóstico del cuestionario GINA (en particular, el cuarto ítem) en la detección de la hiperrespuesta bronquial durante la prueba de esfuerzo en niños y adolescentes asmáticos. Nuestros hallazgos demuestran que el cuestionario GINA tiene un poder insuficiente para predecir la BIE en comparación con la prueba de esfuerzo, con una sensibilidad del 42,1% y una especificidad del 57,1%. Estos resultados concuerdan con los de un estudio previo que encontró una precisión diagnóstica baja (sensibilidad del 70,2% y especificidad del 49,1%) de la puntuación de un cuestionario para la predicción de BIE en la prueba de provocación con metacolina11. Nuestros hallazgos también son consistentes con los de Westergren et al.10, en cuyo estudio las respuestas al ítem «percepción actual de que el asma limita la actividad física» no sirvieron para detectar BIE con precisión. Además, de dos estudios que analizaron la asociación entre el cuestionario Asthma Control Test (ACT) y la prueba de esfuerzo20,21, solo uno encontró una especificidad alta y ambos encontraron una sensibilidad baja para la detección de BIE en niños mayores de 12 años21. Por lo tanto, aunque algunos estudios muestran que ciertas pruebas pueden utilizarse como un método alternativo para diagnosticar BIE y estimar el nivel de inflamación eosinofílica de no estar disponible el patrón de oro22,23, el rendimiento de los cuestionarios existentes en la actualidad continúa siendo pobre en la población pediátrica. Cabe señalar que en el presente estudio se evaluó la precisión diagnóstica con base en el uso específico del cuarto ítem en el cuestionario GINA, por lo que no se puede excluir la posibilidad de que la adición de preguntas adicionales o un cuestionario de síntomas podría haber mejorado los resultados. En cualquier caso, consideramos que debería evitarse su uso en la práctica clínica por facultativos para identificar síntomas inducidos por el ejercicio o para la indicación de ejercicio, y que debería usarse la prueba de esfuerzo siempre que esté disponible y sea necesario.
La prevalencia de BIE en la población pediátrica es muy heterogénea, oscilando entre el 20 y el 90% de los casos totales de asma2. La prevalencia en nuestro estudio estaba dentro de ese intervalo, ya que casi la mitad de los pacientes (48%) recibieron un diagnóstico de BIE en la prueba de esfuerzo. La variabilidad en la prevalencia de BIE podría deberse a diferencias entre regiones geográficas y características poblacionales. Además, la temperatura ambiente, las estaciones, la humedad y otros factores ambientales (polución atmosférica, alérgenos) pueden afectar la prevalencia2. Aunque nuestro estudio encontró una mayor frecuencia de BIE en los pacientes con AGR (21,2% mayor), la diferencia no alcanzó la significación estadística.
No se observaron diferencias en la función pulmonar o el control del asma entre los grupos de ALM y AGR. Algunos estudios muestran que la espirometría podría no ser suficientemente sensible en niños para la detección de alteraciones pulmonares algunas enfermedades respiratorias infantiles, incluyendo el asma24 y la bronquiolitis obliterante postinfecciosa25. Varios estudios han hallado valores de función pulmonar dentro o cerca del rango de la normalidad, incluso en pacientes con AGR24-26. Estos resultados difieren de los encontrados en adultos, que parecen sufrir una mayor disminución de la función pulmonar27. Estos hallazgos en la edad pediátrica podrían explicarse, al menos en parte, por el tiempo de evolución más corto, el uso de nuevas terapias farmacológicas (omalizumab), y un menor grado de remodelado bronquial. En cuanto al control de la enfermedad, el asma no controlada fue más frecuente en el grupo de AGR (diferencia del 15,6%), aunque la diferencia entre los grupos no fue significativa. Puede que estos datos estuvieran influenciados por el hecho de que estos pacientes se encuentran en seguimiento ambulatorio con visitas regulares, lo que permite optimizar el tratamiento.
Nuestros datos también demuestran que valores iniciales más bajos del FEV1 (z-score < -1) se asocian con una frecuencia mayor de BIE. En conformidad con las guías internacionales, el FEV1 es uno de los parámetros clínicos más utilizados en el diagnóstico y monitorización del asma1. Nuestros hallazgos fueron consistentes con los de estudios previos28,29, encontrándose una asociación de valores bajos del FEV1 con empeoramiento clínico, exacerbaciones y BIE. Un estudio reciente en niños y adolescentes asmáticos30 encontró una asociación significativa entre los valores del FEV1 y el control clínico del asma (GINA), lo que sugiere que el FEV1 es un marcador de exacerbación. Otros datos indican que el FEV1 está asociado con marcadores clínicos importantes en niños con asma, como por ejemplo síntomas y exacerbaciones28.
El presente estudio tiene algunas limitaciones. En primer lugar, debido a su diseño transversal, el estudio analizó la pregunta clínica y la prueba de esfuerzo realizadas en un solo punto en el tiempo. Es sabido que el asma tiene una naturaleza cambiante y dinámica en lo que concierne a sus síntomas y su control. Un estudio longitudinal podría proporcionar una comprensión mejor del asunto. En segundo lugar, algunos pacientes recibieron omalizumab (terapia anti-IgE), lo que podría haber resultado en tasas superiores de control de asma y una prevalencia menor de BIE en pacientes con AGR. No obstante, dados los beneficios del omalizumab en pacientes con AGR30, la interrupción de este tratamiento durante el período de estudio no estaría justificada.
En conclusión, nuestros resultados demuestran que la pregunta sobre la actividad física del cuestionario GINA tiene un bajo poder diagnóstico para la detección del BIE en niños y adolescentes asmáticos, independientemente de la gravedad del asma. Por lo tanto, la indicación de la prueba de esfuerzo para el diagnóstico de BIE debería discutirse con mayor profundidad en las guías y recomendaciones con objeto de prevenir una alta frecuencia de falsos positivos o falsos negativos en la población pediátrica.
FinanciaciónEste trabajo ha recibido apoyo de la Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), código de financiación 001, y del Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.anpedi.2020.06.031.