La hiperuricemia secundaria al síndrome de lisis tumoral (SLT) es una complicación importante en neoplasias con rápida proliferación y destrucción celular.
El objetivo del estudio fue comparar la eficacia de la rasburicasa con la del alopurinol en la reducción de los niveles plasmáticos de ácido úrico, creatinina y fósforo en niños con SLT.
Pacientes y métodoSe realizó un estudio comparativo observacional no aleatorizado del tratamiento con alopurinol o rasburicasa en 32 niños con enfermedad oncohematológica ingresados en la unidad de cuidados intensivos pediátricos con SLT establecido o alto riesgo de desarrollarlo. Desde enero de 1991 hasta enero de 2003 16 pacientes recibieron alopurinol (10mg/kg/día cada 8h) y desde febrero de 2003 hasta junio de 2009 16 pacientes recibieron rasburicasa (0,2mg/kg/día, una dosis diaria). Se determinaron los niveles plasmáticos de ácido úrico, creatinina y fósforo previo al tratamiento y a las 4, 12, 24, 36, 48, 72 y 96h.
ResultadosLos niveles basales de ácido úrico fueron similares en ambos grupos. A las 4h tras la primera dosis del fármaco los pacientes tratados con rasburicasa comparados con alopurinol tuvieron una mayor reducción (p<0,0001) de los niveles plasmáticos de ácido úrico, al igual que en las determinaciones posteriores. Los niveles de creatinina fueron más elevados en el grupo de alopurinol que en el de rasburicasa. Los niveles de fósforo fueron similares en ambos grupos. El 56% de los pacientes tratados con alopurinol requirió hemodiálisis, mientras que ningún paciente del grupo de rasburicasa la precisó.
ConclusionesEste estudio demuestra un control más rápido y niveles significativamente menores de ácido úrico tras tratamiento con rasburicasa comparado con alopurinol en el SLT así como niveles más bajos de creatinina y menor necesidad de hemodiálisis.
Hyperuricaemia accompanying tumour lysis syndrome (TLS) is a serious complication in neoplasias with rapid proliferation and cellular destruction. The aim of the study was to evaluate the effects of rasburicase versus allopurinol on plasma uric acid, creatinine and phosphorus levels in paediatric patients with TLS.
Patients and methodA comparative study of treatment with rasburicase or allopurinol was performed in 32 paediatric patients with haematological-oncological malignancies and with established TLS or a high risk of developing it, admitted to the Paediatric Intensive Care Unit (PICU). Allopurinol (10mg/kg/day every 8h) was administered to 16 patients between January 1991 and January 2003, and 16 patients received rasburicase (0.2mg/kg/day, once daily), from February 2003 to June 2009. Plasma uric acid, creatinine and phosphorus levels were measured at baseline and 4, 12, 24, 36, 48, 72 and 96h after therapy in both study groups.
ResultsBaseline uric acid levels were similar in both groups. Four hours after the first dose, patients treated with rasburicase achieved a greater reduction (p<0.0001) of initial plasma uric acid levels compared to allopurinol, as in the other serial determinations. Creatinine levels were higher in the allopurinol group than in the rasburicase one. Plasma phosphorus levels were similar in both groups. Haemodialysis was required in 56% of patients in the allopurinol group, whereas none of rasburicase group needed this.
ConclusionThis study demonstrated that there is more rapid control and lower plasma uric acid levels in patients at high risk for tumour lysis syndrome who received rasburicase compared to allopurinol, as well as lower levels of creatinine and a lower percentage of haemodialysis.
El síndrome de lisis tumoral (SLT) es un conjunto de anomalías metabólicas provocadas por la rápida destrucción de las células neoplásicas y la liberación de su contenido intracelular al espacio extracelular1, bien de forma espontánea por necrosis tumoral o secundaria al tratamiento con citotóxicos2. Se caracteriza por hiperuricemia, hiperpotasemia, hiperfosfatemia e hipocalcemia. Estas alteraciones pueden exceder la capacidad de eliminación renal y producir precipitación de cristales de ácido úrico y fosfato cálcico en el riñón, fallo renal agudo secundario (hasta el 30% en el linfoma de Burkitt)3,4 y secuelas renales, a veces, irreversibles5.
Es más frecuente en tumores con elevada tasa de crecimiento, grandes masas tumorales y alta quimiosensibilidad, como el linfoma no hodgkiniano (LNH), especialmente tipo Burkitt, y la leucemia linfoblástica aguda de estirpe T. El alopurinol (4–hidroxipurinol) es un inhibidor de la enzima xantino oxidasa hepática cuya acción es bloquear la conversión de hipoxantina y xantina en ácido úrico. Aunque ha demostrado ser eficaz en la prevención y el tratamiento de la hiperuricemia secundaria al SLT, existen ciertas limitaciones en su uso. En primer lugar, el alopurinol inhibe la formación de nuevas moléculas de ácido úrico, pero no degrada el ácido úrico preformado. En segundo lugar, bloquea el catabolismo de sus precursores (hipoxantina y xantina), lo que podría llevar a la precipitación de estos metabolitos en los túbulos renales y al desarrollo potencial de una nefropatía obstructiva. En tercer lugar, reduce el aclaramiento de determinados quimioterápicos (azatioprina, 6-mercaptopurina y metrotrexate), y requiere un uso de menor dosis cuando se administran concomitantemente con alopurinol. Por último, se han descrito reacciones de hipersensibilidad asociadas al tratamiento con alopurinol, como rash cutáneo y fiebre6.
La enzima urato oxidasa cataliza la oxidación del ácido úrico en alantoína, una sustancia 5 a 10 veces más soluble que el ácido úrico y fácilmente excretable5. Esta enzima se encuentra en la mayoría de los mamíferos, aunque no existe en los humanos por una mutación genética que se produjo durante la evolución de los homínidos.
La rasburicasa es una forma recombinante de la urato oxidasa, obtenida por clonación del gen de Aspergillus flavus y expresada por una cepa modificada de Saccharomyces cerevisiae. Previamente se había utilizado una forma no recombinante de urato oxidasa (uricozyme), y existía un mayor riesgo de reacciones alérgicas o de hipersensibilidad asociadas a su uso6.
El mejor tratamiento del SLT es la prevención6. Es fundamental la identificación de los pacientes de riesgo, iniciar precozmente las medidas preventivas y reconocer y tratar de forma temprana y agresiva las posibles complicaciones.
En los pacientes con bajo riesgo de desarrollar SLT está indicada la monitorización y la observación clínica. No existe una recomendación claramente definida sobre el tratamiento ideal de los pacientes con un riesgo medio. Inicialmente, se debe utilizar alopurinol como agente antihiperuricémico, aunque se ha considerado también en pacientes pediátricos el uso de una dosis única de rasburicasa7,8. En estos pacientes está recomendado el tratamiento con rasburicasa si se desarrolla hiperuricemia a pesar de la profilaxis con alopurinol. Por último, la rasburicasa se recomienda para el tratamiento del SLT establecido y en la profilaxis de pacientes de alto riesgo6. Hay que recordar que el alopurinol no reduce el ácido úrico formado previo, por lo que ante pacientes con hiperuricemia preexistente (≥7,5mg/dl) se prefiere tratamiento con rasburicasa6.
El objetivo de este estudio fue comprobar la eficacia del tratamiento con rasburicasa o alopurinol en la reducción de los niveles plasmáticos de ácido úrico, creatinina y fósforo y sus consecuencias en niños con enfermedades oncohematológicas con SLT establecido o alto riesgo de desarrollarlo.
Pacientes y métodoDescripción del estudioDesde enero de 1991 hasta junio de 2009 se realizó un estudio comparativo observacional no aleatorio del tratamiento con alopurinol o rasburicasa en 32 niños con enfermedad oncohematológica ingresados en la unidad de cuidados intensivos pediátricos (UCI-P) con SLT establecido o alto riesgo de desarrollarlo.
Los pacientes se distribuyeron en 2 grupos:
Grupo A: 16 pacientes tratados con alopurinol a dosis de 10mg/kg/día cada 8h por vía oral desde enero de 1991 hasta enero de 2003.
Grupo B: 16 pacientes tratados con rasburicasa a dosis de 0,2mg/kg/día intravenosa en dosis única diaria desde febrero de 2003 hasta junio de 2009.
Pacientes con enfermedad oncohematológica y SLT establecido o con alto riesgo de desarrollarlo (al menos un criterio):
- •
Gran masa tumoral: recuento de leucocitos superior a 50.000/l o lactato deshidrogenasa (LDH) superior a 500UI/l.
- •
Ácido úrico superior o igual a 8mg/dl o creatinina sérica superior a 2mg/dl.
- •
Antecedentes de SLT en ciclos previos de quimioterapia.
Historia documentada de hipersensibilidad a rasburicasa o alopurinol, asma, atopia, déficit de glucosa-6-fosfato-deshidrogenasa u otras alteraciones metabólicas que causen anemia hemolítica.
Datos recogidos y seguimientoLas variables analizadas fueron edad y sexo, antecedentes personales y familiares, tipo de tumor, estadio del tumor al comienzo del tratamiento, manifestaciones clínicas, síntoma de alerta o diagnóstico del tumor, grupo de estudio, niveles plasmáticos seriados de ácido úrico, creatinina y fósforo en ambos grupos de estudio (niveles basales previos al tratamiento y a las 4, 12, 24, 36, 48, 72 y 96h), necesidad de instaurar técnicas de depuración extrarrenal, efectos secundarios o toxicidad, número de días de ingreso en UCI-P, número de días de tratamiento y fallecimiento.
Efectos secundarios y toxicidadSe realizó en todos los pacientes un análisis de la toxicidad y de los efectos secundarios tras la administración de los 2 fármacos mediante vigilancia clínica estrecha.
Evaluaciones previas al tratamiento. Exploración y pruebas complementariasAntes de iniciar el tratamiento se realizó:
- •
Analítica general: hemograma, bioquímica sanguínea (urea, creatinina, calcio, fósforo, sodio, potasio, ácido úrico, proteínas totales y LDH).
- •
Exploración física y monitorización de constantes (frecuencia cardíaca, presión arterial, presión venosa central y diuresis) previo al inicio del tratamiento y de forma seriada después del comienzo de éste.
Se realizó mediante el programa SPSS 16.0 para Windows. Estadística básica descriptiva para variables cuantitativas. En el estadístico de contraste se utilizó la prueba no paramétrica de Mann Whithney para variables cuantitativas y Chi cuadrado para comparación de variables cualitativas. Se consideraron valores estadísticamente significativos aquéllos con p<0,05.
ResultadosLa edad media de los pacientes estudiados fue de 95,4±42 meses (mínimo un mes; máximo 168 meses). No se encontraron diferencias significativas entre grupos en cuanto a edad o a distribución por sexo.
El tipo de tumor más frecuente fue el LNH tipo Burkitt, que correspondió a 15 de los 32 casos (47%), y la leucemia linfoblástica aguda de estirpe T, que correspondió a 8 de los 32 casos (25%). Todos los pacientes con LNH tipo Burkitt se encontraban en estadio iii antes de iniciar el estudio.
El signo guía de diagnóstico fundamental del tumor fue el hallazgo de una masa abdominal a la exploración en el 37,5% de los casos.
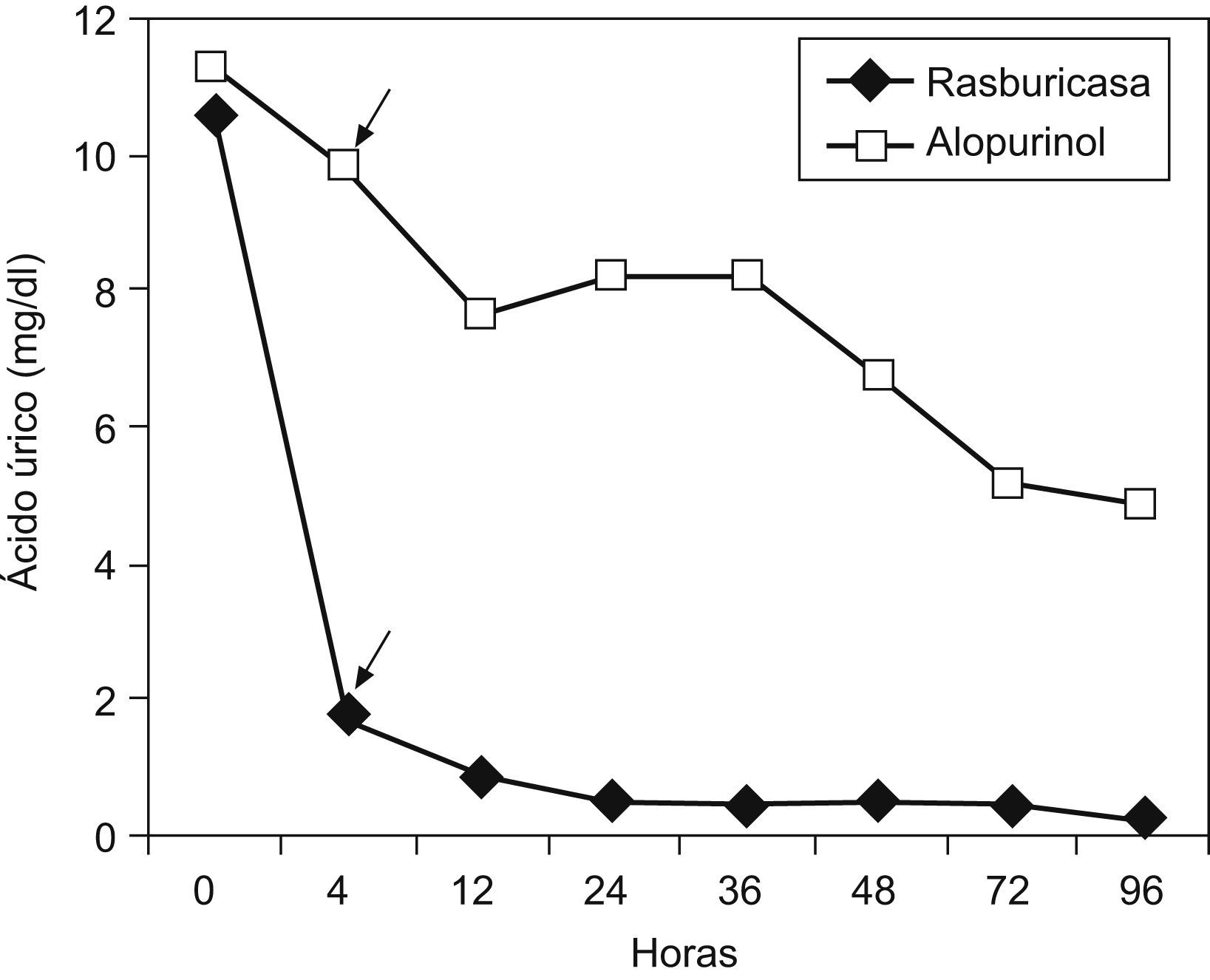
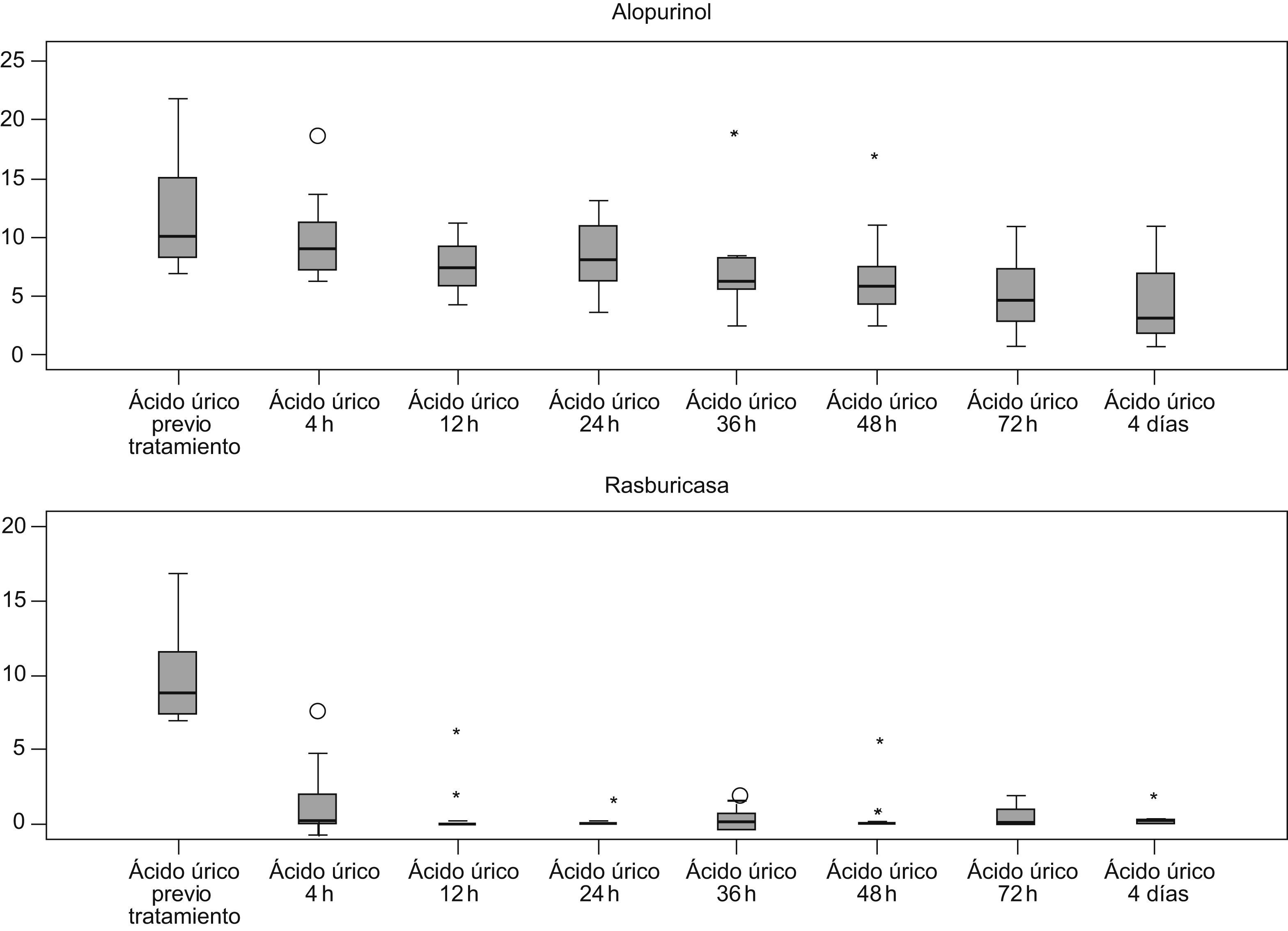
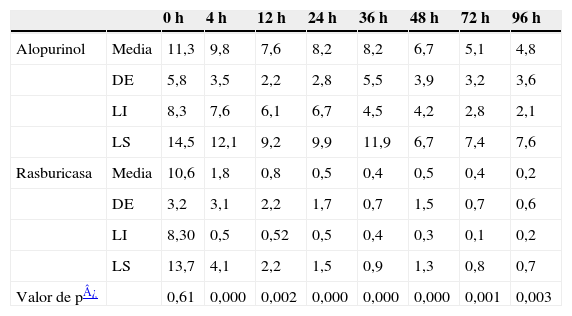
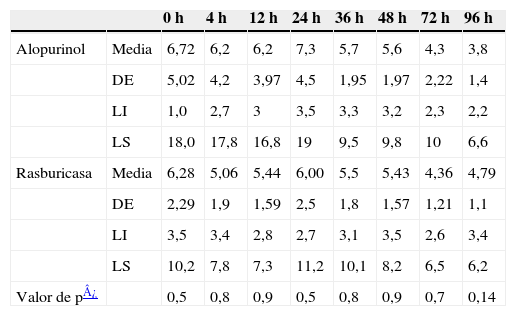
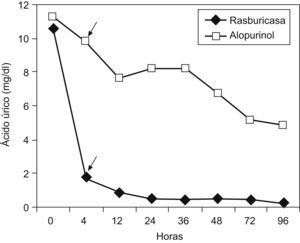
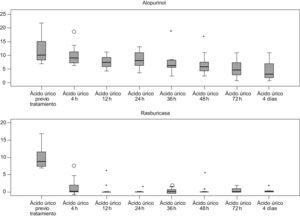
Se observó una disminución progresiva de los niveles de ácido úrico en los 2 grupos, si bien en el grupo tratado con alopurinol no se consiguieron cifras normales estables (<7mg/dl) hasta las 48h de tratamiento. En el grupo tratado con rasburicasa se observó una disminución más rápida y llamativa de las cifras de uricemia por debajo de la normalidad desde la primera dosis, y se mantuvo durante todo el tiempo analizado. Al partir de una cifra similar media de ácido úrico plasmático previo al tratamiento (11,3mg/dl en el grupo A y 10,6mg/dl en el grupo B) a las 4h del inicio de éste, encontramos niveles menores de ácido úrico en los niños en los que se administró rasburicasa comparado con los que recibieron alopurinol; esta diferencia fue estadísticamente significativa (p<0,001). Este hecho se repitió en el resto de las determinaciones seriadas realizadas en el tiempo, con resultados estadísticamente significativos (tabla 1, figs. 1 y 2). En la tabla 1 se reflejan los valores medios, la desviación estándar y el límite inferior y superior para el intervalo de confianza del 95%.
Valores medios, desviación estándar, límite inferior y límite superior con intervalo de confianza para la media del 95% de ácido úrico plasmático (mg/dl) así como significación estadística
| 0h | 4h | 12h | 24h | 36h | 48h | 72h | 96h | ||
| Alopurinol | Media | 11,3 | 9,8 | 7,6 | 8,2 | 8,2 | 6,7 | 5,1 | 4,8 |
| DE | 5,8 | 3,5 | 2,2 | 2,8 | 5,5 | 3,9 | 3,2 | 3,6 | |
| LI | 8,3 | 7,6 | 6,1 | 6,7 | 4,5 | 4,2 | 2,8 | 2,1 | |
| LS | 14,5 | 12,1 | 9,2 | 9,9 | 11,9 | 6,7 | 7,4 | 7,6 | |
| Rasburicasa | Media | 10,6 | 1,8 | 0,8 | 0,5 | 0,4 | 0,5 | 0,4 | 0,2 |
| DE | 3,2 | 3,1 | 2,2 | 1,7 | 0,7 | 1,5 | 0,7 | 0,6 | |
| LI | 8,30 | 0,5 | 0,52 | 0,5 | 0,4 | 0,3 | 0,1 | 0,2 | |
| LS | 13,7 | 4,1 | 2,2 | 1,5 | 0,9 | 1,3 | 0,8 | 0,7 | |
| Valor de p¿ | 0,61 | 0,000 | 0,002 | 0,000 | 0,000 | 0,000 | 0,001 | 0,003 |
DE: desviación estándar; LI: límite inferior; LS: límite superior.
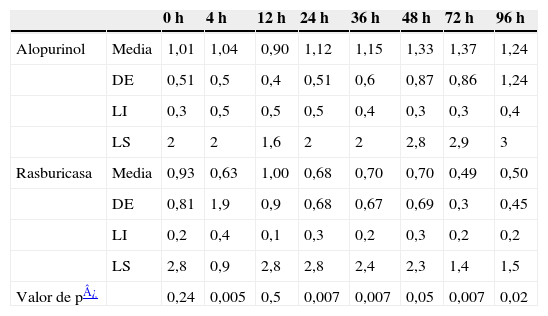
Las cifras de creatinina fueron menores en el grupo B que en el grupo A, con valores estadísticamente significativos a las 4, 24, 36, 72 y 96h. Los valores de fósforo plasmáticos se mantuvieron similares en ambos grupos, sin diferencias estadísticamente significativas. En las tablas 2 y 3 se representan las cifras medias, la desviación estándar y el límite inferior y superior de creatinina y fósforo plasmáticos en ambos grupos de estudio.
Valores medios, desviación estándar, límite inferior y límite superior con intervalo de confianza para la media del 95% de creatinina sérica (mg/dl) así como significación estadística
| 0h | 4h | 12h | 24h | 36h | 48h | 72h | 96h | ||
| Alopurinol | Media | 1,01 | 1,04 | 0,90 | 1,12 | 1,15 | 1,33 | 1,37 | 1,24 |
| DE | 0,51 | 0,5 | 0,4 | 0,51 | 0,6 | 0,87 | 0,86 | 1,24 | |
| LI | 0,3 | 0,5 | 0,5 | 0,5 | 0,4 | 0,3 | 0,3 | 0,4 | |
| LS | 2 | 2 | 1,6 | 2 | 2 | 2,8 | 2,9 | 3 | |
| Rasburicasa | Media | 0,93 | 0,63 | 1,00 | 0,68 | 0,70 | 0,70 | 0,49 | 0,50 |
| DE | 0,81 | 1,9 | 0,9 | 0,68 | 0,67 | 0,69 | 0,3 | 0,45 | |
| LI | 0,2 | 0,4 | 0,1 | 0,3 | 0,2 | 0,3 | 0,2 | 0,2 | |
| LS | 2,8 | 0,9 | 2,8 | 2,8 | 2,4 | 2,3 | 1,4 | 1,5 | |
| Valor de p¿ | 0,24 | 0,005 | 0,5 | 0,007 | 0,007 | 0,05 | 0,007 | 0,02 |
DE: desviación estándar; LI: límite inferior; LS: límite superior.
Niveles basales (0h), 4, 12, 24, 36, 48, 72 y 96h en los 2 grupos de estudio.
Valores medios, desviación estándar, límite inferior y límite superior con intervalo de confianza para la media del 95% de fósforo sérico (mg/dl) así como significación estadística
| 0h | 4h | 12h | 24h | 36h | 48h | 72h | 96h | ||
| Alopurinol | Media | 6,72 | 6,2 | 6,2 | 7,3 | 5,7 | 5,6 | 4,3 | 3,8 |
| DE | 5,02 | 4,2 | 3,97 | 4,5 | 1,95 | 1,97 | 2,22 | 1,4 | |
| LI | 1,0 | 2,7 | 3 | 3,5 | 3,3 | 3,2 | 2,3 | 2,2 | |
| LS | 18,0 | 17,8 | 16,8 | 19 | 9,5 | 9,8 | 10 | 6,6 | |
| Rasburicasa | Media | 6,28 | 5,06 | 5,44 | 6,00 | 5,5 | 5,43 | 4,36 | 4,79 |
| DE | 2,29 | 1,9 | 1,59 | 2,5 | 1,8 | 1,57 | 1,21 | 1,1 | |
| LI | 3,5 | 3,4 | 2,8 | 2,7 | 3,1 | 3,5 | 2,6 | 3,4 | |
| LS | 10,2 | 7,8 | 7,3 | 11,2 | 10,1 | 8,2 | 6,5 | 6,2 | |
| Valor de p¿ | 0,5 | 0,8 | 0,9 | 0,5 | 0,8 | 0,9 | 0,7 | 0,14 |
DE: desviación estándar; LI: límite inferior; LS: límite superior.
Niveles basales (0h), 4, 12, 24, 36, 48, 72 y 96h en los 2 grupos de estudio.
En el 56% de los pacientes tratados con alopurinol se realizó hemodiálisis debido a insuficiencia renal o a oligoanuria, mientras que ninguno de los pacientes tratados con rasburicasa precisó hemodiálisis u otra técnica de depuración extrarrenal (p<0,02).
La estancia media en la UCI-P para el grupo A y B fue de 5 y 2,5 días, respectivamente, y la duración media del tratamiento fue de 5,7 días para el grupo tratado con alopurinol y de 3,6 días para el grupo tratado con rasburicasa.
No se observó ningún efecto secundario a los fármacos en los 2 grupos de estudio.
Dos de los 16 pacientes (12,5%) tratados con alopurinol fallecieron durante el tratamiento (el primero a consecuencia de un cuadro de fracaso multiorgánico y el segundo por una arritmia grave secundaria a hiperpotasemia). No se produjo ningún fallecimiento en el grupo de pacientes tratados con rasburicasa.
DiscusiónLa rasburicasa es un agente uricolítico muy seguro y altamente efectivo en el tratamiento de la hiperuricemia secundaria al SLT en pacientes con leucemia o linfoma, incluyendo pacientes pediátricos con extrema hiperleucocitosis9–11. El uso de esta enzima recombinante en pacientes pediátricos se aprobó en Europa en el 2001 y en Norteamérica en el 200212. Aunque hay escasas publicaciones en pacientes pediátricos, los resultados de los estudios que comparan la eficacia y la seguridad de rasburicasa frente al alopurinol han demostrado que en los pacientes que recibieron rasburicasa se consigue un control más rápido y unos niveles inferiores de ácido úrico plasmático5.
Los resultados de este estudio apoyan la eficacia de este fármaco, en consonancia con otros estudios realizados en Estados Unidos que muestran una eficacia del 98% en pacientes oncológicos pediátricos con hiperuricemia14 y otro estudio multicéntrico que muestra un 100% de eficacia en adultos y niños13.
Pui et al9 realizaron un estudio fase i/ii y evaluaron la seguridad y la eficacia de rasburicasa en 131 pacientes menores de 20 años con enfermedad oncohematológica y riesgo de desarrollar hiperuricemia. Se administró rasburicasa entre 5 y 7 días, y se inició la quimioterapia 4h tras la administración de ésta. En todos los pacientes que presentaron hiperuricemia se observó una importante disminución de los niveles de ácido úrico (desde 9,7mg/dl previo al inicio del estudio hasta 1,0mg/dl después del tratamiento). Asimismo, se observó una disminución de los niveles de fosfato sérico en las primeras 48h de tratamiento y de creatinina sérica en las primeras 24h. Ninguno de los pacientes del estudio precisó diálisis ni presentó complicaciones graves del SLT ni efectos adversos secundarios al tratamiento.
En un estudio multicéntrico aleatorizado realizado por Goldman et al5 se comparó el tratamiento con rasburicasa y alopurinol en 52 pacientes pediátricos con linfoma y leucemia con alto riesgo de desarrollar un SLT. Los valores medios de uricemia previos al inicio del estudio eran similares en los 2 grupos. Como resultados, obtuvieron que el área media bajo la curva para los niveles de ácido úrico era significativamente inferior en el grupo tratado con rasburicasa comparado con el otro grupo. A las 4h de la primera dosis del fármaco, los niveles de uricemia se redujeron un 86% en el grupo de rasburicasa, mientras que en el grupo de alopurinol sólo se observó una disminución del 12%. Se observó también una disminución de los niveles de creatinina sérica en el grupo de rasburicasa.
Estos mismos resultados se han obtenido en un estudio realizado para evaluar la eficacia y la seguridad de rasburicasa en pacientes adultos con LNH. Se observó una disminución de los niveles de ácido úrico a las 4h de la dosis inicial de rasburicasa así como un mantenimiento de los niveles normales de creatinina sérica. Ninguno de los 100 pacientes incluidos en el estudio requirió diálisis15.
Estos resultados son similares a los encontrados en nuestros pacientes, en los que el 100% de los tratados con rasburicasa tuvo una reducción muy significativa de las cifras de ácido úrico desde la primera dosis administrada, que se mantuvo durante todos los días de estudio. Sin embargo, los pacientes tratados con alopurinol necesitaron 48h hasta obtener cifras estables de ácido úrico por debajo de 8mg/dl. Debemos destacar el descenso tan llamativo de la uricemia que se produce a las 4h del inicio del tratamiento con rasburicasa en comparación con el otro grupo de estudio, dato que coincide con lo publicado recientemente en la literatura médica.
Otros trabajos publicados obtienen resultados en la misma línea, y se confirma la superioridad de rasburicasa sobre alopurinol en el tratamiento y la profilaxis de la hiperuricemia en niños y adultos con enfermedad tumoral12,16–18.
En algunos estudios se ha observado una reducción significativa de los niveles de fósforo y creatinina plasmáticos tras el tratamiento con rasburicasa1,10–12. En el estudio realizado por Goldman et al se observó en los pacientes que recibieron tratamiento con rasburicasa una mejoría de los niveles ajustados de creatinina entre el primer y el cuarto día de tratamiento, hecho que no se observó en el grupo de pacientes hiperuricémicos tratados con alopurinol. Estos hallazgos indican que el control más rápido de la uricemia podría traducirse en una mejor función renal durante la quimioterapia en pacientes tratados con rasburicasa5.
La hiperfosfatemia es la segunda causa de fallo renal agudo en el SLT. La rasburicasa no puede prevenir las complicaciones secundarias a la hiperfosfatemia, sin embargo, en algunos estudios se ha comprobado que al mejorar la función renal y al disminuir la precipitación de ácido úrico y sus precursores en los túbulos renales, se podría facilitar también la excreción de fósforo9,10,12. En nuestro estudio las cifras de creatinina son inferiores en el grupo de rasburicasa, con valores estadísticamente significativos a las 4, 24, 36, 72 y 96h; sin embargo, no se encontraron diferencias en las cifras plasmáticas de fósforo entre los 2 grupos. Son necesarios más estudios y pacientes para determinar si el control más rápido y la reducción de la uricemia secundarios al tratamiento con rasburicasa implican una disminución de las complicaciones metabólicas, de la morbilidad asociada al SLT y de la necesidad de técnicas de depuración extrarrenal en estos pacientes5.
Según algunos estudios recientes, la necesidad de hemodiálisis en pacientes con enfermedad oncohematológica tratados con rasburicasa oscila entre un 0,4 y un 1,7% comparado con el 20% en pacientes que reciben alopurinol9,19. Ninguno de los pacientes de este estudio tratados con rasburicasa necesitó hemodiálisis frente al 56% (9 de 16 pacientes) de los tratados con alopurinol (p<0,02).
Las últimas recomendaciones publicadas para la administración de rasburicasa aconsejan una dosis de 0,15–0,20mg/kg una vez al día en una infusión intravenosa de 30min con una duración del tratamiento de 5 días. Sin embargo, en algunos ensayos clínicos la rasburicasa ha demostrado ser eficaz a dosis inferiores y con menos días de tratamiento. Es muy importante monitorizar regularmente los niveles de ácido úrico y usarlos como guía para modular la dosis de rasburicasa6.
La rasburicasa es un fármaco bastante más costoso que el alopurinol. El coste medio de tratamiento diario con rasburicasa para un paciente de unos 70kg es de 560 euros. Numerosos estudios actuales publicados evalúan dosis y pautas alternativas de rasburicasa que mantengan la misma efectividad y reduzcan su coste19. Estudios realizados mayoritariamente en pacientes adultos avalan la efectividad de una dosis única de rasburicasa para el tratamiento de la hiperuricemia asociada al SLT20–27. En la población pediátrica existen algunos trabajos sobre el uso de dosis única de rasburicasa, aunque aún son escasos para poder llegar a conclusiones sólidas25,28. La rasburicasa es efectiva en pacientes con hiperuricemia previa a la quimioterapia, pero las cifras normalizadas de ácido úrico pueden reelevarse una vez iniciada ésta, por esto, en pacientes con alto riesgo de desarrollar SLT tras iniciar el tratamiento quimioterapéutico son necesarios una estrecha monitorización de los niveles de ácido úrico y un tratamiento continuo con rasburicasa1.
A pesar de ser un fármaco costoso, el tratamiento con rasburicasa se ha relacionado con una menor necesidad de técnicas de depuración extrarrenal y una reducción de los días necesarios de estancia en cuidados intensivos y de hospitalización, por lo que ofrece una buena relación coste-efectividad19. En nuestro estudio ambos grupos realizaron similares días de tratamiento, pero los que recibieron rasburicasa precisaron menos días de ingreso en la UCIP-P que los tratados con alopurinol (2,5 días en el primer grupo frente a 5 días en el segundo).
En décadas pasadas, antes de disponer de rasburicasa, se empleaba para el tratamiento de la hiperuricemia la forma no recombinante de urato oxidasa (uricozyme). Esta enzima poseía también una alta actividad uricolítica, pero su uso se asoció a reacciones de hipersensibilidad en un 4,5% de los pacientes10. El uso de la forma recombinante de urato oxidasa ha supuesto una gran mejoría en este aspecto y se han observado menos reacciones alérgicas o de hipersensibilidad, hecho que se pone de manifiesto en numerosos estudios1,5,9. La rasburicasa está contraindicada en pacientes con déficit de glucosa 6-fosfato-deshidrogenasa, ya que puede inducir anemia hemolítica o metahemoglobinemia1. En ningún paciente de este estudio tratado con rasburicasa se observó hemólisis, metahemoglobinemia ni reacciones de hipersensibilidad.
A pesar de las limitaciones de este estudio, comprobamos que la rasburicasa es un fármaco seguro y efectivo para el tratamiento de la hiperuricemia en niños con SLT o alto riesgo de desarrollarlo. Comparada con el alopurinol, consigue un control más rápido y un descenso más llamativo de los niveles de ácido úrico plasmáticos. Los pacientes tratados con rasburicasa tienen menor necesidad de técnicas de depuración extrarrenal que aquellos que recibieron alopurinol, necesitaron menos días de ingreso en la UCI-P y tuvieron menor mortalidad, si bien sería necesario un estudio aleatorizado con muestra poblacional más amplia para corroborar estas conclusiones.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.