Los niños son la mayor fuente de transmisión y el principal reservorio del virus de la gripe. Se estima que el control del virus es peor en la población pediátrica, y que por lo tanto el período de eliminación del virus es mayor en este grupo en comparación con otras edades1. El objeto del presente estudio fue analizar la cinética y aclaramiento del virus de la gripe A (H1N1)pdm09 en niños hospitalizados y establecer su asociación con distintas variables clínicas.
Estudio prospectivo observacional realizado en los servicios de pediatría y microbiología de dos hospitales en Valladolid y el Centro Nacional de Gripe de Valladolid. El período de estudio fue desde la semana 40 del 2015 a la semana 20 del 2016, correspondiente a la temporada gripal 2015-2016. Se incluyeron pacientes hospitalizados menores de 14 años con infección por virus de la gripe A(H1N1)pdm09 confirmada por laboratorio. Para dicho diagnóstico, se obtuvieron muestras de frotis faríngeo en pacientes mayores de dos años y muestras de lavado nasofaríngeo en pacientes menores. El uso de este último método permite la obtención de una muestra más representativa, aunque también podría sobreestimar la carga de ARN viral (CAV) en este grupo de pacientes. Para analizar la CAV se recogieron muestras el día del ingreso y a los cuatro, ocho y 12 días de ingreso o hasta que el resultado fue negativo, de ocurrir antes de los 12 días. Las variables del estudio incluyeron el tiempo de evolución desde el inicio de los síntomas, el número de excretores a largo plazo (ELP, definido como aquellos pacientes con períodos de excreción viral [EV] mayores de ocho días desde el inicio), y el número de excretores a corto plazo (ECP, definido como aquellos pacientes con EV menor a ocho días). Se obtuvo consentimiento informado por escrito de los padres o tutores legales de cada participante.
La infección por virus de la gripe A(H1N1)pdm09 se confirmó por reacción en cadena de la polimerasa en transcripción reversa (RT-PCR) en tiempo real con reactivos MAGPIX y NxTAG-RPP (Luminex; Austin, Tejas, EE. UU.). La EV se midió por qRT-PCR en muestras positivas para el virus de la gripe con el sistema 7500 Fast de RT-PCR (Applied Biosystems; Foster City, California, EE. UU.) y reactivos LightMix-Kit Influenza A Virus M2 (Roche; Basilea, Suiza). En todos los pacientes se empleó el kit de reactivos Allplex Respiratory Full Panel (Seegene), que puede detectar 19 dianas virales y siete bacterianas, incluyendo los genes M2 y H de las principales cepas endémicas circulantes en España. El análisis estadístico se centró en la comparación de distintas variables clínicas y su asociación con la duración de la EV. Se empleó el software SPSS versión 20.0 para las pruebas estadísticas.
Durante el período de estudio se reclutó a 24 pacientes (54% varones; edad mediana: 17,5 meses; rango de edad: 0-120 meses). Las únicas comorbilidades fueron el asma grave y la fibrosis quística detectadas en dos pacientes (8%), que fueron los únicos que habían recibido la vacuna de la gripe. Las CAV más altas se encontraron en las muestras obtenidas el día del ingreso, correspondiendo a la CAV máxima en el 87,5% de los pacientes (CV1 media: 7032,9 copias/mL; intervalo de confianza [IC] 95%: 1131,2-16 418,5), observándose valores menores en la segunda muestra (CV2 media: 239,5 copias/mL; IC 95%: 51,4-547,9). Los resultados de la tercera muestra fueron negativos en todos los pacientes. El 50% de los pacientes (12/24) fueron ELP. La estancia hospitalaria media fue de 7,4 días (IC 95%: 5,1-9,9) en el grupo de pacientes ELP, en comparación con 5,6 días (IC 95%: 3,4-8,0) en el grupo de ECP, sin diferencias estadísticamente significativas (t de Student, p = 0,294) (tabla 1).
Características demográficas y clínicas de los 24 pacientes pediátricos hospitalizados con infección por virus de la gripe
| Código de paciente | Sexo | Edad(meses) | CAV1(copias/mL) | CAV2(copias/mL) | Eliminación | Confección | Días de evolución | Estancia hospitalaria (días) | Ingreso en UCIP | Tratamiento |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | F | 17 | 3280 | 14 | ELP | Bacteriana(MC) | 1 | 5 | No | AC |
| 2 | F | 16 | 6240 | ID | ECP | No | 4 | 9 | No | ACOseltamivir |
| 3 | M | 14 | 246 | 2900 | ELP | Bacteriana (SP, HI) | 3 | 5 | No | AC |
| 4 | F | 4 | 89 200 | ID | ECP | No | 2 | 2 | No | C |
| 5 | F | 48 | 11 400 | 811 | ELP | No | 21 | 6 | Yes | Sin ATB/AV |
| 6 | F | 7 | 489 | 823 | ELP | Bacteriana (MC) | 4 | 7 | No | C |
| 7 | F | 48 | 781 | 16 | ELP | No | 1 | 6 | No | C + V |
| 8 | M | 26 | 1330 | 32 | ELP | Viral (B) | 5 | 7 | Yes | AZT |
| 9 | F | 15 | 27 | ID | ECP | Viral (A) | 1 | 4 | No | C |
| 10 | F | 0 | 27 | ID | ECP | Viral (VRS) | 2 | 13 | Yes | AMP + G |
| 11 | M | 12 | 41 800 | ID | ECP | No | 2 | 1 | No | Sin ATB/AV |
| 12 | M | 18 | 53 | ID | ELP | Viral (B) | 5 | 1 | No | AC |
| 13 | M | 35 | 17 | ID | ECP | No | 1 | 10 | No | AC |
| 14 | M | 18 | 651 | 720 | ELP | No | 8 | 8 | Yes | C + AZT |
| 15 | M | 48 | 7540 | ID | ECP | No | 1 | 5 | Yes | Sin ATB/AV |
| 16 | M | 0 | 749 | 309 | ELP | Bacteriana(MC) | 1 | 10 | No | AC |
| 17 | M | 0 | 267 | 48 | ELP | Bacteriana(SA) | 1 | 15 | No | AC |
| 18 | M | 48 | 22 | ID | ELP | No | 7 | 6 | No | Sin ATB/AV |
| 19 | M | 120 | 3100 | ID | ECP | No | 1 | 5 | No | C Oseltamivir |
| 20 | M | 13 | 86 | ID | ECP | Viral(B, VRS) | 7 | 5 | No | AC |
| 21 | M | 84 | 359 | ID | ECP | No | 3 | 3 | No | Oseltamivir |
| 22 | F | 108 | 832 | ID | ECP | No | 1 | 9 | No | AMP |
| 23 | F | 48 | 252 | 76 | ELP | No | 6 | 16 | Yes | AMP + COseltamivir |
| 24 | F | 1 | 42 | ID | ECP | Bacteriana(MC) | 1 | 1 | No | AC |
A: adenovirus; AC: amoxicilina-ácido clavulánico; AMP: ampicilina; ATB/AV: antibiótico/antiviral; AZT: azitromicina; B: bocavirus; C: cefotaxima; CAV1: carga de ARN viral RNA en la muestra inicial; CAV2: carga de ARN viral RNA en la segunda muestra; ECP: excretor a corto plazo; ELP: excretor a largo plazo; F: femenino; G: gentamicina; HI: Haemophilus influenzae; ID: indetectable; M: masculino; MC:, Moraxella catarrhalis; SA: Staphylococcus aureus; SP: Streptococcus pneumoniae; UCIP: Unidad de Cuidados Intensivos Pediátricos; V: vancomicina; VRS: virus respiratorio sincitial.
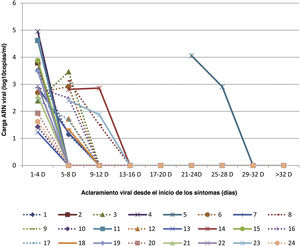
La CAV se volvió indetectable de nueve a 12 días tras el inicio en el 67% de los pacientes (8/12) ELP, de 13 a 16 días en el 25% (3/12) y tras 12 días en el 8% (1/12) (fig. 1). Se detectó coinfección viral o bacteriana con el virus de la gripe en el 58,3% (7/12) de los pacientes ELP (bacteriana en cinco y viral en dos). Seis pacientes requirieron ingreso en la Unidad de Cuidados Intensivos Pediátricos (UCIP), de los que cuatro fueron ELP, los cuales requirieron soporte respiratorio con ventilación no ventilación no invasiva (VNI), y ninguno requirió soporte vasoactivo. Se detectó coinfección viral o bacteriana en el 45,8% de los pacientes (11/24), bacteriana en el 54,5% (6/11) (por Moraxella catarrhalis, Streptococcus pneumoniae, Staphylococcus aureus y Haemophilus influenzae), y viral en el 45,5% (5/11) (por bocavirus, virus respiratorio sincitial y adenovirus). No se observaron diferencias significativas en la CAV detectada en la primera muestra (t de Student, p = 0,180) o en la segunda (t de Student, p = 0,059) entre los ELP y los ECP. El abordaje fue similar en ambos grupos de pacientes: tratamiento sintomático en el 100%, antibioterapia en el 79% (tabla 1), broncodilatadores en el 54%, soporte respiratorio en el 50% (VNI en el 33%). Solo se administró oseltamivir a cuatro pacientes que desarrollaron clínica neurológica, todos ellos en el grupo de ECP.
Los datos del estudio muestran que la mitad de los pacientes pediátricos con infección por virus de la gripe A(H1N1)pdm09 confirmada por laboratorio tenían una CAV detectable pasados ocho días del inicio de los síntomas, y que el 17% tenía CAV detectables en el día 12. Los pacientes con un tiempo de evolución mayor tuvieron períodos de eliminación más largos, aunque la estancia hospitalaria fue similar en ambos grupos. Esto podría apuntar a un peor control del aclaramiento viral en los pacientes ELP en comparación con los ECP, lo que se asociaría a una mayor duración de la clínica respiratoria, pero no al tiempo de ingreso requerido por los pacientes.
Por lo general, la población pediátrica tiene períodos de excreción viral más largos en las infecciones por virus de la gripe en comparación con la adulta2. Esto se ha relacionado con la inmadurez de su sistema inmune, los antecedentes de inmunosupresión, la necesidad de ingreso en la UCIP o la infección por cepas de la gripe resistentes a antivirales3,4. También se ha documentado una frecuencia considerable de coinfección viral o bacteriana en pacientes con infección por virus de la gripe y eliminación prolongada, lo que podría asociarse a mayor gravedad y una mayor frecuencia de ingreso hospitalario5. En nuestra cohorte se observó que la mayoría de los pacientes ingresados en la UCIP o con coinfección bacteriana fueron ELP. No obstante, no se detectó una correlación significativa entre la condición de ELP y el ingreso en la UCIP o la coinfección bacteriana, lo que podría explicarse por el tamaño reducido de la muestra.
En conclusión, nuestros datos muestran que la mitad de los pacientes pediátricos con infección por virus de la gripe A(H1N1)pdm09 confirmada por laboratorio son ELP, y que la mayoría de los que requirieren cuidados intensivos o con coinfección bacteriana también son ELP. La monitorización de los cambios en la CAV en pacientes pediátricos hospitalizados podría utilizarse para predecir la gravedad de la enfermedad e identificar casos en los que es necesario realizar pruebas microbiológicas adicionales.
FinanciaciónEstudio financiado por la Gerencia Regional de Salud de Castilla y León, según Resolución de 27 de febrero de 2015, del Director Gerente de la Gerencia Regional de Salud de Castilla y León, por la que se establecen las modalidades, el procedimiento y los criterios de selección de los Proyectos de Investigación en Biomedicina a desarrollar en los Centros de la Gerencia Regional de Salud de Castilla y León (expediente GRS 1094/A/15).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este trabajo se ha presentado previamente en forma de comunicación oral en el 67 Congreso de la Asociación Española de Pediatría, celebrado en Burgos, España, entre el 6 y 8 de junio de 2019.