Introducción
La fibrosis quística de páncreas es una enfermedad autosómica recesiva, multiorgánica que se presenta con una gran variedad de síntomas: infecciones pulmonares de repetición, malabsorción digestiva e insuficiencia pancreática, cirrosis hepática, diabetes, etc. 1. En las últimas décadas la supervivencia de las diferentes cohortes ha mejorado progresivamente. En el registro Holandés, mientras que solamente el 6 % de los nacidos en la cohorte de 1950-1954 llegaba a los 30 años, el 36 % de los nacidos en los años 1970-1973 ha sobrepasado la edad de 30 años 2. Este cambio en la historia natural de la enfermedad está modificando el espectro de sus manifestaciones clínicas y ha conducido a un aumento de la prevalencia de complicaciones como la diabetes y la nefrolitiasis 3.
Observación clínica
Mujer de 14 años, diagnosticada de fibrosis quística en el período neonatal tras presentar un íleo meconial. Genotipo ΔF508 homozigoto. Afectación respiratoria leve: volumen espiratorio forzado en el primer segundo (FEV1) óptima en el año previo del 86 %. Insuficiencia pancreática en tratamiento sustitutivo con enzimas pancreáticas (Kreon® 10.000 U, 16-20 cáps./día) y suplementos vitamínicos (Rochevit® 2 cáps./día, 200 mg/día de vitamina C). Seguía una dieta hipercalórica e hiperproteica. Seguía también tratamiento continuo inhalado, dos veces al día, con colimicina 1.000.000 U y tobramicina 100 mg. A lo largo de la evolución había presentado varios episodios de seudooclusión intestinal. Tenía 11,4 g/día de grasa en heces en el último Van de Kamer realizado. Consulta por un episodio de dolor intenso de tipo cólico, localizado en el costado izquierdo, acompañado de vómitos y hematuria microscópica aislada. Diuresis corregida de 1.790 ml/ 24 h/1,73 m 2. Su función renal era normal (filtrado glomerular estimado de 115 ml/m/1,73 m 2), así como la excreción urinaria de calcio (0,8 mg/kg/día), magnesio (1,8 mg/kg/día), ácido úrico (463 mg/24 h/ 1,73 m 2) y sodio (3 mEq/kg/día). En la orina de 24 h se detectó hiperoxaluria: 141 mg/24 h/1,73 m 2 (valores normales: 26,3 ± 9 mg/ 24 h/1,73 m 2) y una citraturia de 3,7 mg/kg/24 h, en el rango bajo de la normalidad para nuestra población (valores normales 9,62 ± 4 mg/kg/ 24 h) 4,5. No existían antecedentes familiares de litiasis renal.
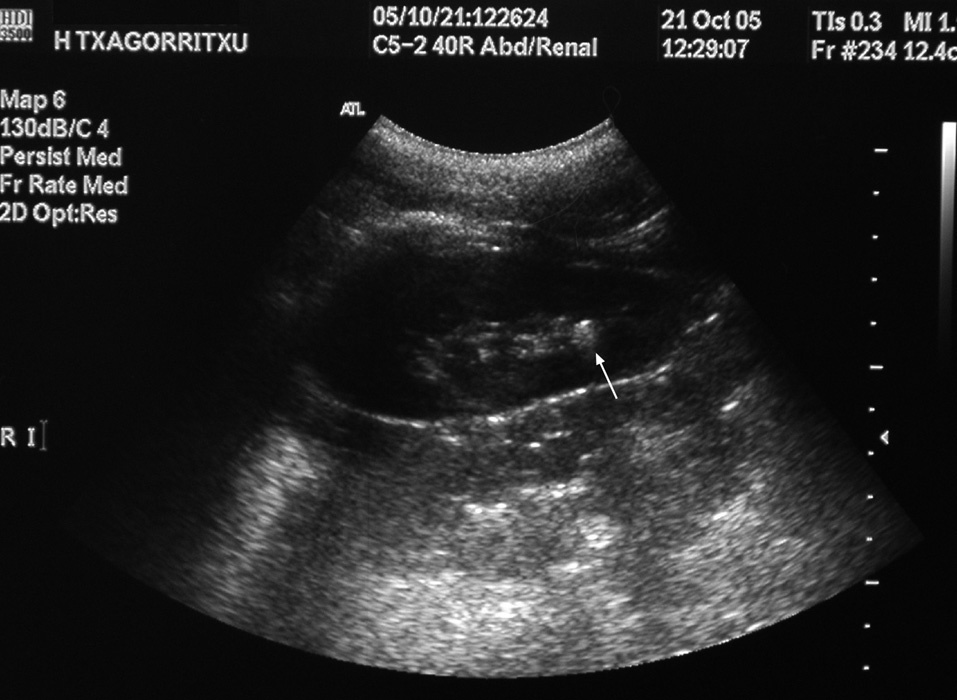
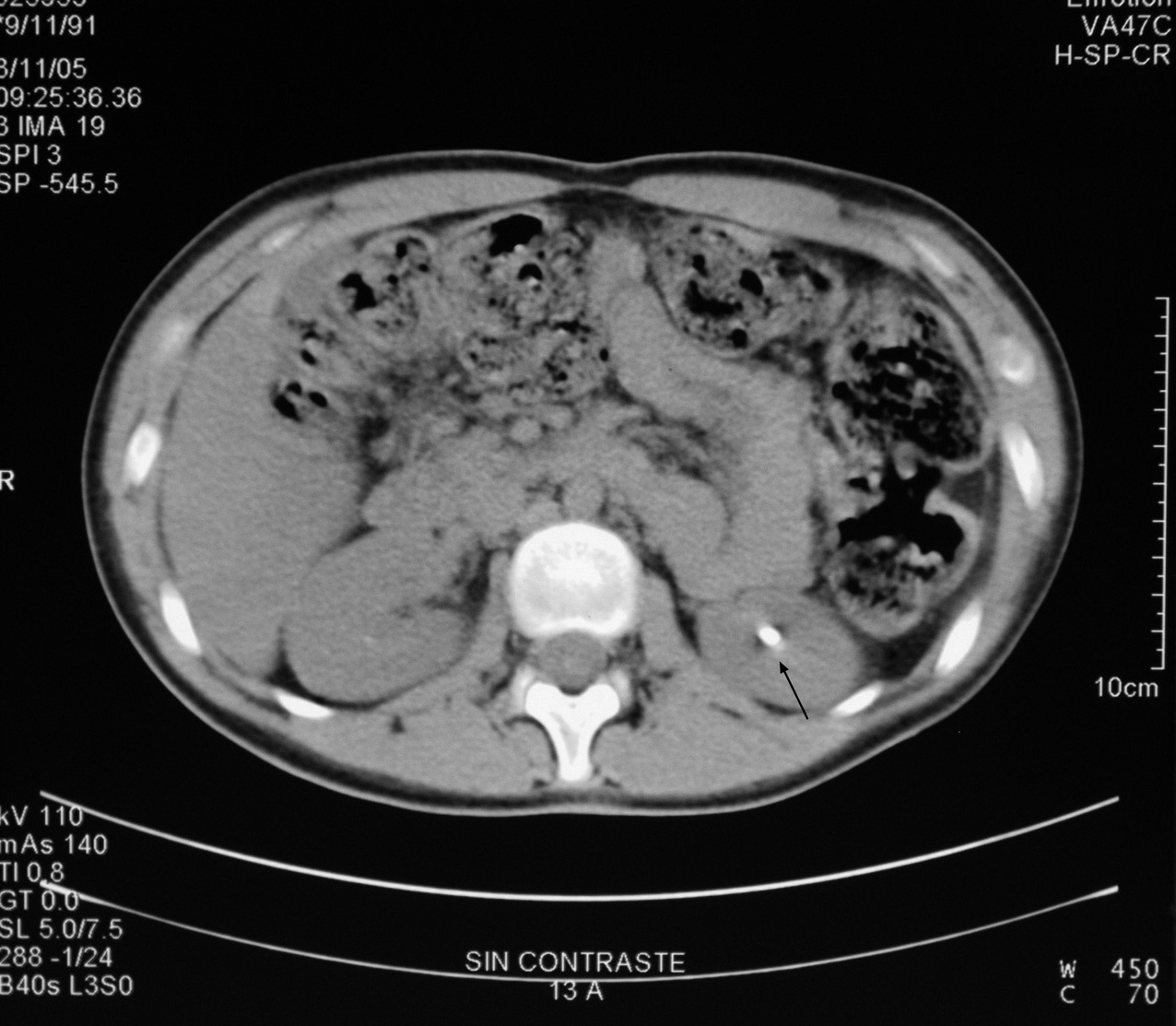
En la ecografía renal, se observaron imágenes con sombra acústica en ambos riñones y en la tomografía computarizada (TC) helicoidal 2 cálculos radioopacos en los grupos caliciales superior e inferior del riñón derecho, y otro más situado en el grupo calicial inferior del riñón izquierdo, excluyéndose la dilatación de la vía urinaria y la presencia de cálculos ureterales (figs. 1 y 2).
Figura 1. Ecografía renal: cálculo en grupo calicial inferior del riñón izquierdo (flecha color blanco).
Figura 2.TC helicoidal sin contraste intravenoso. Cálculo en grupo calicial inferior del riñón izquierdo (flecha color negro).
Discusión
Estudios epidemiológicos han demostrado el alto riesgo de padecer nefrolitiasis que tienen los pacientes con fibrosis quística, encontrándose incidencias de nefrocalcinosis en un porcentaje tan alto como el 92 % en necropsias de estos pacientes, porcentaje mucho más elevado que en la población general 6. Esta complicación no ha sido comunicada como una manifestación clínica habitual en niños afectados de fibrosis quística, pero se estima su prevalencia entre el 3 al 5 %, indudablemente mucho más alta que el 0,2 % estimado en la edad pediátrica 7.
El mecanismo responsable de la litogénesis en estos pacientes no está completamente establecido, pero los datos de excreción urinaria de sustancias, tanto favorecedoras como inhibidoras de la formación de cálculos, demuestran que la hiperoxaluria es el factor de riesgo más importante para desarrollar litiasis en los pacientes con fibrosis quística 8,9.
La hiperoxaluria entérica, producida por la insuficiencia pancreática y la malabsorción, se observa con frecuencia en pacientes con enfermedad inflamatoria intestinal, resecciones ileales, bypass yeyuno-ileal y fibrosis quística. La esteatorrea favorece la unión del calcio con las sales biliares en vez de hacerlo con el oxalato con el que forma un complejo insoluble y no reabsorbible. Por eso, una mayor cantidad de oxalato soluble está disponible para ser reabsorbido en el colon. Por otra parte, este mecanismo se vería favorecido por el aumento de la permeabilidad para el oxalato, que en el colon distal produce la malabsorción de las sales biliares. El tratamiento con enzimas pancreáticas no es capaz de controlar totalmente la hiperoxaluria; el mal cumplimiento del mismo, hace aumentar el nivel de oxalato en orina, siendo un hecho demostrado que el número de pacientes hiperoxalúricos, aumenta con la edad (33 % en niños pequeños frente a 42 % en adolescentes) 9.
Existe un tercer mecanismo para explicar la hiperoxaluria en pacientes con fibrosis quística: la pérdida de bacterias intestinales capaces de degradar el oxalato, inducida por el uso frecuente de antibióticos que estos pacientes precisan para controlar sus frecuentes infecciones respiratorias. Normalmente, el 70 % del oxalato que se genera con la dieta, se degrada en el intestino gracias a estas bacterias (fundamentalmente debido a la acción del Oxalobacter formigenes); cuando esta flora disminuye, aumenta la absorción intestinal de oxalato y por tanto la hiperoxaluria y el riesgo de litiasis. La mayoría de pacientes con fibrosis quística carece de colonización por O. formigenes 9.
La hipocitraturia es también un hallazgo frecuente en estos enfermos 8-10. La importancia de la hipocitraturia como factor favorecedor de la formación de cálculos en pacientes con fibrosis quística fue citada por primera vez por Bohles y Michalk 11 en el año 1982. El citrato, un potente inhibidor de la cristalización, actúa formando complejos con el calcio y reduciendo la concentración de calcio iónico en orina además de inhibir directamente la cristalización de oxalato cálcico. Suele estar disminuido por las pérdidas intestinales de bicarbonato y por el alto contenido proteico de la dieta que se suele recomendar. La absorción de álcalis en el intestino se correlaciona directamente con la citraturia en orina 10. Por la gran dispersión de los valores de citrato en la muestra de nuestra población, no podemos hablar de hipocitraturia 5. Sin embargo, su valor de citrato en orina es claramente anormal si tenemos en cuenta otros valores de normalidad referidas en la literatura especializada. El índice citrato/creatinina era de 0,177 y las cifras de normalidad referidas son de 0,51 ± 0,205 y en niños con litiasis la relación es de 0,181 ± 0,076 12. La citraturia en orina de 24 h de 206 mg/24 h /1,73 m 2, cifra por debajo del límite inferior de la normalidad 8. Presentaba un índice de 177 mg de citrato/g de creatinina (hipocitraturia < 400 mg de citrato/g creatinina) 13.
La disminución del volumen urinario favorece la litiasis en pacientes con fibrosis quística 14. Nuestra paciente no refería disminución de la ingesta de líquidos en los días previos al episodio de cólico renal, el tiempo no era caluroso y la diuresis de 24 h era normal. La hipercalciuria y la hipomagnesuria también se citan como factores favorecedores de la nefrolitiasis en los pacientes con fibrosis quística 8. Sin embargo, la mayoría de los pacientes tienen cifras de calcio urinario normales o bajas y esta hipocalciuria puede ser un factor que protege a estos niños de la formación de cálculos 11,15. Teniendo en cuenta que el oxalato es 10 veces más potente que el calcio para aumentar la saturación en orina de oxalato cálcico, un elevado riesgo de cristalización ocurre solamente en presencia de hiperoxaluria 9,15. Nuestra paciente presentaba cifras de magnesio en orina normales y la calciuria era incluso baja.
La hiperuricosuria se ha descrito como causa de litiasis en la fibrosis quística 3,8. El aumento de ácido úrico en orina en la fibrosis quística se ha asociado con la ingesta de altas dosis de enzimas pancreáticas, con el catabolismo aumentado que tienen estos enfermos y con el aumento del estrés oxidativo 16,17. La descripción de las colonopatías distales y las nuevas recomendaciones sobre el uso de enzimas, han disminuido probablemente la importancia de la hiperuricosuria como causa de litiasis en estos pacientes 16,18,19.
Otros mecanismos que pueden favorecer el desarrollo de litiasis como la disfunción renal en el túbulo proximal (ligado a la actividad de la proteína CFTR y a la alteración de los canales del cloro) están todavía en discusión 20.
Del conocimiento de los mecanismos productores de nefrolitiasis en la fibrosis quística, puede concluirse la necesidad de incluir el cólico nefrítico en el diagnóstico diferencial del dolor abdominal en estos pacientes. Es conveniente realizar estudios periódicos, sobre todo en adolescentes, para controlar los factores litogénicos; optimizar el control de la malabsorción intestinal y recomendar medidas dietéticas como alta ingesta de líquidos, dietas bajas en oxalato y altas en calcio y administrar suplementos de citrato, si es necesario.
Correspondencia: Dra. B. Orive Olondriz.
Nefrología Infantil. Servicio de Pediatría.
Hospital Txagorritxu.
José Atxotegi, s/n. 01009 Vitoria. España.
Correo electrónico: borive@htxa.osakidetza.net
Recibido en febrero de 2006.
Aceptado para su publicación en abril de 2006.