Sr. Editor:
La Hipertensión pulmonar persistente (HTPP) del recién nacido es un grave problema con incidencia de 1-2 casos/1.000 recién nacidos y mortalidad asociada del 10-20 %. La terapia con óxido nítrico inhalado ha demostrado su eficacia. Sin embargo existen pacientes que no responden (hasta un 40 %, especialmente en los casos asociados a hernia diafragmática congénita 1) o que se complican con efectos secundarios. Las técnicas de oxigenación con membrana extracorpórea (ECMO, AREC) para casos refractarios no están al alcance de todas las unidades y el traslado en situación crítica es complejo. Como alternativa o tratamiento complementario se plantea el análogo sintético de prostaciclina I2 (Iloprost) vía inhalatoria. Presentamos nuestra experiencia en un caso de HTPP revisando el estado actual sobre esta terapéutica.
Recién nacido de sexo femenino y 3.100 g de peso nacida en otro centro tras cesárea urgente en la semana 39 de gestación por líquido amniótico meconial. Test de Apgar al minuto de 3 y a los 5 min de 5. Intubado a los pocos minutos de vida; se traslada a nuestro centro en la primera media hora de vida. A su llegada a nuestro centro se observó cianosis generalizada y mala ventilación, drenándose neumotórax izquierdo. La radiografía confirma aspiración meconial bilateral. Se realizaron lavados con agente tensioactivo, se administra dexametasona y se inicia soporte inotrópico. Se establecen medidas antihipertensión pulmonar (ventilación agresiva, alcalinización, sedación profunda, etc.). Se inicia óxido nítrico inhalado (NOi) (20 ppm) con buena respuesta inicial y estabilización progresiva en las primeras 48 h. La ecografía cardíaca confirma HTPP (presión en ventrículo derecho 70 mmHg). En días posteriores presenta empeoramiento favorecido por un proceso infeccioso. Se aumenta el NOi a 40 ppm con elevación de metahemoglobina. Al sexto día, dada la gravedad del caso (índice de oxigenación [IO] 30) ante la imposibilidad de traslado a centro dotado de oxigenación por membrana extracorpórea (ECMO), se decide solicitar la administración como uso compasivo del análogo de prostaciclina I2 (iloprost, Ilomedin® solución 50 μg/0,5 ml) por vía inhalatoria. Se solicita consentimiento familiar. Se administran 200 ng/cada 4 h. Se mantiene la administración de NOi. De modo inmediato se produce un descenso en el IO y aumento de la presión arterial de oxígeno (fig. 1). Las cifras de presión arterial pulmonar descienden tras las dos primeras dosis (40 mmHg). Se reduce progresivamente el soporte respiratorio y hemodinámico (fig. 2). La administración de iloprost se espacia cada 6-8 h. El NOi se retira al octavo día de tratamiento sin rebote. Tras la extubación, iloprost se administra en nebulización (14 días de tratamiento total). La paciente es dada de alta a los 27 días de vida sin dependencia de oxigenoterapia. El seguimiento clínico a los 6 meses muestra ausencia de problemas respiratorios. La ecografía cerebral al alta mostraba discretas lesiones de leucomalacia a nivel frontal confirmadas posteriormente en la RM craneal. En el seguimiento neurológico la paciente presenta una afectación motora de extremidades superiores por lo que actualmente está en un programa de rehabilitación y estimulación precoz.
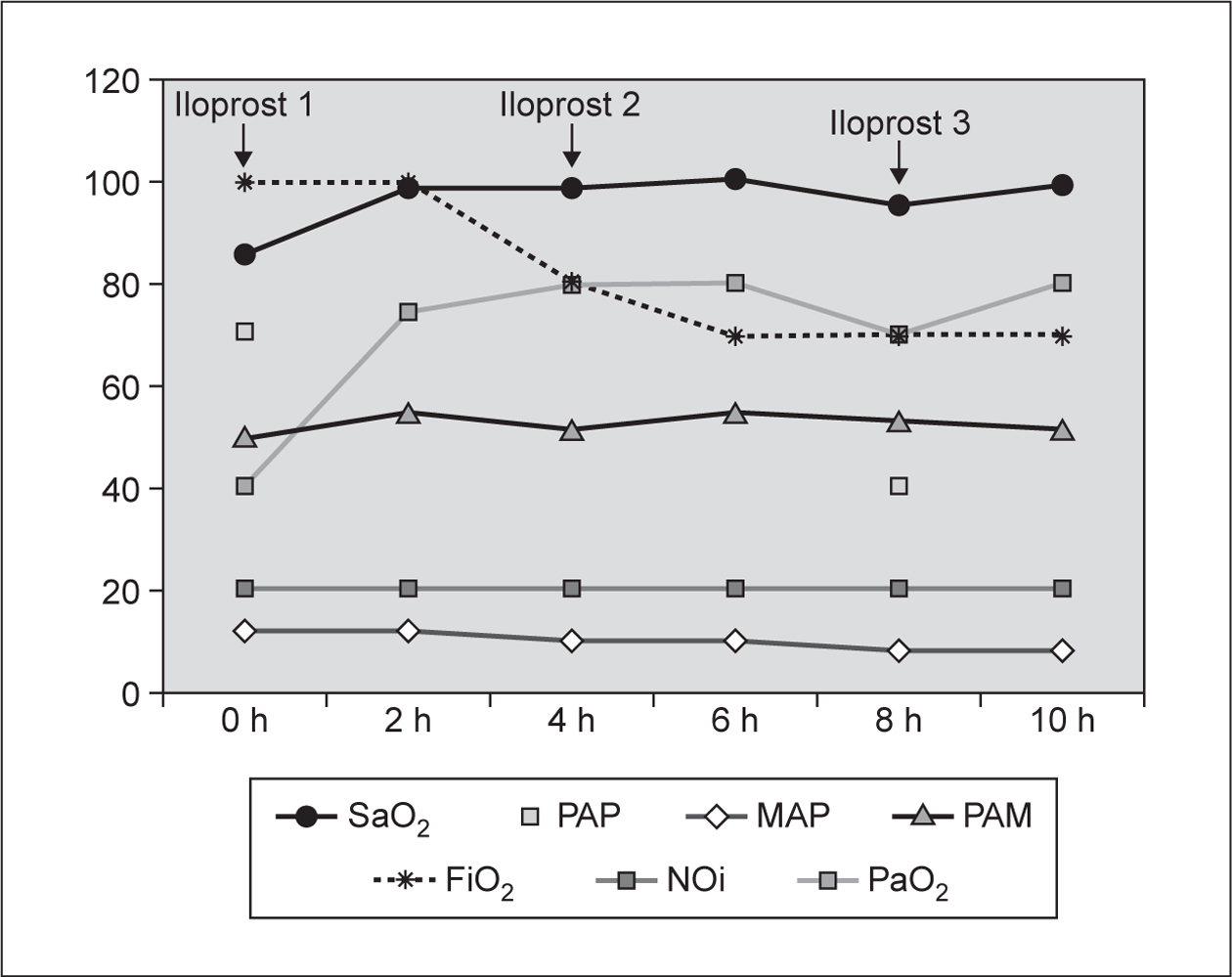
Figura 1.Efecto de iloprost sobre la oxigenación (aumento de saturación de hemoglobina y presión arterial de oxígeno [PaO2]). A partir de la tercera hora tras iniciar tratamiento se inicia un descenso en la asistencia ventilatoria (presión media de la vía aérea [MAP] y fracción inspiratoria de oxígeno [FiO2]). La presión en la arteria pulmonar disminuye 30 mmHg (40 %) tras las primeras 2 dosis. No se detectan variaciones en la presión arterial media sistémica (PAM). La dosificación de NOi no se modifica (20 ppm).
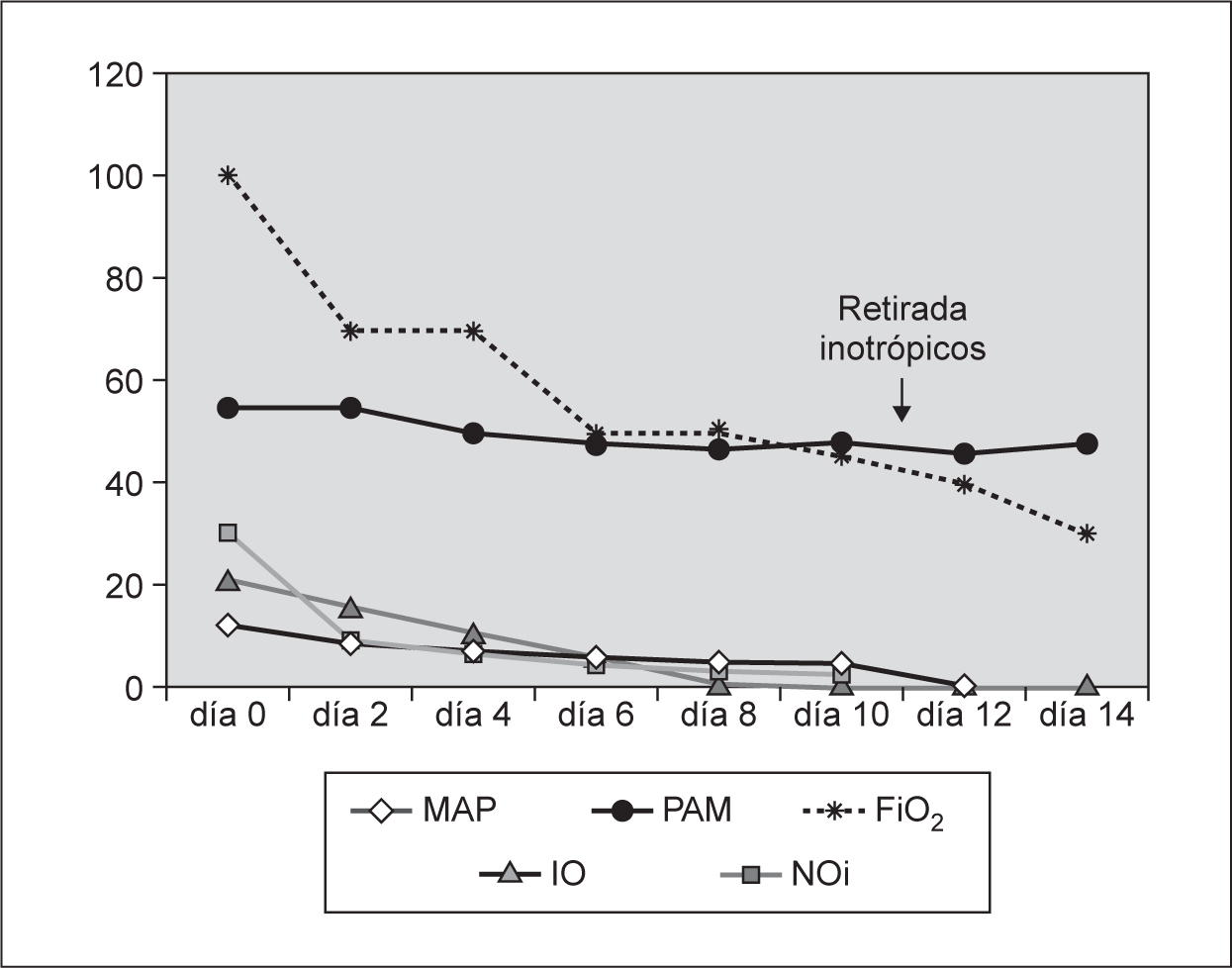
Figura 2. Evolución clínica del paciente durante el tratamiento con iloprost (14 días). El índice de oxigenación desciende de 30 a 9 tras las primeras 24 h y a 4 tras 96 h. Descenso progresivo de la asistencia ventilatoria, oxigenoterapia, soporte inotrópico y terapia con NOi. Se precisan cifras menores de presión arterial sistémica (MAP) para contrarrestar la presión pulmonar (suprasistémica al inicio del tratamiento) e invertir el shunt.
La prostaciclina es un metabolito del ácido araquidónico producido en el endotelio. Su mecanismo de acción es diferente, aunque complementario al del NOi, de ahí que se plantee su utilización conjunta 2,3. Ambos actúan como vasodilatadores de la arteria pulmonar mediante la liberación de sustancias que relajan la musculatura lisa. La prostaciclina presenta acción antiagregante plaquetaria e inhibidora de la proliferación del músculo liso.
En pediatría, la prostaciclina I2 (epoprostenol) y sus análogos se han utilizado en el tratamiento de la hipertensión pulmonar primaria y en la secundaria a cardiopatías congénitas 4,5. En la HTPP del recién nacido existe experiencia con epoprostenol en perfusión intravenosa o vía inhalatoria (administración continua). La vía nebulizada ha demostrado igual eficacia con menos efectos secundarios sistémicos (hipotensión, antiagregación, etc.) 2,6.
Recientemente se utilizado el análogo sintético de la prostaciclina I2 (iloprost) 3-5 que presenta ventajas frente a la prostaciclina I2 como mayor estabilidad y solubilidad en medios isotónicos. También presenta mayor vida media (20-30 min) y mayor duración de efecto 60-120 min (frente a 10-30 min del epoprostenol) lo cual permite su administración intermitente 7.
La experiencia en neonatología es limitada y referida casi exclusivamente a pacientes con hipertensión pulmonar secundaria a cardiopatía congénita y/o cirugía cardiovascular 8. Ehlen et al 9 presentan un caso de HTPP neonatal e iloprost por vía inhalatoria y endotraqueal. Existen trabajos con casos de HTPP sin ventilación mecánica con menor porcentaje de intubación 10.
En nuestro caso, destaca la respuesta favorable a pesar de iniciarse tardíamente. El NOi precisa de instauración precoz para una respuesta satisfactoria 1. La dosificación es una cuestión abierta dada la escasa experiencia en neonatos. La dosis fue deducida a partir de la empleada en adultos (30-200 μg/día) 7 y pediatría (10-25 ng/kg/min) 3,8,9. La estabilidad clínica al descender dosis sugiere la necesidad de ensayos clínicos o experimentales que intenten definir la dosis mínima eficaz. Igualmente serán necesarios estudios con el mayor número de pacientes para valorar la eficacia en función del aumento de supervivencia o la no necesidad de ECMO.