Factores genéticos
La fibrosis quística es la enfermedad genética letal más frecuente en la población caucasiana. La herencia es de patrón autosómico recesivo. Su incidencia es de 1 afectado por 2.000-4.000 nacimientos, dependiendo del origen étnico y la zona geográfica de procedencia. En el año 1989, Riordan et al, identificaron el gen responsable de la fibrosis quística. Se localiza en la región 7q311. Abarca una región de 250 kb con 27 exones, que contienen la información para una proteína de 1.480 aminoácidos (cystic fibrosis transmembrane conductance regulator protein, CFTR), responsable en la regulación del transporte iónico a través de la membrana celular2. En la actualidad se conocen alrededor de 1.200 mutaciones del gen de la fibrosis quística. Las distintas mutaciones se han agrupado en seis clases diferentes: clase I, provocan alteración de la síntesis de la proteína; clase II, alteración del procesamiento y transporte de la misma; clase III, defecto en los mecanismos de regulación de la función de la CFTR; clase IV, descenso de la conductancia; clase V, se reduce la función de los canales de la CFTR en la membrana apical; clase VI, descenso de la estabilidad de la proteína y, por lo tanto, alteración de la función transportadora. La correlación entre genotipo y fenotipo sólo se ha podido constatar para la insuficiencia pancreática, no así para la gravedad de la enfermedad pulmonar. Se ha postulado la existencia de factores genéticos secundarios, denominados modificadores, que modulan la gravedad de la enfermedad y la influencia de factores epigenéticos3-5.
Fisiopatología
La proteína codificada por el gen de la fibrosis quística, la CFTR, funciona como un canal del cloro6,7, y se localiza en la membrana apical de las células epiteliales. Esta proteína es anormal en estos pacientes, y el resultado final es un transporte alterado de agua y electrolitos, así como un aumento en la absorción de sodio en los órganos afectos. Todo esto, unido al ADN procedente de los neutrófilos, produce en la vía aérea un espesamiento de las secreciones, originando alteración en el transporte mucociliar, dificultad para la eliminación bacteriana, infección y predisposición al daño pulmonar8 (fig. 1).
Figura 1. Etiopatogenia de la fibrosis quística. Adaptada de García Novo. Rev Esp Pediatr, 1999.
Hasta hace relativamente poco tiempo, se creía que la obstrucción de la vía aérea asociada a la infección crónica, eran los principales factores en el desarrollo de la enfermedad. Actualmente, ha ido adquiriendo mayor importancia el papel que la inflamación por sí misma ocupa en el proceso de lesión pulmonar. Se ha demostrado que la inflamación ya está presente en los estadios iniciales de la enfermedad, incluso en ausencia de infección, y que, además, progresa durante toda la vida. Los neutrófilos y sus productos: citocinas, radicales libres de oxígeno y enzimas proteolíticas, desempeñan un papel fundamental en el proceso de lesión pulmonar en fibrosis quística9. En estos pacientes, la respuesta inflamatoria es excesiva e inefectiva. Está demostrado que en el lavado broncoalveolar de niños con 4 semanas de vida se encuentran niveles elevados de interleucina 8 (IL-8) y neutrófilos activados, en ausencia de infección bacteriana. No obstante, ésta también puede detectarse desde las primeras 8 semanas de vida10.
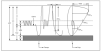
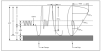
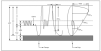
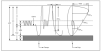
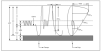
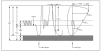
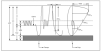
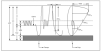
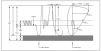
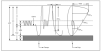
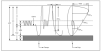
En la figura 2 se observa la cronología de la colonización bacteriana de estos pacientes7. No obstante, en la enfermedad pueden estar implicados otros gérmenes como: micobacterias atípicas, hongos, Burkolderia cepacia, etc.
Figura 2. Fibrosis quística. Colonización bacteriana según edad. Adaptada de Salcedo et al, 1998.
Enfermedad pulmonar
La enfermedad respiratoria asociada a malabsorción constituye el modo clásico de presentación. No obstante, existen una serie de características fenotípicas en las que se ha de sospechar fibrosis quística (tabla 1).
También es obligado descartar este proceso en pacientes con neumonías de repetición, asma de mala evolución, hallazgo de un mucocele y otros posibles cuadros clínicos más infrecuentes como vasculitis leucocitoplástica, osteoartropatía pulmonar hipertrófica, artropatía episódica y poliarticular asociada a fibrosis quística.
Criterios diagnósticos
La fibrosis quística es una enfermedad multisistémica que suele manifestarse en los primeros años de vida, aunque pueden existir formas leves de diagnóstico tardío.
El test del sudor sigue siendo una prueba fundamental en el diagnóstico11. El método descrito por Gibson y Cooke (1959) se basa en la medición del cloro en sudor estimulado mediante iontoforesis con pilocarpina12. Las unidades de fibrosis quística deben utilizar siempre el test cuantitativo de iontoforesis con pilocarpina o QPIT. Siempre se ha de tener en cuenta al interpretar los resultados del test del sudor, la posibilidad de falsos positivos (tabla 2) o falsos negativos (tabla 3). Para el estudio de fibrosis quística puede ser útil el algoritmo siguiente (fig. 3)13.
Figura 3. Protocolo de diagnóstico y seguimiento de los enfermos con fibrosis quística. Adaptada del Grupo de Trabajo Fibrosis Quística de la SENP13.
Las Conclusiones de la Conferencia de Consenso de la CFF para el Diagnóstico de fibrosis quística son las siguientes14:
1. Se precisa una o más de las tres siguientes circunstancias:
a)Rasgos fenotípicos característicos de fibrosis quística. Considerando como tales los siguientes:
Enfermedad sinopulmonar crónica sugestiva.
Alteraciones gastrointestinales y/o nutricionales características.
Alteraciones del tracto urogenital masculino, originando azoospermia obstructiva.
Síndromes debidos a pérdidas excesivas de sal por el sudor: pérdida aguda de sal, alcalosis metabólica crónica.
b)Historia de enfermedad en hermanos o primos hermanos.
c)Test de cribado neonatal con tripsina inmunorreactiva elevada.
2. Junto con lo que se denomina "evidencia de disfunción de la CFTR", mediante uno o más, de los tres siguientes hallazgos14,15:
a)Concentración de cloro en sudor superior a 60 mmol/l (se recomiendan dos determinaciones).
b)Presencia de dos mutaciones "causantes de enfermedad".
c)Anomalías características en la diferencia de potencial transepitelial nasal.
3. En ausencia de fenotipo clínico característico de la enfermedad, podemos establecer el diagnóstico de fibrosis quística en los siguientes casos:
a)Existencia de un familiar de primer grado afecto de fibrosis quística y una prueba del sudor positiva.
b)Cribado neonatal positivo (incluyendo estudio de mutaciones).
c)Cribado neonatal exclusivamente con detección de tripsina inmunorreactiva, más dos pruebas de sudor positivas.
d)Existencia de dos mutaciones fibrosis quística efectuadas en estudio prenatal.
Recientemente se ha comunicado una nueva clasificación de la fibrosis quística en: prefibrosis quística genética, eléctrica o química, subclínica y enfermedad16.
Por último, no debe olvidarse que el diagnóstico molecular constituye un elemento indispensable en la prevención de las enfermedades genéticas hereditarias. En el caso de la fibrosis quística, esta prevención es factible mediante la identificación de los portadores, el diagnóstico prenatal que se efectúa en muestra de vellosidad corial (8-10 semanas), y por amniocentesis (16-18 semanas). Más recientemente es posible la realización del diagnóstico preimplantacional2. El interés del diagnóstico molecular se extiende también al conocimiento de la etiopatogenia y del tratamiento de este proceso.
Los programas de cribado neonatal en fibrosis quística, están siendo ampliamente discutidos en la actualidad, fundamentalmente en la relación coste-beneficio. Este beneficio parece tener más relación con el estado nutricional que con el funcionalismo pulmonar.
Tratamiento específico
Está demostrado ampliamente que la supervivencia y la calidad de vida de los pacientes aumentan de forma notable cuando son tratados en unidades multidisciplinarias de fibrosis quística13,17.
Entre las medidas preventivas importantes se encuentran:
1. Evitar el tabaquismo.
2. Indicación de vacuna antigripal anual.
3. Valorar vacunación antineumocócica.
Los objetivos del tratamiento son los siguientes:
1. Prevenir la progresión de la enfermedad pulmonar.
2. Aportar la nutrición adecuada.
3. Efectuar control ambiental correcto.
4. Proporcionar una buena calidad de vida al paciente y a su familia, brindándoles en todo momento la estabilidad emocional que necesiten7.
Para todo ello se dispone de fisioterapia respiratoria y broncodilatadores.
Fisioterapia respiratoria
Debe ser dirigida por especialista en rehabilitación y fisioterapia respiratoria.
Broncodilatadores
Están indicados en pacientes con hiperreactividad bronquial, en las exacerbaciones respiratorias y en los que refieran mejoría subjetiva tras su empleo. Se recomiendan previos a la fisioterapia respiratoria y a la administración de antibióticos inhalados.
Tratamiento de la infección respiratoria
Debe ser siempre agresivo y precoz. Está perfectamente demostrada la necesidad obligada del empleo de antibióticos, que constituyen la base del tratamiento de estos pacientes, tanto de la infección aguda como de la infección bronquial crónica, pero no existe en la actualidad ninguna pauta al respecto aceptada de forma unánime. Las dosis de los antibióticos empleados es siempre más alta de lo habitual, para lograr concentraciones eficaces en las secreciones bronquiales. Se administran por diferentes vías: intravenosa, oral o inhalatoria, dependiendo de las características individuales de cada paciente. En las tablas 4 a 613 se describen los antibióticos, dosis y vías de administración que deben utilizarse.
Infección reciente por Pseudomonas aeruginosa
El tratamiento precoz ante el primer aislamiento de Pseudomonas aeruginosa en esputo, en los pacientes clínicamente estables, puede retrasar la infección bronquial crónica.
La mayoría de los autores recomiendan administrar ciprofloxacino por vía oral, asociado a colistina o tobramicina aerosolizados durante un período mínimo de 21 días, o bien un ciclo de antibióticos a los cuales sea sensible este germen, administrados por vía intravenosa.
Si la P. aeruginosa no se logra erradicar en esputo, debe repetirse de nuevo el ciclo. Si aun así continúa persistiendo, debe considerarse que existe una colonización-infección bronquial crónica y se tratará siguiendo las pautas de colonización pulmonar crónica por P. aeruginosa.
Infección reciente por Staphylococcus aureus
No existe aún evidencia científica suficiente que demuestre la eficacia del tratamiento precoz y continuado de la infección bronquial crónica por S. aureus, por lo que la mayoría de los pacientes son tratados con antibióticos sólo durante las exacerbaciones.
Colonización-infección bronquial crónica
Se considera colonización-infección bronquial crónica el aislamiento de un mismo germen en el esputo, al menos en tres cultivos sucesivos durante un período de 6 meses.
En pacientes con infección bronquial crónica por P. Aeruginosa, la vía de administración de antibióticos más ampliamente recomendada es la inhalada.
En la infección bronquial crónica por otros gérmenes no existe evidencia científica suficiente sobre la eficacia de esta vía de administración.
Los antibióticos más frecuentemente utilizados son: tobramicina (100-200 mg/12 h), gentamicina (80-200 mg/ 12 h); y colistina (1-2 millones de unidades/12 h).
La administración periódica de ciclos de antibióticos intravenosos (cada 3 o 4 meses) en pacientes con infección crónica por Pseudomonas, aportan buenos resultados clínicos y de supervivencia, pero conllevan un incremento importante en el coste.
Tratamiento antibiótico en las exacerbaciones respiratorias
El diagnóstico de una exacerbación infecciosa no siempre es fácil. Se define por una asociación de síntomas, signos y resultados de exploraciones complementarias. Entre los síntomas compatibles destacan: aumento en la frecuencia y duración de la tos, aumento de la producción de esputo, así como cambios en la consistencia y coloración de éste, aumento de la disnea, disminución de la tolerancia al ejercicio, astenia y anorexia, pérdida de peso, fiebre y hemoptisis. A esto hay que añadir, para nuestro "apoyo diagnóstico": nuevos hallazgos auscultatorios en el tórax, descenso en los parámetros funcionales respiratorios (capacidad vital forzada [FVC], volumen espiratorio máximo en el primer segundo [FEV1]), disminución de la saturación arterial de oxígeno y leucocitosis18,19.
La valoración de la gravedad de la exacerbación también es imprecisa, ya que depende en gran parte del grado de afectación pulmonar previa del paciente. En general, la exacerbación se considera leve, moderada o grave, en función de que el paciente presente o no afectación del estado general, disnea a mínimos esfuerzos u ortopnea, o hipoxemia respirando aire ambiental13,19.
El tratamiento se basa en tres pilares fundamentales: antibioticoterapia, fisioterapia respiratoria y nutrición adecuada. Siempre que sea posible, los antibióticos deben ser elegidos en función de los microorganismos aislados en el esputo y de su sensibilidad antibiótica.
Exacerbaciones leves-moderadas. Inicialmente, si es posible, debe utilizarse la antibioticoterapia por vía oral y, como norma general, en ciclos de 14 días de duración. Los antibióticos orales disponibles para las exacerbaciones por P. aeruginosa son escasos. El más eficaz es el ciprofloxacino. También pueden ser útiles cotrimoxazol, cloranfenicol, tianfenicol y fosfomicina18.
Exacerbaciones graves. Toda exacerbación grave exige tratamiento hospitalario. Requiere la administración de antibioticoterapia intravenosa, según la sensibilidad del germen responsable. El régimen antibiótico utilizado habitualmente consiste en la asociación de una cefalosporina activa frente a Pseudomonas y un aminoglucósido. La ceftazidima suele ser el antibiótico de primera elección. La antibioticoterapia se administrará en dosis elevadas y con una duración de 14-21 días. Marcar una duración estándar puede no ser apropiada para todos los pacientes18,19. La decisión de mantener más o menos tiempo la antibioticoterapia suele apoyarse en el grado de recuperación de la función pulmonar, la disminución de la carga bacteriana en esputo y en la mejoría de los scores clínicos19.
El tratamiento antibiótico intravenoso en domicilio se ha mostrado útil en las exacerbaciones leves o moderadas, para mejorar la calidad de vida de los pacientes y disminuir el coste hospitalario.
La vía inhalada se ha empleado de forma empírica en las exacerbaciones pulmonares19,20.
Algunos clínicos utilizan la combinación de antibioticoterapia intravenosa e inhalada, para lograr incrementar al máximo los niveles del fármaco en el lugar de la infección. El tratamiento de los pacientes colonizados por S. aureus y Haemophilus influenzae pueden tratarse solamente con betalactámicos, por vía oral o intravenosa. A esta terapia hay que añadir la intensificación de la fisioterapia respiratoria, contemplar el uso de broncodilatadores, a ser posible efectuando una prueba broncodilatadora previa para valorar su utilización, y una adecuada nutrición.
Antibióticos nebulizados en fibrosis quística
Para la correcta nebulización de los antibióticos, se recomienda emplearlos mediante un compresor de alto flujo ($ 6-8 l/min) (Medic Aid CR 60 o similares) y un nebulizador tipo Jet (Ventstream, Sidestream o equivalentes), que genere el mayor número posible de partículas entre 3 y 5 m de diámetro en el menor tiempo posible18,21,22. La solución del antibiótico que se va nebulizar debe prepararse con 4 a 6 ml (2,5 ml en nebulizadores con bajo volumen residual) de agua destilada o suero fisiológico, para conseguir soluciones lo más isotónicas posibles. Con el fin de mejorar el acceso del antibiótico inhalado a la vía respiratoria, se recomienda la administración previa de broncodilatadores y fisioterapia respiratoria.
Indicaciones. La antibioticoterapia nebulizada en pacientes con fibrosis quística está indicada en la infección bronquial crónica por P. aeruginosa. En la colonización bronquial inicial por este germen, también está indicada asociada a ciprofloxacino oral. No está indicada en las exacerbaciones como alternativa a la administración intravenosa. Los antibióticos de primera línea para utilizar nebulizados son colistina y tobramicina. También pueden emplearse gentamicina y ceftazidima, en los casos en los que no pueda administrarse colistina o tobramicina (las dosis están referidas en la tabla 6). La duración del tratamiento no debe ser inferior a 3 meses, cuando se indican en la colonización inicial por P. aeruginosa (colistina inhalada y ciprofloxacino oral), y continua en la infección bronquial crónica por este germen. Debe asegurarse un correcto mantenimiento y limpieza de los sistemas de nebulización.
Cuando se prescriben varios fármacos nebulizados, el orden de utilización de éstos, debe de ser el siguiente: broncodilatadores, DNasa, fisioterapia respiratoria, antibiótico y glucocorticoides inhalados o cromoglicato sódico21,22.
Actualmente se dispone de nuevas aportaciones en la terapia antibiótica:
1. Tobramicina inhalada. Tobramicina inhalada preparada específicamente para inhalación, a la concentración de 300 mg en 5 ml. Ramsey et al23 han efectuado un trabajo en 520 pacientes (edad media, 21 años) colonizados crónicamente por P. aeruginosa. Demostraron que la prescripción de TOBI en dosis de 300 mg cada 12 h por vía inhalatoria, administrado de forma intermitente durante ciclos de 28 días puede resultar beneficiosa. Tras 6 meses que duró el estudio demostraron una clara mejoría de la función pulmonar, disminución de la concentración de Pseudomonas en esputo y del número de ingresos hospitalarios.
2. Macrólidos. Se han empleado últimamente en fibrosis quística, debido a las propiedades antiinflamatorias que poseen. Disminuyen la producción de IL-2, IL-5, y sobre todo, IL-1, IL-6, IL-8 y factor de necrosis tumoral alfa (TNF-a), siendo responsables de la acción antiinflamatoria. La disminución de citocinas y de la quimiotaxis tiene lugar en tratamientos largos4,24.
3. Protegrina. Recientemente se está ensayando esta sustancia polipeptídica de origen porcino, que ha demostrado tener propiedades antibacterianas25.
Fluidificación de secreciones
DNasa humana recombinante
Obtenida mediante técnicas de ingeniería genética. Se usa por vía inhalatoria. Existen ensayos clínicos que demuestran su eficacia. No obstante, la respuesta individual ha sido muy variable, por lo que unido al elevado coste económico se recomienda efectuar un "ensayo" de 3 a 6 meses de duración y evaluar respuesta. Se está desarrollando un estudio multicéntrico para valorar si la administración regular de DNasas en niños con enfermedad pulmonar leve (FEV1 > 80 %) limita el deterioro del FEV1 a lo largo de 2 años25.
Suero salino hipertónico
Aumenta el aclaramiento mucociliar. Se utiliza en nebulización. Existe la posibilidad en algunos pacientes de sufrir "broncospasmo paradójico"4,26.
Gelsolina
Se trata de una proteína que rompe los filamentos de actina. Todavía se encuentra en fase de investigación.
Terapias antiinflamatorias
Las terapias antiinflamatorias probablemente deberían iniciarse desde épocas tempranas de la vida, y ser utilizadas de forma crónica27 (tabla 7).
Corticoides orales
Trabajos realizados con prednisona oral28 han demostrado numerosos efectos secundarios severos, motivo por el cual no se aconseja su uso rutinario. Están indicados en pautas cortas, en el tratamiento de las exacerbaciones agudas que cursan con broncospasmo, que no responden al tratamiento convencional con antibióticos, y en la aspergilosis broncopulmonar alérgica.
Glucocorticoides inhalados
Presentan menor incidencia de efectos secundarios. Nikolaizik et al29 realizaron un estudio, constatando sólo una discreta mejoría de la función pulmonar en pacientes tratados con glucocorticoides inhalados. Se precisan más estudios.
Ibuprofeno
El ibuprofeno es un antiinflamatorio no esteroideo. Puede constituir una alternativa al tratamiento con corticoides en el control de la inflamación. Interfiere con la IL-4, e inhibe en altas dosis la liberación de elastasa. Trabajos de Konstan et al30 demuestran que en dosis elevadas y administrado por vía oral enlentece el deterioro de la enfermedad pulmonar leve. Por los efectos secundarios del tratamiento prolongado, y porque es obligado monitorizar sus valores plasmáticos, es por lo que no se utiliza de forma sistemática.
Otras opciones terapéuticas en fase de investigación son las siguientes: antiproteasas, alfa-1-antitripsina humana recombinante y el inhibidor de la leucoproteasa secretora humana: disminuyen los niveles de IL-8 y elastasa y se administran en aerosol. La pentoxifilina inhibe la acción de la IL-1 y el TNF. Antielastasa: DMPP 777 (aún en investigación). Antioxidantes: dismutasa superoxidasa y gammaglobulina hiperinmune.
Tratamiento de las complicaciones
Atelectasia pulmonar
En fibrosis quística se produce fundamentalmente por obstrucción de la vía aérea debido a la impactación de moco. Suele acompañar a las exacerbaciones respiratorias, pero también pueden verse en la aspergilosis broncopulmonar alérgica, o tratarse de un hallazgo radiológico. El tratamiento consiste en intensificación de la fisioterapia respiratoria, administración de antibióticos, broncodilatadores inhalados y, en ocasiones, corticoides sistémicos.
Si no se resuelve con estas terapias, se añadirá alguna de las siguientes:
1. Aerosolterapia con DNasa recombinante o suero salino hipertónico.
2. Distensión de las vías aéreas mediante: flúter, presión positiva espiratoria, ventilación con presión positiva intermitente, ventilación con presión positiva continua o ventilación con percusión intrapulmonar.
3. Otra opción es la fibrobroncoscopia o la broncoscopia rígida, en la que al final del broncoaspirado y lavado, se administra DNasa. Los resultados con este método son discordantes. En atelectasias de larga evolución con bronquiectasias importantes en el lóbulo afectado, se valorará la lobectomía31.
Neumotórax
Su tratamiento suele constituir una urgencia. Se recomienda terapia conservadora si se puede. Si supera el 20 % del volumen del tórax afectado o dificulta la función respiratoria, se colocará un tubo de drenaje durante un mínimo de 5-7 días y un máximo de 15. En casos de persistencia o recidiva, se resecarán las bullas por toracoscopia si es posible, o mediante toracotomía.
La pleurodesis mediante toracoscopia puede efectuarse mecánicamente o por láser de Nd:YAG o CO2. La pleurodesis mecánica extensa o la instilación de sustancias esclerosantes, deben evitarse, para disminuir riesgos futuros en un posible trasplante pulmonar18.
Hemoptisis
En la mayoría de los casos acompaña a una exacerbación infecciosa y se resuelve con el tratamiento de la misma.
La hemoptisis masiva o amenazante consiste en: una pérdida hemática superior a 250 ml/24 h, presencia de tres o más episodios recurrentes de 100 ml/día en una semana, o bien, un sangrado crónico lentamente progresivo. Es más frecuente en adolescentes. En el tratamiento de ésta, además de las medidas habituales en la hemoptisis masiva, debe instaurarse antibioticoterapia por vía intravenosa. Se evitará la fisioterapia respiratoria, antibioticoterapia inhalada, y fármacos que interfieran en la coagulación, durante las primeras 48-72 h tras la hemoptisis.
La fibrobroncoscopia está indicada para localizar el origen del sangrado y aplicar medidas tópicas. Si tras ello no cede el sangrado, se procederá a la embolización selectiva de la arteria sangrante. Si no se controla el sangrado con las medidas descritas, en ocasiones hay que contemplar la segmentectomía o lobectomía, si la función pulmonar lo permite. En caso de afectación muy grave, se valorará el trasplante pulmonar.
Aspergilosis broncopulmonar alérgica
Su diagnóstico se establece en función de criterios clínicos, radiológicos e inmunológicos: broncoconstricción reversible/asma, infiltrados pulmonares, elevación de la IgE y/o IgG específicas frente a Aspergillus fumigatus, aislamiento del mismo en esputo, y presentar buena respuesta a los esteroides orales. A esto se añaden los siguientes criterios inmunológicos: tests cutáneos positivos frente a A. fumigatus, IgE total sérica superior a 1.000 kU/l, y presencia de precipitinas séricas frente a A. fumigatus.
El tratamiento de elección son los esteroides por vía oral: prednisona en dosis de 0,5-1 mg/kg/día, diariamente, durante 2 semanas y, posteriormente, se continuará con la misma dosis a días alternos, durante 3 a 6 meses, según evolución clínica, radiológica e inmunológica.
Se ha investigado la asociación de itraconazol a los corticoides orales, en dosis de 5-10 mg/kg/día o 100-400 mg/día durante 1-6 meses, aunque la duración ideal no está establecida. En casos de escasa respuesta al tratamiento expuesto, pueden valorarse los corticoides inhalados o anfotericina B inhalada.
El control de la respuesta al tratamiento se llevará a cabo mediante la valoración de la mejoría clínica, de la función pulmonar, así como del descenso de la IgE sérica total.
Insuficiencia respiratoria crónica. Asistencia respiratoria
Debe intensificarse el tratamiento habitual: antibioticoterapia intravenosa en dosis elevadas durante períodos de tiempo más prolongados, broncodilatadores, corticoides, DNasa, fisioterapia respiratoria con sesiones más frecuentes e intensas, buen manejo nutricional y ejercicio físico controlado.
Los pacientes con enfermedad pulmonar moderada o grave, o con exacerbación pulmonar, experimentan con frecuencia disnea e hipoxemia que obligan al empleo de oxigenoterapia.
La ventilación mecánica invasiva está indicada en pacientes con insuficiencia respiratoria aguda potencialmente reversible, y en los que se encuentran en lista de espera para el trasplante pulmonar, con un importante deterioro respiratorio.
Una alternativa a la ventilación mecánica es la ventilación mecánica no invasiva, utilizada en pacientes con importantes desaturaciones de oxígeno nocturnas e hipercapnia.
La ventilación no invasiva con presión positiva, se ha empleado con éxito para estabilizar a pacientes con fibrosis quística e insuficiencia respiratoria hipercápnica, como paso previo al trasplante pulmonar19,32.
Durante las exacerbaciones agudas, la ventilación nasal permite incrementar las concentraciones de oxígeno inspirado, sin empeorar la retención de CO2.
En estadios terminales de la enfermedad, se dispone del trasplante pulmonar. Sus indicaciones son las siguientes:
1. FEV1 # 30 % del teórico, hipoxemia y/o hipercapnia grave.
2. Deterioro respiratorio progresivo, evidenciado por un aumento de la frecuencia y duración de las exacerbaciones pulmonares graves.
3. Complicaciones pulmonares con riesgo vital, como la hemoptisis masiva recurrente.
Tratamiento del defecto básico (tabla 8)
Todas ellas están en fase de investigación. La terapia génica se basa en la introducción y expresión dentro de las células epiteliales, de una copia de un gen normal de la CFTR. Existen aún problemas importantes con esta terapia, unos en cuanto a la seguridad (vectores virales), y otros con respecto a la eficiencia (liposomas). En la actualidad, se continúa trabajando en la búsqueda del vector ideal. La realidad es que aún falta tiempo para que esta terapia resulte efectiva8,25.
Nuevas perspectivas
Es posible que pronto se disponga de vacunas antipseudomonas efectivas. También parece cercana la vacunación frente al S. aureus33.
Existen ensayos clínicos en curso para valorar el beneficio del interferón gamma administrado por vía inhalatoria frente a micobacterias no tuberculosas en fibrosis quística.
Parecen prometedoras las investigaciones recientes sobre nuevas moléculas denominadas "furanonas", para el tratamiento de la colonización por P. aeruginosa. Actúan inhibiendo "los biofilms" formados por estos agentes, y no presentan efectos secundarios.
También se encuentra en investigación la terapia con ácidos grasos (docosohexanoico), por su papel en la regulación de la función de las membranas celulares.
Por último, una posibilidad futura para la corrección génica podría ser "la cirugía molecular". Consiste en intentar corregir en el ADN genómico la mutación de la CFTR. Una gran ventaja es que esta corrección sería persistente34.
*Nicolás Cobos Barroso - Unidad de Neumología Pediátrica y Fibrosis Quística. Hospital Universitario Materno-Infantil Vall d'Hebron. Barcelona. Amparo Escribano Montaner - Unidad de Neumología Infantil. Hospital Clínico Universitario. Universidad de Valencia. Gloria García Hernández - Sección de Neumología y Alergia Pediátricas. Hospital 12 de Octubre. Madrid. Eduardo González Pérez-Yarza - Unidad de Neumología Infantil. Hospital Donostia. Servicio Vasco de Salud-Osakidetza. San Sebastián. Santos Liñán Cortés- Unidad de Neumología Pediátrica y Fibrosis Quística. Hospital Universitario Materno-Infantil Vall d'Hebron. Barcelona. Martín Navarro Merino - Sección de Neumología Infantil. Hospital Universitario Virgen de la Macarena. Sevilla. Concepción Oliva Hernández - Unidad de Neumología. Departamento de Pediatría. Hospital Ntra. Sra. de la Candelaria. Santa Cruz de Tenerife. Javier Pérez Frías - Sección de Neumología Pediátrica. Hospital Materno-Infantil Carlos Haya. Málaga. Josep Sirvent Gómez - Unidad de Neumología Pediátrica. Hospital Juan Canalejo. A Coruña. José Ramón Villa Asensi - Sección de Neumología Infantil. Hospital Universitario Infantil del Niño Jesús. Madrid.