El síndrome de la escaldadura estafilocócica (SSS) es una enfermedad poco habitual en nuestro medio, aunque parece que su incidencia está aumentando en los últimos años1, con una potencial morbimortalidad sin un adecuado manejo. Así mismo puede ser la primera manifestación de enfermedades congénitas. La recurrencia del SSS es rara, pudiendo asociarse a trastornos subyacentes como la ictiosis, donde la degradación prematura de estructuras del estrato córneo puede facilitar la colonización/infección por Staphylococcus aureus (S. aureus) productor de toxinas exfoliativas (ET)2.
Recién nacido sin antecedentes prenatales, ni familiares de enfermedades cutáneas. No factores de riesgo infecciosos excepto prematuridad (edad gestacional 36+6-semanas; detección de estreptococo en cultivo recto vaginal negativo). A las 24 h de vida comienza con lesiones ampollosas en el tronco y las extremidades, en lugares de manipulación y de presión (Nikolsky positivo), afectación de aproximadamente el 30% de la superficie corporal (SC); sin otros datos clínicos ni analíticos de sepsis. Recibe antibioterapia con cloxacilina y medidas de aislamiento, además de sedoanalgesia. Fluidoterapia para reposición de pérdidas cutáneas (aportes máximos 100 cc/kg/día), manteniendo la ingesta. Mejoría progresiva desde el quinto día de tratamiento, con resolución de lesiones el día 14, cuando se suspende la antibioterapia. Crecimiento de S. aureus meticilin sensible (SAMS) en muestras de ampollas-cutáneas, no se objetiva S. aureus en la mucosa nasal ni el hemocultivo. Biopsia cutánea con ampolla subcórnea y necrosis epidérmica superficial, compatible con SSS. No aparición de nuevas lesiones tras el alta hospitalaria.
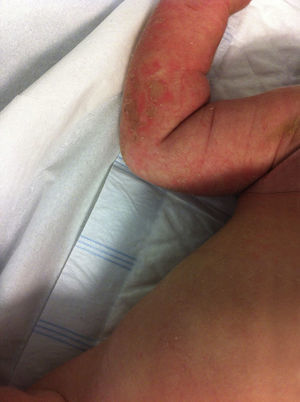
A los 2 meses, observan nuevamente ampollas de las mismas características (fig. 1), además refieren aparición de escamas hiperqueratósicas. No presenta aspecto séptico, ni datos analíticos de infección; afectación de aproximadamente el 10% de la SC. Recibe antibioterapia con cefuroxima, con mejoría. Se realiza una nueva biopsia en la que se evidencian depósitos granulares de IgM en la membrana basal epidérmica, hiperqueratosis epidermolítica compatible con ictiosis. Actualmente, presenta escamas hiperqueratósicas en pliegues y codos, sin presentar nuevos episodios de SSS.
El SSS es una enfermedad exfoliativa ampollosa debido a las ET del S. aureus. Este se aloja en las mucosas, donde las toxinas, principalmente ET-A y ET-B, viajarán por vía hematógena produciendo la formación de ampollas y descamación epidérmica característica3. Predomina en el periodo neonatal debido a la inmadurez renal, que contribuye a la persistencia de las toxinas en sangre, además de la ausencia de anticuerpos específicos anti ET-A y ET-B3,4.
Aunque el aislamiento del S. aureus en las mucosas es diagnóstico, la detección de la producción de toxinas o del gen productor de toxina es característica. Una sospecha clínica precoz es fundamental, ya que el inicio temprano del tratamiento disminuye la morbimortalidad asociada, que en los niños, especialmente en el periodo neonatal dada la inmadurez inmunológica, puede tener un desenlace fatal3,4.
El tratamiento con betalactámicos, en especial cloxacilina, continúa siendo el tratamiento de elección en las infecciones por SAMS5,6. En 2009, el estudio del grupo de infección por S. aureus resistente a meticilina (SARM) en pediatría encontró una prevalencia del 8,8% de SARM adquirido en la comunidad, en pacientes de 4 hospitales españoles7, por lo que en nuestro medio, donde la frecuencia de infecciones pediátricas por SARM se estima baja, es decir menor del 10%6,7, la cloxacilina es el tratamiento de primera línea.
La vancomicina o el linezolid deberían emplearse en casos de aislamiento de SARM, mala evolución en niños con cultivo negativo, entre otros. La clindamicina se ha demostrado eficaz en el tratamiento de infecciones invasivas por SARM, por lo que podría ser utilizado siempre que no exista resistencia6.
En caso de aislamiento de SAMS, el uso de cefalosporinas de primera o segunda generación y amoxicilina/clavulánico, entre otros, es de utilidad; sin embargo, en infecciones graves que asocian alto inóculo la posibilidad de fracaso es menor con cloxacilina5,8.
En las unidades neonatales, además del tratamiento antibiótico y sintomático, es imprescindible el aislamiento para evitar la transmisión-nosocomial.
Existen pocos casos de pacientes descritos en la literatura en los que se observa recurrencia (tabla 1). Todos los niños descritos con SSS recurrente presentaban factores predisponentes asociados (prematuridad, muy bajo peso, ictiosis).
Pacientes con SSS recurrente y patología subyacente
| Pacientes con SSS recurrente, procedencia | Patología subyacente | Cita |
| Dos hermanos procedentes de Taiwán | Síndrome de Netherton | Chao et al.2 |
| Recién nacido holandés | Prematuridad (edad gestacional 26+6 sem) | Duijsters et al.9 |
| Recién nacido alemán | Prematuridad (edad gestacional 25 semanas), bajo peso (364 g) | Rieguer-Fackeldey et al.10 |
Nuestro paciente no ha presentado nuevas recurrencias de SSS, probablemente la madurez renal y el desarrollo de anticuerpos favorezcan la ausencia de nuevos episodios. El tratamiento precoz del SSS evita las complicaciones y el riesgo de infección nosocomial en las unidades neonatales. En caso de recurrencias, la posibilidad de una enfermedad subyacente debe ser valorada.