Nuestro modelo organizativo posibilita la realización anual de 1.000 trasplantes hepáticos, de los cuales el trasplante hepático pediátrico constituye el 5% y proporciona, en niños con hepatopatía grave, progresiva e irreversible, una supervivencia del 90% al año y superior al 80% a los 15 años de seguimiento. La principal indicación es la atresia de vías biliares seguida de hepatopatías metabólicas e insuficiencia hepática aguda, realizándose el 50% de los procedimientos en menores de 2 años y el 25-30% en el primer año de vida.
La lista de espera se mantiene en torno a los 35 pacientes, con un promedio de 100 pacientes incluidos anualmente y 60 trasplantados tras un tiempo medio de espera de 136,3 días. La priorización de los candidatos utiliza el PELD como herramienta objetiva de apoyo en la toma de decisiones. No obstante, el progresivo envejecimiento de los donantes, con un perfil cada vez más alejado de los requerimientos de los pacientes infantiles incluidos en lista de espera, precisa impulsar estrategias como el trasplante hepático de donante vivo y la modalidad split, para incrementar las probabilidades de trasplante reduciendo la mortalidad en lista de espera y el tiempo de permanencia en la misma.
El trasplante intestinal/multivisceral pediátrico registra una baja indicación pero conlleva unos requisitos que perfilan un donante muy infrecuente en nuestro país, lo que, unido a la ausencia de alternativas que contrarresten el impacto negativo de estas dificultades, lastra las probabilidades de trasplante de estos pacientes.
Our organizational model allows an annual 1,000 liver transplants. Pediatric liver transplantation constitutes 5% of such activity and provides, in children with severe, progressive and irreversible liver disease, a 1 year-survival of 90% and more than 80% after 15 years of follow-up. The main indication is biliary atresia followed by metabolic liver disease and acute liver failure. Around half of the procedures are performed in children under two years and 25-30% in the first year of life.
The waiting list remains at around 35 patients, with an average of 100 patients enrolled annually and 60 of them finally transplanted after an average of 136.3 days on the waiting list. The prioritization of the candidates uses the PELD as an objective tool for decision-making. However, the progressive aging of donors, with a profile increasingly different from the requirements of the pediatric patients included in the waiting list, requires strategies such as living donor liver transplantation and the split liver transplantation, to increase the probability of transplant while reducing both time and mortality on the waiting list at the same time.
Pediatric intestinal transplantation registers a low indication but involves strict requirements that outline a very uncommon donor in our country which, together with the absence of alternatives that outweigh the impact of these difficulties, penalizes the chances of transplant for these patients.
El modelo organizativo español de donación y trasplante ha hecho posible que España registre de forma continuada desde principios de la década de los 90 la máxima tasa de donación a nivel mundial —superando los 35 donantes pmp1. Como consecuencia directa, es posible realizar cada año en nuestro país entre 1.000 y 1.100 trasplantes hepáticos, alcanzando una tasa de 23 procedimientos pmp, entre las más altas registradas a nivel internacional2,3. De ellos, el trasplante hepático pediátrico representa, con una media de 60 trasplantes anuales, el 5% de la actividad realizada en el ámbito nacional.
Cabe destacar que el trasplante hepático pediátrico es un procedimiento infrecuente tanto por la baja incidencia de las patologías que dan lugar a su indicación como por la decreciente disponibilidad de donantes cuyo perfil se adecue a los receptores en lista de espera, dado su progresivo envejecimiento. Este hecho se pone de manifiesto al analizar el incremento experimentado en nuestro país por la edad media de los donantes, que prácticamente se ha duplicado, al pasar de 36 a 60 años durante las 2 últimas décadas. En este sentido, los datos de 2014 revelan que solo el 1,5% de los donantes registrados en España eran menores de 15 años1. La comorbilidad presente en los donantes actuales asociada a la evolución descrita dificulta la adecuación donante-receptor con un impacto negativo de mayor magnitud en la población infantil.
Con objeto de paliar las repercusiones negativas derivadas de las peculiaridades del trasplante hepático pediátrico, el Consejo Interterritorial del Sistema Nacional de Salud considera CSUR (Centros, Servicios y Unidades de Referencia) a los centros que lo llevan a cabo. Esta consideración tiene como objetivo garantizar la equidad en el acceso independientemente del lugar de residencia dando una atención de calidad, a las personas con patologías complejas e infrecuentes que requieren una elevada especialización profesional que exige la concentración de casos y recursos sanitarios.
Indicación de trasplante y gestión de lista de esperaLa indicación de trasplante hepático pediátrico se realiza ante una enfermedad hepática grave no susceptible de otro tratamiento eficaz, cuando se ha valorado que el trasplante puede proporcionar mejor supervivencia y calidad de vida que la alternativa de no llevarlo a cabo, para cuya valoración resulta imprescindible asegurar un diagnóstico preciso4,5.
Los buenos resultados en supervivencia postrasplante en niños han modificado la actitud de tratamiento de la hepatopatía infantil grave6,7. En las enfermedades crónicas, el riesgo de mortalidad por la hepatopatía no es el único factor determinante de la decisión de trasplante, sino también la afectación severa de la calidad de vida por una patología no susceptible de otro tratamiento de similar eficacia y suficientemente evolucionada para compensar el riesgo de mortalidad precoz asociado al trasplante.
Es fundamental, por tanto, estimar el riesgo de mortalidad con el objetivo de decidir el momento más adecuado para la realización del trasplante, anticipándose a la previsible aparición de complicaciones graves y, además, con objeto de establecer una priorización entre los pacientes que cada centro gestiona en lista de espera.
Los datos de actividad muestran que en torno al 5% de los pacientes incluidos en lista de espera para trasplante hepático corresponden a pacientes infantiles, porcentaje similar al que representan en el conjunto de la población trasplantada, manteniendo las probabilidades de trasplante pesar de sus dificultades específicas.
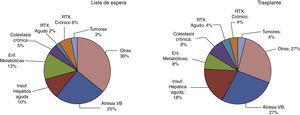
Las enfermedades de la infancia susceptibles de trasplante hepático son principalmente colestasis, enfermedades metabólicas, cirrosis e insuficiencia hepática aguda grave. La principal indicación de trasplante hepático en niños es la atresia de vías biliares, que supone el 25% de los pacientes incluidos en lista de espera en nuestro país. Le siguen en frecuencia de casos en lista de espera las hepatopatías metabólicas y la insuficiencia hepática aguda que suponen, respectivamente, el 13 y 10% de las indicaciones (fig. 1).
Asimismo, si analizamos los trasplantes realizados en 2014 (fig. 1), la atresia de vías biliares se mantiene como la patología más frecuente entre los niños que reciben un trasplante hepático en España (27%) pero la insuficiencia hepática aguda pasa a ser la segunda indicación en frecuencia (18%) por delante de las enfermedades metabólicas (8%). Este cambio se ve favorecido porque estos casos adquieren consideración prioritaria, lo que incrementa sus probabilidades de trasplante. En torno al 3-4% de los trasplantes son realizados como parte del tratamiento de tumores hepáticos no resecables tanto benignos y malignos, constituyendo una proporción similar en lo que a inclusiones en lista de espera se refiere.
En cuanto a la edad de los pacientes pediátricos en lista de espera y trasplante, en torno al 50% de los trasplantes hepáticos se realizan en niños menores de 2 años y en un 25-30% de los casos durante los primeros 12 meses de vida6.
La priorización de los candidatos a trasplante hepático pediátrico entre los pacientes de un centro trasplantador tiene como primera consideración la gravedad clínica. En este ámbito de toma de decisiones, el PELD es el índice comúnmente utilizado, ya que estima el riesgo de mortalidad en los siguientes 3 meses en niños con hepatopatía crónica incluidos en lista de espera para trasplante. Se constituye así en una herramienta de apoyo en la toma de decisiones al posibilitar la asignación de donantes a receptores siguiendo un parámetro objetivo. Asimismo, priorizar a aquellos pacientes en peores condiciones clínicas permite reducir la mortalidad en lista de espera sin que los resultados postrasplante muestren una repercusión negativa a medio y largo plazo8.
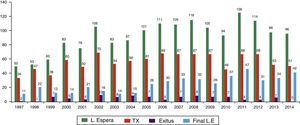
En cuanto a la magnitud de la lista de espera, esta se ha mantenido considerablemente estable a lo largo de la última década situándose en los últimos 5 años —en términos de prevalencia— en torno a los 35 pacientes, con un promedio de 100 pacientes incluidos a lo largo del año de los cuales se trasplantan anualmente una media de 60 pacientes (fig. 2).
Lamentablemente, es preciso señalar que algunos de estos pacientes (6-7 casos anuales) fallecen en lista de espera, aunque en 2014 no se registró ningún fallecimiento, favorecido por el hecho de que las alternativas al trasplante hepático convencional (trasplante hepático de donante vivo y tipo split) permiten incrementar las probabilidades de trasplante de estos pacientes1.
En cuanto el tiempo medio de permanencia en lista de espera para los pacientes pediátricos trasplantados, este se situó en 2014 en 106,8 días, sensiblemente inferior al registrado por la población adulta (136,3 días) gracias de nuevo al impacto positivo que en niños supone el trasplante hepático de donante vivo al incrementar sus opciones de trasplante1.
La gestión comparada de la lista de espera para trasplante hepático se encuentra equilibrada en lo que a población pediátrica se refiere, ya que los niños suponen el 4,5% de los pacientes en lista de espera y una proporción similar de los pacientes finalmente trasplantados, del 4,8%1.
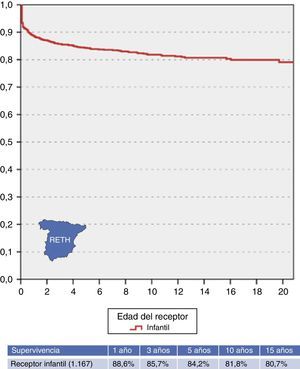
Resultados del trasplante: morbimortalidadActualmente, el trasplante hepático pediátrico constituye una alternativa terapéutica consolidada en la población infantil que ha modificado totalmente las expectativas y calidad de vida de niños con hepatopatía grave, progresiva e irreversible. Esto es valorable analizando los excelentes resultados del mismo, con una tasa de supervivencia al año que se sitúa en torno al 90% y supervivencias superiores al 80% tras 15 años de seguimiento (fig. 3).
En los pacientes pediátricos, sobrevivir el primer año tras el trasplante se ha identificado como un factor asociado a una larga supervivencia, con menos del 10% de mortalidad en los siguientes 10 años (fig. 3). A pesar de la complejidad del curso posterior al trasplante hepático, de la morbilidad asociada y del riesgo siempre presente de complicaciones graves, una vez pasado el postoperatorio inmediato la calidad de vida y el pronóstico de estos pacientes son generalmente muy buenos.
Para valorar la magnitud y la evolución de estos resultados, disponemos de los análisis estadísticos ofrecidos por el Registro Español de Trasplante Hepático (RETH)6 herramienta de gran utilidad al acumular de forma sistemática toda la casuística nacional incorporando información sobre características de donante y receptor, aspectos técnicos o inmunosupresión a corto plazo y, aún más relevante, información actualizada anualmente sobre la evolución de injerto y receptor registrando, si procede, las causas de fallecimiento o retrasplante. Actualmente, el RETH contiene información de los 1.167 trasplantes hepáticos pediátricos realizados en nuestro país hasta diciembre del 2014.
Los datos analizados en el RETH6 (fig. 3) muestran que la supervivencia a los 5-10 años es del 84,2 y el 81,8%, respectivamente, superior a la registrada por los pacientes adultos favorecido por características específicas de la población pediátrica que se constituyen en factores explicativos de esta situación.
A estos resultados han contribuido los progresos en la técnica quirúrgica, una inmunosupresión más eficaz y un mejor control de las infecciones y otras complicaciones postrasplante. El éxito del trasplante en términos generales se fundamenta en aspectos clave, como una correcta indicación, la valoración del momento oportuno para su realización y un apropiado manejo y seguimiento del paciente antes y después del procedimiento9,10.
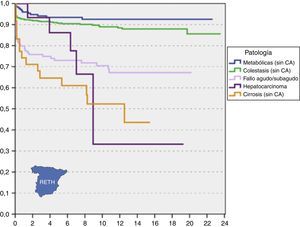
Sin embargo, no todas las patologías que constituyen una indicación para trasplante hepático se asocian al mismo pronóstico ni conllevan los mismos resultados en lo que a morbimortalidad se refiere11-16. Como muestra la figura 4, la indicación del trasplante en receptores infantiles es determinante en la supervivencia, ya que enfermedades metabólicas y colestasis dan lugar a tasas de supervivencia significativamente superiores a cirrosis y tumores, situándose el fallo hepático agudo en un pronóstico intermedio.
Considerable impacto en términos de supervivencia conlleva la existencia de afectación extrahepática. Así, en el 80% de los receptores, la enfermedad afecta exclusivamente al hígado y la recuperación es completa tras el trasplante. Sin embargo, en un 20% de los casos, la enfermedad recidiva en el injerto menoscabando los resultados (como en el caso de hepatitis víricas o autoinmunes, tumores y síndromes con afectación multiorgánica).
Considerando la evolución general en términos de la necesidad de efectuar un retrasplante, es importante señalar la mayor magnitud de esta complicación en población infantil, donde alcanza una tasa del 16,6%, duplicando a la registrada en pacientes adultos, en torno al 8%. Si desglosamos dicha tasa de retrasplante en función de subgrupos de edad pediátrica, no se identifican diferencias significativas, manteniéndose una proporción similar en niños menores de 2 años comparados con el grupo de 2-15 años (tabla 1).
Evolución del primer trasplante en receptores infantiles según indicación
| Evolución del primer trasplante según tipo de patología | ||
|---|---|---|
| Retrasplante | Total | |
| Fallo hepático agudo/subagudo | 28 | 150 |
| 18,7% | 100% | |
| Enfermedades biliares congénitas | 89 | 567 |
| 15,7% | 100% | |
| Síndrome de Alagille | 7 | 58 |
| 12,1% | 100% | |
| Tumores malignos | 5 | 64 |
| 7,8% | 100% | |
| Deficiencia de alfa-1-antitripsina | 5 | 31 |
| 16,1% | 100% | |
| Enfermedad de Byler | 6 | 31 |
| 19,4 | 100% | |
| Global infantil: 0-15 años | 194 | 1.167 |
| 16,6% | 100% | |
| 0-2 años | 103 | 616 |
| 16,7% | 100% | |
| 3-15 años | 91 | 551 |
| 16,5% | 100% | |
Los datos en negrita hacen referencia al número de casos que precisan re-trasplante (el porcentaje que le sigue es sobre el total de trasplantes realizados por esa patología).
Fuente: RETH.
Al valorar las tasas de retrasplante en la población infantil en función de la patología del receptor, destaca el hecho de que las indicaciones más frecuentes registren tasas de retrasplante superiores al 15% (18,7% de los casos trasplantados por insuficiencia hepática aguda y 15,7% en el grupo de enfermedades biliares congénitas). El resto de indicaciones que les siguen en frecuencia presentan tasas superiores al 8%.
Considerando en primer lugar las patologías más frecuentes —enfermedades biliares congénitas y fallo agudo/subagudo—, la principal causa de retrasplante son las complicaciones técnicas, que dan lugar en ambos casos a más del 40% de los retrasplantes y a la mayor mortalidad precoz a la que hacíamos referencia anteriormente. Les siguen en frecuencia el rechazo, que motiva el 33% de los retrasplantes, y el fallo de la función primaria del injerto, causante del 15-20% de los casos. La tabla 2 también muestra los motivos de retrasplante en el resto de patologías, aunque dicha distribución ha de interpretarse de forma prudente dada su baja casuística.
Retrasplante en receptores infantiles según indicación
| Causas de retrasplante tras el primer trasplante en las principales patologías | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Fallo ag/subagudo | Biliares congénitas | Síndrome de Alagille | Tumores malignos | Déficit α1-sntitrips. | Enf. de Byler | |||||||
| n | % | n | % | n | % | n | % | n | % | n | % | |
| Complicación técnica | 11 | 40,7 | 37 | 42 | 1 | 14,3 | 3 | 60 | 3 | 60 | 1 | 16,7 |
| Rechazo | 9 | 33,4 | 29 | 33 | 2 | 28,6 | – | – | 1 | 20 | 2 | 33,3 |
| Fallo función primaria | 4 | 14,8 | 17 | 19,4 | 3 | 42,8 | 1 | 20 | 1 | 20 | 3 | 50 |
| Recidiva enf. de base | 1 | 3,7 | – | – | – | – | – | – | – | – | – | – |
| Hepatitis de novo | – | – | – | – | – | – | – | – | – | – | – | – |
| Tumor de novo | – | – | – | – | – | – | – | – | – | – | – | – |
| Infección | – | – | 1 | 1,1 | – | – | – | – | – | – | – | – |
| Complic. extrahepática | – | – | 1 | 1,1 | – | – | – | – | – | – | – | – |
| Otras | 2 | 7,4 | 3 | 3,4 | 1 | 14,3 | 1 | 20 | – | – | – | – |
| Total | 27 | 100 | 88 | 100 | 7 | 100 | 5 | 100 | 5 | 100 | 6 | 100 |
Hemos referido anteriormente la elevada supervivencia que ofrece el trasplante hepático a la población infantil, al superar el 80% de supervivencia a los 15 años de seguimiento. Sin embargo, a pesar de la reducida tasa de mortalidad, resulta de interés analizar las causas de dan lugar a los fallecimientos registrados con objeto de conocer la previsible evolución de los pacientes trasplantados.
En este sentido, la información registrada en el RETH permite además valorar la distribución de las principales causas de muerte en función de la indicación de trasplante, lo que supone identificar los principales riesgos de los pacientes en función de su patología de base, así como prevenir su aparición o minimizar el impacto de los mismos.
Es preciso señalar que la tasa de supervivencia es significativamente menor en el caso de los trasplantes por fallo hepático agudo debido a la mayor mortalidad en el período postoperatorio. En este grupo de pacientes, la causa más frecuente de fallecimiento es la patología infecciosa —responsable del 26,3% de las defunciones—, seguida de las complicaciones extrahepáticas (23,7%) y del fallo primario del injerto (13,2%) (tabla 3). La información del RETH permite identificar las principales causas de muerte en el resto de las indicaciones.
Mortalidad en receptores infantiles según indicación
| Causas de muerte tras el primer trasplante en las principales patologías | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Fallo sub/agudo | Biliares congénitas | Síndrome de Alagille | Tumores malignos | Déficit α1 antitripsina | Enf. de Byler | |||||||
| n | % | n | % | n | % | n | % | n | % | n | % | |
| Infección | 10 | 26,3 | 15 | 24,6 | 2 | 22,2 | 2 | 8,8 | 1 | 50 | – | – |
| Complicación extrahepática | 9 | 23,7 | 9 | 14,8 | 2 | 22,2 | 1 | 4,3 | – | – | 1 | 100 |
| Recidiva enferm de base | – | – | – | – | – | – | 14 | 60,9 | – | – | – | – |
| Tumor de novo | 1 | 2,6 | 3 | 4,9 | 1 | 11,1 | 1 | 4,3 | – | – | – | – |
| Complicación técnica | 1 | 2,6 | 8 | 13,1 | 1 | 11,1 | 1 | 4,3 | – | – | – | – |
| Muerte perioperatoria | 1 | 2,6 | 6 | 9,8 | 2 | 22,2 | – | – | – | – | – | – |
| Rechazo | 3 | 7,9 | 3 | 4,9 | 1 | 11,1 | – | – | – | – | – | – |
| Fallo función primaria | 5 | 13,2 | 9 | 14,8 | – | – | – | – | 1 | 50 | – | – |
| Hepatitis de novo | – | – | 1 | 1,6 | – | – | – | – | – | – | – | – |
| Fallo multiorgánico | 2 | 5,3 | 1 | 1,6 | – | – | – | – | – | – | – | – |
| Otras | 6 | 15,8 | 6 | 9,8 | – | – | 4 | 17,4 | – | – | – | – |
| Total | 38 | 100 | 61 | 100 | 9 | 100 | 23 | 100 | 2 | 100 | 1 | 100 |
Se incluyen bajo este epígrafe aquellas estrategias encaminadas a incrementar las probabilidades de trasplante y reducir tanto la mortalidad en lista de espera como el tiempo medio de permanencia en la misma, máxime teniendo en cuenta que la evolución anteriormente comentada experimentada en nuestro país por el perfil del donante reduce las probabilidades de trasplante de los candidatos infantiles, por la dificultad de encontrar un donante adecuado para ellos en edad y tamaño.
Conscientes de esta necesidad, en los últimos años se han impulsado diversas estrategias tanto por parte tanto de la Organización Nacional de Trasplantes como de las unidades de trasplante pediátrico que pasan necesariamente por el fomento de otras modalidades de trasplante, como es el caso del trasplante hepático de donante vivo y de la bipartición hepática (trasplante hepático «split»).
Trasplante hepático pediátrico de donante vivoSegún datos del 2014, en nuestro país se realizaron 14 trasplantes hepáticos pediátricos de donante vivo, lo que supone el 30% de todos los realizados a pacientes infantiles. Los últimos 5 años arrojan un promedio de 24 trasplantes hepáticos de donante vivo al año, de los que en torno al 70% se ha llevado a cabo en población infantil. Los análisis del RETH muestran en este sentido cómo la supervivencia de los receptores infantiles tras el trasplante hepático es significativamente superior en el caso del donante vivo.
Esta modalidad precisa aplicar unos criterios de selección de donante muy rigurosos y requiere una habilidad técnica muy precisa para asegurar la obtención de un injerto válido con el mínimo riesgo para el donante. La técnica de implante es más compleja que en un injerto de cadáver lo que puede llegar a condicionar el postoperatorio17-19.
Trasplante hepático «split»La bipartición hepática (trasplante hepático «split») posibilita la obtención de 2 injertos a partir de un donante cadáver. El injerto derecho se implanta en un adulto y el izquierdo en un niño o bien, ocasionalmente, en un adulto de poco peso. Se incrementa así el número de órganos disponibles, sobre todo para niños al ser los receptores de la mayoría de los injertos izquierdos, reduciendo —si su uso se hace extensivo— las necesidades del trasplante pediátrico de donante vivo, dado que una adecuada selección de donante y receptor posibilita la obtención de resultados comparables con los de los trasplantes de hígado completo20-23.
Recientemente, el consenso de los grupos de trasplante ha posibilitado la puesta en marcha del Plan Nacional para el Trasplante Hepático tipo split con el objetivo de implementar una sistemática nacional de utilización máxima de injertos hepáticos, obtenidos mediante la bipartición de un injerto hepático idóneo, para su implante simultáneo en 2 receptores, utilizando los segmentos laterales izquierdos para receptores infantiles y los correspondientes lóbulos derechos ampliados para receptores adultos.
Esta iniciativa busca consolidar un sistema justo y eficaz, que contribuya a paliar la mortalidad infantil en lista de espera de trasplante hepático, sin resultar en perjuicio para los candidatos adultos.
Trasplante intestinal/multivisceralAl igual que sucede en el caso del trasplante hepático pediátrico, el trasplante intestinal/multivisceral se incluye en el grupo de procedimientos designados CSUR con objeto de garantizar la equidad en el acceso y una atención de calidad, en patologías complejas e infrecuentes cuyo manejo requiere una elevada especialización, por lo que precisan la concentración de casos y recursos sanitarios en un número reducido de centros.
En nuestro país, la tasa de indicación de esta modalidad de trasplante extremadamente infrecuente es de 0,28 pmp, siendo de 0,17 pmp la tasa de trasplante. Desde 2009, la media de la actividad trasplantadora en España es de 9 casos al año, lo que da lugar a una probabilidad de trasplante intestinal/multivisceral de los pacientes en lista de espera del 60%.
El análisis de los datos revela que, a pesar de la baja incidencia que registran en nuestro entorno las indicaciones para trasplante intestinal/multivisceral, resulta complejo satisfacer la demanda de esta modalidad de trasplante. Esto se debe a que los criterios de idoneidad del donante requeridos por las unidades de trasplante en cuanto a aspectos específicos: estrecho rango de edad y peso, corta estancia en la Unida de Cuidados Intensivos y ausencia de hipotensión o parada… perfilan un donante muy infrecuente en nuestro país. Estos requisitos, unidos a la ausencia —a diferencia de lo que ocurre en el caso del trasplante hepático— de alternativas que contrarresten el impacto de estas dificultades, no permiten incrementar las probabilidades de trasplante de estos pacientes
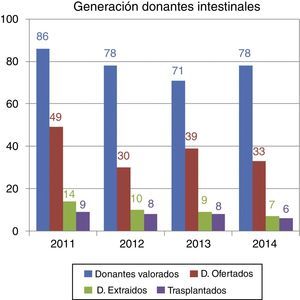
Este escenario se pone de manifiesto al analizar los datos de donación correspondientes al año 2014: de los 78 donantes que fueron valorados para trasplante intestinal/multivisceral solo 33 se ajustaban al perfil requerido para ser ofertados, llevándose a cabo finalmente 6 trasplantes. Evolución similar ha sido la registrada en años previos, como puede constatarse la figura 5.
Como consecuencia de estas dificultades, el tiempo medio en lista de espera para trasplante intestinal/multivisceral asciende a 304 días, aunque es sensiblemente inferior a los 386 días registrados por los pacientes en la franja adulta de edad.
En conclusión, se debe destacar que el trasplante hepático pediátrico es una opción terapéutica que ofrece excelentes resultados en términos de supervivencia y calidad de vida. Sin embargo, el progresivo envejecimiento de los donantes, con un perfil cada vez más alejado de los requerimientos de los pacientes infantiles incluidos en lista de espera, hace necesario impulsar y fortalecer alternativas que incrementen las opciones de supervivencia y calidad de vida de estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.