Evaluar la seguridad y la eficacia de la inducción de tolerancia oral mediante pauta rush en pacientes con alergia a proteínas de leche de vaca persistente.
Material y métodosEstudio prospectivo realizado en 3 hospitales españoles. Se incluyó a niños mayores de 3 años con alergia IgE-mediada a proteínas de leche de vaca, a los que se administraron dosis crecientes de leche durante 5 días, desde 1cc al 1% hasta 200 cc de leche pura en régimen de hospital de día. Las reacciones adversas a la administración de leche fueron registradas y se trataron atendiendo a la clasificación de Clark. Se realizó seguimiento clínico durante 2 años. Se determinaron los niveles de IgE específica basales y a los 6, 12 y 24 meses.
ResultadosSe incluyó a 18 niños (13 varones) entre 3 y 14 años (media 5,96). De 271 dosis administradas, 55 presentaron algún tipo de reacción. Un 84% de las mismas fueron leves. Al finalizar el protocolo, el 100% presentaba algún grado de tolerancia (39% total). Tras 2 años, el 72% de los pacientes realizaba una dieta sin restricción de productos lácteos. Dos pacientes presentaron pérdida de la tolerancia alcanzada. Se observó un descenso significativo de los niveles de IgE específica a leche de vaca y α-lactoalbúmina a los 24 meses, y de caseína a los 6, 12 y 24 meses respecto de los niveles basales.
ConclusionesLa desensibilización mediante pauta rush es una opción terapéutica eficaz y segura a medio plazo para pacientes con alergia persistente a proteínas de leche de vaca.
The aim of this study was to evaluate the safety and efficacy of oral rush desensitization in children with cow milk allergy.
Material and methodsProspective study. We included IgE-mediated cow milk allergy children over 3 years in 3 Spanish hospitals. Increasing doses of cow milk for 5 days from 1cc of 1% to 200 cc of pure milk were administered. Clinical follow-up was conducted and we compared specific IgE levels at onset, 6, 12 and 24 months after desensitization.
ResultsWe included 18 children (13 males) between 3 and 14 years (mean 5.96). A total of 271 doses were administered; there were 55 adverse reactions (84% mild). At the end of the protocol, 100% showed some degree of tolerance (39% total). Full tolerance was achieved in 72% of patients after two years. Two children failed to achieve tolerance. There was a significant decrease in the levels of specific IgE to cow milk and alpha-lactalbumin at 24 months, and to casein at 6, 12 and 24 months, compared to baseline.
ConclusionsOral rush desensitization is a safe and effective therapeutic option for patients with persistent cow milk allergy to medium term.
Las proteínas de la leche de vaca son el primer alérgeno alimentario al que se expone el niño, por lo que suelen ser las responsables de las primeras reacciones alérgicas a alimentos que se manifiestan en los lactantes atópicos.
Los datos que aporta la literatura internacional sobre la incidencia de alergia a leche de vaca son muy variables, debido a diferencias conceptuales, metodología diagnóstica o edades estudiadas, y oscilan entre el 0,3 y el 7,5%1. En uno de los últimos estudios prospectivos realizado en Dinamarca por Host, se observó una incidencia del 1,2% en el primer año de vida2. A nivel nacional, los estudios indican que la incidencia en el primer año de vida oscila entre el 0,36 y el 1,9%3,4. Estas cifras sitúan a la alergia a proteínas de leche de vaca, por detrás del huevo, como la segunda alergia alimentaria más frecuente en la edad pediátrica.
La historia natural de este tipo de alergias en la infancia es favorable. La evolución apunta hacia la aparición espontánea de tolerancia en el medio-largo plazo con desaparición de la clínica5. En la evolución natural de la alergia alimentaria, al periodo de sensibilización clínica le sigue otro de sensibilización asintomática, hasta alcanzar la tolerancia total, que suele acompañarse de la desaparición de los anticuerpos IgE específicos. Esta buena evolución ocurre en los pacientes con alergia a proteínas de leche de vaca hasta en el 83% a los 5 años de vida6.
Si la tolerancia no se alcanza en el tiempo habitual se considera alergia persistente y puede acompañarse de clínica grave, incluso por ingesta de cantidades mínimas del alimento7.
La inducción de tolerancia oral a alimentos (ITOA) consiste en la administración por vía oral del alérgeno alimentario causante de los síntomas, en este caso las proteínas de la leche de vaca, comenzando por cantidades mínimas y progresivamente crecientes hasta alcanzar la ración normal para la edad o la máxima dosis umbral tolerada8. Se trata de establecer una tolerancia inmunológica, reeducando el complejo mecanismo celular y serológico, para corregir una reacción inadecuada a través de un proceso de aumento progresivo de la cantidad umbral tolerada.
Esta opción terapéutica se ha venido utilizando principalmente en pacientes con alergia a proteínas de leche de vaca persistente, los cuales debido a la evolución natural de esta alergia, llegados a un determinado momento era improbable que alcanzaran la tolerancia de forma pasiva. Sin embargo, en los últimos años, se está intentando la inducción de tolerancia oral en edades más tempranas con el objetivo de obtener mejores resultados y minimizar los riesgos9.
No existe una única pauta de ITOA estandarizada. Cada centro, según sus medios disponibles y las características de los pacientes, utiliza una pauta basándose en protocolos propuestos por sociedades científicas o utilizados por otros profesionales. En general, podemos clasificar los distintos protocolos en 3 grandes grupos: según su duración (pautas rush o rápidas, lentas, intermedias o mixtas), según el lugar donde se lleva a cabo (ingresado, con ingreso parcial, con incrementos en hospital, con incrementos en domicilio, incrementos semanales, diarios…) y según reciban o no premedicación para su realización.
En la actualidad, existen ensayos clínicos aleatorizados que demuestran la eficacia a corto plazo de este tipo de pautas, con una tasa de éxito de hasta el 90%10,11; sin embargo, existen algunas dudas respecto a su seguridad. Dado que esta opción terapéutica se viene aplicando desde la última década, no existen estudios que nos permitan conocer los efectos a largo plazo en estos pacientes12.
El objetivo de nuestro estudio fue evaluar la eficacia y la seguridad de una pauta de desensibilización tipo rush en pacientes con alergia a proteínas de leche de vaca.
Material y métodosEstudio longitudinal prospectivo multicéntrico en el que participaron 3 hospitales asturianos (Hospital Central de Asturias de Oviedo, Hospital de Cabueñes de Gijón y Hospital San Agustín de Avilés).
Criterios de inclusión: niños mayores de 3 años con alergia a proteína de leche de vaca IgE-mediada definida por presentar IgE específica positiva (> 0,35 kU/l) a leche de vaca, caseína, α-lactoalbúmina o β-lactoglobulina y prueba de exposición controlada al antígeno positiva previa a la desensibilización, salvo en aquellos pacientes con antecedentes de reacción anafiláctica reciente.
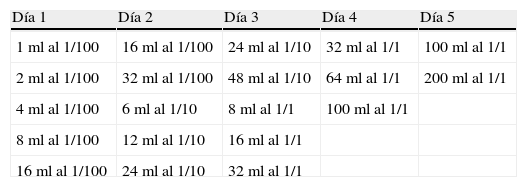
La inducción de tolerancia oral se realizó en 5 días con el paciente ingresado en hospital de día. Se administraron dosis crecientes de leche, desde una dosis inicial de 1cc al 1% (99 cc de agua y 1cc de leche) hasta 200 cc de leche pura. La pauta de administración se recoge en la tabla 1. No se utilizó premedicación en ningún caso.
Protocolo de inducción de tolerancia oral mediante pauta rush
| Día 1 | Día 2 | Día 3 | Día 4 | Día 5 |
| 1 ml al 1/100 | 16 ml al 1/100 | 24 ml al 1/10 | 32 ml al 1/1 | 100 ml al 1/1 |
| 2 ml al 1/100 | 32 ml al 1/100 | 48 ml al 1/10 | 64 ml al 1/1 | 200 ml al 1/1 |
| 4 ml al 1/100 | 6 ml al 1/10 | 8 ml al 1/1 | 100 ml al 1/1 | |
| 8 ml al 1/100 | 12 ml al 1/10 | 16 ml al 1/1 | ||
| 16 ml al 1/100 | 24 ml al 1/10 | 32 ml al 1/1 |
Se registraron todas las reacciones adversas acontecidas durante la administración de las diferentes dosis. Para cuantificar su gravedad se utilizó la clasificación de Clark (tabla 2)13. Si al administrar alguna dosis los pacientes presentaban reacciones adversas leves (exantema, urticaria, alergia oral, rinitis…), se continuaba con los incrementos, mientras que si las reacciones eran severas (angioedema, broncoespasmo severo, shock…), se suspendía la prueba y se reiniciaba al día siguiente con la dosis inmediatamente inferior a la que desencadenó el evento.
Clasificación de Clark de las reacciones adversas alérgicas
| Gravedad | Manifestaciones clínicas |
| 1. Leve | Lesiones cutáneas localizadas (habones, eritema, angioedema o prurito oral) |
| 2. Leve | Lesiones cutáneas generalizadas |
| 3. Leve | Grado 1 o 2 asociando rinoconjuntivitis o síntomas gastrointestinales |
| 4. Moderado | Dificultad respiratoria alta o baja leve-moderada |
| 5. Severo | Dificultad respiratoria severa o síntomas sistémicos (hipotensión, pérdida de conciencia) |
Se consideró que los pacientes desarrollaban tolerancia total cuando eran capaces de tolerar al menos 6.600mg de proteína de leche de vaca al día (equivalente a la contenida en 200 cc de leche entera) y tolerancia parcial cuando eran capaces de tolerar cantidades inferiores sin presentar clínica.
Se cuantificaron los niveles de IgE específica a leche de vaca, caseína, α-lactoalbúmina y β-lactoglobulina. Se realizó una determinación basal previa al inicio del protocolo y posteriormente a los 6, 12 y 24 meses tras la finalización del mismo.
Los datos recogidos se analizaron mediante el programa Statistical Package for the Social Sciences (SPSS) versión 15.0. Se aplicaron técnicas descriptivas básicas, expresando los resultados como mediana y el rango entre paréntesis. Para la comparación de los niveles de IgE específica previos a la desensibilización, a los 6, 12 y 24 meses se aplicó el test de Wilcoxon. Se consideraron significativos valores de p<0,05.
ResultadosSe incluyó a 18 pacientes (13 varones), con edades comprendidas entre los 3 y 14 años (media±desviación estándar 5,96±0,75 años). Un 82% tenía antecedentes personales de asma, el 27% sensibilización concomitante a neumoalérgenos y un 33% a otros trofoalérgenos. Dos pacientes tenían antecedentes de reacción anafiláctica secundaria a la ingesta accidental de leche.
Los niveles de IgE específica, expresados como mediana y rango entre paréntesis, previos a la realización de la desensibilización fueron: α-lactoalbúmina 2,28 (0,4-42) kU/l, β-lactoglobulina 0,85 (0,12-15) kU/l, caseína 6,33 (0,34-100) kU/l y leche de vaca 5,80 (0,82-168) kU/l. El 83% de los pacientes presentaron algún tipo de reacción adversa tras recibir la dosis correspondiente, todas ellas en los 30 min posteriores a su ingesta. Se observaron reacciones adversas en un 20,3% de las 271 dosis administradas (55 en total). La gran mayoría de las reacciones observadas fueron leves (un 84% tipo 1-3 de la clasificación de Clark). En una de las dosis se produjo una reacción anafiláctica. Se administraron antihistamínicos en 47 ocasiones, corticoides en 7, salbutamol nebulizado en 12 y adrenalina intramuscular en una ocasión.
Al finalizar el protocolo, todos los pacientes alcanzaron algún grado de tolerancia (39% total, 61% parcial). La cantidad media tolerada fue de 103±77 (5-200) ml de leche pura. Los pacientes con tolerancia parcial recibían diariamente en el domicilio la última dosis que fueron capaces de tolerar al quinto día de la ITOA y se realizaron incrementos semanales en el hospital siguiendo el mismo protocolo de actuación (tabla 1). Tras 2 años de seguimiento, la tolerancia fue de 149±71 (0-200) ml de leche pura y el 72% de los pacientes realizaban una dieta sin restricción de productos lácteos.
Dos pacientes perdieron la tolerancia que habían adquirido. El primero, a los 2 meses de la finalización del protocolo comenzó con síntomas de alergia oral, así como vómitos y dolor abdominal (Clark 1-3), por lo que se disminuyó progresivamente la ingesta de leche hasta su suspensión total a los 12 meses. Sus niveles medios de IgE específica a leche de vaca y caseína descendieron de forma significativa a los 6 y 12 meses para posteriormente elevarse a los 2 años de la ITOA. El segundo, tras finalizar el protocolo, no continuó en su domicilio con la dosis diaria de leche recomendada, cuando se intentó reintroducirla en el hospital sufrió una reacción anafiláctica y no volvió intentar la desensibilización.
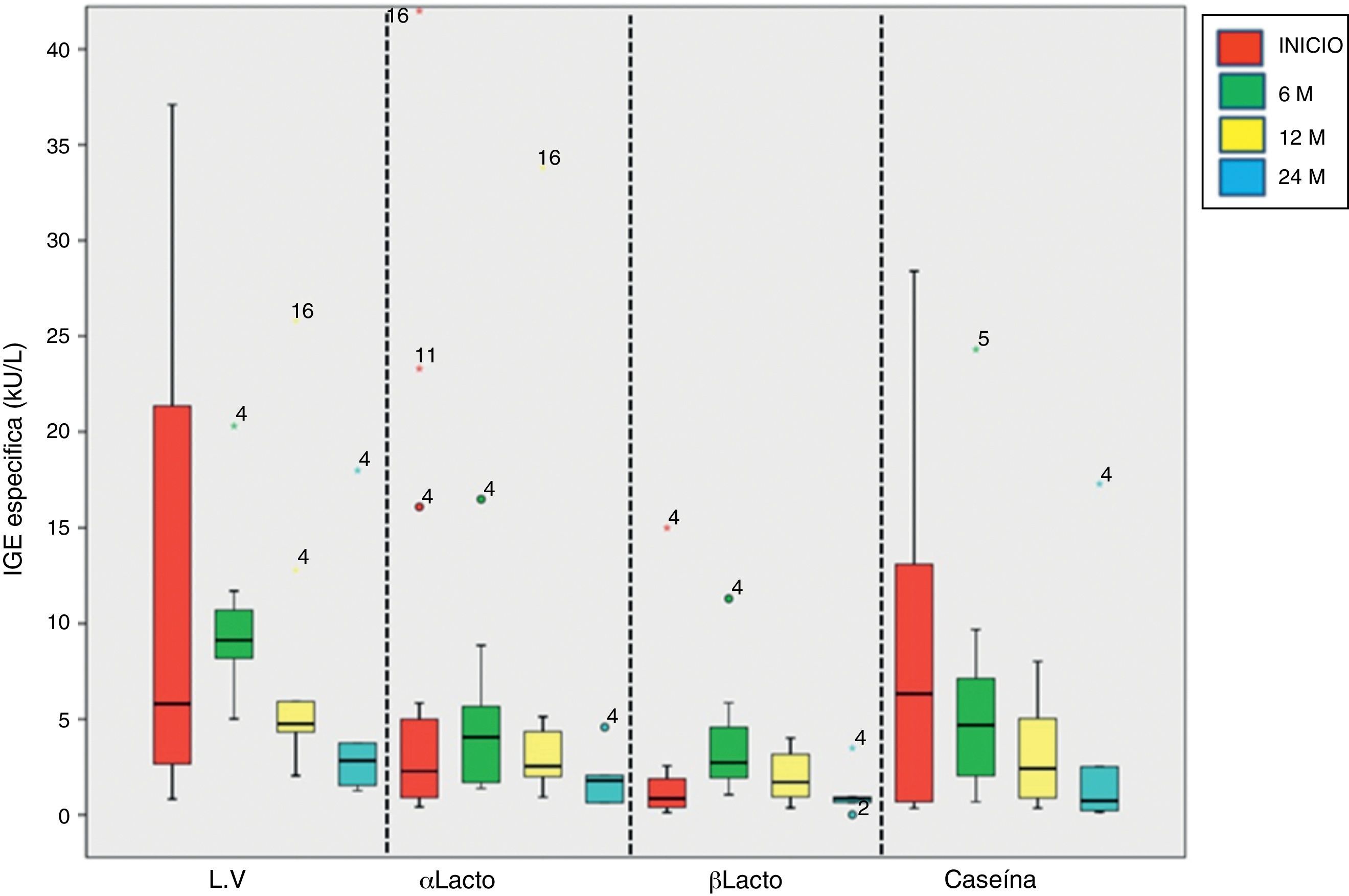
Los niveles de IgE específica a leche de vaca y α-lactoalbúmina a los 24 meses presentaron un descenso significativo respecto al inicio de la desensibilización: 2,83 (1,26-18) kU/l (p=0,043) y 1,79 (0,62-4,58) kU/l (p=0,043), respectivamente. Los niveles de caseína fueron significativamente menores a los 6, 12 y 24 meses de la desensibilización: 4,69 (0,68-24,30) kU/l (p=0,028), 2,42 (0,35-8,02) kU/l (p=0,012) y 0,73 (0,14-17,30) kU/l (p=0,043). No se encontraron diferencias en los niveles de β-lactoglobulina. Los niveles séricos de IgE específica a proteínas de leche de vaca se muestran en la figura 1.
Niveles séricos de IgE específica a proteínas de leche de vaca al inicio y a los 6, 12 y 24 meses tras la desensibilización. Los bordes superior e inferior de las cajas corresponden a los percentiles 75 y 25, la línea central que las divide indica la mediana y los bigotes, los límites superior e inferior.
LV: leche de vaca; m: meses; αlacto: α-lactoalbúmina; βlacto: β-lactoglobulina.
La inducción de tolerancia oral a alimentos se empezó a realizar de forma mayoritaria en la última década. Los resultados de los estudios publicados hasta la fecha son bastante esperanzadores, con una tasa de éxito a corto plazo de entre el 40 y el 90%10,11,14, cifras similares a nuestro estudio, donde todos los pacientes alcanzaron algún grado de tolerancia tras la finalización del protocolo de inducción y hasta el 89% tras 2 años de seguimiento. Sin embargo, todavía existen muchas cuestiones sin resolver, principalmente relacionadas con la seguridad y las complicaciones a medio y largo plazo de esta nueva opción terapéutica.
La aparición de síntomas de gravedad variable durante el procedimiento, así como la necesidad de repetir dosis, es prácticamente constante en todos los protocolos utilizados para la inducción de tolerancia oral. La mayor parte de estos síntomas no son graves y generalmente no requieren medicación o es suficiente con la administración de antihistamínicos orales. Este patrón se repite en nuestra serie, donde más de la mitad de nuestros pacientes sufrió algún tipo de reacción, siendo la mayoría de ellas leves.
Por otra parte, en las series publicadas hasta la fecha, un porcentaje no desdeñable de pacientes (5-15%) presentó reacciones severas y requirió la administración de adrenalina por vía intramuscular tanto en el ámbito hospitalario, como en el domicilio11,14. Barbi et al.15 utilizaron una pauta rush inicial hospitalaria con incrementos en el domicilio en 132 pacientes con alergia a proteínas de leche de vaca severa (IgE específica>100kU/l). En dicha serie, el 64% de los pacientes presentó algún tipo de reacción en el domicilio, siendo el 27% de ellas secundarias al incremento de la fórmula, requiriendo la administración de adrenalina un 4% de los pacientes. En nuestro estudio, solamente un paciente requirió adrenalina y apenas se produjeron reacciones en el domicilio. La pauta rush realizada íntegramente en el hospital disminuye la probabilidad de reacciones en el domicilio, reduciéndose a aquellos casos en los cuales se produzca un fracaso de la inducción de la tolerancia o bien sean desencadenadas por ejercicio físico intenso o infección, dado que los incrementos siempre se realizan en medio hospitalario.
Se necesitan más estudios para conocer si este riesgo se asemeja al de sufrir una reacción severa tras la ingesta accidental en pacientes que no reciban tratamiento mediante desensibilización. Por lo tanto, es muy importante estrechar las medidas de vigilancia en estos pacientes, educar a la familia y a ellos mismos sobre el reconocimiento y el tratamiento de los síntomas, no realizar ejercicio físico en las 3 horas siguientes a la toma diaria de leche, así como disminuir la cantidad coincidiendo con cuadros infecciosos y aumentarla una vez superado estos16.
Se debe disponer de un servicio de atención continuada para prestar asistencia a los pacientes y utilizar protocolos de desensibilización en los que al menos las fases iniciales y los incrementos se lleven a cabo en ámbito hospitalario y en unidades con personal entrenado y medios suficientes que permitan controlar las reacciones graves que pudieran surgir durante el proceso.
Los mecanismos inmunológicos que explican el fenómeno de la inducción de la tolerancia oral todavía son desconocidos. Los valores de IgE específica, junto con la edad y los antecedentes personales de asma grave o reacción anafiláctica, son circunstancias que debemos tener en cuenta a la hora de plantearnos un tratamiento mediante desensibilización oral. Los 3 pacientes con niveles superiores a 30 kU/l (clase 4-5) de IgE específica al inicio del protocolo fueron aquellos que nos plantearon mayores dificultades; 2 de ellos a pesar de completar el protocolo, perdieron progresivamente la tolerancia adquirida por distintas razones y el otro presentó una reacción anafiláctica durante la inducción, alcanzando finalmente una tolerancia de 50 cc de leche entera tras 2 años de seguimiento.
Los valores de IgE específica tienden a bajar muy lentamente, permaneciendo semejantes o superiores al alcanzar la cantidad máxima tolerada y disminuir posteriormente a lo largo de los siguientes 12-18 meses17,18. En nuestro estudio, con un seguimiento de 2 años, observamos un descenso a los 12 y 24 meses de todos los niveles de IgE específica, salvo los de β-lactoglobulina. Si analizamos los niveles de IgE en el paciente con pérdida de tolerancia, observamos cómo durante los 12 primeros meses, mientras continuaba con el tratamiento, los niveles descendieron progresivamente; sin embargo, el paciente tenía reacciones frecuentes a pesar de disminuir la dosis diaria de leche. Tras suspender el tratamiento, los niveles de α-lactoalbúmina y caseína volvieron a elevarse. Por lo tanto, las IgE no nos fueron de utilidad para distinguir en qué paciente fracasó la inducción de tolerancia oral. El hecho de que los cambios inmunológicos se observaran a posteriori hace pensar que las IgE específicas desempeñan un papel secundario respecto a la tolerancia, siendo un epifenómeno de otro tipo de cambios inmunológicos en relación con las células T reguladoras y las citocinas, cuyo conocimiento y modulación constituyen el objetivo actual de las investigaciones en este terreno.
A pesar de alta tasa de éxito, definido como tolerancia parcial o total tras completar el protocolo de desensibilización, en la literatura se cita algún caso de pérdida de tolerancia tras la suspensión, durante unos meses, del alimento ya tolerado a través de ITOA. Este fenómeno puede ocurrir tanto en la tolerancia natural, como en la inducida19. Meglio et al.18, tras un seguimiento de 4 años, observaron cómo todos los pacientes que habían completado el protocolo de desensibilización mantenían su nivel de tolerancia salvo 3 pacientes, 2 de ellos que por decisión materna decidieron suspender el tratamiento y uno de ellos que, tras un episodio de gastroenteritis vírica, estuvo un mes sin consumir leche y cuando se intentó reintroducirla no pudo debido a la aparición de reacciones tipo urticaria y asma. Esta circunstancia se vuelve a poner de manifiesto en nuestra serie, donde un paciente por error dejó de consumir su dosis diaria de leche que había alcanzado tolerar al finalizar el protocolo y cuando intentamos volver a introducirla el paciente presentó una reacción anafiláctica. Algunos autores16 incluyen en sus protocolos la suspensión sistemática del alimento una vez alcanzada la tolerancia y encuentran hasta un 25% de recaídas. Todos estos hallazgos sugieren que la tolerancia puede no ser permanente.
Se desconoce cuánto tiempo es preciso continuar tomando el alimento para que se mantenga la tolerancia, una recomendación aceptada es la siguiente: durante la etapa de inducción y a lo largo de los primeros 12 meses, se debe garantizar la ingestión diaria de una ración normal (200ml de leche) para asegurar la tolerancia y, posteriormente, se debe incorporar el alimento a la dieta, sin forzar y sin control diario de las cantidades, como en cualquier otro niño.
En los últimos años, se han publicado casos sospechosos20 y confirmados21,22 de trastornos eosinofílicos primarios, principalmente en forma de esofagitis eosinofílica, como causa de fracaso de la inducción de tolerancia oral a alimentos. Se necesitan estudios para confirmar cuál es la verdadera asociación entre ambos procesos. Mecanismos alérgicos mixtos son los responsables de la aparición de los trastornos eosinofílicos primarios, por lo tanto, la alergia no mediada por IgE debería tener un papel en esta asociación. Por otra parte, la ITOA parece modificar la historia natural de la alergia a alimentos, provocando un aumento progresivo de la cantidad umbral tolerada para el desarrollo de determinadas reacciones adversas; sin embargo, la exposición continua al alérgeno a nivel digestivo podría inducir el desarrollo de este tipo de trastornos23.
Somos conscientes de las limitaciones de nuestro estudio principalmente marcadas por la ausencia de grupo control con placebo u otras pautas de inducción de tolerancia oral que no nos permite comparar la eficacia de la pauta rush con otras opciones terapéuticas. A pesar de ello, la nuestra es una de las series más amplias y con mayor seguimiento de niños sometidos a pauta rush en alergia a proteínas de leche de vaca.
Nuestros datos reflejan que la inducción de tolerancia oral a proteínas de leche de vaca mediante una pauta rush, en pacientes con niveles de IgE específica moderados, es segura y eficaz tras 2 años de seguimiento. La pauta rush tiene como principales ventajas la rapidez y la menor probabilidad de reacciones en el domicilio. Es un procedimiento que no puede efectuarse ambulatoriamente por los riesgos que puede comportar. Los niveles de IgE descienden tras 2 años de seguimiento; sin embargo, no parecen predecir la evolución clínica de los pacientes. A pesar de los beneficios de esta nueva opción terapéutica, se necesitan nuevos estudios para tratar de unificar los protocolos de inducción de tolerancia oral, conocer las repercusiones a largo plazo en estos pacientes, así como cuáles son los principales mecanismos que llevan en algunas ocasiones al fracaso de la misma.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.