El rol de la obstrucción al tracto de salida del ventrículo izquierdo (OTSVI) en la miocardiopatía hipertrófica obstructiva (MCHO) debe concretarse aún en pediatría, pero se considera al menos un factor menor o modificador de riesgo de muerte súbita, siendo su control y el de la sintomatología asociada uno de los objetivos principales del tratamiento de estos pacientes1. Se recomienda tratar la OTSVI en todos los pacientes sintomáticos, y aquellos asintomáticos cuyo gradiente de presión pico (GP) del tracto de salida del ventrículo izquierdo es superior a 25mmHg en reposo, con el objetivo de mantenerlo inferior a 50mmHg1. Entre las medidas terapéuticas se encuentran la miectomía septal quirúrgica y la ablación septal alcohólica percutánea, sin embargo, la experiencia con estas intervenciones en pediatría es limitada, siendo el tratamiento farmacológico el primer escalón terapéutico2. El fármaco de elección es un betabloqueante a dosis mínimas equivalentes a 6mg/kg/día de propranolol2. Sin embargo, es relativamente frecuente que estén contraindicados, aparezcan efectos secundarios, o no sean efectivos a las dosis máximas toleradas, siendo necesario cambiar o asociar fármacos de segunda línea. Aunque los antagonistas del calcio son la primera alternativa en adultos, su uso en MCHO pediátrica es limitado, sobre todo en lactantes menores de un año, donde se han descrito reacciones adversas graves2. Además, podrían ser incluso contraproducentes en casos con OTSVI, dado su efecto vasodilatador periférico.
La disopiramida es un antiarrítmico de clase IA de administración oral, que disminuye la excitabilidad y la velocidad de conducción miocárdicas, teniendo además efectos anticolinérgicos, vasoconstrictores periféricos e inotrópicos negativos. Su eficacia en el control de la OTSVI se debe especialmente a estas 2 últimas características, siendo superior en estudios de comparación directa con otros fármacos para este objetivo2. Su eficacia y seguridad en adultos como tratamiento adyuvante a betabloqueantes o verapamilo está ampliamente demostrada. Sin embargo, la evidencia científica del uso de disopiramida en MCHO pediátrica es escasa. Östman-Smith utilizó disopiramida en 10 casos (edad media 9 años) en una cohorte de 66 niños con MCHO durante una media de 8 años, observando mayor supervivencia en este grupo con buena tolerancia3. Todos eran casos de MCHO severa, pero no siempre se indicó para controlar la OTSVI, sino como antiarrítmico. Además, todos los casos asociaban tratamiento con betabloqueantes a altas dosis, no pudiendo establecer un beneficio claro sobre la supervivencia de la disopiramida per se. ÓConnor et al. publican recientemente una serie de 9 casos (edad media 5,6 años; 4 menores de un año) donde asocian disopiramida a betabloqueantes o calcioantagonistas con el objetivo de controlar la OTSVI, demostrando un porcentaje en la reducción de GP mediana del 58%4. Sin embargo, fue necesario suspender el tratamiento en 6 casos en 2,5 años de seguimiento, sólo uno por efectos secundarios (emesis). El resto se suspendió por necesidad de miectomía (4) o de trasplante cardiaco (1), sugiriendo que la eficacia para el control a largo plazo de OTSVI no se mantiene en el tiempo. El resto de publicaciones se limita a casos clínicos aislados, siempre como tratamiento de rescate en casos resistentes a otros fármacos5,6.
Nuestra experiencia con disopiramida en MCHO pediátrica es similar (tabla 1). Presentamos 4 casos tratados en los que indicó por clínica de insuficiencia cardíaca y ecocardiografía con OTSVI, movimiento sistólico anterior con insuficiencia mitral y dilatación de aurícula izquierda secundaria, no controlada por betabloqueantes a dosis altas, presentando 2 de los pacientes efectos secundarios a dichas dosis (broncoespasmos graves y trastornos del sueño). Destacamos el rápido control clínico y ecocardiográfico de nuestros pacientes en las primeras 48h de tratamiento, incluso en un caso de shock cardiogénico secundario a la OTSVI en un lactante, sin presentar efectos secundarios graves a las dosis utilizadas (10-20mg/kg/día), permitiendo mantener el control del gradiente y la clínica a largo plazo, retrasando una posible miectomía e incluso disminuir la dosis de betabloqueantes hasta desaparecer sus efectos secundarios. La principal limitación del estudio son su carácter retrospectivo con muestra pequeña y heterogénea, y la ausencia de un grupo control (tabla 2).
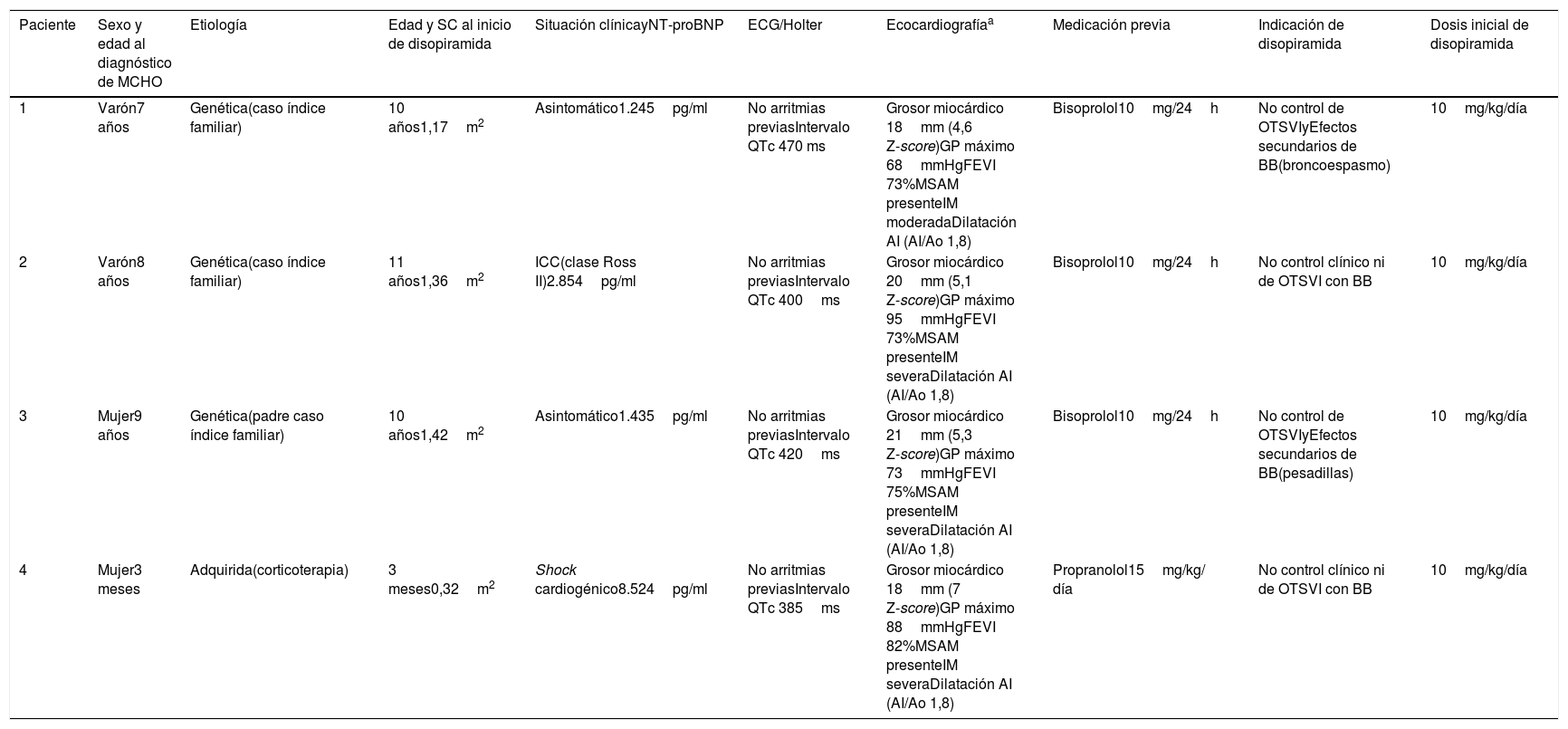
Características de los pacientes pediátricos tratados con disopiramida por MCHO en nuestro centro entre los años 2015-2019. Se describe la situación previa al inicio del tratamiento con disopiramida
| Paciente | Sexo y edad al diagnóstico de MCHO | Etiología | Edad y SC al inicio de disopiramida | Situación clínicayNT-proBNP | ECG/Holter | Ecocardiografíaa | Medicación previa | Indicación de disopiramida | Dosis inicial de disopiramida |
|---|---|---|---|---|---|---|---|---|---|
| 1 | Varón7 años | Genética(caso índice familiar) | 10 años1,17m2 | Asintomático1.245pg/ml | No arritmias previasIntervalo QTc 470 ms | Grosor miocárdico 18mm (4,6 Z-score)GP máximo 68mmHgFEVI 73%MSAM presenteIM moderadaDilatación AI (AI/Ao 1,8) | Bisoprolol10mg/24h | No control de OTSVIyEfectos secundarios de BB(broncoespasmo) | 10mg/kg/día |
| 2 | Varón8 años | Genética(caso índice familiar) | 11 años1,36m2 | ICC(clase Ross II)2.854pg/ml | No arritmias previasIntervalo QTc 400ms | Grosor miocárdico 20mm (5,1 Z-score)GP máximo 95mmHgFEVI 73%MSAM presenteIM severaDilatación AI (AI/Ao 1,8) | Bisoprolol10mg/24h | No control clínico ni de OTSVI con BB | 10mg/kg/día |
| 3 | Mujer9 años | Genética(padre caso índice familiar) | 10 años1,42m2 | Asintomático1.435pg/ml | No arritmias previasIntervalo QTc 420ms | Grosor miocárdico 21mm (5,3 Z-score)GP máximo 73mmHgFEVI 75%MSAM presenteIM severaDilatación AI (AI/Ao 1,8) | Bisoprolol10mg/24h | No control de OTSVIyEfectos secundarios de BB(pesadillas) | 10mg/kg/día |
| 4 | Mujer3 meses | Adquirida(corticoterapia) | 3 meses0,32m2 | Shock cardiogénico8.524pg/ml | No arritmias previasIntervalo QTc 385ms | Grosor miocárdico 18mm (7 Z-score)GP máximo 88mmHgFEVI 82%MSAM presenteIM severaDilatación AI (AI/Ao 1,8) | Propranolol15mg/kg/ día | No control clínico ni de OTSVI con BB | 10mg/kg/día |
AI: aurícula izquierda; AI/Ao: índice aurícula izquierda/aorta; Ao: aorta; BB: betabloqueantes; FEVI: fracción de eyección de ventrículo izquierdo; GP: gradiente pico en tracto de salida de ventrículo izquierdo; ICC: insuficiencia cardiaca congestiva; IM: insuficiencia mitral; MCHO: Miocardiopatía hipertrófica obstructiva; MSAM: movimiento sistólico anterior de la válvula mitral; OTSVI: obstrucción de tracto de salida de ventrículo izquierdo; SC: superficie corporal.
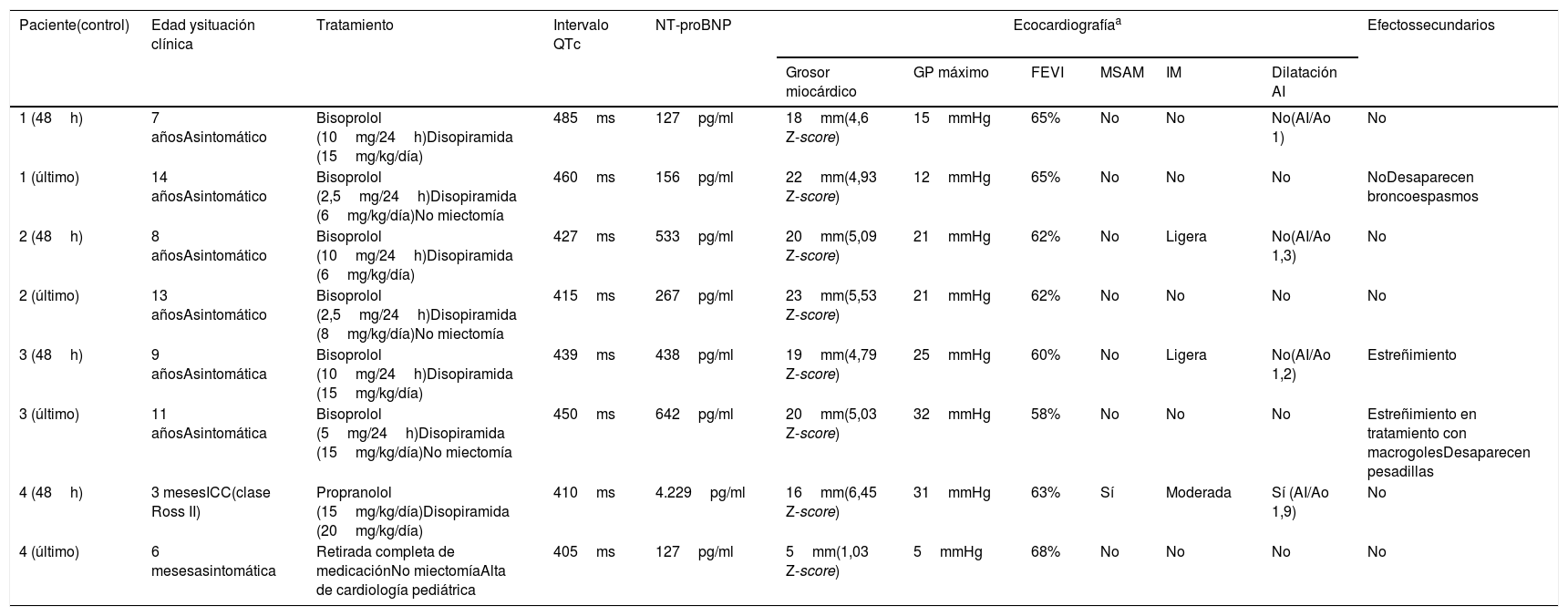
Evolución de los casos tratados con disopiramida. Se describe la situación tras 48 h del inicio del tratamiento y en el último control realizado
| Paciente(control) | Edad ysituación clínica | Tratamiento | Intervalo QTc | NT-proBNP | Ecocardiografíaa | Efectossecundarios | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Grosor miocárdico | GP máximo | FEVI | MSAM | IM | Dilatación AI | ||||||
| 1 (48h) | 7 añosAsintomático | Bisoprolol (10mg/24h)Disopiramida (15mg/kg/día) | 485ms | 127pg/ml | 18mm(4,6 Z-score) | 15mmHg | 65% | No | No | No(AI/Ao 1) | No |
| 1 (último) | 14 añosAsintomático | Bisoprolol (2,5mg/24h)Disopiramida (6mg/kg/día)No miectomía | 460ms | 156pg/ml | 22mm(4,93 Z-score) | 12mmHg | 65% | No | No | No | NoDesaparecen broncoespasmos |
| 2 (48h) | 8 añosAsintomático | Bisoprolol (10mg/24h)Disopiramida (6mg/kg/día) | 427ms | 533pg/ml | 20mm(5,09 Z-score) | 21mmHg | 62% | No | Ligera | No(AI/Ao 1,3) | No |
| 2 (último) | 13 añosAsintomático | Bisoprolol (2,5mg/24h)Disopiramida (8mg/kg/día)No miectomía | 415ms | 267pg/ml | 23mm(5,53 Z-score) | 21mmHg | 62% | No | No | No | No |
| 3 (48h) | 9 añosAsintomática | Bisoprolol (10mg/24h)Disopiramida (15mg/kg/día) | 439ms | 438pg/ml | 19mm(4,79 Z-score) | 25mmHg | 60% | No | Ligera | No(AI/Ao 1,2) | Estreñimiento |
| 3 (último) | 11 añosAsintomática | Bisoprolol (5mg/24h)Disopiramida (15mg/kg/día)No miectomía | 450ms | 642pg/ml | 20mm(5,03 Z-score) | 32mmHg | 58% | No | No | No | Estreñimiento en tratamiento con macrogolesDesaparecen pesadillas |
| 4 (48h) | 3 mesesICC(clase Ross II) | Propranolol (15mg/kg/día)Disopiramida (20mg/kg/día) | 410ms | 4.229pg/ml | 16mm(6,45 Z-score) | 31mmHg | 63% | Sí | Moderada | Sí (AI/Ao 1,9) | No |
| 4 (último) | 6 mesesasintomática | Retirada completa de medicaciónNo miectomíaAlta de cardiología pediátrica | 405ms | 127pg/ml | 5mm(1,03 Z-score) | 5mmHg | 68% | No | No | No | No |
AI: aurícula izquierda; AI/Ao: índice aurícula izquierda/aorta; Ao: aorta; BB: betabloqueantes; FEVI: fracción de eyección de ventrículo izquierdo; GP: gradiente pico en tracto de salida de ventrículo izquierdo; ICC: insuficiencia cardiaca congestiva; IM: insuficiencia mitral; MCHO: miocardiopatía hipertrófica obstructiva; MSAM: movimiento sistólico anterior de la válvula mitral; OTSVI: obstrucción de tracto de salida de ventrículo izquierdo; SC: superficie corporal.
En base a nuestra experiencia y la escasa, pero favorable evidencia existente, consideramos que la disopiramida puede constituir una opción terapéutica adecuada como tratamiento adyuvante en casos pediátricos de MCHO con OTSVI no controlada con betabloqueantes, o cuando sea preciso reducir dosis de estos por efectos secundarios, antes de considerar terapias más agresivas como la miectomía septal. Su uso en monoterapia como alternativa a betabloqueantes en casos contraindicados no se ha descrito, pero podría considerarse sobre todo en lactantes menores de un año, incluso en casos críticos como el nuestro, población donde los calcioantagonistas no se recomiendan y donde el tratamiento quirúrgico es de alto riesgo.