Las recomendaciones internacionales del International Liaison Committee on Resuscitation (ILCOR), mediante una revisión exhaustiva de la evidencia disponible en el desarrollo de las medidas de soporte a la transición y de reanimación del recién nacido tras su nacimiento, aportan una guía universal a partir de la cual cada grupo o comité local puede adaptarla a su realidad e idiosincrasia, y elaborar sus propias guías o recomendaciones.
El objetivo de esta revisión es analizar los principales cambios, abordar las controversias generadas desde 2010, contrastarlas con las de otras organizaciones nacionales e internacionales como son la European Resuscitation Council (ERC), American Heart Association (AHA) o la Australian-New Zealand Committee on Resuscitation (ANZCOR). De esta forma, el Grupo de Reanimación Neonatal de la Sociedad Española de Neonatología (GRN-SENeo) consensúa respuestas claras sobre muchas de las preguntas que ofrecen diferentes opciones de actuación, y genera las próximas recomendaciones de nuestro país para el soporte a la transición o la reanimación del recién nacido tras su nacimiento, con seguridad y eficacia.
The International Liaison Committee on Resuscitation (ILCOR) recommendations provide a universal guide of measures to support the transition and resuscitation of newborn after their birth. This guide is expected to be adapted by local groups or committees on resuscitation, according to their own circumstances.
The objective of this review is to analyse the main changes, to discuss several of the controversies that have appeared since 2010, and contrasting with other national and international organisations, such as European Resuscitation Council (ERC), American Heart Association (AHA), or the Australian-New Zealand Committee on Resuscitation (ANZCOR). Thus, the Neonatal Resuscitation Group of the Spanish Society of Neonatology (GRN-SENeo) aims to give clear answers to many of the questions when different options are available, generating the forthcoming recommendations of our country to support the transition and/or resuscitation of a newborn after birth, safely and effectively.
En octubre de 2015, el International Liaison Committee on Resuscitation (ILCOR)1 (tabla 1) actualizó y publicó las normas internacionales de reanimación, tras revisar la evidencia sobre diferentes temas controvertidos. Como en las anteriores recomendaciones del 20102, el GRN-SENeo ha preparado un documento que analiza los principales cambios desde 2010, revisando la evidencia en las opciones de actuación, especialmente en temas controvertidos. Surgen así las actuales recomendaciones en estabilización y reanimación neonatal de nuestro país. Son una extensión de las guías publicadas por el ERC3, AHA4, ANZCOR5. Se aportan algoritmos y unas actuaciones precisas en cada una de las secciones donde hay temas con respuestas abiertas o controvertidas, y va dirigido a profesionales que intervienen en la estabilización del recién nacido (RN) en paritorio.
Delegaciones participantes del ILCOR
| American Heart Association (AHA) |
| European Resuscitation Council (ERC) |
| Heart and Stroke Foundation of Canada (HSFC) |
| Australian and New Zealand Committee on Resuscitation (ANZCOR) |
| Resuscitation Councils of Southern Africa (RCSA) |
| Inter American Heart Foundation (IAHF) |
| Resuscitation Council of Asia (RCA, miembros actuales Japón, Corea, Singapur, Taiwán) |
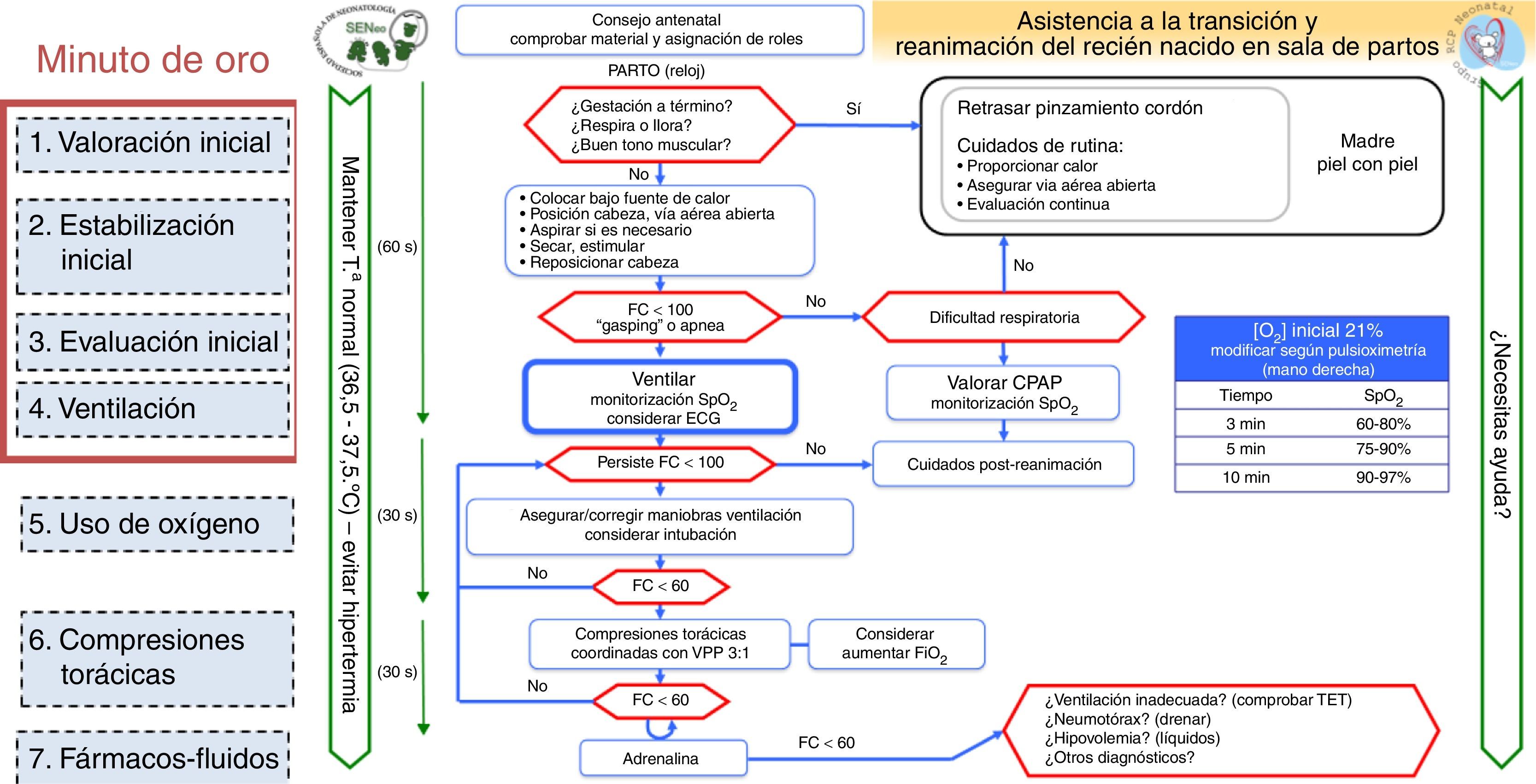
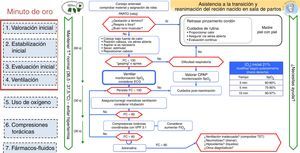
El algoritmo de reanimación neonatal completa de SENeo refleja gráficamente la secuencia de actuación en la reanimación de un RN en paritorio (fig. 1), incorporando aspectos de versiones internacionales.
- •
Del algoritmo del ERC se incorpora el mantenimiento de la temperatura desde el inicio y la petición de ayuda durante el proceso.
- •
De AHA e ILCOR se incluye el «minuto de oro», que comprende medidas de estabilización y evaluación inicial, inicio de ventilación con presión positiva intermitente (VPPI) y monitorización mediante pulsioximetría preductal y ECG.
- •
De ERC y AHA, se incorpora: comunicación con la familia del presumible desarrollo del parto, comprobación del material y asignación de roles del personal (briefing).
- •
Se destaca visualmente el retraso del pinzamiento del cordón en RN que no precisan estabilización.
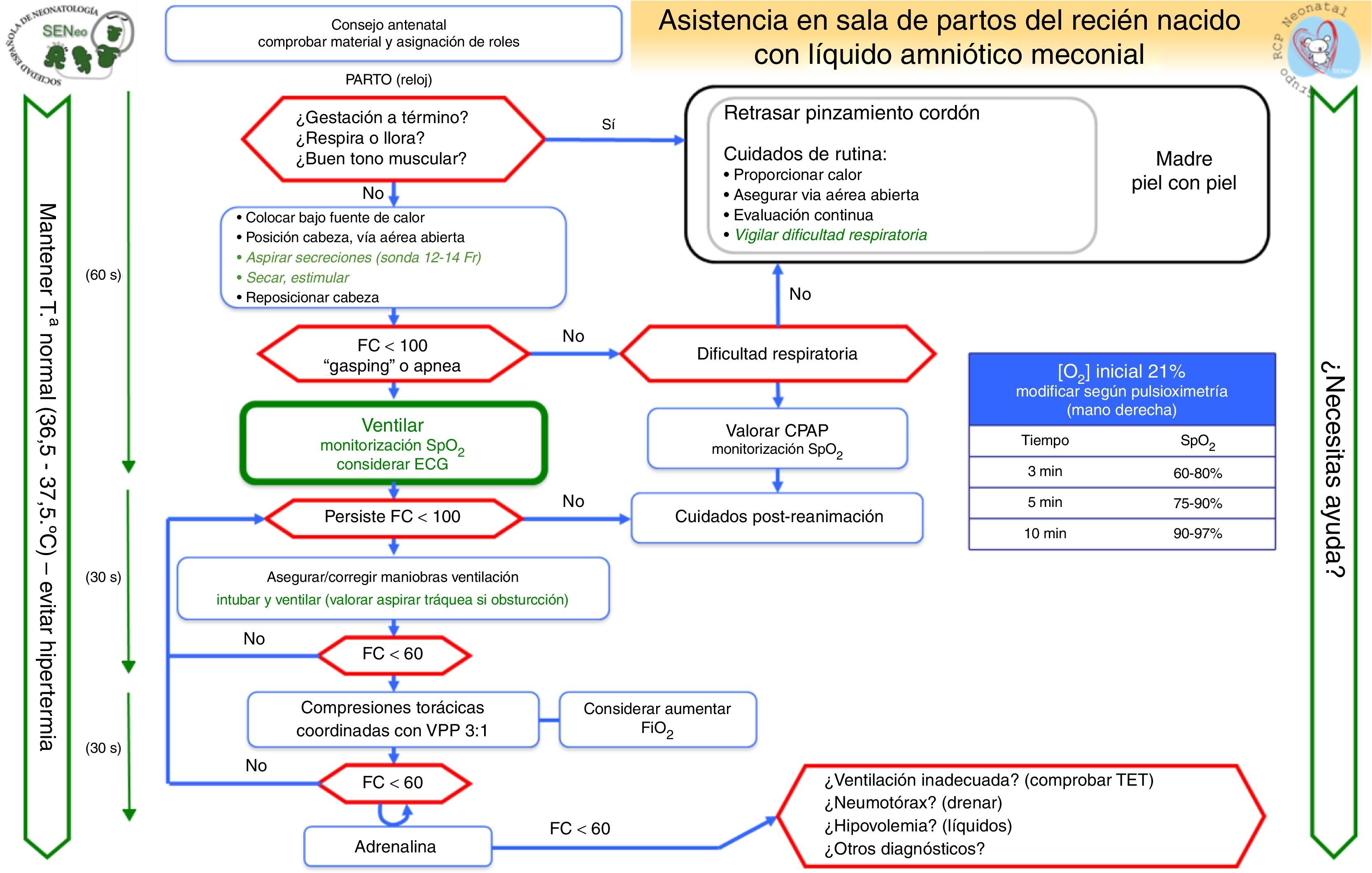
En este artículo, se detallan otros algoritmos realizados por el GRN-SENeo sobre situaciones clínicas especiales: prematuro y RN con líquido amniótico meconial (LAM).
Principales cambios y novedades ILCOR 2015 respecto a 2010Soporte a la transiciónDurante la transición de la vida intrauterina a la extrauterina, el RN puede requerir cuidados de rutina o medidas de estabilización inicial («soporte a la transición»), hecho este que se distingue de las «medidas de reanimación».
Pinzamiento tardío del cordón umbilicalEn el pinzamiento tardío del cordón umbilical (PTC) se aconseja retrasar 30-60 s en RN a término y prematuros que no necesitan reanimación. No hay suficiente evidencia para utilizar el ordeño como alternativa, contraindicándolo en <28 semanas de gestación (SG) por falta de evidencia para la seguridad. Se resalta el «minuto de oro» para realizar los pasos iniciales, evaluar el estado del RN y no retrasar el inicio de la ventilación en caso de precisarla.
Temperatura corporal del recién nacidoSe recomienda mantenerla entre 36,5-37,5°C en RN no asfícticos después de nacer y durante el ingreso.
Sistemas de monitorizaciónSe analiza el ECG para estimar de forma más precoz y precisa la frecuencia cardíaca (FC) y facilitar la toma de decisiones.
Recién nacido con líquido amniótico teñido de meconioEn RN deprimidos no está recomendada de forma rutinaria la intubación y aspiración traqueal: se limita exclusivamente ante sospecha de obstrucción traqueal. El énfasis se dirige a iniciar la ventilación dentro del primer minuto de vida.
Aire/oxígenoEn RN a término se mantiene el uso inicial de aire ambiente. En prematuros de <32 SG, se recomiendan concentraciones bajas de oxígeno si presentan dificultad respiratoria (21 al 30%). Cabe considerar incrementar su concentración, si a pesar de una ventilación efectiva la oxigenación se mantiene en rangos inadecuados6.
Presión positiva continua en la vía aéreaAumenta la evidencia en recomendarla a prematuros de <30 SG que respiran espontáneamente y presentan dificultad respiratoria para prevenir la intubación y la ventilación mecánica.
Presión positiva al final de la espiraciónEl uso de la presión positiva al final de la espiración (PEEP) se recomienda en prematuros ventilados.
Existen muchas controversias en la asistencia inicial del RN: reanimación en el límite de la viabilidad, Apgar 0 a los 10 min de reanimación como predictor de morbimortalidad, monitorización de función respiratoria, capnografía o uso clínico de insuflación sostenida (IS), entre otros, y se proponen diferentes estudios aleatorizados.
Asistencia a la transición y reanimación neonatalLa mayoría de los RN (85%) solo van a precisar cuidados de rutina (PTC y contacto materno «piel con piel»). Ante determinadas situaciones patológicas, la transición feto-neonatal puede comprometerse y desembocar en una situación de asfixia perinatal, manifestándose en el RN en forma de apnea, bradicardia e hipotensión. En este punto nuestra actuación es necesaria mediante la realización de medidas de estabilización inicial. El proceso global representa un verdadero «soporte a la transición del RN» que debe distinguirse de las intervenciones que restauran funciones vitales o «maniobras de reanimación».
Comunicación, anticipación y preparación (recursos humanos y material)Es novedoso mencionar explícitamente3 la planificación de la actuación del equipo reanimador, el asesoramiento prenatal familiar, sus preferencias y su implicación en la toma de decisiones mediante una aproximación pronóstica lo más objetiva y actualizada posible. Este hecho incluye el redireccionamiento del cuidado (redirection of care) y puesta en marcha, si fuera preciso, de medidas de cuidados paliativos perinatales (bienestar, acompañamiento y duelo). Cada hospital debe asumir sus propias capacidades sin que el RN sufra riesgos adicionales.
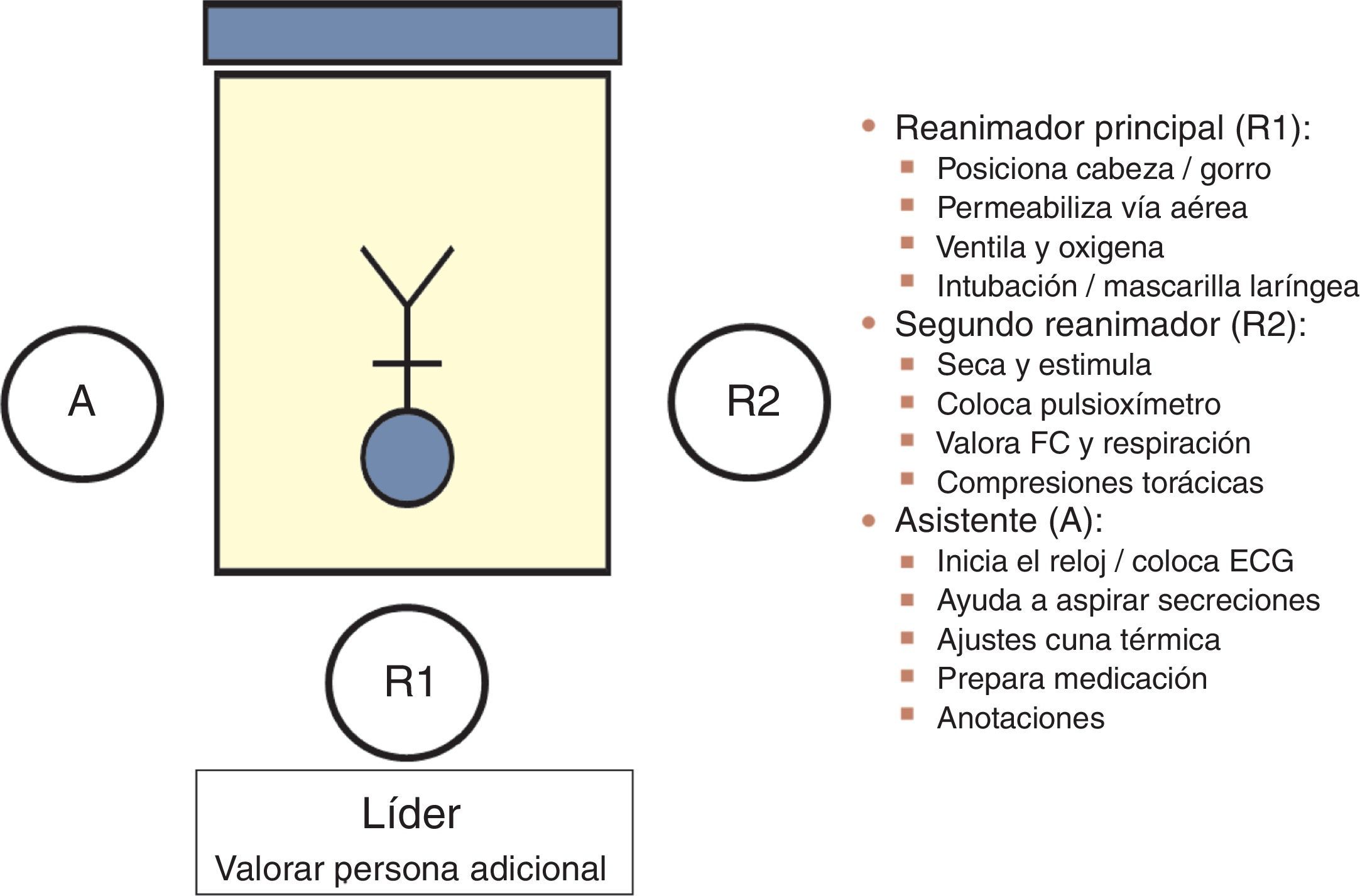
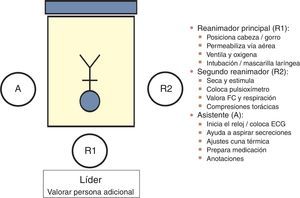
La comunicación entre el equipo obstétrico y neonatal permite «preparar» un entorno seguro: conocer la situación y factores de riesgo (anticipación), preparar el material necesario (check-list), el equipo humano (distribuyendo roles: coordinador y ayudantes) y la valoración global de nuestra actuación mediante análisis reflexivo del tipo debriefing que optimice el trabajo en equipo. El GRN-SENeo propone un esquema de asignación de roles (fig. 2) entre los reanimadores7. Es importante mantener una actitud tranquila, comunicación clara en bucle cerrado y aportaciones abiertas (técnica estructurada SBAR). En cuanto al número de reanimadores, ante un RN de riesgo, al menos uno debe estar entrenado en reanimación neonatal completa y de presencia física. En situaciones de alto riesgo o especiales, deben ser al menos 2 reanimadores y un asistente. La reanimación debería realizarse en el mismo paritorio, con todo el material para resolver cualquier situación de riesgo1.
Acertadamente, el ERC-2015 aborda la atención y planificación del parto domiciliario, a pesar de la variedad entre países. De presencia física se debe incluir un profesional entrenado en reanimación completa y otro en reanimación inicial. Deben existir limitaciones a tales partos (conocidas por los padres), como el riesgo de complicaciones (materna o neonatal) o que la distancia a un centro hospitalario dificulte una adecuada asistencia si surgen complicaciones3.
Evaluación y estabilización inicialTemperaturaLa temperatura del RN sin asfixia tras el nacimiento debe mantenerse entre 36,5 y 37,5°C, hecho muy importante a menor edad gestacional (EG). El procedimiento «piel con piel» con valoración continua del RN es preferible a cualquier otra fuente de calor, al evitar pérdidas de calor de 50-90% y favorecer el vínculo materno.
Retraso del pinzamiento de cordón y ordeño (milking)En RN que no necesitan reanimación se recomienda el PTC (30-60 s)2. No hay datos suficientes que permitan recomendarlo en RN que sí la precisan, ni evidencias para utilizar el ordeño (3 veces, 20cm de cordón umbilical, RN a nivel del introito) como alternativa. El único estudio clínico, publicado recientemente, aleatoriza prematuros de <32 SG nacidos por cesárea, y muestra una mejoría del flujo sistémico tras el ordeño frente al PTC, no presente en nacidos por vía vaginal8. El problema de los estudios de PTC es que no están diseñados ventilando el pulmón primero y pinzando el cordón umbilical después. Katheria et al. describen sus recomendaciones del PTC con ventilación previamente al pinzamiento9. Ensayos clínicos en curso con estabilización pulmonar previamente al PTC y resultados del neurodesarrollo de los realizados, ayudarán en próximas recomendaciones.
Monitorización de la frecuencia cardíacaEl ECG de 3 derivaciones es el método más rápido y preciso para detectar la FC10. No obstante, hay que interpretar con prudencia datos precoces y evitar medidas de reanimación innecesarias, especialmente en prematuros extremos, en los que el pinzamiento inmediato del cordón, previo a la estabilización pulmonar, produce bradicardia transitoria (<100 lpm), que mejora tras la aireación pulmonar11. El uso del ECG complementa la pulsioximetría y la auscultación, sin eliminarlas, para evaluar, respectivamente, oxigenación y ventilación. La recomendaciones ILCOR1 no resuelven el orden de la monitorización; puede establecerse que el segundo reanimador asume las siguientes tareas: auscultación, colocación del pulsioxímetro y posteriormente del ECG para aumentar la precisión de la monitorización.
Ventilación y oxigenaciónAlrededor del 5% de los RN no inician los esfuerzos respiratorios adecuados tras las maniobras de estabilización: se aplican VPPI antes del minuto de vida y se dispone de tiempo adicional en caso de ventilación ineficaz. Un 2% precisarán intubación para optimizarla.
Con base en la FC y en la respiración, tras la estabilización inicial, clasificamos la actuación en el RN (fig. 1)4. No es necesario aspirar secreciones orofaríngeas rutinariamente, solamente si causan obstrucción: sonda de aspiración 8-10 French, presión <100mmHg, 5 s máximo, primero boca y después nariz. Aspiraciones más enérgicas pueden producir retraso en el inicio de la respiración, espasmo laríngeo y bradicardia vagal.
VentilaciónLos parámetros ventilatorios necesarios para establecer una capacidad residual funcional (CRF) efectiva no se han determinado clínicamente. Los dispositivos de monitorización de función respiratoria y capnografía ofrecen información muy valiosa del volumen corriente: pueden optimizar la ventilación, evitar volutrauma o barotrauma y detectar eventos adversos12. Se requieren estudios para determinar el volumen corriente según la EG y poder fijarlo como parámetro objetivo13, adecuando la presión inspiratoria, y así minimizar el daño en la estabilización neonatal.
Se han revisado las diferentes mejoras para establecer una adecuada CRF o volumen pulmonar, y se han abierto debates sobre la monitorización del volumen corriente administrado durante la reanimación de RN prematuros1,14.
Por otro lado, se ha evaluado la eficacia de IS con tiempos inspiratorios prolongados para establecer una mejor CRF en la transición del RN sin respiración espontánea15. Nuestro algoritmo no incluye la IS al no cambiar la incidencia de morbilidades a largo plazo, aumentar la incidencia de neumotórax16 y al faltar una forma de administración estandarizada17 a pesar de que experimentalmente es eficaz15 (su uso se acepta en el contexto de investigación) y de que clínicamente disminuye la intubación y necesidad de ventilación mecánica en las primeras 72 h de vida16.
En neonatos a término con respiración espontánea y distrés respiratorio se propone el uso de presión positiva continua en la vía aérea, aunque faltan datos sobre su eficacia, incluso se ha alertado sobre los peligros de su uso excesivo en esta edad.
DispositivosSegún ILCOR1, no existe evidencia para recomendar un determinado dispositivo ventilatorio (tubo-T vs. diferentes bolsas). Ante la imposibilidad de intubación y tras fracasar la VPPI, la mascarilla laríngea se recomienda para la reanimación de RN de ≥34 SG. Futuros estudios podrían evaluarla como primera interfase, que disminuye la necesidad de intubación18.
OxigenaciónEl uso del pulsioxímetro se establece en todo RN cuya situación clínica prevea necesidad de reanimación o presente cianosis central persistente.
El ERC3 determina los valores diana de oxigenación en el p25 de la SatO2 normal durante los primeros 10min de vida6, similares a AHA4. Un reciente ensayo clínico mostraba mayor mortalidad en el subgrupo de <29 SG reanimado con aire ambiente (16,2%) frente al grupo reanimado con O2 al 100% (6%; p = 0,013)19. Un estudio de cohortes retrospectivo muestra un mayor riesgo de daño neurológico severo o mortalidad en ≤27 SG tras el cambio en 2006 de la práctica de iniciar reanimación con altas concentraciones de O2 (100%) frente a concentraciones intermedias (21-40%)20. Tras las recomendaciones, han surgido otros análisis sobre FiO2 inicial desde otros grupos21,22 para grandes prematuros, así como su regulación tras iniciar la administración de oxígeno. En RN prematuros, ante la falta de ensayos clínicos con muestras representativas, debemos ser cautelosos al iniciar la reanimación con aire ambiente y con los valores diana de SatO2 preductal que determinan los ajustes de FiO2 en ellos. El GRN-SENeo ha fijado el valor mínimo de SatO2 por encima del p15 del nomograma6 en los primeros 5 min de vida.
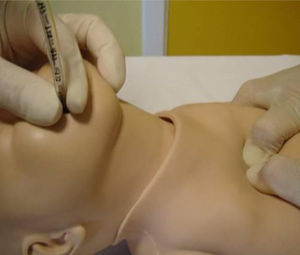
Compresiones torácicasCon relación a la técnica de compresiones torácicas (CT), la posición de los reanimadores respecto al RN debe ser latero-inferior. Nuevos métodos como el pulgar-índice no superan a la de los 2pulgares (fig. 3)1.
Se sigue manteniendo un ratio 3:1 (CT/ventilaciones), por el frecuente origen respiratorio de la bradicardia23. El incremento de oxígeno durante las CT es controvertido. Experimentalmente, altas concentraciones de oxígeno no parecen beneficiosas para restablecer la circulación espontánea y solo en un estudio mejoran la supervivencia, asociando daño neuronal1. Si tras la ventilación efectiva con baja FiO2 es necesario realizar CT, puede ser razonable incrementar dicha FiO2 para optimizar la oxigenación, regulándola guiados por pulsioximetría tras una FC >60/min.
Cuidados posreanimación (temperatura, glucosa)GlucosaSegún la evidencia disponible, no hay datos para recomendar un rango específico de glucemia asociado con menor daño neurológico tras la reanimación por asfixia. Sussman et al. indican un límite inferior de 60mg/dL24.
En estudios con neonatos25 y en experimentales con modelos neonatales asfícticos26 la hipoglucemia se ha asociado con evolución neurológica adversa y menor supervivencia. Diversos estudios determinan que la hiperglucemia en RN hipóxicos no se asocia a un efecto dañino, y que incluso puede tener un efecto protector25,27. No obstante, un estudio reciente con 528 RN de >35 SG muestra un daño en el neurodesarrollo con glucemias elevadas, incluso dentro de rango (47-150mg/dL)28. En RN asfícticos, la administración de glucosa en perfusión debe ser iniciada durante la estabilización para mantener el rango de glucemia entre 47 y 150mg/dL.
Temperatura al ingresoEn niños no asfícticos es un fuerte predictor de morbimortalidad e indicador de calidad en todas las EG, especialmente en prematuros. Hay evidencia de relación dosis efecto sobre la mortalidad, con un aumento del riesgo de al menos el 28% por cada °C por debajo de 36,5°C de temperatura al ingreso29. El nuevo algoritmo refleja mantener la temperatura axilar al ingreso de 36,5 a 37,5°C, evitando hipertermia e hipotermia1.
Cuidados en hipotermia inducidaLas guías internacionales de reanimación neonatal, salvo las de AHA4, no especifican la EG a partir de la cual estaría indicada. Todas coinciden en que en encefalopatía hipoxico isquémica moderada/grave hay que seguir protocolos claramente definidos y consistentes utilizados en los ensayos clínicos aleatorizados. En nuestro medio, desde 2011 (guías de estándares nacionales para neuroprotección30, programas multicéntricos nacionales31), así como metaanálisis y diferentes ensayos clínicos32, indican e incluyen a los RN de ≥35 SG. Su beneficio neuroprotector es tiempo-dependiente, por lo que debe iniciarse hipotermia pasiva entre 33 y 34°C central ante un paciente susceptible33. La hipotermia activa debe iniciarse antes de las 6 h de vida, pero iniciada antes de 3 h de vida marca un cambio en el pronóstico, sobre todo en los casos más graves34. La novedad es que puede ser aplicada en países y entornos con pocos recursos1,3.
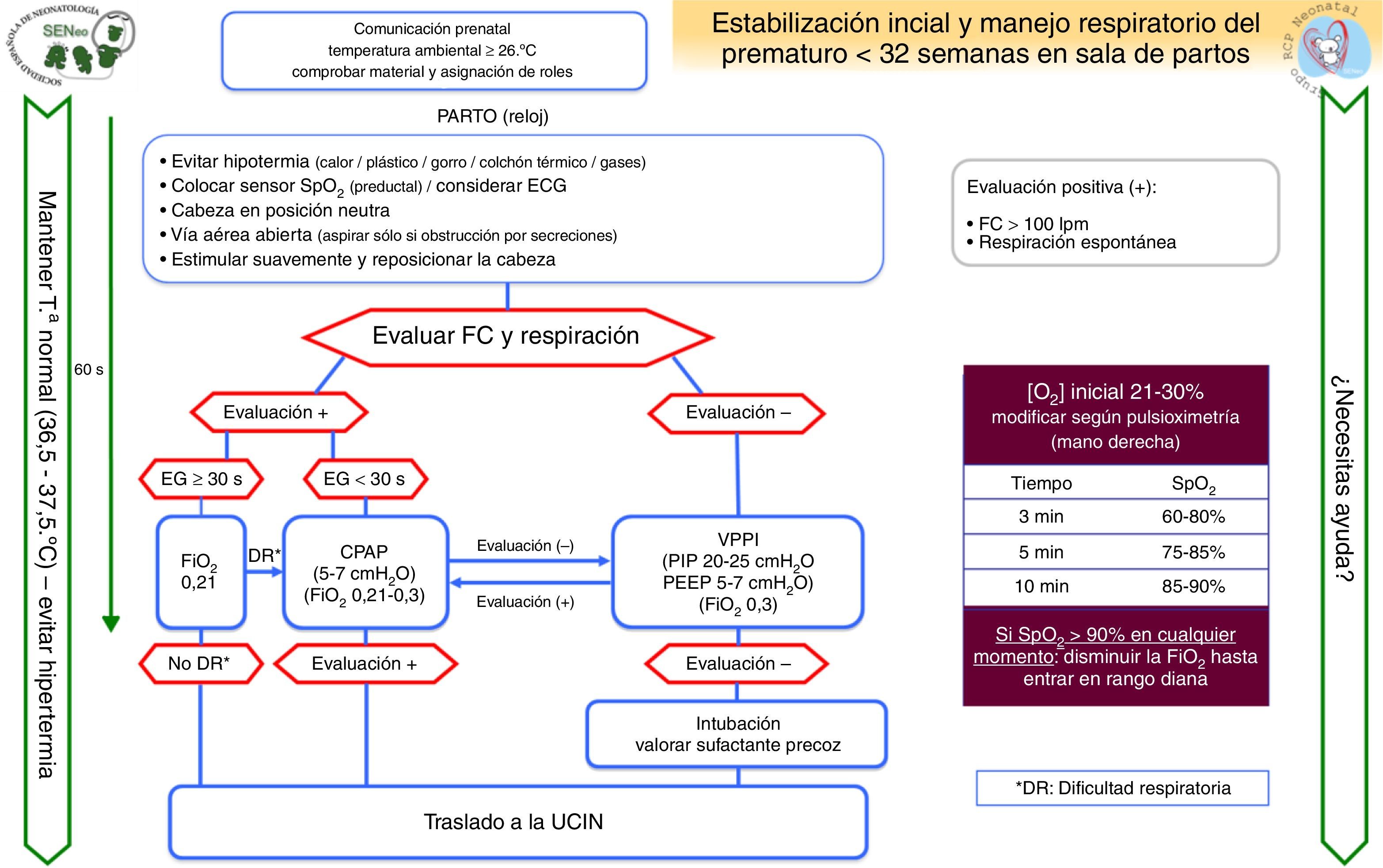
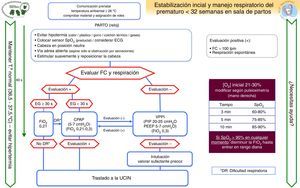
Situaciones clínicas especialesPrematuridadSe muestra el algoritmo de reanimación del prematuro menor de 32 SG elaborado por el GRN-SENeo (fig. 4).
Scores pronósticos: ILCOR 2015 revisa, para <25 SG, el uso conveniente de un score pronóstico, en lugar de solo la EG, para estimar la probabilidad de supervivencia al mes y a los 18-22 meses de vida. No existe evidencia suficiente para demostrar su valor pronóstico35. Es razonable considerar otras variables como el peso fetal estimado, sexo, corticoides prenatales, oligoamnios, gestación única o múltiple, antecedentes de corioamnionitis, nivel de cuidados del centro y guías de actuación.
Temperatura: la estabilización térmica es esencial, durante el parto (temperatura ambiental de 23-25°C en paritorio, cuna térmica precalentada, envoltorios de polietileno, gorrito), el ingreso y la estabilización.
Administración de oxígeno: se limita el inicio de FiO2 con aire ambiente a los ≥30 SG y <30 SG sin distrés, aumentando a 0,3 en estos últimos pacientes cuando presentan distrés. Los valores diana de SatO2 preductal aumentan por encima del p10 en los primeros 3 min de vida21, considerando un valor normal 60% (p15).
Insuflación sostenida (>5 s): no se recomienda su uso en RN pretérmino sin respiración espontánea, pero una IS puede ser considerada en circunstancias clínicas individualizadas.
PEEP: el uso de PEEP es beneficioso para el RN prematuro en apnea que requiere VPPI; se requieren más estudios aleatorizados que evalúen sus beneficios.
Milking: en <28 SG se contraindica; no hay datos de seguridad ni efectos favorables a largo plazo.
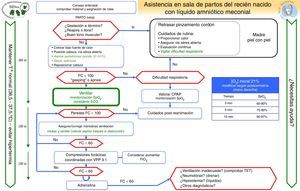
Manejo de la vía aérea en presencia de líquido meconial (fig. 5)La intubación y succión intratraqueal profiláctica de RN no vigorosos con LAM fue controvertida en las recomendaciones del 2010. Un reciente estudio clínico llevado a cabo en India por Chettri et al.36 aborda dicha cuestión. Se aleatorizó a 122 pacientes en 2grupos: intubación y VPPI vs. aspiración endotraqueal seguido de VPPI. Un estudio similar en India fue presentado en su Congreso de las Sociedades Académicas de Pediatría 201437. Ninguno de los 2 estudios encuentran diferencias entre grupos. Las recomendaciones ILCOR quedan abiertas a 3opciones de tratamiento: «considerar en algunos casos sin que sea de rutina, considerarlo solo si se sospecha obstrucción o bien en contra de la recomendación»1,3,4,38. Nuestro grupo recomienda que la intubación traqueal no debe ser rutinaria en RN no vigoroso con LAM y se debe seguir el mismo algoritmo general. Puede considerarse visualización y aspiración orotraqueal si hay signos de obstrucción de la vía aérea por meconio a pesar de haber iniciado la ventilación, si el reanimador es experto en intubación. No se aconsejan intubaciones repetidas y lo más importante es no retrasar las medidas de reanimación, con especial énfasis en iniciar la ventilación en el primer minuto de vida (fig. 5).
Aspectos éticos. Límite de la viabilidadEn los casos con pronóstico incierto o supervivencia en el límite, con una morbilidad y secuelas altas, se recomienda individualizar la actuación y, si ha podido realizarse entrevista y se ha obtenido la aprobación de los padres, valorar si iniciar reanimación o abstención terapéutica con cuidados de bienestar. Cuando esta situación se refiere a una gestación entre la 230/7 y la 236/7SG, deberían ser consideradas otras circunstancias perinatales39.
En menores de 23 SG y recién nacidos con cromosomopatías letales o malformaciones congénitas graves1 debe establecerse la abstención terapéutica, iniciando medidas de bienestar/cuidados paliativos. En ≥240/7 SG la actitud en principio es activa, aunque es fundamental, en la toma de decisiones, la información y opinión de los padres tras aportarles los datos de supervivencia de la SENeo, así como los datos de morbimortalidad propios del hospital.
Otro aspecto importante se refiere a la suspensión de la reanimación, si el Apgar inicial y tras 10 min es de 040. ILCOR 2015 indica que debería individualizarse teniendo en cuenta factores como lugar de nacimiento, recursos materiales, experiencia del equipo, posibilidad de hipotermia inducida y la comunicación familiar.
Existe un gran vacío documental y asistencial en el proceso de atención a la periviabilidad y sobre el concepto de cuidado paliativo perinatal, que este grupo considera dentro de nuestras competencias profesionales. Se hace necesario un protocolo de actuación: calor, analgesia y sedación, acompañamiento e información continua y detallada a los padres, permitir que estén con su hijo el tiempo que ellos precisen y como deseen (arropamiento, acompañamiento familiar, asesores espirituales o religiosos…) y favorecer un lugar apropiado con intimidad.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Motserrat Izquierdo Renau (Hospital Sant Joan de Déu-Hospital Clínic), Asunción Pino Vázquez (Hospital Clínico Universitario de Valladolid), Eva González Colmenero (Hospital Álvaro Cunqueiro de la Estructura Organizada de Xestión Integrada de Vigo), César W. Ruiz Campillo (Hospital Vall d’Hebron de Barcelona), Dolores Elorza Fernández (Hospital Universitario La Paz, Madrid), Miguel Sánchez Mateos (Hospital Universitario Puerta de Hierro de Mahadahonda, Madrid), Alejandro Ávila Álvarez (Complexo Hospitalario Universitario de A Coruña), Elena García Victori (Hospital Universitario Virgen del Rocío, Sevilla) y Máximo Vento Torres (Hospital Universitario y Politécnico La Fe, Valencia; Facultad de Medicina, Universidad de Valencia).