Ante la actual situación de pandemia de gripe causada por el virus A H1N1 2009, se han definido planes de actuación específicos desde distintas instituciones, administraciones y sociedades científicas. En este documento se definen las recomendaciones de la Asociación Española de Pediatría para el tratamiento de la gripe en la infancia para la estación gripal 2009–2010. Para la gripe A H1N1 2009, los factores de riesgo en edad pediátrica, el curso clínico, la gravedad y las complicaciones son similares a los de la gripe estacional. Además, el diagnóstico de gripe será, en la gran mayoría de los casos, por sospecha clínica sin diferenciación del subtipo viral. Ante un paciente con gripe, los criterios de derivación e ingreso hospitalario se basarán globalmente en la presencia de signos de gravedad clínica o de complicaciones, independientemente del virus causante. Los niños con gripe sin signos de gravedad ni complicaciones no requieren tratamiento con antivirales. Las medidas físicas de higiene y el aislamiento son fundamentales para reducir la transmisibilidad de la enfermedad. La vacunación antigripal en la infancia, tanto para gripe estacional como para gripe A H1N1 2009, debe dirigirse de forma prioritaria a los pacientes con factores de riesgo.
Specific action plans from various institutions, governments and scientific societies have been identified and implemented to combat the A H1N1 2009 influenza virus pandemic. This document sets out the recommendations of the Spanish Association of Pediatrics for the management of influenza in children for influenza season 2009–2010. The risk factors for influenza A H1N1 2009 in pediatric patients, the clinical course, severity and complications are similar to seasonal influenza. In most cases, the diagnosis of influenza will be based on clinical suspicion, without viral subtype differentiation. In a patient with influenza virus infection, the criteria for referral and hospital admission will be based broadly on the signs of clinical severity or complications, regardless of the causative virus. Children with influenza but with no signs of clinical severity or complications do not require antiviral treatment. Physical measures of hygiene and isolation are essential to reduce the transmissibility of the disease. The influenza vaccines in infancy, for both seasonal influenza and for influenza A H1N1 2009, should be directed primarily at patients with risk factors.
Desde la declaración de la Organización Mundial de la Salud (OMS) el 11 de junio de 2009 de la situación de pandemia por el virus de la gripe A H1N1 2009 se han realizado periódicamente y por parte de distintas instituciones, países, administraciones públicas y sociedades científicas recomendaciones sobre el protocolo diagnóstico-terapéutico, el tratamiento y la prevención de esta enfermedad1.
Los datos epidemiológicos conocidos hasta la actualidad sobre el impacto de esta gripe pandémica nos permiten afirmar que la gripe A H1N1 2009, a pesar de su elevada contagiosidad, causa una enfermedad más leve que la gripe estacional y con una mortalidad inferior. Cabe esperar que en la gran mayoría de las personas (>95%) que contraigan la enfermedad en los próximos meses, ésta sea leve y se resuelva en pocos días sin necesidad de otras medidas que las habituales frente a la gripe estacional de cada invierno2.
Los datos disponibles señalan que la transmisión del virus de la gripe A H1N1 2009 es más elevada en niños en edad escolar y en adultos jóvenes, al igual que sucede en la gripe estacional, mientras que la mayoría de las hospitalizaciones y las formas graves de la enfermedad se han producido en mujeres embarazadas y adultos con ciertas enfermedades de base1–4.
Para la gripe A H1N1 2009, los factores de riesgo en edad pediátrica, el curso clínico, la gravedad y las complicaciones son similares a los de la gripe estacional2. Además, el diagnóstico de gripe será, en la gran mayoría de los casos, por sospecha clínica sin posibilidad ni necesidad de diferenciar el subtipo viral. Por tanto, es necesario definir unas recomendaciones generales y prácticas para el enfoque global de la gripe en la edad pediátrica para este nuevo período, y éste es el objetivo del presente documento.
Diagnóstico de la gripeDiagnóstico clínicoEl cuadro clínico de la gripe A H1N1 2009 no difiere de la gripe estacional, incluso presenta una mayor tendencia a ser leve y autolimitado. A continuación, se proponen criterios clínicos para el diagnóstico de sospecha del síndrome gripal en la infancia, aunque la expresividad clínica será variable en función de la edad del paciente.
En niños mayores (más de 6 años de edad), los criterios que permiten una mejor aproximación a un diagnóstico de sospecha de gripe son los siguientes:
- 1.
Aparición súbita de los síntomas.
- 2.
Al menos 1 de los 4 síntomas generales siguientes: fiebre (≥38°C), malestar general, cefalea o dolores musculares.
- 3.
Y, además, al menos 1 de estos 3 síntomas respiratorios: tos, dolor de garganta o dificultad respiratoria.
- 4.
Ausencia de otra sospecha diagnóstica.
En niños de 2 a 6 años, la sintomatología puede ser sólo de fiebre (>38°C) asociada a síntomas respiratorios de vías altas o bajas, e indistinguible de cualquier otro proceso viral. En menores de 2 años es aún más inespecífica, en ocasiones, con sólo fiebre que puede ir acompañada de irritabilidad, llanto o rechazo del alimento5–7.
A todas las edades pueden presentarse síntomas digestivos de diarrea y vómitos. Se refuerza la sospecha si existe como antecedente epidemiológico el contacto estrecho con un caso de gripe en los 7 días anteriores al inicio del proceso.
El espectro de entidades clínicas asociadas al virus de la gripe es muy amplio y pueden observarse infecciones de vías altas, laringitis, bronquitis, bronquiolitis y neumonía viral (neumonitis), que pueden ser indistinguibles clínicamente de las producidas por otros virus respiratorios.
Pruebas complementariasMuestras: las muestras con mejor rendimiento diagnóstico son el frotis nasofaríngeo o el aspirado nasofaríngeo. Deben obtenerse idealmente al inicio del cuadro (primeros 3–4 días), cuando la excreción viral es máxima.
Técnicas diagnósticas8:
- 1.
Test rápidos: debido a su baja sensibilidad no se recomienda su uso habitual. No obstante, dada su alta especificidad, que permite confirmar el diagnóstico de gripe, pueden ser de utilidad en situaciones clínicas concretas. Permiten identificar el serotipo viral A o B, pero no distinguen el subtipo viral (H1N1 2009 o estacional, H3N2).
- 2.
RT-PCR a tiempo real del virus de la gripe: permite identificar el serotipo y el subtipo viral y confirmar si se trata de gripe A H1N1 2009 u otro subtipo de gripe estacional. Es un método de alta sensibilidad y especificidad.
Recomendaciones para la toma de muestras y confirmación diagnóstica: no existen unos criterios bien establecidos que definan las circunstancias clínicas concretas en las que sea conveniente la toma de una muestra nasofaríngea para investigar la presencia del virus de la gripe. Esta decisión quedará a criterio del facultativo en cada centro o institución sanitaria6,7,9,10. En general, se recomienda la determinación en:
- •
Pacientes con sospecha de infección por virus de la gripe que requieran ingreso hospitalario. En los pacientes que se controlen de forma ambulatoria no es preciso realizar el estudio.
- •
Pacientes con neumonía que requieran ingreso hospitalario, especialmente en la UCI.
Además de estas indicaciones, puede contemplarse la realización de un test diagnóstico cuando a juicio clínico se considere relevante.
Actuación en el paciente con diagnóstico de sospecha o confirmadoGrupos de riesgo de complicacionesSe definen así determinadas situaciones y procesos médicos de base que se relacionan con un aumento del riesgo de presentar complicaciones en caso de tener una infección por el virus de la gripe (tabla 1)1,4,7.
Factores de riesgo de complicaciones relacionadas con la infección por el virus influenza
| Sistema respiratorio |
|
| Sistema cardiovascular |
|
| Sistema metabólico |
|
| Sistema inmunitario |
|
| Sistema nervioso |
|
| Otras situaciones |
|
IMC: índice de masa corporal; VIH: virus de la inmunodeficiencia humana.
Los criterios de derivación al hospital son precisamente los criterios que plantean la necesidad de ingreso hospitalario. No existe ningún criterio específico de ingreso hospitalario de la gripe A H1N1 2009 ni de la gripe estacional. Los criterios orientativos, matizados según los protocolos de cada comunidad autónoma y centro sanitario, pueden ser los siguientes6,7,9,10:
Datos clínicos de gravedad- •
Afectación del estado general (decaimiento, postración o mala coloración).
- •
Estado séptico o hipotensión.
- •
Dificultad respiratoria moderada/grave.
- •
Hipoxemia (saturación de Hb ≤94%) al respirar aire ambiente (si el paciente es portador de enfermedad cardiopulmonar crónica, considerar valores menores de saturación).
- •
Afectación del sistema nervioso central (alteración del nivel de conciencia, agitación o convulsiones).
- •
Incapacidad para la ingesta oral o vómitos incoercibles.
- •
Diarrea grave.
- •
Deshidratación moderada/grave.
Los niños pertenecientes a los grupos de riesgo de desarrollar formas graves de gripe o complicaciones se valorarán de forma individualizada en función de la situación clínica de su enfermedad de base.
Paciente afectado de neumonía que presenta- •
Antecedentes clínicos: factores de riesgo de complicaciones (tabla 1) y sobre la base del juicio clínico del grado de riesgo.
- •
Factores socioepidemiológicos: edad menor de 6 meses o un entorno social que impida un adecuado tratamiento ambulatorio.
- •
Datos clínicos de gravedad o evolución desfavorable.
- •
Criterios radiológicos: derrame pleural significativo (>1cm), absceso pulmonar, neumatoceles, patrón intersticial grave o afectación multifocal.
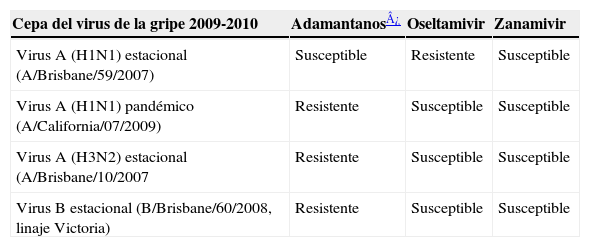
Los criterios de profilaxis y de tratamiento establecidos previamente para la gripe en los niños deben mantenerse en esta nueva situación. Lo que era válido para la profilaxis y para el tratamiento de la gripe A y B de años previos es válido para la gripe A H1N1 2009, pero con variación del antiviral de primera elección en caso de que estuviera indicado debido a la diferente sensibilidad antiviral de unas u otras cepas (tabla 2)11.
Sensibilidades frente a los fármacos antivirales de las cepas de virus de la gripe que se esperan que circulen durante la estación gripal de 2009-2010
| Cepa del virus de la gripe 2009-2010 | Adamantanos¿ | Oseltamivir | Zanamivir |
| Virus A (H1N1) estacional (A/Brisbane/59/2007) | Susceptible | Resistente | Susceptible |
| Virus A (H1N1) pandémico (A/California/07/2009) | Resistente | Susceptible | Susceptible |
| Virus A (H3N2) estacional (A/Brisbane/10/2007 | Resistente | Susceptible | Susceptible |
| Virus B estacional (B/Brisbane/60/2008, linaje Victoria) | Resistente | Susceptible | Susceptible |
Los fármacos antitérmicos deberían utilizarse prioritariamente para aliviar el malestar y el dolorimiento propio de la gripe más que para bajar la fiebre. Los fármacos de elección son el paracetamol y el ibuprofeno en las dosis habituales. Está contraindicada la aspirina por su supuesta relación con el desarrollo del síndrome de Reye2.
Los descongestionantes nasales, los antihistamínicos y los «antigripales» en general no están indicados en los niños. En los lactantes es importante aspirar las secreciones nasales o nasofaríngeas cuando dificultan la respiración.
Es conveniente que el niño ingiera alimentos suaves y bebidas que mejoren la hidratación de las mucosas, compensen las pérdidas hídricas por la fiebre y aporten calorías (agua, zumos o leche).
Debe evitarse el exceso de ropa cuando el paciente está febril; procurar un ambiente confortable, moderar la calefacción, no abrigar en exceso y airear con frecuencia la habitación. La utilización de paños fríos o el baño en agua fría están contraindicados, ya que interfieren con los mecanismos fisiológicos de producción y pérdida de calor propios de la fiebre. No fumar en el entorno del paciente.
Utilización de antiviralesLos niños con un cuadro clínico de gripe sin signos de gravedad ni complicaciones no requieren tratamiento antiviral2.
Las indicaciones de tratamiento recomendadas actualmente son aplicables tanto a las cepas estacionales como a la nueva cepa pandémica, ya que las tasas de morbimortalidad en la infancia de la gripe ocasionada por el virus A H1N1 2009 no difieren sustancialmente de las provocadas por los virus gripales estacionales.
Las indicaciones de tratamiento antiviral no son estrictas, la decisión debe fundamentarse en el criterio clínico y sobre la base de una ponderada valoración del beneficio/riesgo. Se recomienda considerar la instauración de tratamiento en11:
- •
Niños con infección por virus de la gripe sospechada o confirmada y que tienen factores de riesgo de mala evolución o complicaciones (tabla 1), independientemente de que se hayan vacunado o no. Debe tenerse en cuenta el nivel de riesgo de la enfermedad de base y el grado de afectación del paciente, y es razonable optar por no tratar inicialmente a algunos de estos pacientes si están estables y su presentación clínica es leve, con un seguimiento evolutivo estrecho que permita reconsiderar la indicación del tratamiento en función del curso clínico.
- •
Niños con infección por virus de la gripe sospechada o confirmada, con o sin factores de riesgo, que presentan una forma grave o complicada de la enfermedad que motivan su hospitalización.
Excepcionalmente podría plantearse en algún otro niño previamente sano con infección por virus de la gripe, en el que por juicio clínico se considere importante disminuir la duración de la sintomatología. Los antivirales reducen la duración de la sintomatología de la gripe estacional en aproximadamente 0,5–1,5 días si el tratamiento se instaura en las primeras 48h del inicio del proceso.
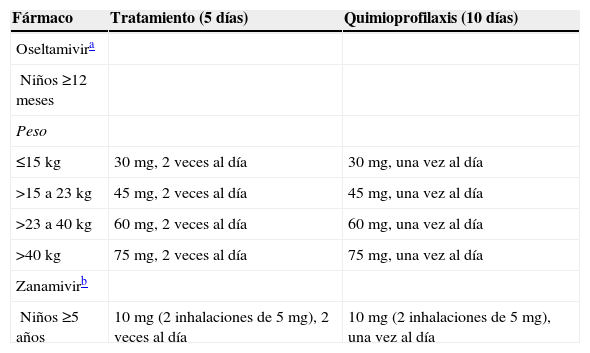
En la tabla 3 se exponen las pautas de tratamiento y de quimioprofilaxis con oseltamivir y zanamivir actualmente recomendadas para la gripe A H1N1 2009. Si se tratara de una gripe A H1N1 estacional, se puede usar el zanamivir en igual dosis, o bien amantadina en la dosis de 2,5mg/kg cada 12h (máximo 150mg/día) para niños de 1 a 9 años de edad y de 100mg cada 12h a partir de los 10 años (si pesan menos de 40kg se mantiene la dosis de 5mg/kg cada 12h). En los casos en que por criterios clínicos de gravedad estuviese indicado el tratamiento antiviral pero se desconociese qué subtipo concreto de virus de la gripe A es el causante de la enfermedad, debería valorarse administrar tanto amantadina como oseltamivir11.
Recomendaciones de dosificación de los fármacos antivíricos usados en el tratamiento y la quimioprofilaxis de la gripe causada por el virus A H1N1 2009
| Fármaco | Tratamiento (5 días) | Quimioprofilaxis (10 días) |
| Oseltamivira | ||
| Niños ≥12 meses | ||
| Peso | ||
| ≤15kg | 30mg, 2 veces al día | 30mg, una vez al día |
| >15 a 23kg | 45mg, 2 veces al día | 45mg, una vez al día |
| >23 a 40kg | 60mg, 2 veces al día | 60mg, una vez al día |
| >40kg | 75mg, 2 veces al día | 75mg, una vez al día |
| Zanamivirb | ||
| Niños ≥5 años | 10mg (2 inhalaciones de 5mg), 2 veces al día | 10mg (2 inhalaciones de 5mg), una vez al día |
El oseltamivir se ha autorizado para uso de urgencia en lactantes cuando se considere necesaria su prescripción. Es aconsejable la hospitalización de los menores de 3 meses en los que se indique tratamiento antiviral. En la tabla 4 se exponen las dosis recomendadas según la edad12.
Recomendaciones de dosificación de oseltamivir para tratamiento y quimioprofilaxis antiviral en lactantes
| Edad | Tratamiento (5 días) | Quimioprofilaxis (10 días) |
| <3 meses | 12mg, 2 veces al día (2 mg/kg, 2 veces al día) | No recomendado. Empleo solo si se considera imprescindible, debido a la escasez de datos en esta edad |
| 3–5 meses | 20mg, 2 veces al día (2,5 mg/kg, 2 veces al día) | 20mg, una vez al día |
| 6–11 meses | 25mg, 2 veces al día (3 mg/kg, 2 veces al día) | 25mg, una vez al día |
El diagnóstico de sospecha de neumonía por el virus influenza se basa en la existencia de fiebre o de sintomatología respiratoria aguda asociados a infiltrados nuevos en la radiografía de tórax. Todo paciente con sospecha de neumonía por virus influenza debe ingresarse en el hospital en caso de pertenecer a algún grupo de riesgo o de existir cualquiera de los criterios de ingreso hospitalario definidos previamente. En todos los casos en que se decida el ingreso está indicada la realización de RT-PCR de gripe para confirmar el diagnóstico e identificar el serotipo y el subtipo viral3,4,7.
Neumonía que no requiere hospitalizaciónEn los pacientes con gripe sospechada o confirmada afectados de una neumonía primaria indicativa de etiología viral pero que no presentan criterios de derivación hospitalaria (ausencia de signos de gravedad y de factores de riesgo), no existe evidencia del beneficio de un tratamiento antiviral. En estos pacientes deben seguirse las recomendaciones establecidas para el tratamiento en atención primaria de la neumonía comunitaria que no precisa hospitalización. En ellas no se recomienda, en general, la utilización de antivirales y, en cambio, sí debe valorarse, según los datos clínicos, radiológicos y analíticos, el inicio de un tratamiento antibacteriano por vía oral que ofrezca una cobertura adecuada frente a Streptococcus pneumoniae.
Neumonía que requiere hospitalización en plantaMedidas generales: oxigenoterapia, antitérmicos, fluidoterapia, etc.
Tratamiento antiviral: oseltamivir durante 5 días (si presenta un empeoramiento progresivo, reconsiderar prolongar el tratamiento hasta la mejoría). Indicado en todos los pacientes que ingresan con sospecha de neumonía por virus influenza A H1N1, al menos hasta tener los resultados de la RT-PCR. Si se identifica un subtipo viral distinto, deberá ajustarse el antiviral a la sensibilidad de la cepa (tabla 2). Si el resultado es negativo, se suspenderá el fármaco.
Tratamiento antibiótico: en aquellos pacientes con sospecha de infección por virus influenza y neumonía bacteriana como complicación, debe iniciarse un tratamiento antibiótico que ofrezca cobertura adecuada frente a los principales agentes etiológicos asociados en este tipo de casos, como S. pneumoniae (el fundamental en nuestro medio), Staphylococcus aureus, Streptococcus pyogenes e, incluso, Haemophilus influenzae.
Neumonía que requiere hospitalización en la unidad de cuidados intensivos pediátricosTodo paciente que requiera asistencia médica deberá evaluarse respecto a la posible existencia de insuficiencia respiratoria aguda y a la necesidad de ingreso en la unidad de cuidados intensivos pediátricos (UCIP). De igual manera, debe evaluarse a los pacientes hospitalizados en planta respecto a la presencia de datos evolutivos que indiquen la necesidad de su traslado a la UCIP. En estos casos, además del tratamiento antiviral contra el virus influenza, se procederá según los protocolos habituales de tratamiento en la UCIP de las neumonías graves o complicadas.
Prevención: medidas físicas y farmacológicasDada la gran contagiosidad de la gripe y la mayor susceptibilidad poblacional ante el nuevo virus A N1H1 2009, las medidas preventivas son muy importantes para reducir la transmisibilidad del virus y la expansión de la enfermedad en la población. Además, son esenciales para proteger a los individuos pertenecientes a los grupos de riesgo.
Medidas físicas y aislamiento6–10- 1.
Recomendaciones para adoptar en los niños con gripe sospechada o confirmada.
- •
Si un niño presenta síntomas indicativos de gripe debe permanecer en su domicilio (sin asistir a la escuela, viajes, compras, eventos sociales y reuniones públicas) hasta al menos 24h después de la desaparición de la fiebre (sin haber recibido tratamiento antitérmico).
- •
Los niños podrán asistir de nuevo a la escuela cuando hayan permanecido sin fiebre durante 24h y siempre que los padres comprueben una evolución favorable.
- •
Se debe enseñar y explicar a los niños mayores la importancia de cubrirse la boca y la nariz con pañuelos desechables cada vez que tosan o estornuden.
- •
Si se trata de un niño pequeño, se utilizarán pañuelos desechables que aplicará su familiar o cuidador, quien realizará la limpieza y la aspiración de secreciones por los procedimientos habituales.
- •
Los niños mayores se lavarán las manos con agua y jabón (durante 15–20s) y con frecuencia durante todo el día. El familiar encargado o el cuidador deberá lavar a los niños más pequeños.
- •
Los utensilios de comida de los pacientes enfermos (vajilla, cubiertos, etc.) no se compartirán con los demás miembros familiares o cuidadores. Su limpieza debe ser la habitual y apropiada (lavavajillas con agua caliente) y no precisan separarse de los del resto de la familia.
- •
Se utilizarán toallas y ropa distintas del resto de los convivientes. El lavado de ropa no necesita un tratamiento especial ni precisa lavarse de forma separada a la del resto de la familia.
- •
Durante el período de duración de la enfermedad deben observarse y vigilarse la presencia de signos y síntomas que pudieran indicar complicaciones o mayor gravedad, y prestar una vigilancia especial a los cambios de temperatura y de la tos. Si aparecen signos de gravedad, deben contactarse con los servicios sanitarios.
- •
- 2.
Recomendaciones para los contactos familiares y cuidadores.
- •
Las personas que pertenezcan a los grupos definidos de riesgo deben evitar, en lo posible, el contacto próximo (distancia<1m) con enfermos de gripe.
- •
Los familiares con factores de riesgo no deberían encargarse de los cuidados de un niño u otro familiar afectado. En caso de que fuera inevitable, se recomienda que utilicen protección con mascarilla o preferiblemente equipos de protección respiratoria (ver más adelante el uso de mascarillas).
- •
Debe evitarse que una mujer embarazada cuide a un paciente con sospecha de gripe.
- •
Los familiares que cuiden al niño enfermo deberán permanecer el menor tiempo posible en compañía de éste (de forma razonable y adecuada a la edad y situación del niño) y siempre que sea posible a una distancia mayor de 1m.
- •
Debe evitarse la exposición próxima y cara a cara con el niño siempre que sea posible.
- •
Deben lavarse las manos con agua y jabón (o con soluciones hidroalcohólicas) cada vez que se limpien secreciones, manipulen o cambien pañales al niño y cuando se toquen objetos manipulados por éste. El lavado debe ser frecuente, cuantas más veces, mejor.
- •
- 3.
Recomendaciones para la protección respiratoria: uso de mascarillas y equipos de protección respiratoria.
Puede ser recomendable su utilización en condiciones concretas, en las que se considera un alto riesgo de contagio y, de forma especial, para proteger a individuos pertenecientes a los grupos de riesgo.
Existen en el mercado 2 tipos de protectores respiratorios para evitar la transmisión del virus de la gripe pandémica: las mascarillas quirúrgicas habituales, que filtran el aire inspirado y espirado (pueden utilizarse en enfermos y en individuos sanos), y los protectores respiratorios de partículas (FFP2, FFP3, N95, etc.), con mucha mayor capacidad de filtrado pero que, al disponer de válvula inspiratoria, no dejan pasar partículas virales cuando se inspira, pero sí lo permiten al espirar (no deben utilizarse en enfermos).
Recomendaciones para los enfermos y contactos en el domicilio y en la comunidad.
- •
Aunque se ha recomendado la utilización de mascarillas quirúrgicas en personas enfermas y en sus contactos en el propio domicilio, su efectividad en el entorno familiar es controvertida dada la dificultad de un cumplimiento estricto y persistente, y su uso resulta poco práctico.
- •
Los cuidadores afectados de enfermedades crónicas (grupos de riesgo para gripe) deberán emplear mascarilla quirúrgica o preferiblemente equipos de protección respiratoria si no pueden abstenerse de cuidar a familiares con gripe.
- •
También es recomendable su uso cuando se lleven a cabo traslados de pacientes con gripe sospechada o confirmada a centros sanitarios, hospitales o desde la propia escuela hasta su trasladado al domicilio.
- •
- 4.
Recomendaciones preventivas en los centros sanitarios.
Medidas preventivas en centros de atención primaria y en servicios de urgencias
- •
Ante la detección de un caso sospechoso de gripe deberán utilizarse medidas de protección y de aislamiento frente a los demás niños en las salas de espera. Deberán habilitarse, si es posible, 2 salas de espera (una para los casos sospechosos y otra para el resto de las enfermedades). Los niños con síntomas indicativos de gripe deberían utilizar, si es factible, la mascarilla quirúrgica.
- •
El personal sanitario adoptará las medidas de higiene habituales y debería utilizar mascarilla quirúrgica como medida de protección. Es recomendable el uso de guantes de exploración no estériles, si cabe la posibilidad de contacto con secreciones del paciente (toma de muestras, aspiración de secreciones, etc.).
- •
Si el paciente requiere cuidados que generen aerosoles (tratamiento con nebulizador/inhaladores) o técnicas más intensivas (broncoscopias, intubación naso u orotraqueal, etc.), el personal sanitario debe utilizar protectores respiratorios de partículas, guantes de exploración no estériles y gafas protectoras.
Medidas preventivas en situación de hospitalización
- •
Aislamiento respiratorio estricto o el recomendado según su enfermedad de base (inmunodeficiencias, transplantados, etc.).
- •
Habitación individual, si es posible, o habitaciones compartidas con pacientes con un mismo diagnóstico, con una distancia de al menos 1m o más entre las cunas/camas.
- •
Limitar las visitas a un solo familiar. Deberá lavarse las manos al entrar y al salir de la habitación y cada vez que esté en contacto con el paciente. Debe utilizar protección respiratoria con mascarilla quirúrgica.
- •
El personal sanitario y no sanitario (servicios generales) en contacto con el enfermo utilizará mascarilla quirúrgica, guantes desechables no estériles, bata desechable de manga larga y se lavará las manos al entrar y al salir de la habitación.
- •
El personal encargado de la limpieza llevará mascarilla quirúrgica cuando entre en la habitación del enfermo.
- •
El personal sanitario que pertenezca a los grupos de riesgo o mujeres embarazadas no deberán atender a los pacientes con gripe sospechada o confirmada.
- •
Ante la situación actual de gripe pandémica deben seguirse las mismas recomendaciones de quimioprofilaxis establecidas para la gripe estacional: no se recomienda el uso generalizado de antivirales para la profilaxis de la infección gripal2. Debe valorarse en cada caso la relación beneficio/riesgo. En personas con factores de alto riesgo de complicaciones se valorará individualmente su empleo en función del grado de riesgo, el momento y el nivel de exposición (contactos cercanos) y el grado de certeza del diagnóstico del contacto. La profilaxis podría estar indicada en algunas situaciones, cuando un individuo presenta una exposición con riesgo de contagio de gripe y pertenece a uno de los siguientes grupos11:
- •
Niños en situación de alto riesgo no vacunados, o durante las 2 semanas siguientes a la vacunación, o cuando esté contraindicada la vacunación de la gripe, o, además de la vacunación, en algunos inmunodeprimidos que podrían no responder adecuadamente a la vacuna.
- •
Familiares no inmunizados que van a tener una exposición estrecha con niños no vacunados de alto riesgo.
- •
Niños no vacunados de un centro institucional cerrado con residentes pediátricos de alto riesgo para controlar un brote de gripe.
Debido a la alta tasa de resistencias a amantadina y a rimantadina que presentan las cepas del virus de la gripe A H3N2, el nuevo virus A H1N1 2009 y los virus B, y la resistencia del virus de la gripe A H1N1 estacional al oseltamivir, las recomendaciones de pautas quimioprofilácticas dependerán de los virus circulantes según los patrones de sensibilidad (tabla 2)11.
En las tablas 3 y 4 se exponen las pautas de quimioprofilaxis con oseltamivir y zanamivir actualmente recomendadas para la gripe A H1N1 2009.
Prevención: vacunación antigripalVacunación frente a la gripe estacionalLa vacunación antigripal frente a la gripe estacional es una estrategia especialmente efectiva cuando se dirige a los niños con procesos de base que condicionan un mayor riesgo de complicaciones cuando tienen una infección por el virus de la gripe3. Las recomendaciones de vacunación en la infancia deben dirigirse a:
- 1.
Niños mayores de 6 meses y adolescentes pertenecientes a los grupos con factores de riesgo de complicaciones (tabla 1).
- 2.
Niños mayores de 6 meses y adolescentes que son contactos domiciliarios (convivientes) de pacientes (niños o adultos) pertenecientes a grupos de riesgo.
También deben vacunarse frente a la gripe estacional los adultos que son contactos domiciliarios (convivientes o cuidadores) de niños, adolescentes o adultos que pertenecen a los grupos de riesgo. Es especialmente importante la vacunación del entorno familiar cuando existen lactantes menores de 6 meses de edad con factores de riesgo, ya que éstos no pueden recibir la vacuna11.
Los niños mayores de 6 meses no pertenecientes a los grupos de riesgo pueden vacunarse frente a la gripe estacional si sus padres lo solicitan o si su pediatra lo considera oportuno.
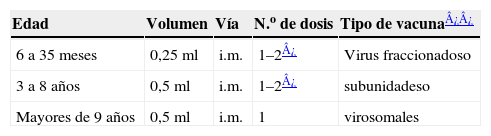
Las vacunas disponibles son trivalentes, con 2 cepas de serotipo A (subtipos H1N1 y H3N2) y una de serotipo B, y la composición de cada serotipo se modifica anualmente según las recomendaciones de la OMS para cada campaña vacunal antigripal. La vacuna está autorizada para individuos a partir de 6 meses de edad y debe administrarse anualmente preferiblemente entre los meses de septiembre a noviembre. La pauta de administración se esquematiza en la tabla 5.
Vacunación frente al virus de la gripe A H1N1 2009Justificación de la vacunaciónEs muy importante definir una adecuada estrategia sobre el uso de la vacunación frente al virus A H1N1 2009 y priorizar cuidadosamente los distintos grupos de población a los que va a dirigirse. Los beneficios que ofrezca la vacunación deben ser siempre claramente superiores a los riesgos potenciales, especialmente en individuos sanos en los que la enfermedad se presenta de forma benigna.
Es necesario analizar de forma crítica múltiples factores a la hora de decidir los grupos prioritarios de vacunación.
Estrategia de la vacunaciónBasándose en los datos epidemiológicos, clínicos y farmacológicos actualmente disponibles, en las guías establecidas por el European Centre for Disease Prevention and Control y por la OMS, el 25 de agosto de 2009 el European Union Health Security Committee propuso a la Comisión Europea las siguientes recomendaciones de vacunación frente a la gripe pandémica3:
1. Primeros grupos prioritarios: las primeras personas que deberían vacunarse:
- •
Mayores de 6 meses de edad con enfermedades de base que incrementan el riesgo de desarrollar enfermedad grave (tabla 1).
El grupo de edad de 0 a 6 meses se excluye porque no puede vacunarse y debe protegerse mediante otras medidas.
- •
Mujeres embarazadas.
- •
Personal sanitario.
2. Grupos diana posteriores: cada Estado Miembro continuará vacunando a su población según estrategias nacionales hasta cubrir sus objetivos. Debe considerarse de forma especial a los individuos que conviven con personas en las que la vacuna puede resultar menos eficaz (inmunodeprimidos de cualquier origen) o que no pueden vacunarse (menores de 6 meses, grupo en el que las vacunas de la gripe no están aprobadas por falta de datos sobre inmunogenicidad y seguridad).
La vacunación de los grupos prioritarios debe iniciarse en cuanto la vacuna esté disponible y posteriormente se continuará con los grupos diana.
Vacunas disponibles en Europa frente al virus de la gripe A H1N1 2009: la Comisión Europea y la EMEA han establecido 3 posibles procedimientos para el desarrollo y la autorización de nuevas vacunas frente al virus A H1N1 20093,5:
1. A partir de vacunas pandémicas prototipo (mock-up vaccines) para la gripe pandémica ya registradas
Son vacunas prototipo desarrolladas y registradas antes del inicio de la pandemia actual y que utilizaron como antígeno la cepa H5N1 para su desarrollo. Los ensayos clínicos para el registro de estas vacunas incluyeron a más de 6.000 sujetos, incluidos niños y adultos, y permitieron obtener datos de seguridad e inmunogenicidad de éstas. En el momento en que se declara oficialmente la pandemia con el virus A H1N1 2009, las compañías fabricantes sólo deben reemplazar la cepa de virus gripal de la vacuna modelo por la actual, ya que los datos de seguridad e inmunogenicidad son extrapolables. Además, deben documentarse todos los requerimientos de calidad sobre el proceso de fabricación de la formulación definitiva para obtener la aprobación final de la EMEA y, en última instancia, de la Comisión Europea, que se autorizan bajo circunstancias excepcionales, como es una situación de pandemia, y sobre la base de una estricta valoración del cociente beneficio/riesgo. Las 3 vacunas recientemente autorizadas en Europa se basan en vacunas pandémicas prototipo.
2. Nuevas vacunas autorizadas por proceso de emergencia
Es un procedimiento de registro acelerado para nuevas vacunas frente al virus influenza A H1N1 2009 que permite reducir el período de registro dada la situación de emergencia. No obstante, se requieren datos completos de la nueva vacuna (fabricación, seguridad e inmunogenicidad), lo que implica un proceso más prolongado que el requerido para las vacunas prototipo. No existe ninguna vacuna autorizada mediante este proceso actualmente, aunque 2 compañías fabricantes están desarrollando nuevas vacunas para su registro en Europa.
3. Modificación de las vacunas antigripales estacionales
Existe la posibilidad de que se desarrollen en un futuro vacunas para la gripe estacional que incorporen la cepa frente A H1N1 2009. No existe ningún procedimiento de autorización acelerado para esta modificación y el registro de estas vacunas debe seguir el procedimiento habitual de las vacunas estacionales. No existe actualmente ninguna vacuna autorizada ni en desarrollo con esta estrategia en Europa.
Vacunas autorizadas (actualización del 17 de noviembre de 2009)5Existen 3 vacunas autorizadas en Europa frente a la gripe A H1N1 2009, todas ellas basadas en vacunas pandémicas prototipo registradas: Focetria®, Novartis; Pandemrix®, GlaxoSmithKline y Celvapan®, Baxter. Difieren en su composición y en su estrategia de desarrollo: Focetria® y Pandemrix® contienen adyuvante (emulsión de aceite en agua) que potencia la respuesta inmunitaria y permite reducir la dosis de antígeno, y ambas se desarrollan en huevos embrionados. Celvapan® no contiene adyuvante y se desarrolla en cultivos celulares de células Vero (no contiene proteínas de huevo).
Aunque los datos clínicos de estas vacunas en niños son aún limitados, sobre la base de éstos y de toda la experiencia previa con las distintas vacunas frente a la gripe estacional, la EMEA ha autorizado estas 3 vacunas para su utilización en adultos, mujeres embarazadas y niños a partir de los 6 meses de edad.
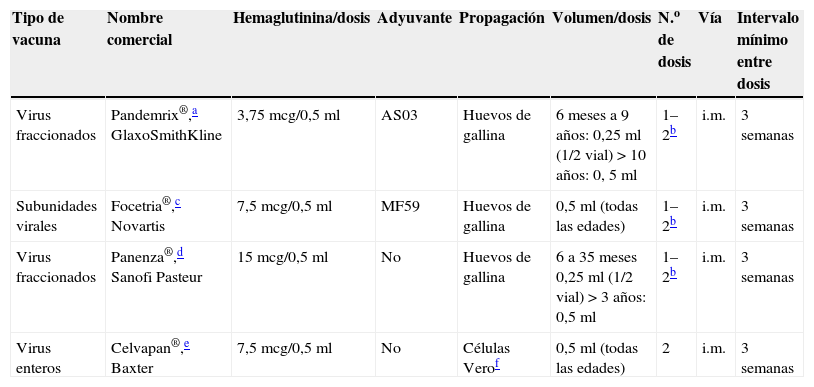
En España, la Agencia Española de Medicamentos y Productos Sanitarios concedió el 14 de noviembre de 2009 la autorización de comercialización a otra nueva vacuna denominada Panenza®, Sanofi Pasteur13. Esta autorización se ha realizado por un procedimiento descentralizado (no a través de la EMEA) y mediante mutuo acuerdo de las Agencias Sanitarias reguladoras de varios países de Europa. Se trata de una vacuna no adyuvada, desarrollada en huevos embrionados. Esta vacuna será la que, según las recomendaciones oficiales de vacunación, se utilice en mujeres embarazadas en España. En la tabla 6 se detalla la composición y la pauta de administración de todas estas vacunas.
Composición y posología de las vacunas monovalentes frente a la gripe A H1N1 2009 autorizadas en Europa
| Tipo de vacuna | Nombre comercial | Hemaglutinina/dosis | Adyuvante | Propagación | Volumen/dosis | N.o de dosis | Vía | Intervalo mínimo entre dosis |
| Virus fraccionados | Pandemrix®,a GlaxoSmithKline | 3,75mcg/0,5ml | AS03 | Huevos de gallina | 6 meses a 9 años: 0,25ml (1/2 vial) >10 años: 0, 5ml | 1–2b | i.m. | 3 semanas |
| Subunidades virales | Focetria®,c Novartis | 7,5mcg/0,5ml | MF59 | Huevos de gallina | 0,5ml (todas las edades) | 1–2b | i.m. | 3 semanas |
| Virus fraccionados | Panenza®,d Sanofi Pasteur | 15mcg/0,5ml | No | Huevos de gallina | 6 a 35 meses 0,25ml (1/2 vial) >3 años: 0,5ml | 1–2b | i.m. | 3 semanas |
| Virus enteros | Celvapan®,e Baxter | 7,5mcg/0,5ml | No | Células Verof | 0,5ml (todas las edades) | 2 | i.m. | 3 semanas |
i.m.: intramuscular.
Recomendada oficialmente en España para la inmunización de personas de 18 a 60 años de edad, excepto en embarazadas.
Los datos preliminares con la formulación con virus de la gripe A H1N1 2009 indican, tanto en adultos como en niños, que puede ser suficiente una dosis. En las actuales recomendaciones oficiales españolas se recomienda una dosis única para todas las edades, aunque en los menores de 2 años se valorará la necesidad de una segunda dosis en función de la disponibilidad de nuevos datos.
Recomendada oficialmente en España para la inmunización de niños y adolescentes de 6 meses a 17 años (presentación en monodosis) y en adultos mayores de 65 años de edad.
Los datos de seguridad y reactogenicidad de las vacunas autorizadas por la EMEA se basan en los datos evaluados para el registro de las vacunas prototipo que contienen H5N1. Además de los estudios en adultos, Focetria® se ha evaluado en niños y en adolescentes de 6 meses a 17 años, y Pandemrix® en niños de 3 a 9 años. Panenza® con H1N1 2009 se ha evaluado en un número reducido de niños de 3 a 8 años, en adolescentes de 9 a 17 años y en adultos. Celvapan® se ha evaluado en adultos mayores de 18 años y no tiene datos en niños. En los estudios realizados, las vacunas se han mostrado seguras y con una reactogenicidad similar a las vacunas antigripales estacionales, excepto para las reacciones locales y especialmente el dolor local, más frecuente en las vacunas adyuvadas, aunque de intensidad leve y tolerable.
Contraindicaciones específicasContraindicada en menores de 6 meses.
Focetria®, Pandemrix® y Panenza® están contraindicadas en pacientes con antecedentes de anafilaxia a las proteínas del huevo.
Antecedentes de anafilaxia a alguno de sus componentes.
Coadministración con otras vacunasNo existen estudios de coadministración con otras vacunas. Por tratarse de vacunas inactivadas, si se considera la necesidad de coadministración con otras vacunas del calendario de vacunaciones sistemáticas, pueden administrase simultáneamente con otras vacunas, aunque en jeringuillas y en lugares anatómicos distintos. En caso de administración no simultánea, no es necesario mantener ningún intervalo entre éstas y otras vacunas del calendario. Existen estudios que han evaluado la vacunación simultánea de Focetria® con vacunas no adyuvadas frente a la gripe estacional, sin evidencia de interferencia inmunológica ni incremento de la reactogenicidad. Al tratarse de vacunas inactivadas, en caso necesario, pueden coadministrarse simultáneamente las vacunas frente a la gripe A H1N1 2009 con las vacunas frente a la gripe estacional no adyuvadas en lugares anatómicos distintos. En caso de administración no simultánea, no es necesario mantener ningún intervalo entre éstas5,12.
Intercambiabilidad de vacunasNo existen datos de intercambiabilidad entre las distintas presentaciones frente a la gripe A pandémica y, por tanto, debe completarse la pauta posológica con esta presentación comercial para la segunda dosis si esta se considera necesaria.
Recomendaciones de vacunación en España
Es potestad de las autoridades sanitarias definir las estrategias de vacunación para hacer frente a la pandemia. En España, el Ministerio de Sanidad y Política Social ha acordado seguir las directrices de la Comisión Europea en la consideración de los grupos prioritarios de vacunación señalados anteriormente en este capítulo, incluyendo además algunos colectivos esenciales del país. Existe disposición por parte del Ministerio para ampliar estos grupos si existen nuevas recomendaciones por parte de los grupos de expertos. En la reunión mantenida el 23 de octubre de 2009 entre el Ministerio de Sanidad y el Consejo Interterritorial del Sistema Nacional de Salud se acordó8 lo siguiente:
- •
Iniciar la vacunación frente a la gripe A H1N1 2009 a partir del 16 de noviembre de 2009, con carácter voluntario.
- •
Ratificar la recomendación de vacunar a adultos y a niños mayores de 6 meses con enfermedades crónicas con riesgo de complicaciones (tabla 1), mujeres embarazadas, trabajadores sanitarios y trabajadores de servicios públicos esenciales.
- •
Recomendar una sola dosis para los adultos entre 18 y 60 años incluidos en los grupos de riesgo sobre la base de las recomendaciones de la Agencia Española del Medicamento.
El 17 de noviembre de 2009, el Ministerio de Sanidad y Política Social ha establecido las recomendaciones oficiales para la campaña de vacunación frente al virus gripal pandémico en España y ha definido los preparados comerciales y las posologías para niños, adolescentes, adultos y mujeres embarazadas (tabla 6)8.
La evolución de la pandemia, la disponibilidad de nuevas vacunas, y la ampliación de datos de la inmunogenicidad y seguridad de estas en niños y adultos permitirán decidir la conveniencia o no de extender la vacunación a niños sanos y a otros grupos de población, con la máxima seguridad y con un adecuado perfil de beneficio/riesgo. El seguimiento de la evolución de la enfermedad y su impacto en nuestro país será clave para tomar esta decisión.
Recién nacido de madre con gripe A sospechada o confirmadaEn el caso de que la madre contraiga la enfermedad o exista una sospecha fundada, se recomienda extremar las medidas higiénicas, y la madre y el resto de los contactos afectados deben emplear mascarilla durante la estancia con el neonato. Algunos organismos, como los Centers for Disease Control and Prevention, abogan por una actitud mucho más estricta y recomiendan separar al niño de la madre hasta que aquélla haya recibido medicación antiviral durante 48h, no presente fiebre y pueda controlar la tos4,7,9.
Desde el momento en que la madre enferma conviva con el recién nacido, debe llevar mascarilla facial, cambiarse de ropa, seguir las normas de lavado de manos y cubrirse al toser. Estas medidas de precaución deben realizarse hasta 7 días después del comienzo de la enfermedad.
Se desconoce si la gripe se transmite a través de la leche materna; actualmente no hay casos descritos. Como medida de carácter general, es aconsejable iniciar la lactancia materna debido a los beneficios que se derivan para el niño, que debe mantenerse aunque la madre contraiga la gripe o haya estado en contacto con casos confirmados o sospechosos. En el caso de enfermedad grave de la madre en que precise la separación del niño, se recomienda extraer la leche con un dispositivo extractor para su administración posterior por parte de otra persona asintomática. El tratamiento o la quimioprofilaxis con antivirales no contraindican la lactancia materna.
Debe vigilarse de cerca la aparición de manifestaciones clínicas de gripe en el recién nacido de una madre afectada. Si presenta síntomas se valorará, según su situación clínica, la necesidad de derivación hospitalaria, se enviará una muestra para la detección viral por RT-PCR y, a juicio clínico, se considerará la indicación de tratamiento con oseltamivir. En el caso de iniciarse éste, se recomienda realizarlo siempre en el hospital y monitorizar de cerca la posible aparición de efectos adversos. En general, no está recomendado realizar quimioprofilaxis con oseltamivir en el recién nacido en estos casos.
Conflictos de interesesJ. Marès ha participado como investigador en ensayos clínicos promovidos por GlaxoSmithKline y Wyeth, ha participado como ponente en eventos científicos esponsorizados por Sanofi Pasteur MSD, GlaxoSmithKline y Wyeth, y ha participado como consultor en el Advisory Board de GSK, actividades por la que ha percibido honorarios.
C. Rodrigo es miembro del Consell Asesor en Vacunacions y del Consell Asesor de Grip Pandémica del Departament de Salut de la Generalitrat de Catalunya, ha participado como investigador en ensayos clínicos promovidos por Pfizer, GlaxoSmithKline y Sanofi Pastéur MSD, ha participado como consultor en diversos grupos asesores de Laboratorio Esteve, GSK Biogicals, Sanofi Pasteur MSD, Novartis y Wyeth, y ha participado como ponente en actividades científicas patrocinadas por Pfizer, GlaxoSmithKline, Sanofi Pasteur MSD y Wyeth por las que, en ocasiones, ha percibido honorarios.
D. Moreno-Pérez ha participado como investigador en ensayos clínicos promovidos por GlaxoSmithKline, ha participado como ponente en eventos científicos esponsorizados por Sanofi Pasteur MSD, GlaxoSmithKline y Wyeth, actividades por la que ha percibido honorarios.
M.J. Cilleruelo ha participado como investigador en ensayos clínicos promovidos por GlaxoSmithKline y Wyeth, ha participado como ponente en eventos científicos esponsorizados por GlaxoSmithKline y Wyeth, actividades por la que ha percibido honorarios.
F. Barrio ha participado como investigador principal en ensayos clínicos promovidos por GlaxoSmithKline y ha colaborado como ponente en eventos científicos esponsorizados por GlaxoSmithKline, actividades por las que ha percibido honorarios profesionales.
J. Arístegui ha participado como investigador en ensayos clínicos promovidos por GlaxoSmithKline y Wyeth, ha participado como ponente en eventos científicos esponsorizados por GlaxoSmithKline y Wyeth, y ha participado como consultor en el Advisory Board de GSK, actividades por la que ha percibido honorarios.
J.C. Buñuel, J. González de Dios, P. González, M. Aparicio y T. Hernández Sampelayo declaran no presentar conflictos de intereses.
Sociedad Española de Infectología Pediátrica: María José Mellado, Fernando Alvez, Carlos Rodrigo, Marisa Navarro, María Jesús García, Fernando Baquero, María Concepción Figueras, Raúl González, Maribel González, David Moreno y María José Cilleruelo.
Comité Asesor de Vacunas: Josep Marès, Diego van Esso, Javier Arístegui, David Moreno, María José Cilleruelo, Francisco Barrio, José González Hachero, Jesús Ruiz Contreras, Francisco José Álvarez, Luis Ortigosa y Manuel Merino.
Grupo de Trabajo de Pediatría Basada en la Evidencia: José Cristóbal Buñuel, Pilar Aizpurua, María Aparicio, José Luis Aparicio, Antonio Bonillo, María Jesús Esparza, María Paz González, Javier González de Dios, Blanca Juanes, Carlos Ochoa, Leo Perdikidis y Juan Ruiz-Canela.
Sociedad Española de Infectología Pediátricaa, Comité Asesor de Vacunasb, y Grupo de Trabajo de Pediatría Basada en la Evidenciac y refrendado por la Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria, la Asociación Española de Pediatría de Atención Primaria y la Sociedad Española de Urgencias Pediátricas.