Introducción
Hace más de 100 años (1897), G. Killian sorprendía a sus ilustres y escépticos colegas, al conseguir la visualización directa de las vías aéreas y la extracción con éxito de un cuerpo extraño (CE) enclavado en el bronquio principal derecho, mediante un broncoscopio rígido (BR). Más tarde, Ch. Jackson contribuiría notablemente a su divulgación, creando la primera escuela de broncoscopistas en 1916. Las posibilidades terapéuticas de este instrumento, lo convertirían en una herramienta de trabajo utilizada por cirujanos y otorrinos, bajo anestesia general, hasta bien pasada la primera parte del siglo xx1.
Pero fue el diseño del broncoscopio flexible (BF) por Ikeda en 1968, el responsable de la extraordinaria difusión de la técnica, al convertir la exploración en un procedimiento sencillo, rápido y de menor riesgo, al no precisar anestesia general, permitiendo su utilización al médico clínico, quien a su vez la convierte en una poderosa herramienta diagnóstica, llegando incluso a vaticinar, la caída del viejo instrumento rígido2.
La fibrobroncoscopia (FBC) se extiende a la pediatría de la mano de R. Wood en la década de los 80, marcando probablemente, la diferenciación de la neumología pediátrica, como tal especialidad3-5. En España, el inicio de la década de los 90, marca los comicios de esta nueva técnica, estando hoy día, en los 2000, consolidada y extendida entre numerosos grupos de trabajo de la Sociedad de Neumología Infantil6-8.
Fibrobroncoscopia pediátrica hoy
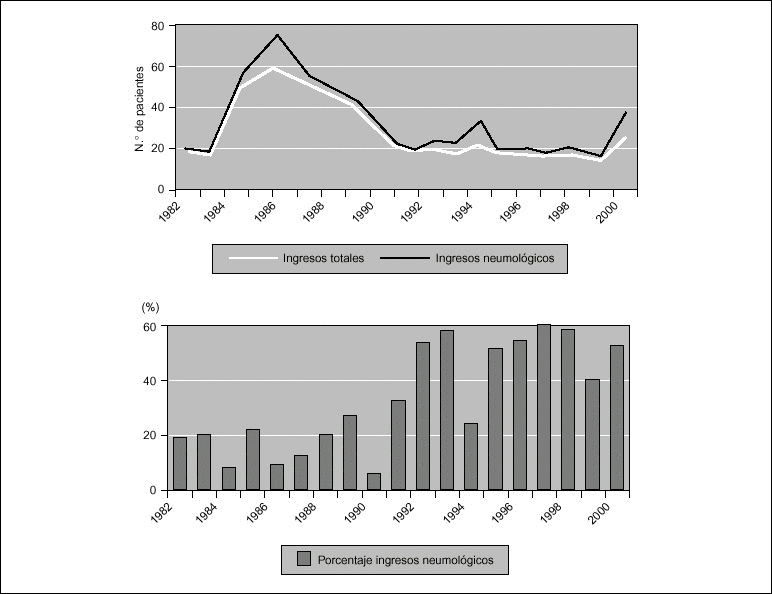
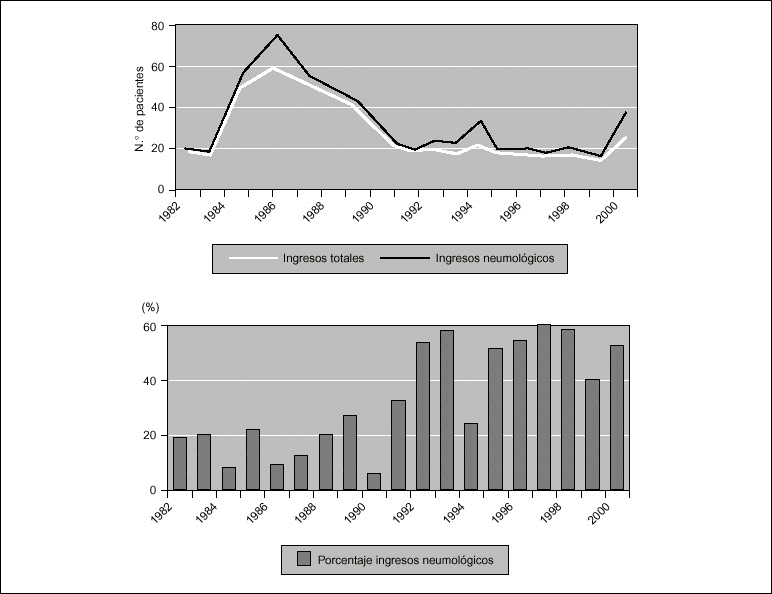
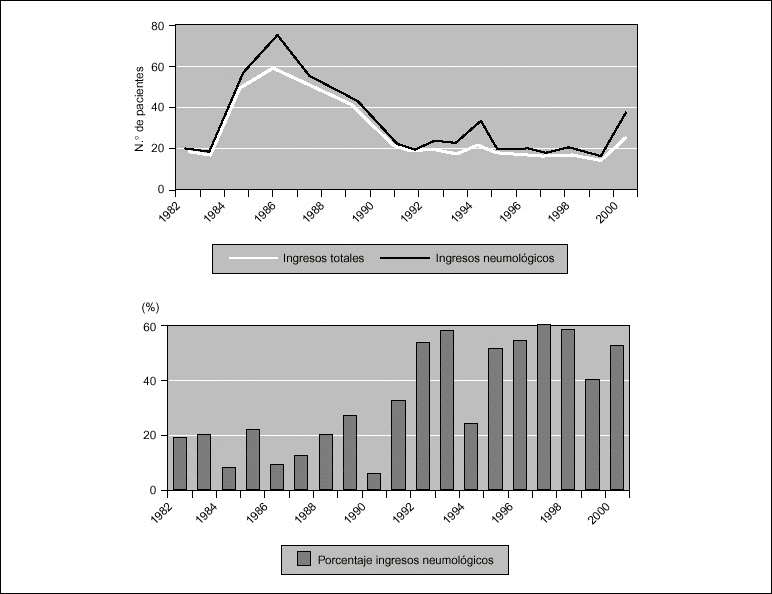
La FBC proporciona dos tipos de información clínica: una directa, a través de la observación anatómica y funcional de cada una de las distintas estructuras que componen las vías aéreas o "FBC exploradora", y otra indirecta, mediante la obtención de muestras biológicas susceptibles de investigación microbiológica y citopatológica o "FBC diagnóstica". Hoy en día, sus posibilidades exploratorias y diagnósticas marcan su campo de actuación, frente a sus escasas posibilidades terapéuticas. Así, de 530 FBC realizadas en los últimos 10 años en nuestra unidad, 390 (73%), se indicaron para una exploración propiamente dicha, 87 (16,4%) iban dirigidas principalmente a la obtención de muestras lavado broncoalveolar (LBA) o biopsia bronquial y sólo en 53 (10%) se ensayaron distintos procedimientos terapéuticos.
Desde sus primeras aplicaciones por Wood, se han producido una serie de avances en la práctica broncoscópica, que vienen determinados principalmente por mejoras continuas en la instrumentación y sedación, los progresos en la investigación clínica de las muestras biológicas obtenidas, y los avances en las técnicas intervencionistas. Son precisamente estos avances, los que han originado nuevos retos diagnósticos-terapéuticos todavía de difícil solución para el fibrobroncoscopista, y los que sin duda, condicionarán un probable cambio en su formación y práctica broncoscópica en esta nueva década.
Instrumentación
La tabla 1, muestra los distintos fibrobroncoscopios de utilización pediátrica actual. Progresivamente, se han ido desarrollando BF con haces fibroópticos más pequeños, permitiendo la colocación de un mayor número de haces por unidad de espacio y por lo tanto, una imagen más amplia y menos artefactada. Así el BF de 2,8 mm (ultra-slim) de reciente introducción (1999) 9, tiene todas las funcionalidades del estándar de 3,5 mm, aunque a expensas de una sección un 40 % más débil. La grabación de las exploraciones, ha facilitado el aprendizaje y la comunicación con diferentes servicios, y gracias al diseño del videobroncoscopio, se está alcanzando una gran resolución y nitidez en las imágenes, las cuales pueden ser además almacenadas en formato digital. Este nuevo instrumento, consiste en un BF equipado con un Charge Coupled Device (CCD) en su extremo distal, desde donde las imágenes son capturadas digitalmente y transmitidas a un procesador de vídeo para su visualización posterior en un monitor de TV1. Apesar de suponer un encarecimiento de los equipos, y mayores necesidades de espacio para el almacenamiento, todo hace prever la transformación gradual de la FBC tradicional en videobroncoscopia hoy sólo disponible para broncoscopios de diámetro mínimo de 4,9 mm y por lo tanto, no, para la mayoría de las aplicaciones pediátricas10.
Disponemos también hoy, de mejor instrumentación accesoria como pinzas de biopsia11 y dispositivos para la extracción de CE12, capaces de atravesar el pequeño canal operador de 1,2 mm, y los pacientes de especial riesgo, con vías aéreas inestables, pueden beneficiarse de una exploración a través de máscaras laríngeas13. No obstante, como se muestra en la tabla 1, quedan por resolver algunas limitaciones: no se dispone aún de catéteres telescopados lo suficientemente pequeños, para la realización del LBA protegido, ni de canal de trabajo en los BF ultrafinos de 2,2 mm útiles por lo tanto sólo en reanimación neonatal y en líneas generales, a menor tamaño, mayor fragilidad con menor durabilidad de los instrumentos y encarecimiento de los costes.
Sedación
Simultáneamente a los avances tecnológicos en broncoscopia, se han ido desarrollando nuevos agentes farmacológicos, que ofrecen mayores ventajas para el confort del paciente durante su realización. Sin sedación, el procedimiento fue calificado como muy desagradable o intolerable, por el 60% de los adultos encuestados14, por lo que la elección de la medicación, es un factor determinante del éxito de ésta técnica, especialmente en niños. Sin embargo, la mayor parte de las complicaciones asociadas a la FBC, están relacionadas precisamente con la sedación. Desarrollar pues, agentes que aseguren el bienestar del enfermo sin aumentar el riesgo, es un objetivo prioritario. No existe un protocolo de actuación uniforme, reflejando la falta de consenso entre la conveniencia de la sedación consciente o profunda. La administración IV de benzodiacepinas (midazolam) y narcóticos (fentanilo) ha sido hasta ahora la pauta más generalizada, ya que combinados, logran un rápido inicio de acción, sedación profunda y amnesia antero-retrógrada5,7. Se dispone además de agentes para su reversión flumacenilo y naloxona, respectivamente en caso de producirse depresión respiratoria. Una nueva estrategia, la constituye la asociación de remifentanilo IV en perfusión continua narcótico con extraordinariamente corta vida media y bolos IV intermitentes del sedante hipnótico propofol, si la sedación es inadecuada15. Se han comunicado sus buenos resultados, sin efectos adversos en FBC con ventilación espontánea. La tabla 2 recoge la dosificación y tiempos de actuación de los fármacos de administración IV más utilizados. Otra posibilidad, la constituye la sedación profunda por la vía inhalatoria, especialmente con sevoflurane16, anestésico que permite la ventilación espontánea durante el procedimiento, aplicándose bien solo o bien combinado con remifentanilo y propofol.
Investigación clínica de las muestras biológicas
En la patología respiratoria pediátrica, de los diversos procedimientos diagnósticos que pueden realizarse con FBC LBA, cepillado bronquial, biopsias bronquiales o transbronquiales, punciones aspirativas transbronquiales, broncografías selectivas etc. el LBA se ha erigido en el más difundido, mejor estudiado y de mayor rendimiento, estando el resto menos extendidos en el particular campo de las indicaciones pediátricas. Así, durante esta década, el LBA estrictamente hablando un volumen suficiente de suero salino, que asegure que el fluido subsecuentemente aspirado, contenga parte del fluido que recubre la superficie alveolar no sólo se ha consolidado como técnica de elección en el diagnóstico de las infecciones oportunistas del enfermo inmunodeprimido, sino que se considera una herramienta poderosa para la investigación clínica, cuyo potencial dista todavía de haber sido alcanzado17.
Así, sucesivos trabajos le han confirmado como una buena traducción de la celularidad existente en el alveolo e intersticio18-21, siendo también objeto de estudio distintos marcadores de inflamación y componentes bioquímicos, presentes en diversas patologías respiratorias22,23. En la tabla 3, se exponen los resultados de los autores más destacables en este campo junto con los obtenidos por nuestro grupo24. En pediatría, no había acuerdo en la estandarización de la técnica, pero el año 2000, se inicia con la publicación de un trabajo de consenso de la European Respiratory Society, por lo que disponemos ya de una guía de referencia autorizada17. Quedan todavía sin embargo, muchas dificultades inherentes a la interpretación de sus resultados, como el área del pulmón muestreado y la falta de un indicador fiable de la cantidad de fluido recuperado entre otros, que traducen un rendimiento en la práctica clínica principalmente orientativo más que diagnóstico para la mayor parte de la patología pulmonar no infecciosa.
En lo que respecta a las infecciones respiratorias, los progresos en técnicas de biología molecular están permitiendo una mejor identificación de distintos patógenos respiratorios25 cuya presencia en el LBA es diagnóstica de enfermedad (M. Tuberculosis, VRS, Influenza, Mycoplasma, P. Carinii, L. pneumophila, Nocardia, Histoplasma, Blastomyces), mientras que el aislamiento de otros microorganismos, que pueden estar como comensales o contaminantes en las vías aéreas (VHS, CMV, aspergillus, bacterias, microbacterias atípicas y candidas). Sigue siendo objeto interminable de discusión, proponiéndose para las bacterias, la realización de cultivos cuantitativos a través de catéteres telescopados (LBA protegidos) desafortunadamente no disponibles en la actualidad, más que para BF > de 4,8 mm y por tanto utilizables sólo para los niños mayores10,17.
Fibrobroncoscopia terapéutica
Además de su clásica utilización, como vehículo de limpieza y aclaramiento de las vías aéreas broncoaspiración de distintas secreciones endobronquiales26, y de las más restringidas instilaciones de fármacos mucolíticos, antibióticos y antifúngicos los BF empiezan a formar parte del arsenal terapéutico rutinario, utilizado por anestesistas y en ambientes de UCIP, al conseguir un rápido acceso en pacientes en los que la intubación convencional es difícil27. Igualmente, gracias a los progresos en instrumentación estamos asistiendo a la publicación de nuevos logros terapéuticos con el BF, como la extracción de CE28, una indicación tradicional para la broncoscopia rígida, lo que podría originar algunos cambios en la clara y teórica división del trabajo propuesta para ambos instrumentos y para los "distintos tipos de broncoscopistas, rígidos o flexibles"29,30. En los adultos se publica un 61% de efectividad con BF frente al 98% con BR28, pareciendo lógica la mayor utilidad del BF en la extracción de los CE demasiado distales para el BR31; Esta complementariedad parece hacer recomendable actualmente, la evaluación del niño en áreas específicas de endoscopia, con personal entrenado en ambas técnicas, capaz de utilizar secuencial o alternativamente, ambos broncoscopios, según los requerimientos de cada situación32.
Otras actuaciones excepcionales, pero posibles, en niños, incluyen la instilación de material adhesivo para el cierre de fístulas broncopleurales, preferiblemente postoperatorias, aunque con las desventajas que supone el hecho de que el pegamento tenga que fluir a través de un catéter introducido en el canal de trabajo, ya que no debe entrar en contacto directo con ninguna parte del BF. La FBC además, es un instrumento al servicio de terapia médicas en fase de investigación, ya que puede ser la única forma de administrar medicamentos, que aunque sea posible su nebulización, no se distribuirían de manera uniforme gen CFTR normal en el epitelio respiratorio de los pacientes con fibrosis quística por ejemplo. En palabras de Wood, sólo estamos limitados por la física y la imaginación29.
Nuevas perspectivas
Como toda nueva técnica en medicina, su desarrollo irá experimentando una evolución paralela a los avances médicos. El progreso médico también significa menor agresividad, tanto en el diagnóstico como en el tratamiento, por lo que asistiremos al indudable desarrollo de una serie de progresos en el campo tecnológico, que probablemente revolucionarán nuestra práctica broncoscópica, pudiéndose hablar ya de los siguientes.
Broncoscopia virtual
Los avances en las imágenes obtenidas por ordenador, han logrado desarrollar la broncoscopia virtual, una técnica en evolución que consigue imágenes de tráquea, carina y bronquios principales, similares a los obtenidos por la broncoscopia tradicional, mediante un software adecuado1. Mediante la integración de los datos obtenidos por la tomografía computarizada helicoidal, se logra la navegación interactiva a través del árbol traqueobronquial, rotando una cámara virtual en todas las direcciones dentro de su luz. Puede así representarse la pared interna y la luz bronquial, visualizando además, la zona distal a una estenosis infranqueable para FBC y permitiendo un mejor conocimiento de la relación con los órganos y estructuras extratorácicas. Aunque la broncoscopia virtual, no añade información a la proporcionada por las imágenes axiales, es útil para "traducir" la información a neumólogos y cirujanos más familiarizados con estas imágenes parecidas a las broncoscópicas. La principal ventaja es obviamente, esta capacidad de visualizar la anatomía endobronquial sin realizar realmente un procedimiento invasivo como la FBC. Y la principal desventaja, la incapacidad para diferenciar entre los distintos tipos de lesiones, que requerirán la realización de una broncoscopia estándar33,34.
Una de las limitaciones de la broncoscopia virtual, es que el software confía en la presencia de aire; los tapones mucosos, CE o secreciones, que ocluyan completamente la luz, pueden originar falsas imágenes de estenosis. Otro inconveniente, principalmente en niños, es la menor calidad de las imágenes, respecto a las obtenidas en adultos, motivada por el menor tamaño de las vías aéreas y por la incapacidad de los niños pequeños de suspender la respiración durante el procedimiento33.
Broncoscopia ultrasónica
Esta nueva técnica, aún en fase de investigación, permite visualizar vía ultrasónica, estructuras circundantes a las vías aéreas que no pueden ser vistas con el BF. Existen ya estudios preliminares que han mostrado su capacidad de identificar estructuras mediastínicas tales como nódulos linfáticos, grandes vasos y esófago, de especial utilidad en el diagnóstico precoz del carcinoma broncogénico y quizá del tromboembolismo pulmonar; así mismo puede resultar muy útil en la medición de la longitud y del diámetro de estenosis bronquiales, facilitando la correcta implantación de prótesis (stents). El principal problema técnico, es la incapacidad de asegurar el perfecto acoplamiento de la sonda ultrasónica a la pared bronquial, por lo que los BF están siendo provistos de balones hinchables con agua, con la intención de lograr un contacto permanente 360 grados entre la pared de las vías aéreas y la sonda ultrasónica que permita obtener imágenes de mayor fiabilidad1,35.
Broncoscopia intervencionista
La irrupción de nuevas modalidades terapéuticas endoscópicas en la neumología de adultos prótesis, láser y ciertas alternativas al mismo, de menor coste y mayor facilidad en el aprendizaje como la crioterapia y electrocauterio han supuesto la nueva entrada en escena después de muchos años de olvido del broncoscopio rígido1,2, y no hay razones para pensar, que no sucederá lo mismo en la pediatría.
De hecho, el cambio en la fisonomía de nuestros pacientes tratamientos más agresivos de afecciones respiratorias, incluyendo el trasplante de pulmón está conduciendo al desarrollo de las llamadas técnicas de repermeabilización bronquial; así, la dilatación endoscópica de unas vías aéreas estenóticas, es posible mediante catéteres provistos de balones hinchables, sobre todo si son intrínsecas o de corta longitud36. Para las estenosis mayores, compresiones extrínsecas o traqueobroncomalacias graves, están disponibles en el mercado prótesis de distintas formas y materiales silicona (Dumon),37 metálicas, expandibles a través de balones de dilatación (Palmaz) y otras38,39. La prótesis ideal para el niño no existe aún pequeña, adherente, autoexpansible, inmóvil y extraíble y dado el grado de complicaciones actuales, deben indicarse sólo en casos de imposibilidad de extubación, o mala tolerancia clínica con dificultad respiratoria grave o episodios apneicos10. Disponemos también ya de láser aplicables a través del FB (Nd: YAG y KTP/532), con los que pueden solucionarse obstrucciones de las vías aéreas principales granulomas, papilomatosis, etc.. El coste de los equipos, lo complicado del aprendizaje y las restringidas indicaciones pediátricas, hacen que su utilización pediátrica no esté muy extendida40. La mayoría de estas técnicas intervencionistas en niños, se llevan a cabo actualmente con el BR, aunque cabe pensar que en un futuro, al simplificarse el instrumental, pudieran realizarse con BF.
Y es que el espectro completo de las aplicaciones en endoscopia respiratoria, no se ha logrado ni con el flexible, ni con el rígido, por lo que parece necesaria la experiencia en ambos procedimientos. La complementariedad, incluso, de los dos instrumentos se ha puesto de manifiesto en algunas actuaciones, como la aplicación de la terapia láser o la extracción de CE en las vías aéreas distales, en las que el BF es introducido a través del rígido, combinándose así, el control de la vía aérea conseguido con este instrumento, y la maniobrabilidad del flexible.
Probablemente el nuevo milenio, originará nuevas generaciones de broncoscopistas pediátricos, con entrenamiento y capacitación en ambas técnicas, para lo que urge el diseño de programas de aprendizaje y habilitación de unidades específicas, que realicen un número suficiente detécnicas anuales, para mantener la habilidad y aplicar las nuevas tecnologías.
Conclusiones
Infrautilizada hasta ahora, la FBC pediátrica, con su gran magnitud de posibilidades diagnóstico-terapéuticas, precisa una continua y cuidadosa reevaluación de sus indicaciones. Pero en la actualidad, una adherencia firme a alguno de los dos broncoscopios disponibles, BF o BR, para intentar resolver todos los problemas que plantea la clínica diaria, debido a la falta de entrenamiento en alguna de las dos técnicas, origina una práctica broncoscópica insuficiente.
El uso juicioso de la herramienta más apropiada, probablemente logrará en este nuevo siglo, el reto de conseguir la "broncoscopia óptima" dícese de la broncoscopia ideal desde el punto de vista del broncoscopista y del enfermo, sin olvidar el cociente coste-efectividad y del "broncoscopista óptimo" dícese del que tiene amplios conocimientos de los aspectos clínicos de la medicina pulmonar, de la anatomía de las vías aéreas, y entrenamiento en ambas técnicas, rígida y flexible, así como todos los procedimientos con ellas relacionados41.
¿Ha existido alguno en los 90?