La prescripción de un fármaco fuera de ficha técnica (PFFT) es correcta, muchas veces necesaria y realizada frecuentemente en Pediatría1, aunque no exenta de riesgos. La escasa realización de ensayos clínicos pediátricos y que la ficha técnica (FT) no se actualiza según evidencia, hacen que la PFFT forme parte de la práctica habitual. En atención primaria (AP) a nivel mundial, las tasas son muy variables (1,2-62%2, 9-52%3). En España, por cualquier fármaco, oscila entre el 27-51%.
Nuestro objetivo fue conocer las características de la PFFT y no autorizada (NA) en AP de un Área de Salud.
Se realizó un estudio observacional con medicamentos de seis consultas de pediatría (tres pediatras vía médico interno residente [MIR] y tres médicos de familia) del Área de Salud de Alcázar de San Juan (16 consultas). Estudio retrospectivo para evitar el efecto Hawthorne. Incluimos niños de 0-14 años con prescripción en junio y/o diciembre de 2018. Los fármacos según FT cumplieron la FT en indicación, dosis, frecuencia, edad/peso y vía de administración; los clasificados como fuera FT (FFT) no cumplían FT en alguna variable; Los NA no estaban aprobados, estaban contraindicados o administrados tras modificación de fórmula farmacéutica.
Los fármacos se codificaron según el índice Anatomical Therapeutic Chemical Classification System (ATC). Se obtuvo consentimiento paterno/tutores para acceso a la historia y la aprobación del Comité de Ética, Investigación y Medicamentos del Área de Salud, en cumplimiento del Real Decreto 957/2020, de 3 de noviembre, por el que se regulan los estudios observacionales con medicamentos de uso humano.
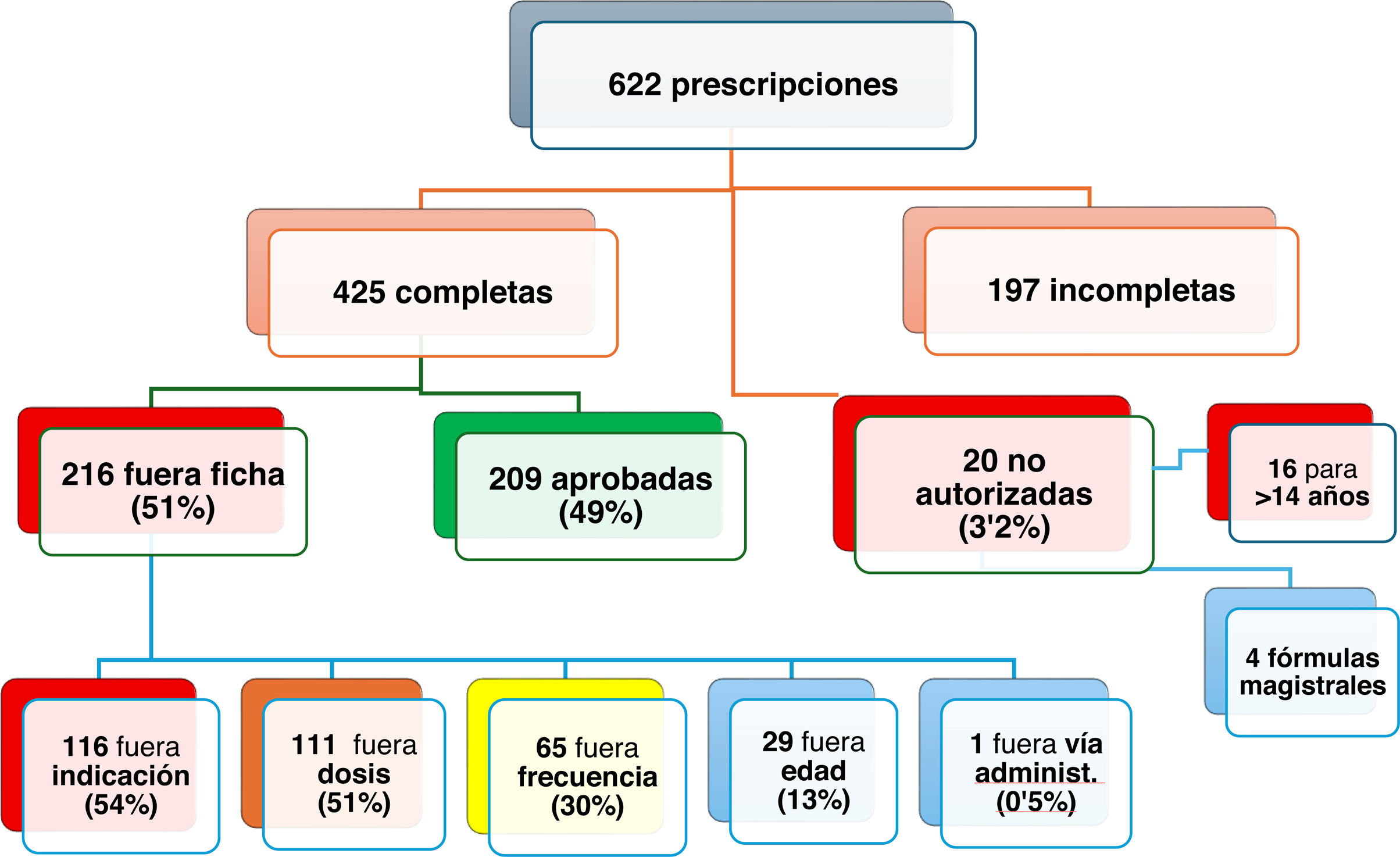
Como resultados, se analizaron 622 prescripciones en 418 pacientes. Hubo 192 medicamentos, 82 principios activos y 1,4 medicamentos/paciente. Edad media 8,6 años (cuatro días-14,4 años). Niños ≥ 6 años (65,5%).
Cuatrocientas veinticinco prescripciones tenían recogidas las variables para el análisis. La figura 1 muestra el porcentaje de PFFT, de NA y sus causas. Los fármacos más prescritos FFT: ibuprofeno (14,8%), paracetamol (12%), salbutamol MDI (9,3%), amoxicilina (8,8%), cetirizina (6,9%), budesonida MDI (6%) y domperidona (5,5%).
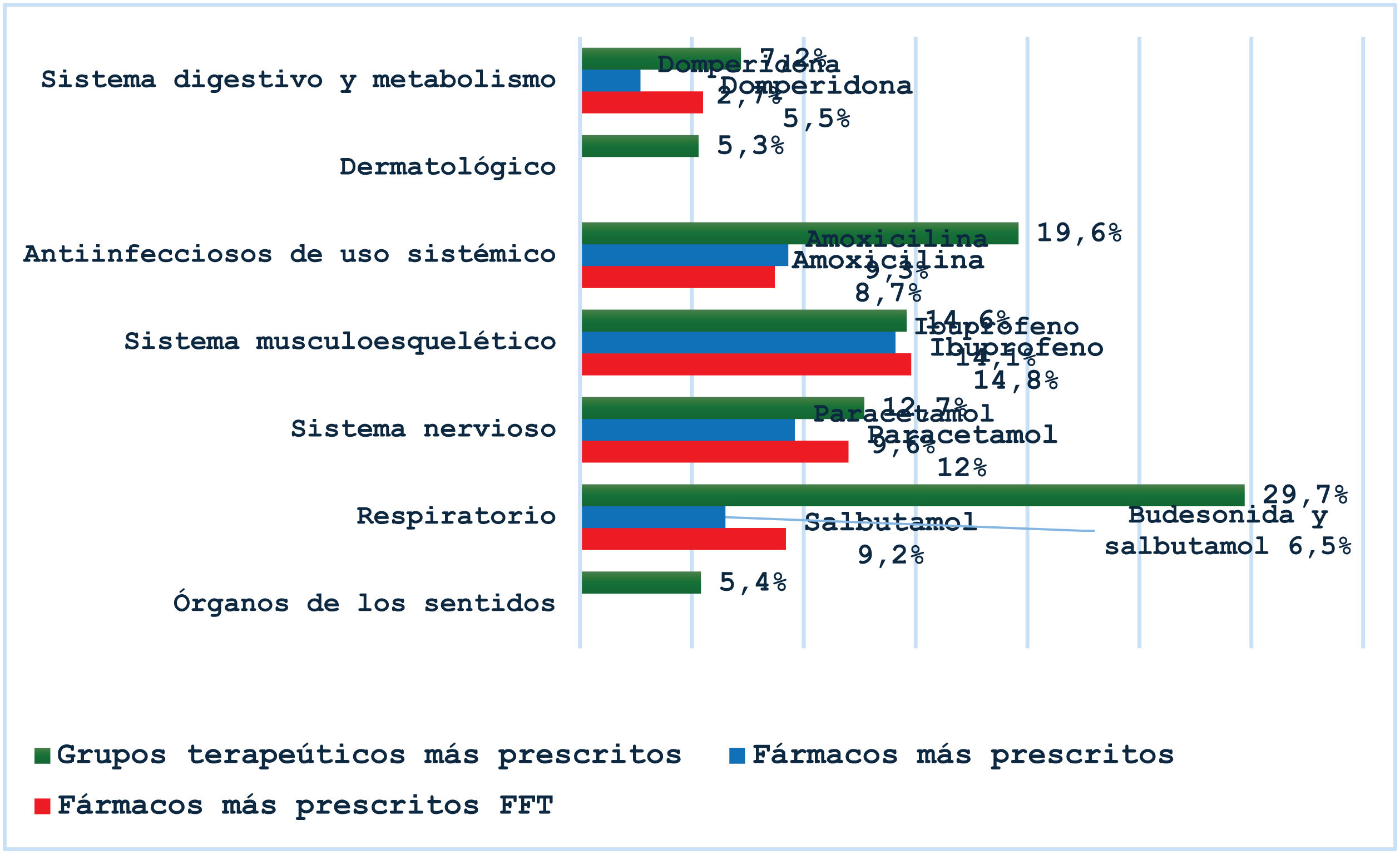
La figura 2 muestra los grupos terapéuticos más frecuentes, los fármacos más prescritos y los más prescritos FFT.
No hubo diferencias significativas en PFFT según estación.
Los factores que provocaron mayor PFFT según el análisis multivariante fueron: Grupo Respiratorio, factor de riesgo (FR) 11,2 (IC 95% 3-41,9), p <0,0001; Grupo Digestivo y metabolismo FR 7,3 (IC 95% 1,7-31,7), p 0,008; Grupo Músculo-esquelético FR 6,4 (IC 95% 1,6-25,2), p 0,008; Grupo Neurológico FR 5,7 (IC 95% 1,4-22,85), p 0,014; Médico no pediatra FR 3,8 (IC 95% 2,3-6,15), p <0,0001 y edad (por cada año más) FR 0,8 (IC 95% 0,8-0,99), p <0,0001.
En ningún paciente se registró la justificación de utilización del fármaco ni se había reflejado el consentimiento paterno verbal o escrito (Figura 1 suplementariaFigura 2 suplementaria).
La PFFT sigue siendo alta, es un problema mundial, mayor a menor edad del niño, con mayor riesgo de efectos secundarios y que apenas ha mejorado tras los esfuerzos legislativos de las autoridades sanitarias. Su importancia fue señalada por el Comité de Medicamentos de la Asociación Española de Pediatría en 20211. Por las diferencias existentes en las definiciones de PFFT y NA y en la metodología y fuente de datos, los resultados son dispares1. Muchos trabajos en AP se basan en grandes registros farmacéuticos, pero sin recoger la indicación y la dosificación, lo que infraestima la verdadera tasa de PFFT. En una revisión de Balan et al2, solo la mitad de los estudios incluyeron todas las variables para definir adecuadamente la PFFT.
Nuestros resultados cifran la PFFT en el 51%, que es elevada, datos similares a los de Morales-Carpí et al. en AP en 20104 y otros estudios europeos2,3. Cifras menores de PFFT obtuvieron Blanco-Reina et al. (27%), en 2014, pero a nivel urbano (2 centros de salud y urgencias hospitalarias)5 y otros estudios en AP de nuestro entorno2,3.
La prescripción NA (3,2%) fue bastante inferior a la de Morales Carpí (12%)4, similar a otros estudios europeos2,3 y superior a la de Blanco-Reina et al. (1%)5.
La causa más frecuente de PFFT fue no cumplir la indicación y dosis, al igual que la mayoría de los estudios2–4,6. Los fármacos más prescritos FFT fueron los del grupo respiratorio, antiinfecciosos sistémicos, sistema nervioso y tracto digestivo y metabolismo, similar a lo descrito2,3.
Como conclusiones, se observa un alto porcentaje de prescripciones FFT y ningún registro escrito de la justificación de su uso ni del consentimiento paterno. Debemos informar sobre el uso de un medicamento FFT siempre respaldado por los conocimientos científicos y registrarlo en la historia clínica tras el consentimiento paterno.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores agradecen a Dña. Beatriz Navarro Bravo y al Dr. Ángel Árias Árias su análisis estadístico. Agradecer también al Dr. Ramón Garrido Palomo y al Dr. Juan Trigo Moreno su revisión crítica del artículo.
Presentado en XIV Jornada Científica de la Asociación de Pediatría de Atención Primaria de Castilla La-Mancha, en línea, 26 de septiembre de 2020.