La aplasia medular adquirida es un trastorno con una incidencia estimada de 1-2 casos por millón de habitantes al año1, caracterizado por una hipocelularidad de las células madre de la médula ósea, que resulta en pancitopenia. El tratamiento estándar en niños es el trasplante de progenitores hematopoyéticos (TPH) de donante familiar idéntico; si este no es posible, la terapia inmunosupresora2, y si no funciona, el TPH de donante no emparentado HLA idéntico. Eltrombopag, un análogo de la trombopoyetina, se ha presentado recientemente como posible arma terapéutica en la aplasia refractaria. Existen en la literatura pruebas de su efectividad en adultos, pero su papel en pacientes pediátricos no ha sido evaluado.
Presentamos el caso de una niña de 11 años con diagnóstico de aplasia medular adquirida grave, que presentó datos de recuperación trilineal en sangre periférica tras iniciar tratamiento con eltrombopag.
La paciente consultó por petequias y equimosis generalizadas, astenia y metrorragia de 15 días de evolución. La analítica reveló pancitopenia grave con datos de anemia hiporregenerativa (hemoglobina 7,6g/dl, reticulocitos 0,69%), plaquetas 8×1.000/μl y neutrófilos 0,5×1.000/μl, sin afectación del perfil bioquímico, datos de hemólisis ni coagulopatía. Frotis de sangre periférica sin elementos blásticos y serologías negativas. Se realizó aspirado-biopsia de médula ósea compatible con aplasia medular grave. La hemoglobinuria paroxística nocturna fue descartada; el estudio de fragilidad cromosómica realizado fue negativo.
Dado que la paciente no tenía donante familiar HLA idéntico, se inició tratamiento inmunosupresor con timoglobulina y ciclosporina junto con G-CSF. La respuesta inicialmente fue buena, encontrándose en situación de buena respuesta parcial en el día +60. Posteriormente presentó empeoramiento progresivo hasta que en el día +120 presentaba datos de «no respuesta» con necesidades transfusionales semanales. Debido al fracaso de la terapia inmunosupresora, se consideró a la paciente candidata a TPH de donante no emparentado dado que no existía donante familiar. Tras 6 meses de búsqueda sin aparición de posible donante y dada la situación de aplasia medular grave se decidió iniciar tratamiento con eltrombopag a dosis de 50mg cada 24h vía oral. En control analítico a las 3 semanas ya se objetivó respuesta en las 3 líneas hematológicas, presentando desde la semana 7 de tratamiento cifras mantenidas de hemoglobina en torno a 12g/dl, plaquetas ≥50.000/μl y neutrófilos de 1.500/μl. En la semana 15 se inició el descenso progresivo de la dosis de ciclosporina, que pudo suspenderse en la semana +44 sin evidenciarse alteración en los recuentos celulares.
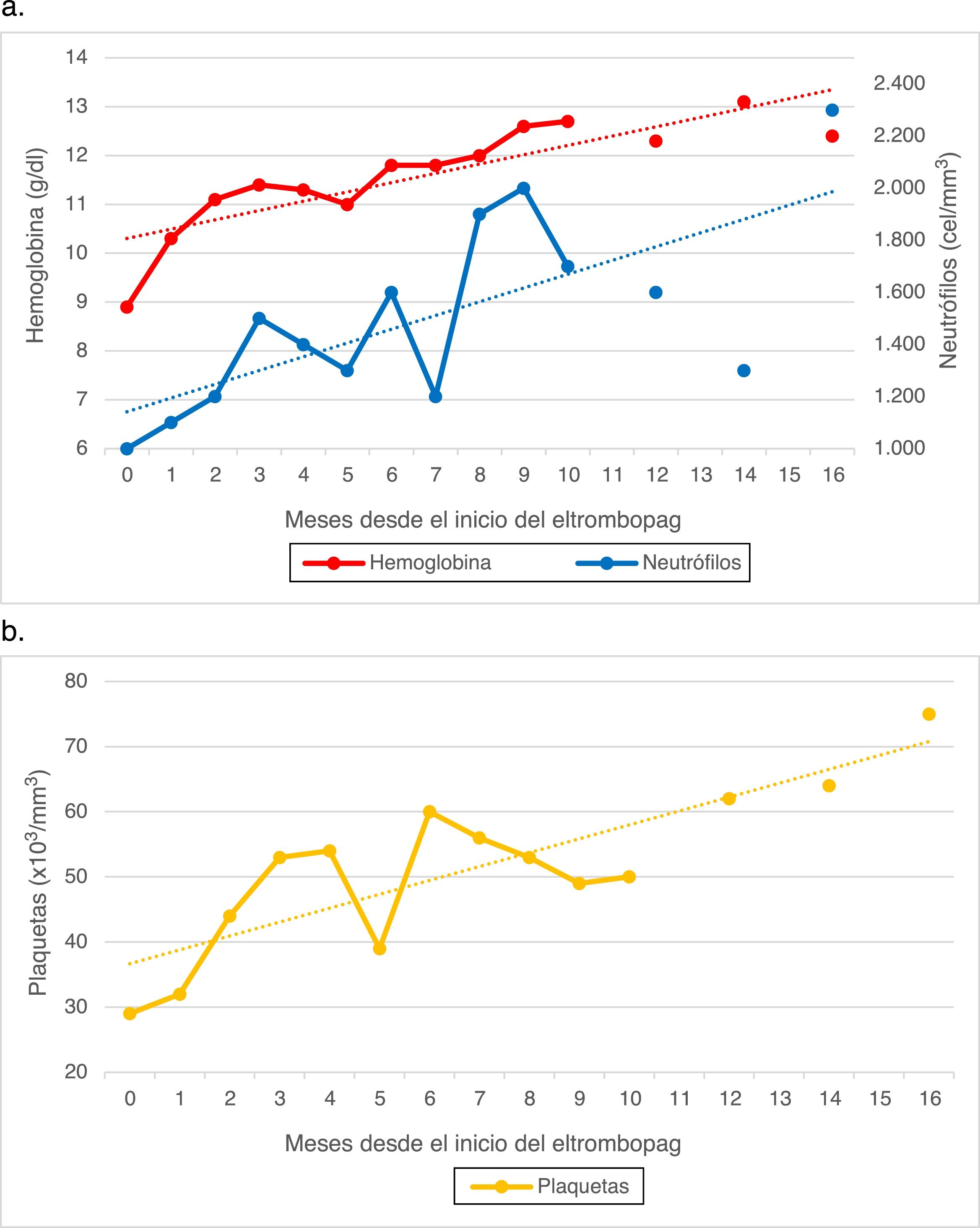
En la actualidad, tras 16 meses de tratamiento con eltrombopag a 50mg/24h, 5 de ellos en monoterapia, el estudio de médula ósea de control muestra discreta hipocelularidad con aumento de todas las líneas hematopoyéticas en comparación con estudios previos. En sangre periférica persisten cifras estables (fig. 1). Durante este tiempo la paciente no ha presentado ningún efecto secundario al tratamiento.
La aplasia medular adquirida idiopática es la causa más frecuente de aplasia en niños. En los casos graves, como el que presentamos, se trata de una entidad amenazante para la vida dado el riesgo de hemorragia e infección, siendo fundamental instaurar el tratamiento óptimo. En nuestra paciente se utilizó inicialmente el régimen de tratamiento de primera línea que consiste en una combinación de timoglobulina y ciclosporina3, incluyéndose nuestro caso en el 30% de no respondedores a esta terapia. Varias estrategias han sido probadas para este grupo de pacientes; el primer ensayo clínico publicado de eltrombopag en aplasia medular fue realizado por Olnes et al. en 2012 en adultos. Posteriormente, nuevos ensayos han continuado evidenciando el papel de este análogo de la trombopoyetina en la elevación de los recuentos no solo plaquetarios sino trilineales de la sangre periférica4 en pacientes adultos con aplasia medular. Los ensayos con eltrombopag en pacientes pediátricos han sido realizados únicamente para el tratamiento de la trombocitopenia inmune primaria crónica5 y en la aplasia postrasplante6, en ambas entidades con buenos resultados. No está descrita en la literatura su utilización en niños con aplasia medular idiopática.
El interés de nuestro caso radica en que se ilustra por primera vez la eficacia de este tratamiento en un caso de aplasia medular infantil, habiéndose demostrado una respuesta celular mantenida tras un año de tratamiento. Cabe destacar que no se han constatado efectos secundarios en estos 16 meses, si bien el seguimiento es limitado para valorar su toxicidad a largo plazo.
Aunque estos resultados sugieren que eltrombopag u otros agonistas del receptor de la trombopoyetina pueden representar un nuevo enfoque para el tratamiento de esta enfermedad en niños, deben llevarse a cabo ensayos clínicos específicos que confirmen esta premisa.