El objetivo de este estudio ha sido analizar el estado de nutrición, la alimentación y las complicaciones digestivas de los niños que precisan técnicas de depuración extrarrenal continua (TDEC).
Material y métodosEstudio retrospectivo realizado sobre una base de datos prospectiva de los niños tratados con TDEC entre 2013 y 2017. Se analizaron las características de los pacientes, la técnica de depuración, el tipo de nutrición, el aporte calórico y proteico, las complicaciones digestivas y la evolución clínica.
ResultadosSesenta y cinco niños (61,5% varones) fueron tratados con TDEC y 24 (37%) precisaron soporte con oxigenación con membrana extracorpórea. Un 27,7% tenían un peso inferior al percentil 3 y un 48,4% una talla inferior al percentil 3. Al inicio de la TDEC 31 niños (47,7%) recibían nutrición enteral y 52 (80%) al final de la misma. La nutrición enteral fue por sonda transpilórica en el 76% de los casos. La mediana de aporte calórico fue de 63kcal/kg/día y la del aporte proteico de 1,6g/kg/día. Cuarenta y ocho pacientes (73,8%) presentaron complicaciones digestivas: 29 (44,6%) distensión gástrica o restos gástricos excesivos, 22 (33,8%) estreñimiento, 8 (12,3%) vómitos y 4 (6,1%) diarrea. Un paciente con oxigenación con membrana extracorpórea presentó isquemia intestinal. En 3 pacientes (4,6%) se tuvo que suspender la nutrición enteral por complicaciones. No existió relación entre las complicaciones y el tipo de alimentación o la asistencia en oxigenación con membrana extracorpórea.
ConclusionesUn elevado porcentaje de niños tratados con TDEC presentan malnutrición, pero la mayoría pueden ser alimentados con nutrición enteral. Aunque el porcentaje de complicaciones digestivas es elevado, en pocos pacientes se tiene que suspender la nutrición enteral.
The aim of this study was to analyse the nutritional state, diet and gastrointestinal complications of children that require continuous renal replacement therapy (CRRT).
Material and methodsA retrospective analysis of a database, which included the information about patients who required CRRT between the years 2013 and 2017. Data were collected on the replacement technique, type of nutrition, calorie and protein intake, gastrointestinal complications, and clinical course.
ResultsA total of 65 children (61.5% male) were treated with CRRT, and 24 patients (37%) also needed ECMO support. Just over one-quarter (27.7%) of patients had a weight less than P3, and 48.4% of them a height less than P3. At the beginning of the technique, 31 children (47.7%) received enteral nutrition, at the end, there were 52 patients receiving enteral nutrition (80%). The transpyloric tube was used to provide nutrition in 76% of the cases. The median caloric intake was 63kcal/kg/day, and the protein intake was 1.6g/kg/day. There were gastrointestinal difficulties during the process in 48 patients (73.8%), with 29 (44.6%) patients being diagnosed with gastric distension or excessive gastric remains, 22 (33.8%) with constipation, 8 (12.3%) with vomiting, and 4 (6.1%) diarrhoea. One patient treated with ECMO presented with intestinal ischaemia. Enteral nutrition was cancelled in 3 patients (4.6%) due to the complications. There was no relationship between complications and type of diet or ECMO assistance.
ConclusionsA high percentage of children treated with CRRT showed undernutrition but they had adequate tolerance to the enteral nutrition. Although the gastrointestinal complications percentage was high in few subjects, these complications are the reason why enteral nutrition was stopped.
Un importante porcentaje de niños que ingresan en unidades de cuidados intensivos pediátricos (UCIP) presentan daño renal agudo (DRA) y aproximadamente un 5% precisan técnicas de depuración extrarrenal1,2. Las técnicas de depuración extrarrenal continua (TDEC) son las más utilizadas, ya que consiguen la eliminación controlada de líquidos y permiten una alimentación sin restricciones3,4.
Los niños con DRA presentan un mayor riesgo de malnutrición, que se relaciona con un aumento de la morbimortalidad1–6. Además, frecuentemente presentan otros factores como alteraciones hemodinámicas, ventilación mecánica y disminución de la motilidad gástrica por la administración de fármacos sedantes y relajantes musculares que aumentan el riesgo de mala tolerancia de la nutrición1,2,4.
Por otra parte, las técnicas de depuración pueden producir pérdida de nutrientes, aminoácidos, vitaminas, folato o minerales como el selenio, a través del filtro6.
Existen pocos estudios que hayan analizado las características de la nutrición de los niños que reciben TDEC4,6–8. Un estudio previo encontró que las complicaciones digestivas en los niños con DRA eran más frecuentes que en el resto de los niños en estado crítico, y la mayor incidencia de estas complicaciones estaba relacionada con la mayor gravedad de estos pacientes4.
Los objetivos de este estudio han sido analizar el estado de nutrición, las características de la nutrición y las complicaciones digestivas en los niños tratados con TDEC.
Pacientes y métodosSe realizó un análisis retrospectivo de una base de datos prospectiva de los niños ingresados en el Servicio de Cuidados Intensivos Pediátricos y tratados con TDEC entre enero de 2013 y diciembre de 2017. El estudio fue aprobado por el comité de ética local. Se excluyeron los pacientes tratados con otras técnicas de depuración extrarrenal (diálisis peritoneal, inmunoabsorción, plasmafiltración).
Se recogieron las siguientes variables: datos epidemiológicos y clínicos (edad, sexo, peso, talla, superficie corporal, diagnóstico), indicación y características de la TDEC, tipo de nutrición, vía de nutrición enteral (sonda nasogástrica, sonda transpilórica, alimentación oral), tipo de dieta, máximo aporte nutricional (calorías y proteínas), tiempo en alcanzar el máximo aporte enteral, características de la nutrición parenteral (volumen total, proteínas, hidratos de carbono y lípidos del primer día), complicaciones digestivas (distensión abdominal significativa a criterio del médico responsable del paciente, restos gástricos [50% de lo administrado en las anteriores 4h], diarrea [más de 8 deposiciones líquidas en lactantes hasta los 3 meses, más de 4 deposiciones líquidas en los lactantes entre 3 y 12 meses, y más de 2 deposiciones líquidas en mayores de 12 meses], estreñimiento [>72h sin realizar deposición a pesar de recibir nutrición enteral], vómitos [>2 vómitos en 24h]), isquemia intestinal (signos clínicos [hemorragia digestiva, distensión abdominal, mala perfusión de la pared abdominal] unidos a hallazgos de isquemia intestinal en la ecografía o la TAC), hipertransaminemia (ALT>65U/L y AST>400U/L), necesidad de oxigenación por membrana extracorpórea (ECMO) y evolución del paciente (supervivencia, causa del fallecimiento y duración del ingreso en la UCIP).
Aunque la nutrición se adaptó de forma individual a cada paciente, de acuerdo con nuestro protocolo, el objetivo de aporte calórico inicial fue de 60 a 65kcal/kg metabólico y 1,5 a 2g/kg de proteínas, y en los casos en que se puede realizar la calorimetría indirecta, 1,3 el valor del consumo calórico.
Para el cálculo de los percentiles de peso y talla y la puntuación z se usó la aplicación nutricional de la Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (https://www.seghnp.org/nutricional) utilizando como referencia las tablas de Fernández, y para clasificar el estado de nutrición se utilizaron los Índices de Waterlow para talla y peso (IWt e IWp), según las fórmulas: IWt=(talla real/p50 de talla para la edad)×100. IWp=(peso real/peso para p50 de talla)×100. El estado de nutrición se clasificó en9: IWp normal>90%, IWt normal>95%, desnutrición aguda (leve IWp: 80-90%, moderada 70-80%, grave<70%), sobrenutrición (IWp>115%), desnutrición crónica (leve IWt 90-95%, moderada: 85-90%, grave<85%).
Se estudió la relación de la tolerancia a la alimentación y las complicaciones digestivas con las características del paciente, la nutrición y el tratamiento simultáneo con ECMO y TDEC.
Se realizó estudio estadístico con el programa IBM SPSS versión 21.0. Las variables cuantitativas con distribución normal se presentan con medias y desviaciones estándar y aquellas que no cumplen los supuestos de normalidad, como mediana y rango intercuartílico (RIC) (p25-p75). Las variables cualitativas se presentan como porcentajes. Para la comparación de variables cualitativas se utilizaron la prueba de χ2 y el test exacto de Fisher. Para la comparación de medias en variables cuantitativas se utilizó la prueba t de Student. Se consideró significativo un valor de p<0,05.
ResultadosSe estudiaron 65 niños tratados con TDEC en 5 años, el 61,5% eran varones. La mediana de edad fue de 13,9 meses (RIC 4,6-80,7 meses). Los diagnósticos al ingreso fueron: cardiopatía 75%, postoperatorio de cirugía abdominal 5%, insuficiencia renal crónica agudizada 2%, sepsis 3%, síndrome hemolítico urémico 3%, insuficiencia respiratoria 3%, otros 9%. El 92,3% recibían ventilación mecánica y un 36,9% ECMO.
La mediana de peso era de 8,9kg (RIC 5,6-18,7kg). La mediana de la puntuación z fue de −1,28 (RIC −0,78 a −1,93). Dieciocho pacientes (27,7%) tenían un peso inferior al p3 y 31 (48,4%) una talla inferior al p3. Un 32,8% tenían malnutrición aguda (IWp<90%): 61,9% desnutrición leve; 19% moderada y 19% grave. Un 60,9% tenían malnutrición crónica (IWt<95%): 38,5% desnutrición leve, 33,3% moderada y 28,2% grave.
La TDEC se inició a los 3 días de ingreso en la UCIP (RIC 1-7 días). La TDEC fue en todos los casos hemodiafiltración venovenosa realizada con el monitor Prismaflex® (Baxter). La duración de la TDEC fue de 7 días (RIC 4-16 días). La razón de finalización de la TDEC fue la recuperación de la función renal en un 70,8%, exitus en un 24,6% y el paso a otra técnica de depuración en un 4,6%.
Al inicio de la TDEC un 81,5% recibían nutrición (47,7% por vía enteral y 33,8% por vía parenteral). Un 18,5% estaba a dieta con fluidoterapia.
En un 75,5% de los pacientes la nutrición enteral se realizó por sonda transpilórica, en un 20,8% por sonda nasogástrica y en un 3,8% alimentación oral.
Las dietas de nutrición enteral fueron: fórmula infantil 6%, leche materna 9%, dieta hipercalórica de lactante (Infatrini®) 21%, hidrolizado de proteínas 19%, dieta hipercalórica de niño (Isosource® Junior) 30%, fórmula con alto contenido en ácidos grasos de cadena media (Monogen®) 9%, fórmula de insuficiencia renal (Suplena®) 6%. La mediana de tiempo para alcanzar el aporte máximo de nutrición enteral fue de 6h (RIC 3-12h). El volumen máximo de la nutrición enteral fue de 64ml/kg/día (RIC 36-100ml), con un aporte calórico de 63kcal/kg/día (RIC 43-72kcal) y 1,6g de proteínas/kg/día (RIC 0,97-2,2g). No existieron diferencias significativas en el aporte calórico y proteico entre los que recibieron nutrición vía gástrica (mediana de aporte calórico 60kcal/kg y proteico 1,62g/kg) y los que recibieron nutrición transpilórica (mediana de aporte calórico 67kcal/kg y proteico 1,55g/kg).
El volumen de nutrición parenteral el primer día fue de 50ml/kg/día de mediana (RIC 39,4-62,9ml), con un aporte calórico de 53,3kcal/kg/día (RIC 49-66,7kcal), de proteínas de 2,0g/kg/día (RIC 1,5-2,9g), 8,2g/kg/día de hidratos de carbono (RIC 7,7-10,2g) y 1,1g/kg/día de lípidos (RIC 1-2g).
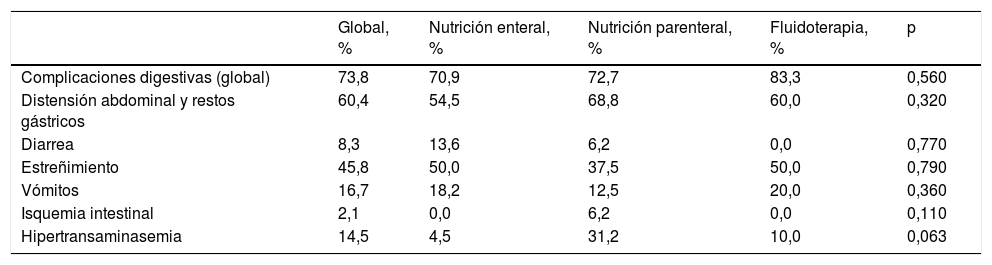
Cuarenta y ocho pacientes (73,8%) presentaron complicaciones digestivas durante la TDEC. La tabla 1 recoge las complicaciones digestivas en relación con el tipo de nutrición. No existieron diferencias en la frecuencia de distensión o restos gástricos, vómitos, diarrea o estreñimiento entre los pacientes tratados inicialmente con nutrición enteral, parenteral o fluidoterapia. Solamente un paciente (2,1%), que recibía nutrición parenteral, presentó isquemia intestinal. La hipertransaminemia fue más frecuente con la alimentación parenteral, sin existir diferencias estadísticamente significativas. En 3 pacientes se suspendió la nutrición enteral por sospecha de isquemia intestinal, íleo paralítico y rabdomiosarcoma de la vía biliar, y en 4 tuvo que reducirse y añadir nutrición parenteral (por hematoma intramural duodenal o distensión abdominal). No existieron diferencias en la incidencia de complicaciones digestivas entre los niños alimentados por vía gástrica (distensión abdominal 40%, diarrea 10%, estreñimiento 50%) y vía transpilórica (distensión abdominal 48,2%, diarrea 6,8%, estreñimiento 51,7%), excepto en la incidencia de vómitos, que fue mayor con la nutrición gástrica (40%) que con la transpilórica (6,8%) (p=0,01).
Frecuencia de complicaciones digestivas. Comparación entre los tipos de nutrición
| Global, % | Nutrición enteral, % | Nutrición parenteral, % | Fluidoterapia, % | p | |
|---|---|---|---|---|---|
| Complicaciones digestivas (global) | 73,8 | 70,9 | 72,7 | 83,3 | 0,560 |
| Distensión abdominal y restos gástricos | 60,4 | 54,5 | 68,8 | 60,0 | 0,320 |
| Diarrea | 8,3 | 13,6 | 6,2 | 0,0 | 0,770 |
| Estreñimiento | 45,8 | 50,0 | 37,5 | 50,0 | 0,790 |
| Vómitos | 16,7 | 18,2 | 12,5 | 20,0 | 0,360 |
| Isquemia intestinal | 2,1 | 0,0 | 6,2 | 0,0 | 0,110 |
| Hipertransaminasemia | 14,5 | 4,5 | 31,2 | 10,0 | 0,063 |
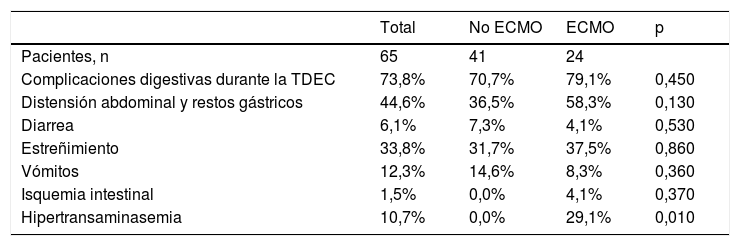
Veinticuatro niños (36,9%) fueron tratados simultáneamente con ECMO y TDEC. Presentaron complicaciones digestivas el 79,1% de los pacientes tratados con ECMO y TDEC, frente al 70,7% de los que recibieron únicamente TDEC (p=0,45). La tabla 2 recoge las complicaciones digestivas en pacientes con y sin ECMO.
Complicaciones digestivas en los niños con ECMO y sin ECMO
| Total | No ECMO | ECMO | p | |
|---|---|---|---|---|
| Pacientes, n | 65 | 41 | 24 | |
| Complicaciones digestivas durante la TDEC | 73,8% | 70,7% | 79,1% | 0,450 |
| Distensión abdominal y restos gástricos | 44,6% | 36,5% | 58,3% | 0,130 |
| Diarrea | 6,1% | 7,3% | 4,1% | 0,530 |
| Estreñimiento | 33,8% | 31,7% | 37,5% | 0,860 |
| Vómitos | 12,3% | 14,6% | 8,3% | 0,360 |
| Isquemia intestinal | 1,5% | 0,0% | 4,1% | 0,370 |
| Hipertransaminasemia | 10,7% | 0,0% | 29,1% | 0,010 |
ECMO: oxigenación por membrana extracorpórea; TDEC: técnicas de depuración extrarrenal continua.
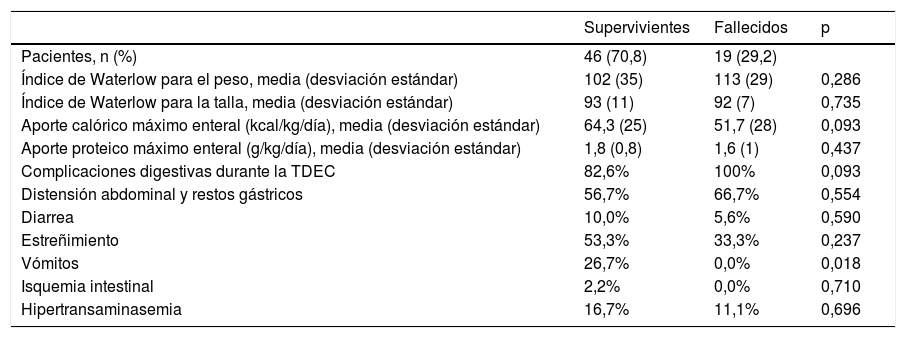
La mediana de estancia en la UCIP fue de 34,5 días (RIC 21-58,2 días). Diecinueve pacientes fallecieron (29,2%). La causa más frecuente de exitus fue el fallo multiorgánico (57,9%), seguido de la causa cardiaca (21,1%), la muerte cerebral (5,3%) y la isquemia intestinal (5,3%). Un 28,9% de los supervivientes y un 21,1% de los fallecidos tenían un peso inferior al p3 (p=0,758). Fallecieron un 23,5% de los niños con un peso<p3 y un 31,9% de los niños con>p3 (p=0,758). Un 46,5% de los supervivientes y un 50% de los fallecidos tenían una talla inferior al p3 (p=0,810). No existieron diferencias en el IW de peso y talla entre los niños supervivientes y los fallecidos (tabla 3).
Comparación del estado nutricional, el aporte nutricional y las complicaciones digestivas entre los niños supervivientes y los fallecidos
| Supervivientes | Fallecidos | p | |
|---|---|---|---|
| Pacientes, n (%) | 46 (70,8) | 19 (29,2) | |
| Índice de Waterlow para el peso, media (desviación estándar) | 102 (35) | 113 (29) | 0,286 |
| Índice de Waterlow para la talla, media (desviación estándar) | 93 (11) | 92 (7) | 0,735 |
| Aporte calórico máximo enteral (kcal/kg/día), media (desviación estándar) | 64,3 (25) | 51,7 (28) | 0,093 |
| Aporte proteico máximo enteral (g/kg/día), media (desviación estándar) | 1,8 (0,8) | 1,6 (1) | 0,437 |
| Complicaciones digestivas durante la TDEC | 82,6% | 100% | 0,093 |
| Distensión abdominal y restos gástricos | 56,7% | 66,7% | 0,554 |
| Diarrea | 10,0% | 5,6% | 0,590 |
| Estreñimiento | 53,3% | 33,3% | 0,237 |
| Vómitos | 26,7% | 0,0% | 0,018 |
| Isquemia intestinal | 2,2% | 0,0% | 0,710 |
| Hipertransaminasemia | 16,7% | 11,1% | 0,696 |
TDEC: técnica de depuración extrarrenal continua.
Un 54,3% de los niños que sobrevivieron y un 31,6% de los fallecidos recibieron inicialmente nutrición enteral (p=0,110).
Todos los pacientes que fallecieron presentaron alguna complicación digestiva, pero ninguna complicación fue significativamente más frecuente en los fallecidos que en los supervivientes. Por el contrario, los vómitos fueron más frecuentes en los supervivientes que en los fallecidos.
DiscusiónAunque varios trabajos han analizado la relación entre la malnutrición y el DRA y la tolerancia de la nutrición en adultos y niños tratados con TDEC1–7, nuestro estudio es el primero que ha analizado el estado de nutrición de estos niños, las características del soporte nutricional y la relación entre el desarrollo de complicaciones digestivas y el tipo de nutrición, el tratamiento con ECMO y TDEC, y la mortalidad.
Un elevado porcentaje de los niños que ingresan en la UCIP están malnutridos y la malnutrición se asocia con un peor pronóstico9,10. Kyle et al. encontraron que los niños con DRA sin TDEC presentaban malnutrición aguda con mayor frecuencia (33%) que los que no presentaban DRA2. En un estudio previo en el que se analizó el estado nutricional de 174 niños tratados con TDEC, se encontró que el 35% tenían un peso inferior al p3, y el 56% tenía una relación peso/talla inferior a 0,8511. La mortalidad de los niños con un peso<p3 fue significativamente mayor que la del resto (51 frente a 33%; p=0,037). En el estudio multivariante la malnutrición se relacionó con la mortalidad11. Nuestro estudio actual también muestra que los niños tratados con TDEC presentan una elevada frecuencia de malnutrición aguda y crónica, pero no se encontró asociación entre el estado nutricional y la mortalidad.
Las necesidades calóricas en los niños en estado crítico en los primeros días de ingreso en la UCIP suelen variar entre 40 y 60kcal/kg/día12. No hay estudios que hayan analizado el consumo calórico de los niños con DRA y TDEC. Aunque lo ideal es calcular las necesidades calóricas por calorimetría indirecta8, esta técnica solamente está disponible en pocos centros. En nuestro estudio se alcanzó un aporte calórico de 63kcal/kg/día, pero no podemos saber si este es un aporte suficiente.
El aporte proteico es una parte esencial de la nutrición en los niños en estado crítico, ya que es necesario para prevenir el catabolismo y promover la síntesis proteica13. En niños críticamente enfermos se recomienda un aporte proteico de al menos 1,5g/kg/día12. En el DRA se ha recomendado restringir el aporte proteico, pero en los niños tratados con TDEC esta técnica sustituye la función depuradora del riñón y, por tanto, no es necesario realizar restricción proteica. Algunos autores opinan que estos niños deberían recibir un aporte proteico de 1,5 a 2,5g/kg/día para compensar la pérdida que se produce a través del hemofiltro y asegurar un balance de nitrógeno positivo8,14.
En nuestro estudio, los niños tratados con nutrición enteral recibieron un aporte proteico en el límite inferior del recomendado (1,6g/kg/día), aunque no se realizó estudio de balance nitrogenado. Por el contrario, los niños tratados con nutrición parenteral recibieron un aporte proteico superior (2g/kg/día) el primer día de la nutrición. Estos resultados coinciden con lo encontrado por Wong Vega et al. en 41 niños tratados con TDEC, en los que los alimentados por vía enteral recibieron menos proteínas que los alimentados por vía parenteral7.
La nutrición enteral es de elección en la mayoría de los niños en estado crítico debido a que favorece el trofismo intestinal, estimula el sistema inmune, reduce la translocación bacteriana y disminuye la incidencia de sepsis y fallo multisistémico1. La alimentación parenteral debe reservarse para los que no toleren la nutrición enteral o cuando esta no logre aportar una cantidad suficiente de energía y proteínas13. Sin embargo, existe la creencia de que el DRA puede reducir la tolerancia a la nutrición enteral, y por eso muchos de los pacientes críticos con DRA son tratados con nutrición parenteral2,4,7. En un estudio reciente solamente un 12% de los niños con TDEC recibieron nutrición enteral exclusiva7. Sin embargo, en nuestra experiencia la nutrición enteral transpilórica ha demostrado ser una buena alternativa en niños en estado crítico, ya que evita los problemas del vaciamiento gástrico, permitiendo su utilización en pacientes con sedación profunda y relajación muscular, y realizar un rápido incremento de la nutrición hasta alcanzar el objetivo calórico15–17. En nuestro estudio, la nutrición transpilórica fue el método utilizado en el 75% de los pacientes tratados con nutrición enteral, con menor incidencia de vómitos que con la nutrición gástrica. Este hecho podría explicar el mayor porcentaje de pacientes alimentados por vía enteral con respecto a otros estudios. Por ello pensamos que la nutrición enteral transpilórica podría ser la inicial de elección para los niños críticos con TDEC4.
Existen muy pocos estudios que hayan analizado la tolerancia y los efectos adversos de la nutrición enteral en pacientes con DRA4. La frecuencia de complicaciones digestivas en nuestros pacientes fue elevada, coincidiendo con lo encontrado en un estudio previo, en el que la frecuencia de complicaciones fue significativamente mayor en los niños con DRA que en el resto de los niños en estado crítico4.
La complicación digestiva más frecuente en nuestros pacientes fue la distensión abdominal, seguida del estreñimiento, los vómitos y la diarrea, sin existir diferencias significativas entre los niños tratados con nutrición enteral y parenteral. Este hecho apunta a que esas complicaciones no están directamente producidas por la nutrición, sino que están más relacionadas con la enfermedad y la gravedad del paciente.
En nuestro estudio, la nutrición enteral solo se tuvo que suspender definitivamente en 3 pacientes y en ninguno de ellos la suspensión de la nutrición fue debida directamente a la alimentación. Nuestros resultados ponen de manifiesto que a pesar de la elevada incidencia de complicaciones digestivas que aparecen en niños tratados con nutrición enteral, la mayoría son poco importantes y no obligan a suspender definitivamente la alimentación.
Existen pocos trabajos que hayan analizado la nutrición en niños con ECMO. Algunos utilizan fundamentalmente la nutrición parenteral, por el posible riesgo de que una inadecuada perfusión intestinal e isquemia mesentérica produzcan una enterocolitis necrosante, isquemia intestinal, perforación o hemorragia gastrointestinal, mientras que otros utilizan la nutrición enteral18–20.
Un porcentaje importante de nuestros pacientes (36,9%) fueron tratados simultáneamente con ECMO y TDEC. No hemos encontrado ningún estudio previo que haya analizado la nutrición en pacientes críticos tratados simultáneamente con ambas técnicas. En estos niños la incidencia de complicaciones digestivas fue ligeramente superior a la de los tratados solamente con TDEC, pero las diferencias no fueron estadísticamente significativas. Nuestros resultados muestran que la nutrición enteral es segura en los niños tratados con ECMO y TDEC y debe ser considerada como la vía inicial de elección en estos pacientes, una vez asegurada la estabilidad hemodinámica y respiratoria.
Por otra parte, no hay estudios previos que hayan analizado la relación del estado nutricional, el tipo de nutrición, el aporte calórico y proteico y el pronóstico en los niños con DRA tratados con TDEC. En nuestro estudio no existió relación entre el tipo de nutrición (enteral o parenteral) y la mortalidad. Los pacientes que fallecieron no presentaron una incidencia mayor de complicaciones digestivas que los supervivientes. Solo un paciente falleció debido a una complicación digestiva (isquemia intestinal) y esta no fue secundaria a la nutrición. Estos datos apoyan la administración de nutrición enteral como vía inicial de nutrición en estos pacientes.
Nuestro estudio tiene varias limitaciones. Se trata de un estudio retrospectivo con un número de pacientes relativamente pequeño y limitado a una única UCIP, por lo que se necesitan estudios multicéntricos que confirmen nuestros resultados. Además, no se han medido las necesidades calóricas por calorimetría y no se ha realizado balance nitrogenado. Por ello, no se sabe si el aporte calórico y proteico ha sido adecuado en cada paciente. La comparación del aporte calórico y proteico entre la nutrición enteral y parenteral solo se realizó el primer día, al no registrarse el máximo aporte de nutrición parenteral. Por otra parte, no se ha valorado la influencia de otros factores, como el estado de gravedad clínico, el diagnóstico y otros fármacos sobre la tolerancia de la nutrición y la aparición de complicaciones digestivas.
Concluimos que los niños en estado crítico con insuficiencia renal aguda que precisan tratamiento con TDEC presentan una elevada incidencia de malnutrición, pero el estado nutricional no se asocia con una mayor mortalidad. La mayor parte de los niños tratados con TDEC toleran la nutrición enteral, y aunque presentan una levada incidencia de complicaciones digestivas, en pocos casos es necesario suspender la nutrición. Los niños tratados simultáneamente con TDEC y ECMO no presentan un mayor número de complicaciones digestivas que los tratados solo con TDEC.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.