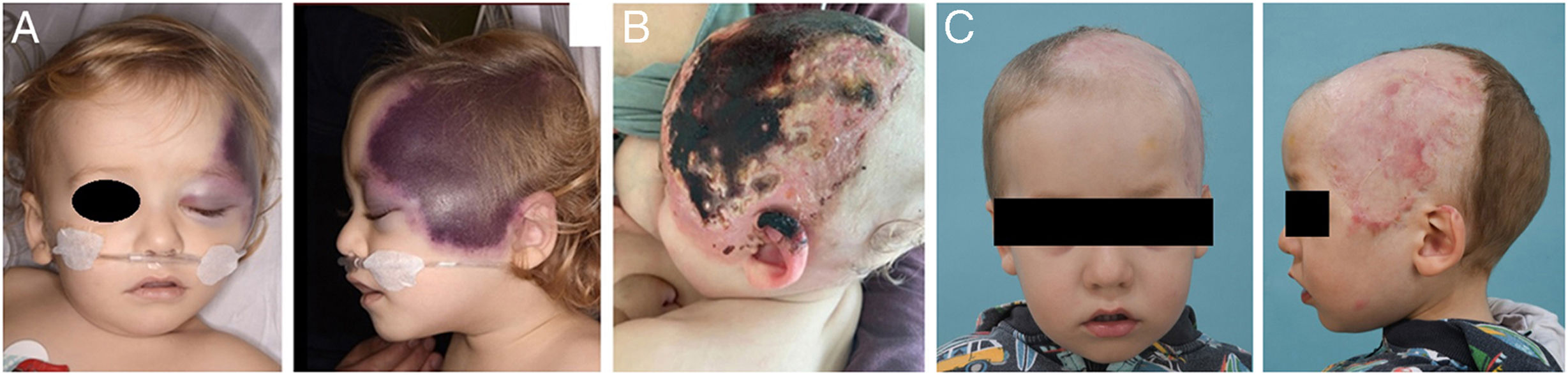
Presentamos el caso de un niño de 16 meses que consulta por aparición hace 8 horas de placa purpuroequimótica parietooccipital izquierda que se extiende hasta párpado y pabellón auricular (fig. 1 A.). Niegan traumatismo. Refieren infección de vías respiratorias altas. Afebril, buen estado general, sin hematomas, petequias ni equimosis en otras localizaciones. En la analítica destaca trombocitopenia (49.000/μl) y coagulopatía grave con ausencia de coagulación, indetectable y dímero D de 976mg/l. No signos de malignidad o hemólisis. Leucocitosis con neutrofilia con mínima elevación de reactantes de fase aguda. Radiografía de tórax con infiltrado perihiliar bilateral inespecífico. Ecografía doppler de la lesión y tomografía computarizada (TC) craneal que confirman cefalohematoma extraaxial sin hemorragia intracraneal ni trombosis asociadas.
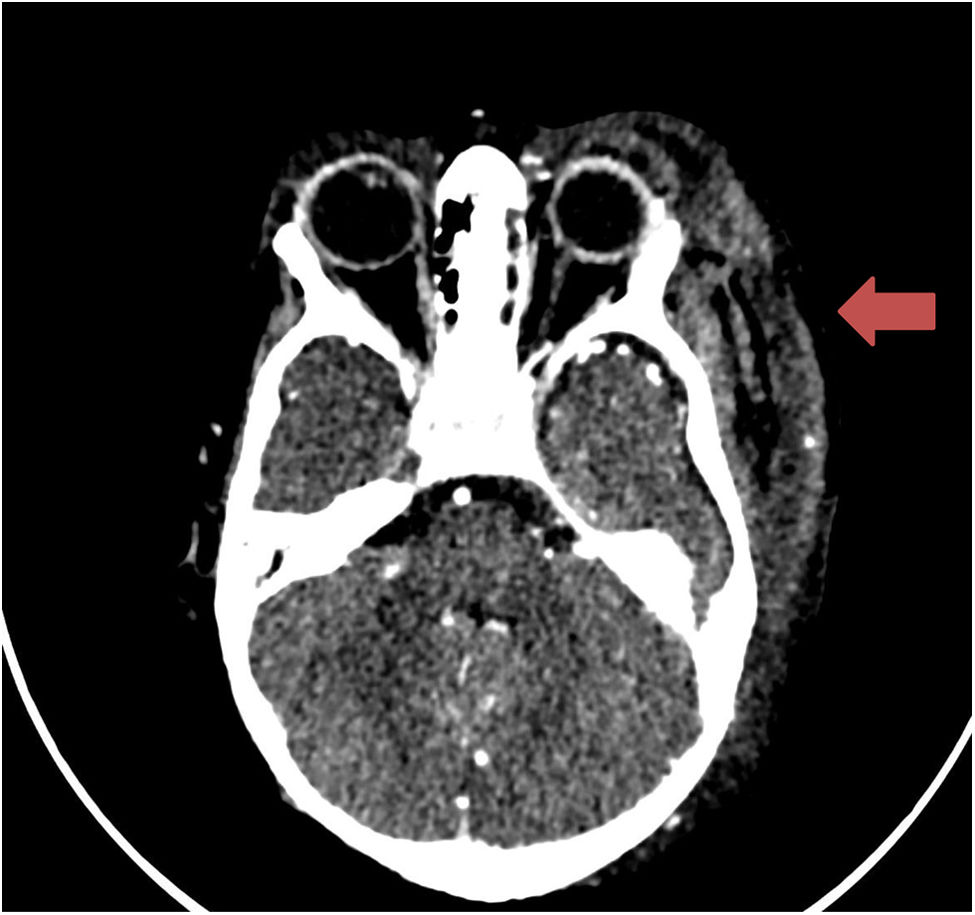
Ante dichos hallazgos, se administran vitamina K, fibrinógeno, plasma fresco congelado (PFC) y transfusión de plaquetas con posterior normalización de la coagulación, asociando tratamiento antibiótico con cefotaxima y azitromicina. Estudios etiológicos infecciosos negativos, excepto PCR positiva de rinovirus en aspirado nasofaríngeo. A las 24 h se realizan angio-TC de control (fig. 2) y angiorresonancia magnética cerebral con estabilidad de la lesión. Se amplía estudio etiológico con factores de coagulación normales, test de Coombs directo C3 positivo débil, antitrombina III y ADAMTS-13 normales. Destaca disminución de la proteína C (PC) del 28% y disminución de la proteína S (PS) del 6,5%. Orientándose como púrpura fulminante asociada a deficiencia de PS, se inicia tratamiento con inmunoglobulinas, corticoides y PFC. A las 48 h presenta trombosis parcial de la vena braquial derecha secundaria a catéter central de inserción periférica recibiendo tratamiento con heparina. Aumento progresivo de los niveles de PS hasta su normalización a las 48 h. Estudio familiar con PS normal. Confirmación de diagnóstico ante la positividad de anticuerpos anti-PS. Se encontró en madre y paciente mutación heterogénea del factor V de Leiden. Debido a evolución a placa necrótica, requirió desbridamiento quirúrgico a las 3 semanas (fig. 1 B) y oxigenoterapia hiperbárica los meses posteriores para mejorar la cicatrización (fig. 1 C).
La PFI es un tipo de púrpura fulminante causada por anticuerpos contra la PS1. Las PS y PC son proteínas de síntesis hepática y endotelial vitamina K dependientes, que actúan como factores antitrombóticos. La PC inhibe la formación del coágulo, uniéndose a la trombina y trombomodulina a través del receptor de PC endotelial inactivándolas. La PS actúa como cofactor de la PC inhibiendo la capacidad coagulante a nivel de los factores Va y VIIIa2.
La aparición de PFI se describe después de 7-10 días de una infección en la que se produce una reactividad cruzada contra el agente infeccioso y el mimetismo molecular de PS, generando anticuerpos anti-PS1,3. Se ha descrito relación con infecciones por varicela, estreptococo o herpes simple tipo 61,3,4. En nuestro caso únicamente se encontró PCR positiva para rinovirus en aspirado nasofaríngeo.
Inicialmente aparecen maculas violáceas que progresan rápidamente desarrollando áreas necróticas que pueden generar infartos hemorrágicos y formar ampollas dolorosas e induradas5. A diferencia de los casos asociados a sepsis meningocócica, con afectación distal de las extremidades, la localización de la PFI ocurre generalmente en muslos respetando parte distal de extremidades, glúteos y en varones, escroto y pene. Es inusual la afectación en parte superior del cuerpo o brazos y extremadamente raro en cabeza y cuello1,3. En nuestro caso solo afectó a cara y pabellón auricular.
Los pacientes presentan buen estado general, sin signos de sepsis, pero con parámetros analíticos de CID2. En la PFI destaca una deficiencia aislada de PS y PC con factores de coagulación normales. La positividad de anticuerpos anti-PS IgG confirma el diagnóstico1. Se ha descrito asociación con trombofilias de base como mutación de factor V Leiden (como el caso descrito), mutación de la protrombina o presencia de anticuerpos anticardiolipina4. El tratamiento debe iniciarse ante la sospecha clínica sin esperar el diagnóstico de confirmación. El tratamiento se basa, por un lado, en corregir el déficit y, por otro, frenar la inmunidad. Se debe administrar PFC de forma seriada hasta corregir la coagulopatía y en casos refractarios, complejo protrombínico. Si aparecen complicaciones trombóticas, se debe asociar heparina1,2. En cuanto al tratamiento inmunomodulador, se debe administrar gammaglobulinas, y si este no funciona, sesiones de plasmaféresis1. La cirugía desempeña un papel importante en el tratamiento de las complicaciones con procedimientos como desbridamiento de las áreas necróticas o realización de fasciotomías precoces para evitar la realización de amputaciones6. No hay descritas recidivas en la literatura. En el caso que se describe, al ser un territorio no descrito antes y donde las posibles complicaciones podrían ser fatales, se asociaron corticoides al tratamiento con gammaglobulinas y no requirió sesiones de plasmaféresis. Se realizó desbridamiento quirúrgico y requirió tratamiento con oxigenoterapia hiperbárica.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.