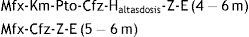La tuberculosis (TB) es la enfermedad infecciosa más importante del mundo, asociando enorme morbimortalidad. La TB pediátrica ha sido una epidemia oculta por su escasa capacidad infectiva y menor incidencia comparada con adultos. El informe-OMS 2015 estimó un millón de niños enfermos de TB en el mundo y 169.000 fallecidos. En Europa, el problema acuciante es la tuberculosis multirresistente, con tasas del 16% en nuevos diagnósticos, especialmente en países del este. En 2014, 219.000 niños se infectaron por cepas-MDR en Europa, 2.120 desarrollaron enfermedad. España es el país de Europa con mayor número de casos pediátricos, con una incidencia en 2014: 4,3/100.000 habitantes. La mortalidad por TB pediátrica en nuestro país es excepcional, pero las formas extrapulmonares ocasionan importantes complicaciones. La TB resistente en niños en España presenta una prevalencia > 4%, superando incluso la notificada en adultos. Estos datos reflejan que la TB en niños en nuestro medio continúa siendo un problema de salud pública prioritario.
Las dificultades diagnósticas del niño y la falta de formulaciones pediátricas óptimas son el mayor desafío para control de TB infantil. El Grupo de expertos de TB pediátrica realiza un análisis de las nuevas tendencias internacionales y guías terapéuticas de tuberculosis en niños, según nuevas evidencias disponibles; y considera una prioridad actualizar las guías pediátricas nacionales de exposición a TB, infección tuberculosa latente y enfermedad, y particularmente los casos de resistencia a fármacos. Este documento, por tanto, sustituye a todos los previos en cuanto a las pautas terapéuticas, aunque siguen estando vigentes las indicaciones diagnósticas.
Tuberculosis (TB) is the most important infectious disease all over the world, with a high morbidity and mortality. Pediatric tuberculosis has been a neglected epidemic, due to the difficulties in assessing its global impact, reduced incidence and lower infectivity compared to adults. In 2015, the WHO reported 1 million cases of paediatric TB and 169,000 deaths. In Europe, the emergence of MDR TB is a major concern, representing 16% of the new diagnosis in Eastern Europe. In 2014, it was estimated that about 219,000 children were infected by MDR-TB-strains in Europe, and 2,120 developed the disease. Spain is the Western European country with more paediatric cases, with an incidence 4.3/100,000 inhabitants in 2014. Paediatric tuberculosis mortality in Spain is rare, but extra-pulmonary disease is associated with significant complications. The prevalence of paediatric drug resistant TB in Spain is over 4%, higher than the estimated incidence in adult population, representing mayor difficulties for therapeutic intervention. These data reveal that paediatric TB is still a Public Health priority in our country.
The difficulties in diagnosis and the lack of optimal paediatric drug formulations are the major challenges for controlling the childhood's tuberculosis epidemic. A group of national paeditric TB experts has reviewed the international guidelines and the most recent evidences, and has established new recommendations for the management of paediatric TB contacts, latent infection and active TB disease, especially focused in drug resistant cases. This document replaces the former national guidelines from the Spanish Society for Pediatric Infectios Diseases, although the prior recommendations on the diagnosis remain valid.
La tuberculosis (TB) es la enfermedad infecciosa más importante del mundo y una de las 10 primeras causas de muerte, aunque su incidencia y mortalidad están en franco retroceso. En 2015, hubo 104 millones de casos nuevos, 480.000 casos de TB-multirresistente (TB-MDR) y 1,4 millones de muertes por esta enfermedad. Mediante la estrategia1End TB, la OMS pretende disminuir un 80% la incidencia y un 90% la mortalidad por TB para 2030.
La TB pediátrica ha sido durante décadas una epidemia global oculta por la dificultad para estimar su verdadero impacto. En países de alta endemicidad, la principal barrera es la pobreza y el escaso acceso al sistema sanitario. Las políticas internacionales han ignorado esta población por su menor incidencia comparada con adultos y su escasa capacidad infectiva. La propia estrategia Stop TB, basada en la cuantificación y el tratamiento de enfermos bacilíferos, excluía a los niños, pues excepcionalmente tienen esputo positivo. Desde 2012, hay mayor sensibilización para incluir a los niños en estos programas2. Los últimos informes1 de la OMS proporcionan datos más precisos sobre el impacto de la TB infantil, con una incidencia real un 25% mayor de lo publicado, estimándose un millón de niños enfermos mundialmente y 169.000 fallecidos por TB en 2015.
En Europa, la prevalencia global de la TB pediátrica disminuye anualmente, pero continúa siendo un problema de salud pública prioritario, con más de 40.000 casos en la última década, una tasa global de TB-MDR del 16% entre los nuevos diagnósticos, y un 48% entre casos previamente tratados. A esto contribuyen mayoritariamente los países de Europa del Este, representando una grave amenaza para el control global de la enfermedad3. En 2014, se estiman 219.000 niños infectados por cepas MDR en Europa, de los cuales 2.120 desarrollaron enfermedad4.
España es el país de Europa occidental con mayor número de casos pediátricos, aunque la incidencia disminuye progresivamente. En 2014, se declararon 303 casos pediátricos, con una incidencia de 4,3/100.000 habitantes3. La epidemiología, marcada por la infección VIH en las últimas 2 décadas del siglo xx, dejó paso a la inmigración5, y a patologías del sistema inmune como principales factores de riesgo6. Las dificultades diagnósticas del niño y la falta de formulaciones pediátricas óptimas representan el mayor desafío en el control de la TB infantil. La mortalidad por TB pediátrica en nuestro país es excepcional, pero las formas extrapulmonares ocasionan importantes complicaciones y secuelas7. Finalmente, no conocemos el impacto de la TB resistente en niños en España. Se estima una prevalencia mayor del 4%, superando incluso la notificada en adultos, incidiendo en las grandes ciudades8.
Exposición a tuberculosisSe considera que existe situación de exposición a TB cuando se cumplen todas las siguientes condiciones9,10:
- a.
Contacto reciente, durante los últimos 3 meses, estrecho (> 4 h diarias en el mismo habitáculo cerrado) con un paciente confirmado/sospechoso de TB bacilífera (pulmonar, laríngea, traqueal o endobronquial).
- b.
Prueba de tuberculina (PT) negativa (< 5mm). Si se realiza test Interferon-Gamma-Release-Assay (IGRA), debe ser negativo.
- c.
Ausencia de síntomas y signos clínicos compatibles con TB.
- d.
En pacientes inmunodeprimidos o niños pequeños, cuando se indique radiografía de tórax (frontal y lateral), debe ser normal.
En esta situación, y debido al riesgo de desarrollar enfermedad TB tras primoinfección no diagnosticada durante el periodo ventana, la Sociedad Española de Infectología Pediátrica (SEIP) recomendaba desde 2006 iniciar profilaxis primaria con isoniazida (H) en todos los menores de 18 años9. En 2010, la American Academy of Pediatrics (AAP) y la American Thoracic Society (ATS) propusieron que solo los < 4 años recibieran profilaxis11. Desde 2014, la OMS recomienda profilaxis en < 5 años12 y la AAP mantiene el límite en los 4 años13. En 2016, la British Thoracic Society (BTS) recorta la edad a < 2 años14. Estas recomendaciones están basadas en estudios que demuestran que no es más ventajoso iniciar profilaxis que mantener vigilancia estrecha a la espera del resultado de la segunda PT/IGRA, salvo en niños pequeños o inmunodeprimidos, con mayor riesgo de infección o enfermedad TB tras la exposición.
Revisada la evidencia, y en línea con estas actualizaciones, la SEIP realiza nuevas recomendaciones sobre la profilaxis postexposición:
- –
Iniciar profilaxis con H (tabla 1):
- ∘
Todos los niños menores de 5 años.
- ∘
Niños de cualquier edad con tratamiento inmunosupresor (uso prolongado de corticoides, anti-TNF-alfa, fármacos inmunosupresores, etc.) o comorbilidades del sistema inmunitario (VIH, insuficiencia renal crónica, tumores sólidos o hematológicos, inmundeficiencias primarias, etc.)12-14.
- ∘
- –
Una vez transcurridas 8-10 semanas13-15, tras el último contacto de riesgo se realizará nueva PT, independientemente de si se inició H o no. Se procederá según resultados:
- ∘
Si la segunda PT es < 5mm (test IGRA negativo, si se hubiese realizado) en ausencia de clínica: retirar profilaxis, si se hubiese iniciado. Excepciones: niños inmunodeprimidos o < 3 meses con contacto de alto riesgo (contacto íntimo no cumplidor, retratamiento, etc.) en los que se recomienda completar tratamiento de infección tuberculosa latente (ITBL) aun en ausencia de conversión del Mantoux.
- ∘
Si la segunda PT es ≥ 5mm (o test IGRA positivo, si se hubiese realizado): actuar según apartado ITBL.
- ∘
Temporalmente, es importante romper el contacto entre niño expuesto y enfermo de TB, recomendando que ocupe una dependencia aislada en el domicilio al menos hasta comprobar que la fuente no es bacilífera13; estimado habitualmente tras al menos 2 semanas de tratamiento adecuado.
En recién nacidos de madres bacilíferas, iniciar profilaxis con H tras descartar infección y enfermedad TB. Cuando la segunda PT sea de 0mm a las 10-12 semanas, ya que el periodo ventana puede ser mayor, si se decide interrumpir la profilaxis, se evaluará la conveniencia de vacuna BCG16. La lactancia materna no está contraindicada, salvo en mastitis tuberculosa16. Se recomienda extraer la leche y administrarla en biberón para evitar contacto con el bebé, en las siguientes situaciones16:
- –
La madre ha recibido < 2 semanas de terapia.
- –
La madre sigue siendo bacilífera, a pesar del tratamiento.
- –
La cepa no es sensible a fármacos de primera línea.
Se consideran en situación de infección tuberculosa latente (ITBL) los niños y adolescentes que se infectan por contacto con enfermo bacilífero sin desarrollar enfermedad activa y evolucionan a un estado de infección latente asintomática.
En la práctica clínica, se considera ITBL a pacientes asintomáticos con radiografía de tórax normal (frontal y lateral) y:
- –
PT positiva.
- –
Contacto con enfermo tuberculoso (fuente) conocido.
- –
En niños sin contacto conocido bacilífero pero que presenten una PT y/o un test IGRA positivos, considerarlos como ITBL, sobre todo si son menores de < 5 años o inmunodeprimidos17.
En ausencia de contacto y sin factores de riesgo, el antecedente de vacunación BCG con PT positiva e IGRA negativo se interpreta como efecto de la BCG. Estos casos no se consideran ITBL.
Pautas de tratamiento de infección tuberculosa latenteTodos los niños y adolescentes diagnosticados de ITBL deben recibir tratamiento en cuanto se diagnostiquen para evitar el desarrollo de la enfermedad, siendo fundamental descartar enfermedad activa antes de iniciarlo. La terminología preferible es «tratamiento de ITBL» evitando términos como profilaxis secundaria o postexposición. Pautas propuestas12,14,18,19 (tabla 1):
- –
H durante 6-9 meses (6H o 9H): si mal cumplimiento, inmunodeprimidos o enfermedades crónicas, valorar prolongar siempre hasta 9 meses.
- –
H y rifampicina (R) durante 3 meses (3HR) o en niños mayores de 12 años, H -rifapentina una dosis semanal durante 12 semanas con admnistración directamente observada: esta pauta es igualmente eficaz que la monoterapia con H, con excelente tolerancia y escasa toxicidad. Especialmente recomendada en adolescentes o en sospecha de mala adherencia. En niños coinfectados con VIH, no se recomienda usar R; es un fármaco fundamental si desarrollara la enfermedad y podría quedar inutilizado. La R interacciona con antirretrovirales, especialmente inhibidores de proteasas, disminuyendo sus niveles y aumentando la toxicidad de R.
- –
R durante 4 meses (4R): indicada en pacientes con toxicidad o contraindicaciones a H, o cepas de Mycobacterium tuberculosis resistentes a H y sensibles a R.
El bajo riesgo de hepatotoxicidad en niños desaconseja realizar un control rutinario de transaminasas durante el tratamiento de ITBL, salvo si aparece clínica de hepatotoxicidad, enfermedad hepática de base o medicación hepatotóxica concomitante. En inmigrantes de países endémicos de hepatitis virales o VIH, deben descartarse antes de iniciar tratamiento.
Tratamiento de la enfermedad tuberculosaTuberculosis pulmonarConsiderando el índice de resistencia a H nuestro medio ≥ 4%, la pauta de elección de inicio sin conocer sensibilidad de cepa, tendrá las siguiente premisas12-14,20 (tabla 1):
- –
Fase de inicio (HRZE 2 meses): el cuarto fármaco más empleado es etambutol (E) por vía oral, vigilando aparición de neuritis óptica (agudeza visual y distinción entre color rojo-verde). Una alternativa, de uso excepcional, son los aminoglucósidos, como amikacina o estreptomicina.
- –
Duración del cuarto fármaco: suspender cuando se conozca la sensibilidad de la cepa (caso fuente). Si no se conoce, mantener 2 meses. Si se emplean aminoglucósidos, valorar retirar tras 4-6 semanas.
- –
Fase de mantenimiento (HR 4 meses): en TB-pulmonar por cepa sensible o desconocida y buena evolución. En los casos de TB extrapulmonar o TB resistente, consultar el apartado específico.
Este tratamiento consigue curación en > 95% casos, con escasos efectos adversos. Los fármacos deberán tomarse juntos y en ayunas. No recomendamos pautas intermitentes, salvo excepciones con terapia directamente observada (TDO). Dosis, preparados y combinaciones dosis/fijas: tablas 1 y 2. Recomendaciones fórmulas magistrales21: tabla 3. Pacientes con comorbilidades o toma concomitante otros fármacos, remitir a unidad especializada14. En riesgo de incumplimiento, inmunodeprimidos o cepas resistentes: tratamiento supervisado o TDO14.
Dosis recomendadas de los fármacos antituberculosos de primera línea más empleados en edad pediátrica12
| Dosis en pautas diarias, mg/kg/d (rango de dosis) | Dosis máxima diaria (mg) | |
|---|---|---|
| Isoniacida | 10 (7-15)a,b | 300 |
| Rifampicina | 15 (10-20)a | 600 |
| Pirazinamida | 35 (30-40) | 2.000 |
| Etambutol | 20 (15-25)c | 2.500 |
| Estreptomicina | 15-20 | 1.000 |
Asociar piridoxina 15-50mg/día (máximo 50mg/día) si lactancia materna exclusiva, vegetarianos, alteraciones nutrición, VIH y adolescentes gestantes.
Se recomienda que durante el periodo de inducción de la enfermedad se utilice etambutol a dosis más bactericidas (20-25mg/kg/día) y durante el periodo de mantenimiento disminuir a 15-20mg/kg/día.
Excepcionalmente pueden considerarse pautas intermitentes de 3 días semanales con incremento de dosis, siempre con tratamiento directamente observado.
Preparados comercializados disponibles de fármacos antituberculosos en España (última actualización: 30 octubre del 2016)
| Primera línea | |
| H | Cemidón B6®: |
| – Comprimidos: 50mg, 150mg, 300mg | |
| – Vial para administración intravenosa: 300mg | |
| R | Rifaldin®: |
| – Cápsulas: 300mg | |
| – Suspensión: 20mg/ml | |
| – Vial para administración intravenosa: 600mg | |
| Rimactan®: | |
| – Comprimidos recubiertos: 300mg | |
| Z | Pirazinamida Prodes®: |
| – Comprimidos: 250mg | |
| E | Myambutol®: |
| – Comprimidos: 400mg | |
| Estreptomicina | Estreptomicina sulfato®: |
| – Vial para administración intramuscular: 1 gramo | |
| Fármacos combinados a dosis fijas (fixed dose combinations [FDC]) | |
| H+R | Rifinah®: |
| – Comprimidos recubiertos: H 150 mg+R 300mg | |
| H+R+Z | Rifater®: |
| – Comprimidos recubiertos: H 50 mg+R 120 mg+Z 300mg | |
| H+R+Z+E | Rimstar®: |
| – Comprimidos recubiertos: H 75 mg+R 150 mg+Z 400 mg+E 275mg | |
E: etambutol; H: isoniacida; R: rifampicina; Z: pirazinamida.
Tomado de Agencia Española del Medicamento y Productos Sanitarios (AEMPS)38.
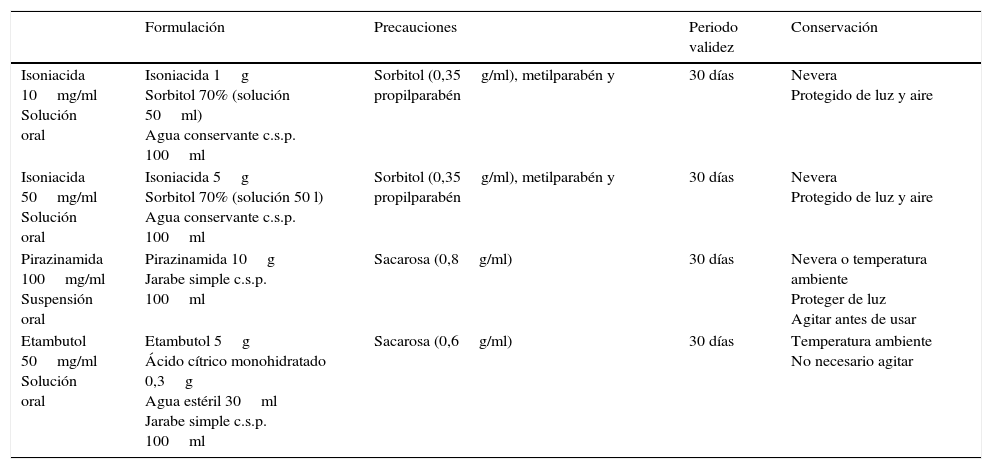
Fórmulas magistrales de fármacos anti tuberculosos. Proyecto Magistral
| Formulación | Precauciones | Periodo validez | Conservación | |
|---|---|---|---|---|
| Isoniacida 10mg/ml Solución oral | Isoniacida 1g Sorbitol 70% (solución 50ml) Agua conservante c.s.p. 100ml | Sorbitol (0,35g/ml), metilparabén y propilparabén | 30 días | Nevera Protegido de luz y aire |
| Isoniacida 50mg/ml Solución oral | Isoniacida 5g Sorbitol 70% (solución 50 l) Agua conservante c.s.p. 100ml | Sorbitol (0,35g/ml), metilparabén y propilparabén | 30 días | Nevera Protegido de luz y aire |
| Pirazinamida 100mg/ml Suspensión oral | Pirazinamida 10g Jarabe simple c.s.p. 100ml | Sacarosa (0,8g/ml) | 30 días | Nevera o temperatura ambiente Proteger de luz Agitar antes de usar |
| Etambutol 50mg/ml Solución oral | Etambutol 5g Ácido cítrico monohidratado 0,3g Agua estéril 30ml Jarabe simple c.s.p. 100ml | Sacarosa (0,6g/ml) | 30 días | Temperatura ambiente No necesario agitar |
Tomado de Piñeiro Pérez et al.21.
Analítica basal con transaminasas pretratamiento y posteriormente, valorar a las 2-3 semanas o antes si clínica (tabla 4).
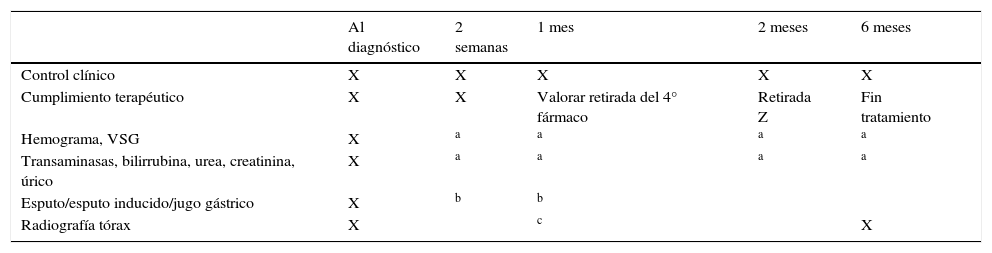
Seguimiento del niño con TB pulmonar en tratamiento
| Al diagnóstico | 2 semanas | 1 mes | 2 meses | 6 meses | |
|---|---|---|---|---|---|
| Control clínico | X | X | X | X | X |
| Cumplimiento terapéutico | X | X | Valorar retirada del 4° fármaco | Retirada Z | Fin tratamiento |
| Hemograma, VSG | X | a | a | a | a |
| Transaminasas, bilirrubina, urea, creatinina, úrico | X | a | a | a | a |
| Esputo/esputo inducido/jugo gástrico | X | b | b | ||
| Radiografía tórax | X | c | X |
Se realizarán las pruebas complementarias y la visitas adicionales que sean necesarias según clínica y características del paciente.
Casos con buena evolución sin enfermedad pulmonar extensa: control radiológico al final de la fase de inicio y al terminar el tratamiento. Casos con hipoventilación, sibilancias focales, enfermedad extensa, cavitación, derrame, incumplimiento o resistencia farmacológica: estudio de imagen o fibrobroncoscopia cuando sea preciso. En los primeros 2 meses de tratamiento, puede aparecer reacción paradójica en un 5-10% de los casos, caracterizada por un empeoramiento clínico-radiológico22; en estos casos se asociarán corticoides orales 2mg/kg/día de prednisona o equivalente, durante 3-4 semanas, con descenso progresivo en 2 semanas20,22.
Tras alta domiciliaria y asegurado cumplimiento, esperar unos días de convalecencia para incorporarse a actividad normal. Adolescentes bacilíferos: esperar resultado de esputo en 2 semanas.
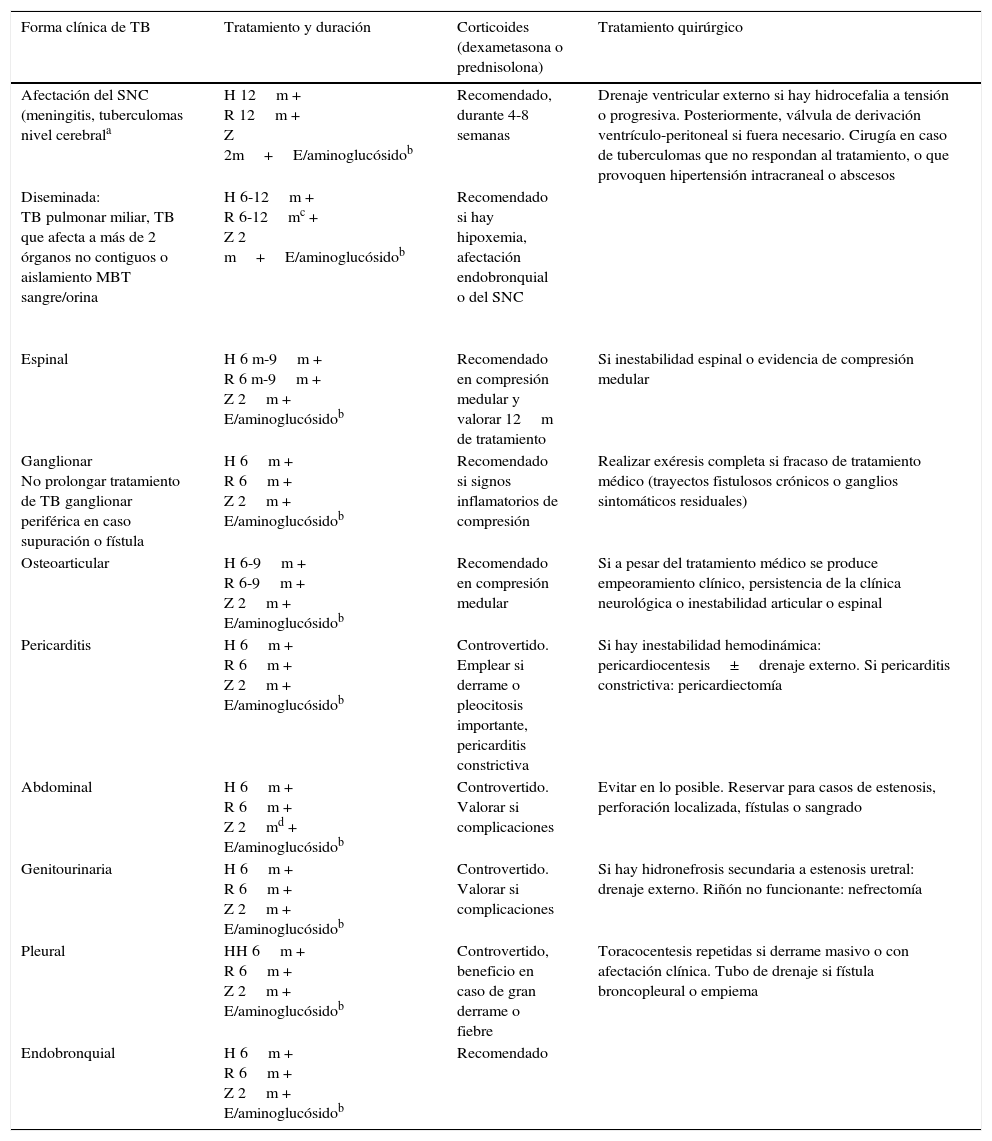
Tuberculosis extrapulmonarRecomendaciones SEIP de tratamiento de formas de TB-extrapulmonar y dosis de fármacos20: tablas 5 y 6. No recomendamos pautas 3por semana, por escasa evidencia20. En adultos, prefieren como cuarto fármaco E, incluso en afectación del SNC20.
Recomendaciones sobre el tratamiento de las principales formas de TB extrapulmonar
| Forma clínica de TB | Tratamiento y duración | Corticoides (dexametasona o prednisolona) | Tratamiento quirúrgico |
|---|---|---|---|
| Afectación del SNC (meningitis, tuberculomas nivel cerebrala | H 12m + R 12m + Z 2m+E/aminoglucósidob | Recomendado, durante 4-8 semanas | Drenaje ventricular externo si hay hidrocefalia a tensión o progresiva. Posteriormente, válvula de derivación ventrículo-peritoneal si fuera necesario. Cirugía en caso de tuberculomas que no respondan al tratamiento, o que provoquen hipertensión intracraneal o abscesos |
| Diseminada: TB pulmonar miliar, TB que afecta a más de 2 órganos no contiguos o aislamiento MBT sangre/orina | H 6-12m + R 6-12mc + Z 2 m+E/aminoglucósidob | Recomendado si hay hipoxemia, afectación endobronquial o del SNC | |
| Espinal | H 6 m-9m + R 6 m-9m + Z 2m + E/aminoglucósidob | Recomendado en compresión medular y valorar 12m de tratamiento | Si inestabilidad espinal o evidencia de compresión medular |
| Ganglionar No prolongar tratamiento de TB ganglionar periférica en caso supuración o fístula | H 6m + R 6m + Z 2m + E/aminoglucósidob | Recomendado si signos inflamatorios de compresión | Realizar exéresis completa si fracaso de tratamiento médico (trayectos fistulosos crónicos o ganglios sintomáticos residuales) |
| Osteoarticular | H 6-9m + R 6-9m + Z 2m + E/aminoglucósidob | Recomendado en compresión medular | Si a pesar del tratamiento médico se produce empeoramiento clínico, persistencia de la clínica neurológica o inestabilidad articular o espinal |
| Pericarditis | H 6m + R 6m + Z 2m + E/aminoglucósidob | Controvertido. Emplear si derrame o pleocitosis importante, pericarditis constrictiva | Si hay inestabilidad hemodinámica: pericardiocentesis±drenaje externo. Si pericarditis constrictiva: pericardiectomía |
| Abdominal | H 6m + R 6m + Z 2md + E/aminoglucósidob | Controvertido. Valorar si complicaciones | Evitar en lo posible. Reservar para casos de estenosis, perforación localizada, fístulas o sangrado |
| Genitourinaria | H 6m + R 6m + Z 2m + E/aminoglucósidob | Controvertido. Valorar si complicaciones | Si hay hidronefrosis secundaria a estenosis uretral: drenaje externo. Riñón no funcionante: nefrectomía |
| Pleural | HH 6m + R 6m + Z 2m + E/aminoglucósidob | Controvertido, beneficio en caso de gran derrame o fiebre | Toracocentesis repetidas si derrame masivo o con afectación clínica. Tubo de drenaje si fístula broncopleural o empiema |
| Endobronquial | H 6m + R 6m + Z 2m + E/aminoglucósidob | Recomendado |
E: etambutol; H: isoniacida; R: rifampicina; SNC: sistema nervioso central; TB: tuberculosis; Z: pirazinamida.
Están contempladas pautas más cortas que utilizan con muy buenos resultados en Sudáfrica39. Además, etionamida/protionamida tienen mejor penetración en SNC, y se consideran fármacos alternativos. Las dosis en TB del SNC deben ser las de mayor rango indicadas.
Como cuarto fármaco hasta llegada de antibiograma. Valorar mantener 2 meses (etambutol) o 4-6 semanas (aminoglucósido) si no se aísla cepa.
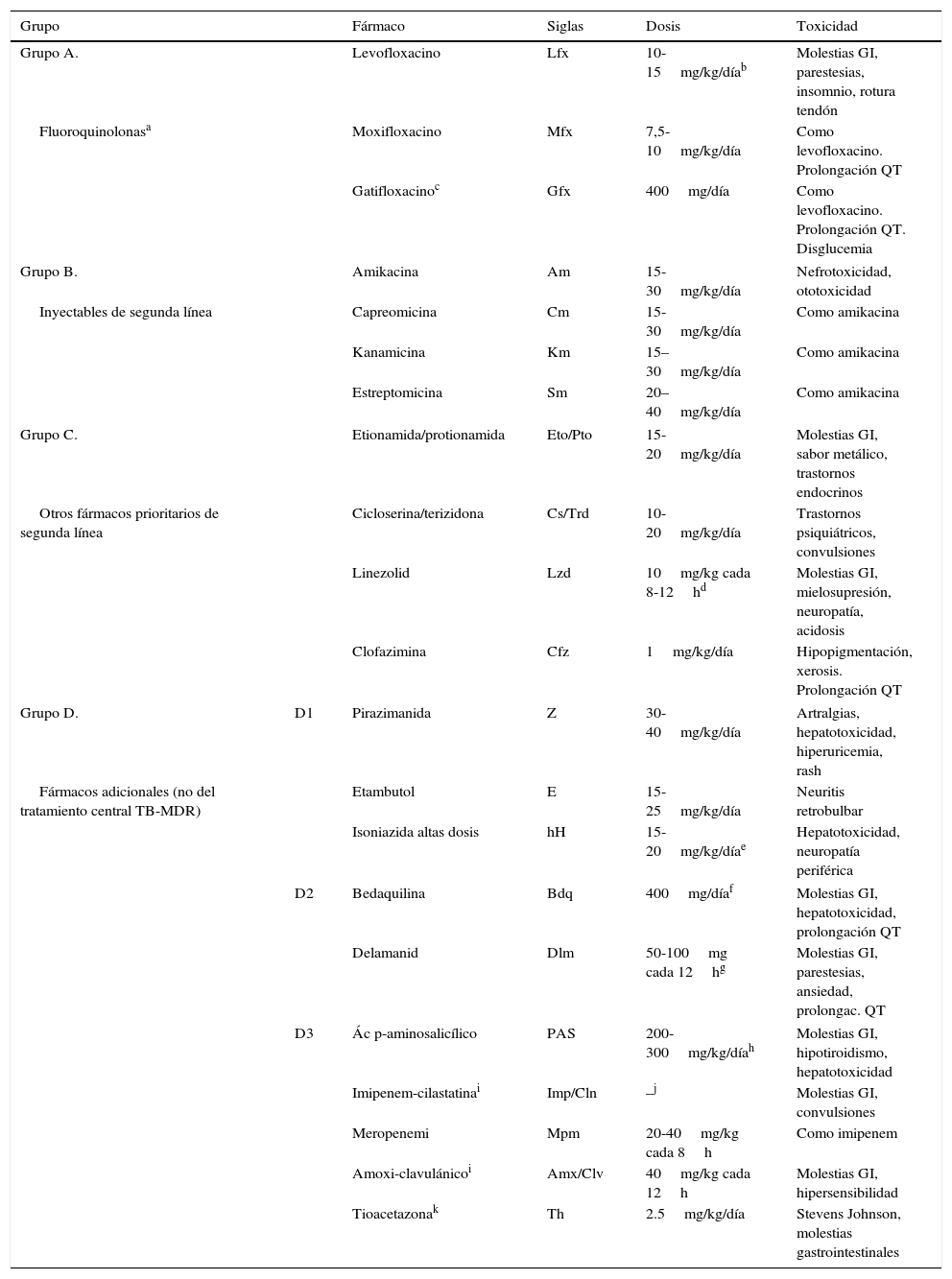
Distribución de fármacos por grupos de prioridad de la OMS y dosis, recomendados en el tratamiento de la TB-RR y TB-MDR
| Grupo | Fármaco | Siglas | Dosis | Toxicidad | |
|---|---|---|---|---|---|
| Grupo A. | Levofloxacino | Lfx | 10-15mg/kg/díab | Molestias GI, parestesias, insomnio, rotura tendón | |
| Fluoroquinolonasa | Moxifloxacino | Mfx | 7,5-10mg/kg/día | Como levofloxacino. Prolongación QT | |
| Gatifloxacinoc | Gfx | 400mg/día | Como levofloxacino. Prolongación QT. Disglucemia | ||
| Grupo B. | Amikacina | Am | 15-30mg/kg/día | Nefrotoxicidad, ototoxicidad | |
| Inyectables de segunda línea | Capreomicina | Cm | 15-30mg/kg/día | Como amikacina | |
| Kanamicina | Km | 15–30mg/kg/día | Como amikacina | ||
| Estreptomicina | Sm | 20–40mg/kg/día | Como amikacina | ||
| Grupo C. | Etionamida/protionamida | Eto/Pto | 15-20mg/kg/día | Molestias GI, sabor metálico, trastornos endocrinos | |
| Otros fármacos prioritarios de segunda línea | Cicloserina/terizidona | Cs/Trd | 10-20mg/kg/día | Trastornos psiquiátricos, convulsiones | |
| Linezolid | Lzd | 10mg/kg cada 8-12hd | Molestias GI, mielosupresión, neuropatía, acidosis | ||
| Clofazimina | Cfz | 1mg/kg/día | Hipopigmentación, xerosis. Prolongación QT | ||
| Grupo D. | D1 | Pirazimanida | Z | 30-40mg/kg/día | Artralgias, hepatotoxicidad, hiperuricemia, rash |
| Fármacos adicionales (no del tratamiento central TB-MDR) | Etambutol | E | 15-25mg/kg/día | Neuritis retrobulbar | |
| Isoniazida altas dosis | hH | 15-20mg/kg/díae | Hepatotoxicidad, neuropatía periférica | ||
| D2 | Bedaquilina | Bdq | 400mg/díaf | Molestias GI, hepatotoxicidad, prolongación QT | |
| Delamanid | Dlm | 50-100mg cada 12hg | Molestias GI, parestesias, ansiedad, prolongac. QT | ||
| D3 | Ác p-aminosalicílico | PAS | 200-300mg/kg/díah | Molestias GI, hipotiroidismo, hepatotoxicidad | |
| Imipenem-cilastatinai | Imp/Cln | –j | Molestias GI, convulsiones | ||
| Meropenemi | Mpm | 20-40mg/kg cada 8h | Como imipenem | ||
| Amoxi-clavulánicoi | Amx/Clv | 40mg/kg cada 12h | Molestias GI, hipersensibilidad | ||
| Tioacetazonak | Th | 2.5mg/kg/día | Stevens Johnson, molestias gastrointestinales | ||
GI, gastrointestinales.
Actualmente, se ha consensuado una terminología más rigurosa acerca de la TB resistente (TB-R) en niños23.
- –
TB monorresistente: TB por cepa resistente a un solo fármaco 1.ª línea.
- –
TB polirresistente: TB por cepa resistente a más de un fármaco diferente a la asociación de H y R.
- –
TB-MDR: TB por cepa resistente, al menos, a H y R.
- –
TB-pre-XDR: TB-MDR con resistencia adicional a fluoroquinolonas (FQ) o fármacos inyectables de 2.ª línea, no a ambos.
- –
TB extremadamente resistente (TB-XDR): TB-MDR resistente además a FQ y fármacos inyectables de 2.ª línea.
- –
TB-R a R (TB-RR): cepa con cualquier tipo de resistencia a R, incluyendo monorresistencia, polirresistencia, TB-MDR y TB-XDR.
Cambios nuevas guías OMS en el tratamiento de la TB Resistente24:
- –
TB-RR: tratar igual que TB-MDR; la resistencia R es un marcador de MDR con sensibilidad > 95%. Recomendado de rutina LPA-assay25. Si posteriormente fuese sensible a H, incluirla en el régimen y prolongar la terapia 9-12 meses.
- –
Reagrupación de fármacos (tabla 6):
- ∘
Grupo A: FQ.
- ∘
Grupos B y C: fármacos prioritarios, que, junto a las FQ, forman el «core» de 2.ª línea.
- ∘
Grupo D: fármacos adicionales.
- •
Grupo D1 add-on agents: fármacos 1.ª línea pirazinamida (Z), H y E, a priori siempre incluidos a no ser resistencia completa confirmada. Escasa correlación in vivo con resistencias in vitro a Z y E.
- •
Nuevo grupo D2: bedaquilina y delamanid.
- •
Grupo D3: alternativos: PAS.
- •
Excluidos definitivamente: macrólidos.
- •
- ∘
- –
Régimen corto de tratamiento TB-MDR: 9-12 meses (actualmente aún no indicado en niños, solo casos muy seleccionados).
- –
Recomendaciones de cirugía, casos seleccionados.
Igual que en TB sensible, se instaurará profilaxis en < 5 años y en inmunodeprimidos. En expuestos a cepas H-resistentes y sensibles a R, se administrará R, y en expuestos a TB-RR, administrar H.
Tratamiento de infección tuberculosa latenteLa ITBL por cepa H-resistente deberá recibir 4 meses de R. Pacientes con ITBL por cepa sensible a H y resistente a otros fármacos, recibirán pauta habitual de H 6-9 meses.
Tratamiento de enfermedad resistente a isoniacidaSe administrará RZE o RZE+FQ durante 6-9 meses o RZ+FQ durante 9-12 meses, manteniendo los mismos fármacos en fase de inducción y mantenimiento o 2RZE+7-10RE.
Tratamiento de enfermedad resistente a rifampicinaRecibirán el mismo tratamiento de TB-MDR, independientemente de resistencia a H, hasta que esta pueda confirmarse; si no es posible, considerarla MDR. Emplear aminoglucósidos, como se detalla a continuación24.
Actuaciones en tuberculosis multirresistenteProfilaxis postexposición a tuberculosis multirresistenteDos alternativas válidas con escasa evidencia, basadas en opiniones de expertos:
- –
Observación clínica sin iniciar profilaxis14,24,25 (guías británicas y OMS).
- –
Administrar uno o 2 fármacos con sensibilidad conocida26,27 (AAP y Consenso de Dubai).
- –
Otras guías europeas: válidas ambas opciones; individualizar según: a) riesgo de progresión, b) perfil de resistencias, y c) riesgo de reacciones adversas. Recomiendan tratar siempre en < 5 años e inmunodeprimidos28.
Regímenes recomendados en niños: FQ (levofloxacino o moxifloxacino); hay evidencia sobre perfil bactericida y seguridad29.
Niños expuestos a TB-MDR con estudio inicial negativo (PT y/o IGRA): puede optarse por profilaxis postexposición combinando FQ y E o Eto, para evitar monoterapia con FQ que podría crear resistencias si luego fuese necesario tratamiento; incluso algunos autores recomiendan añadir H a altas dosis, hasta confirmar la negatividad del segundo PT y/o IGRA a las 10-12 semanas30. Es una opción igualmente válida, especialmente en niños sin factores de riesgo y > 5 años, mantener observación sin profilaxis.
Niños expuestos a TB-XDR o TB-pre-XDR resistente a FQ: se recomienda observación estrecha sin tratamiento; no existe ninguna opción terapéutica adecuada.
El seguimiento debe prolongarse al menos 2 años, inicialmente cada 2-3 meses, y posteriormente cada 6 meses.
Tratamiento de infección tuberculosa latente multirresistenteEl régimen más aceptado es FQ 6-9 meses (moxifloxacino solo en > 12 años), en combinación con otro fármaco (E o Eto), valorando asociar H a altas dosis.
En ITBL por cepa XDR o pre-XDR resistente a FQ, no existe opción terapéutica adecuada; se recomienda observación estrecha sin tratamiento. En < 5 años o inmunodeprimidos, pueden plantearse 2 fármacos de sensibilidad conocida durante 9-12 meses.
Tratamiento de la enfermedad tuberculosa multirresistenteEl tratamiento convencional de TB-MDR debe ser dirigido por un especialista en infectología pediátrica. Su duración será 18-24 meses. Fase inicial de 6-8 meses, puede valorarse acortar a 4-6 meses en adenopatías mediastínicas exclusivamente, incluyendo al menos 5 fármacos con sensibilidad conocida. Fase de mantenimiento: administrar al menos 3 fármacos útiles.
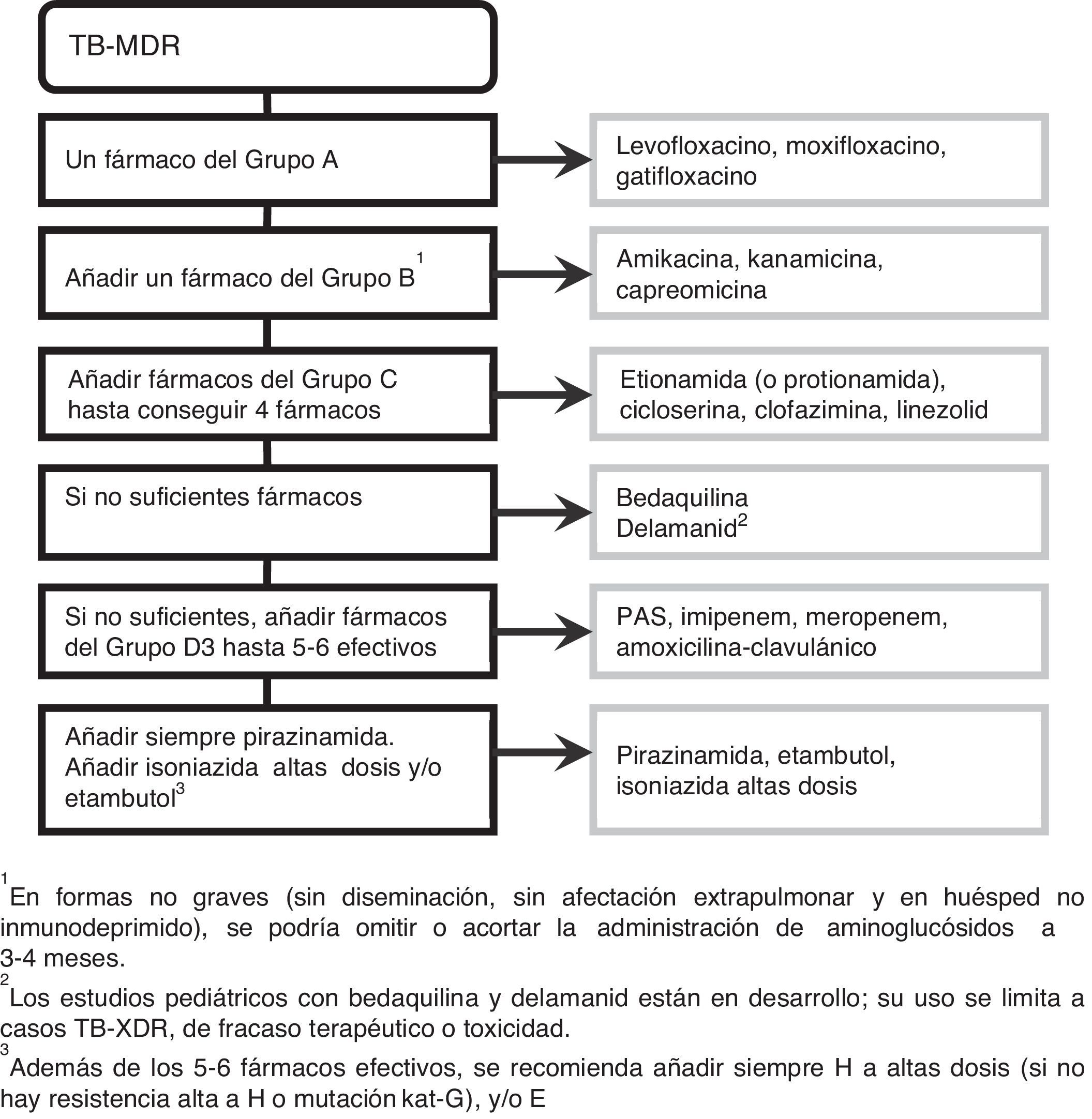
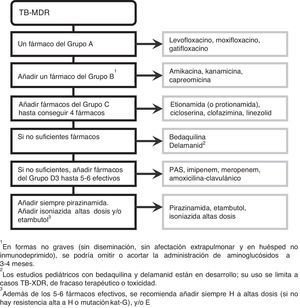
El diseño del régimen se realiza con el siguiente orden (fig. 1): incluir todos los fármacos posibles de 1ª línea del grupo add-on agents D1 (Z+H-alta dosis+E) y:
- –
Un fármaco del grupo A (FQ).
- –
Un fármaco del grupo B (aminoglucósido inyectable de 2.ª línea).
- –
Al menos 2 fármacos del grupo C.
- –
Z: poca concordancia test in vitro y comportamiento in vivo. Añadir de rutina.
Recomendaciones41 para el diseño del régimen de tratamiento de la TB-MDR y TB-XDR.
Si esta combinación no consigue reunir 5 fármacos, añadir un fármaco del grupo D2, y los necesarios del grupo D3. El empleo pediátrico de bedaquilina y delamanaid (D2) está en desarrollo y se limita a cepas confirmadas de TB-XDR, fracaso terapéutico o toxicidad31. Además de los 5 fármacos efectivos, se recomienda añadir siempre H-altas dosis (siempre que no asocie alta resistencia a H, es decir, mutación kat-G) y/o E.
Formas no graves de TB (no diseminadas, sin afectación extrapulmonar, huésped no inmunodeprimido): puede omitirse o acortar aminoglucósidos a 3-4 meses, por riesgo de ototoxicidad y dificultad de administración parenteral. Estudios observacionales demuestran buena evolución clínica en estos pacientes.
Pacientes con TB pulmonar primaria (identificados en estudios de contactos de TB-MDR), asintomáticos y presumible baja carga bacilar, es posible omitir aminoglucósidos inyectables si disponemos de 2 fármacos bactericidas eficaces (FQ+Lnz) y 2 fármacos más útiles asociados (Cs, Eto/Pto, Cfz), añadiendo además Z+H-altas dosis+E). Este perfil de enfermo es común en pediatría, siendo importante retirar pronto o incluso evitar inyectables.
La OMS establece un nuevo régimen corto, incluyendo a los niños, de 9-12 meses de duración, en las siguientes circunstancias:
- –
No haber recibido fármacos de 2.ª línea incluidos en el régimen>1 mes.
- –
Sin resistencia a los fármacos incluidos en este régimen.
- –
No embarazo.
- –
No TB extrapulmonar.
El régimen consta de fase intensiva con 7 fármacos durante 4 meses, que se prolongará hasta 6 meses si continúa siendo bacilífero o mala evolución, y fase de continuación de 5-6 meses; con el siguiente esquema:
Este régimen está basado en el ensayo32 STREAM, que concluirá en 2018. Estudios observacionales muestran mayor eficacia y seguridad de esta pauta comparada con pautas largas32-35; la OMS lo recomienda en adultos y niños. Existen dudas sobre su aplicabilidad en Europa, con países con alta proporción de TB-pre-XDR y TB-XDR36,37. A la espera de más datos pediátricos, es posible utilizar ambas pautas en nuestro medio siempre dirigidas por un experto.
Cuidados y seguimiento del niño con TB-MDREl tratamiento de niños con TB-MDR se realizará en unidades adecuadas, con experiencia en esta patología. El niño, a pesar de no ser bacilífero, permanecerá ingresado en una habitación con presión negativa hasta obtener 3 muestras BK negativas, separadas una semana. Los acompañantes y el personal sanitario llevarán mascarilla con filtro FFP3 hasta asegurar la no contagiosidad. Se procurará disminuir el impacto psicosocial derivado del ingreso prolongado, ofreciendo apoyo social y psicológico.
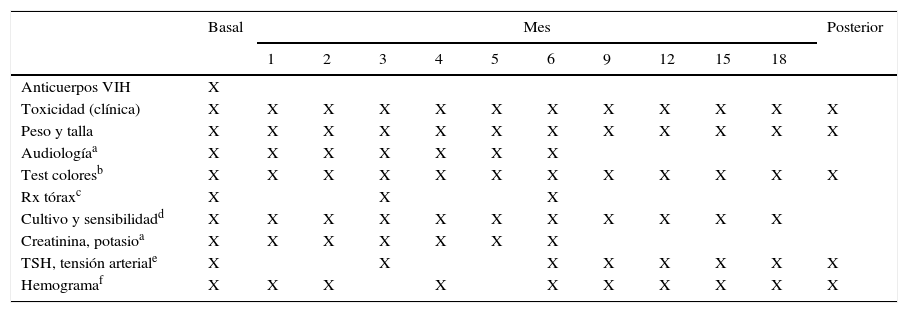
En la tabla 7 se detalla el calendario de seguimiento, monitorización y detección precoz de efectos adversos en estos casos.
Calendario de visitas y monitorización de efectos adversos de TBMDR
| Basal | Mes | Posterior | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 9 | 12 | 15 | 18 | |||
| Anticuerpos VIH | X | |||||||||||
| Toxicidad (clínica) | X | X | X | X | X | X | X | X | X | X | X | X |
| Peso y talla | X | X | X | X | X | X | X | X | X | X | X | X |
| Audiologíaa | X | X | X | X | X | X | X | |||||
| Test coloresb | X | X | X | X | X | X | X | X | X | X | X | X |
| Rx tóraxc | X | X | X | |||||||||
| Cultivo y sensibilidadd | X | X | X | X | X | X | X | X | X | X | X | |
| Creatinina, potasioa | X | X | X | X | X | X | X | |||||
| TSH, tensión arteriale | X | X | X | X | X | X | X | X | ||||
| Hemogramaf | X | X | X | X | X | X | X | X | X | X | ||
Los autores declaran no tener ningún conflicto de intereses.
Coordinadora:
- –
María José Mellado Peña (Hospital Universitario Infantil La Paz, Madrid)
Integrantes:
- –
Fernando Baquero Artiago (Hospital Universitario La Paz-Carlos III, Madrid).
- –
M. José Cilleruelo Ortega (H. Universitario Puerta de Hierro, Majadahonda, Madrid).
- –
Lola Falcón (Hospital Universitario Virgen del Rocío, Sevilla).
- –
Laura Ferreras Antolín (St. George's Hospital, Londres).
- –
Ana Méndez Echevarría (Hospital Universitario La Paz-Carlos III, Madrid).
- –
David Moreno Pérez (Hospital Materno-Infantil, Hospital Regional Universitario de Málaga. Instituto de Investigación Biomédica de Málaga [IBIMA]).
- –
Antoni Noguera de Julián (Hospital Sant Joan de Déu, Barcelona).
- –
Roi Piñeiro Pérez (Hospital General de Villalba, Collado-Villalba, Madrid).
- –
Begoña Santiago García (H. General Universitario Gregorio Marañón, Madrid).
- –
Antoni Soriano Arandes (Hospital Vall d’ Hebron, Barcelona).
Proyecto avalado por todas las sociedades e instituciones firmantes. En el caso de RITIP y TEDDY no existe aval como tal, pues el documento ha sido solicitado desde dichas redes de investigación. El aval de la SENP ha sido concedido.
Los miembros del Grupo de Trabajo de Tuberculosis e Infección por otras Micobacterias de la Sociedad Española de Infectología Pediátrica se presentan en anexo 1.