La histiocitosis de células de Langerhans (HCL) es una enfermedad con comportamiento clínico heterogéneo cuya etiopatogenia inmunológica o neoplásica no está claramente definida. Se han identificado mutaciones somáticas en el protooncogén BRAFV600E en más del 50% de las lesiones de HCL. Nuestro objetivo es validar la inmunohistoquímica con el anticuerpo monoclonal VE1 como herramienta diagnóstica más sencilla y ágil que las técnicas moleculares para las HCL con mutación en BRAFV600E.
En el periodo comprendido entre 1976 y 2015, se estudiaron 91 pacientes con una media de edad al diagnóstico de 4 años (rango: 0,08-17). El 25% presentaron formas clínicas con afectación de un solo órgano o sistema (SS-LCH), con mayor frecuencia en piel o hueso, y el 70% formas multisistémicas (MS-LCH). Con una mediana de seguimiento de 4 años, la supervivencia global fue del 94% (IC 95%: 91-97). En 13 pacientes se obtuvieron muestras del biobanco siguiendo los siguientes criterios: 1) diagnóstico de HCL basado en el análisis morfológico con tinción de hematoxilina-eosina e inmunohistoquímica frente a proteína S100 y CD1a; 2) material histológico en parafina, y 3) exclusión de las muestras de tejido óseo para evitar la afectación de la expresión inmunohistoquímica secundaria a la descalcificación con ácido nítrico requerida en el procesamiento de estas muestras. No se encontraron diferencias significativas en las características clínicas de este subgrupo de pacientes respecto a la muestra total de estudio, considerando por tanto una muestra representativa. Se determinó BRAFV600E mediante reacción en cadena de la polimerasa (PCR) cualitativa (BRAF V600 Mutation Test de Roche®) y mediante análisis inmunohistoquímico frente a BRAFV600E (anticuerpo VE1, VENTANA® Medical Systems). La inmunoreactividad de BRAFV600E fue clasificada a través de una escala semicuantitativa en negativa (−), leve (+), moderada (++) o intensa (+++). Las muestras intensamente teñidas fueron consideradas positivas1,2.
De las 13 muestras seleccionadas, se demostró la presencia de BRAFV600E en 6 de ellas (46%). La concordancia entre el diagnóstico molecular e inmunohistoquímica fue del 100%, detectándose mutación BRAFV600E mediante PCR en todas las muestras con inmunorreactividad intensa (+++) (tabla 1).
Características clínicas y resultados de la mutación BRAFV600E a través de la técnica de inmunohistoquímica utilizando el anticuerpo VE1 (VENTANA® Medical Systems) y PCR en tiempo real (cobas® test Roche)
| Edad al diagnóstico | Forma clínica | Tejido | IHQ VE1 | PCR BRAF V600E | Total IHQ-BRAFV600E | |
|---|---|---|---|---|---|---|
| 1 | 2 años | MS-HCL | Ganglio | Negativa | No mutada | 2 negativas (15,4%)Cero mutadas(0%) |
| 2 | Un mes | SS-HCL | Pulmón | Negativa | No mutada | |
| 3 | 2 meses | SS-HCL | Piel | + | No mutada | 4 leves (30,8%)Cero mutadas(0%) |
| 4 | Un año | MS-HCL | Piel | + | No mutada | |
| 5 | 7 meses | MS-HCL | Ganglio | + | No mutada | |
| 6 | 4 años | SS-HCL | Músculo | + | No mutada | |
| 7 | 8 años | SS-HCL | Partes blandas | ++ | No mutada | Una moderada (7,2%)Cero mutadas(0%) |
| 8 | 4 años | SS-HCL | Partes blandas | +++ | Mutada | 6 intensas (46,2%)6 mutadas(46,2%) |
| 9 | 13 años | SS-HCL | Órbita | +++ | Mutada | |
| 10 | Un año | SS-HCL | Piel | +++ | Mutada | |
| 11 | 10 meses | MS-HCL | Oído | +++ | Mutada | |
| 12 | Un mes | MS-HCL | Encía | +++ | Mutada | |
| 13 | Um mes | MS-HCL | Piel | +++ | Mutada |
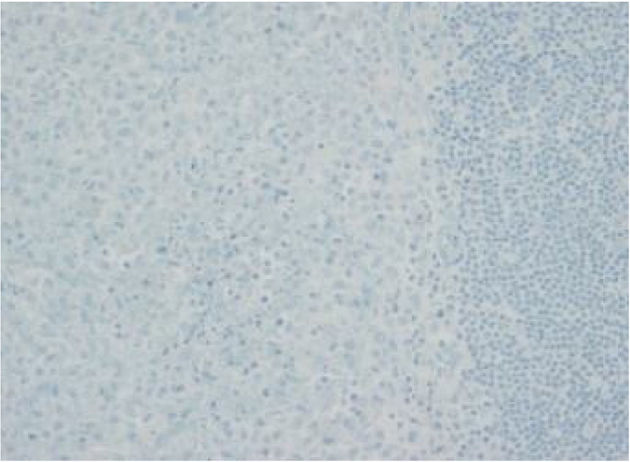
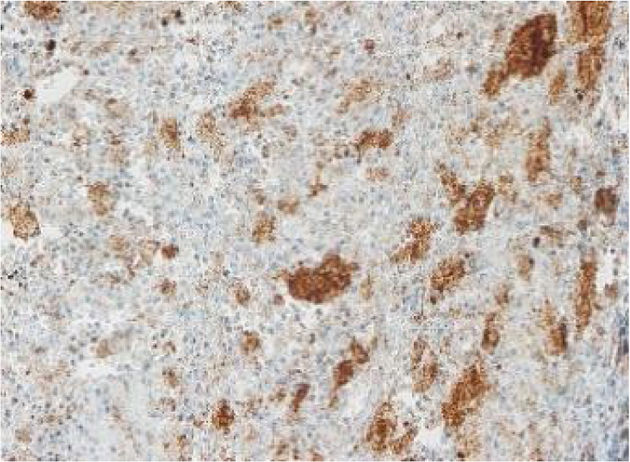
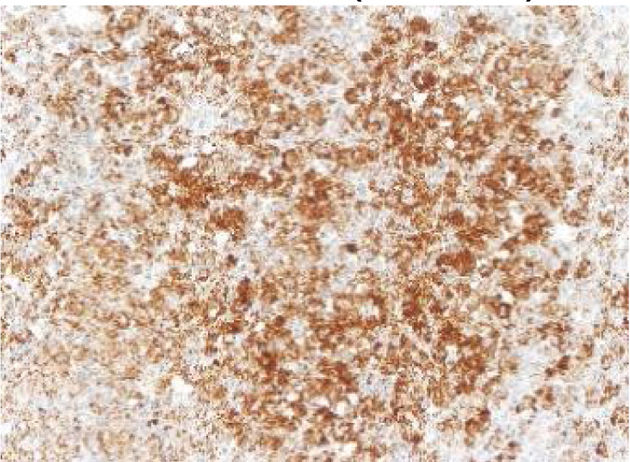
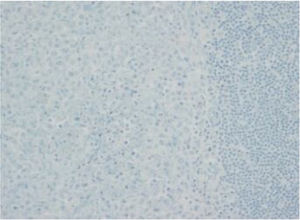
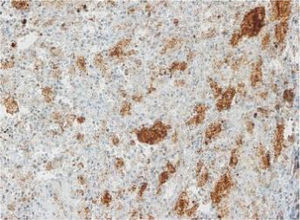
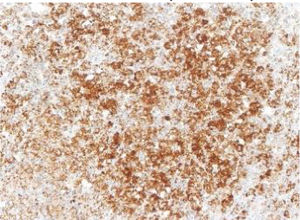
Las imágenes corresponden a un paciente representativo de los grupos con inmunohistoquímica con tinción negativa, leve, moderada o intensa.
IHQ: inmunohistoquímica; MS-LCH: histiocitosis de células de Langerhans multisistémica; PCR: reacción en cadena de polimerasa; SS-LCH: histiocitosis de células de Langerhans afectando a un único sistema.
Los resultados sugieren que la mutación BRAFV600E juega un papel importante en aproximadamente la mitad de los pacientes con HCL. Estas alteraciones genéticas contribuyen a considerar la HCL con mutación en BRAFV600E una neoplasia, debido a la evidencia sobre la clonalidad de las lesiones3,4. Otros autores consideran que las HCL sin esta mutación podría ser una enfermedad con una base de disregulación inmune que provocaría inflamación5.
La importancia de la detección de la mutación BRAFV600E en HCL radica en su potencial como diana terapéutica, planteando nuevas posibilidades terapéuticas en pacientes refractarios6. Además, proponemos la inmunohistoquímica VE1 como método fiable para detectar la mutación BRAFV600E siendo una alternativa a las técnicas de biología molecular por su facilidad técnica y sencilla interpretación.
FinanciaciónEste trabajo ha sido financiado en parte por la Fundación CRIS contra el cáncer https://criscancer.org/es/. La Fundación CRIS contra el cáncer no participó en el diseño ni desarrollo del estudio, ni en la publicación del manuscrito.