Las convulsiones neonatales (CN) afectan a 1,5 de cada 1.000 recién nacidos, siendo más frecuentes en prematuros. Suelen deberse principalmente a asfixia, hemorragias, malformaciones cerebrales, alteraciones electrolíticas, errores congénitos del metabolismo o infecciones1. A la dificultad para su diagnóstico y la decisión de a qué niños tratar, se une la cada vez mayor evidencia de efectos deletéreos de las medicaciones aprobadas para este fin: fenobarbital y fenitoína. Ambas consiguen reducir las crisis en menos del 50% de los casos, y se asocian a apoptosis neuronal en modelos animales. Por ello, cada vez se usan más otros fármacos, fuera de ficha técnica, con menos efectos secundarios aparentes. El levetiracetam (LEV) fue aprobado por la FDA en 20122 para el uso en convulsiones parciales a partir del mes de vida.
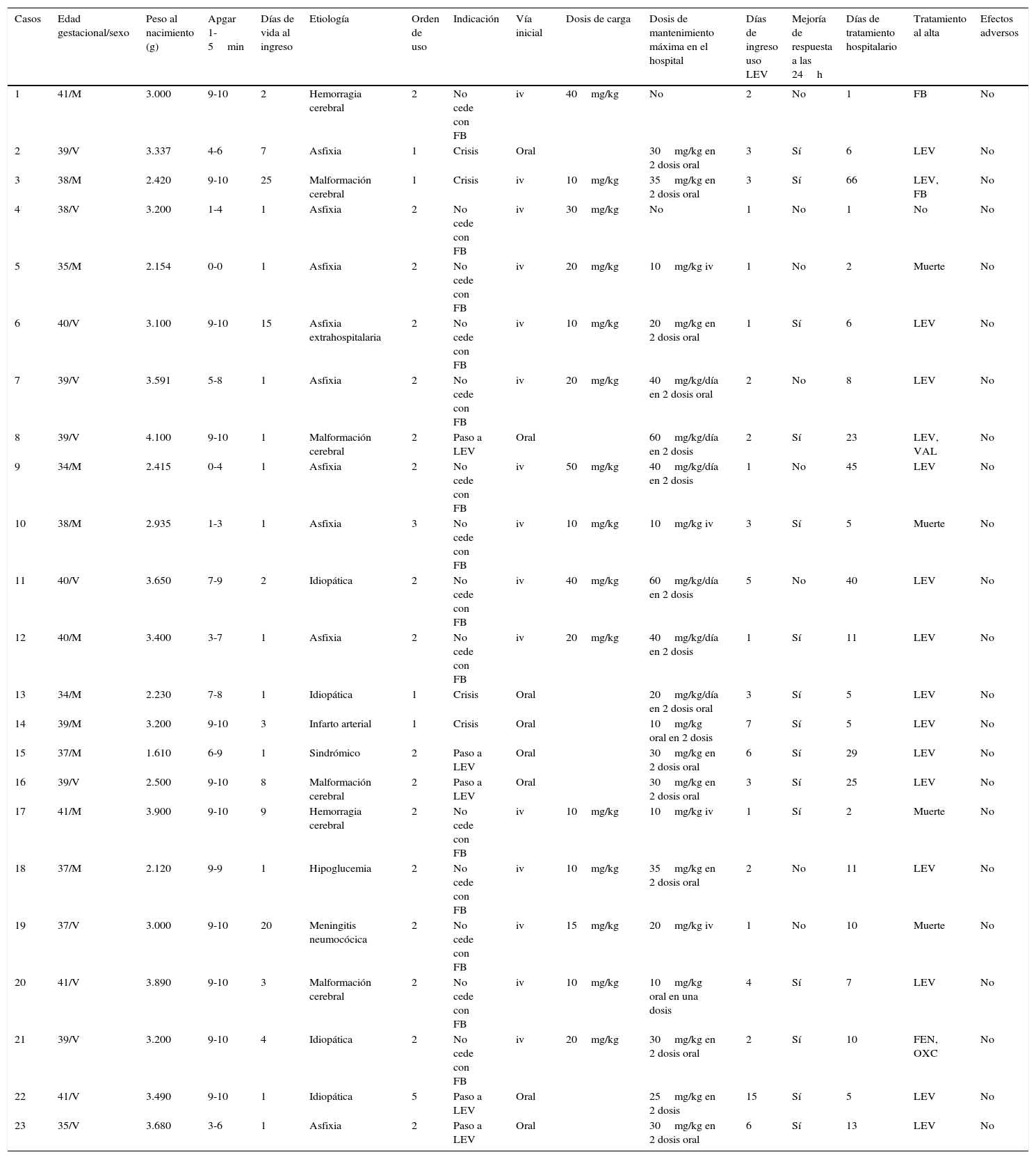
Revisamos el uso de LEV en neonatos hospitalizados en nuestra unidad, desde enero de 2011 a mayo de 2016. Las características de los pacientes aparecen en la tabla 1. Se trataron 23 recién nacidos, con un peso entre 1.610-4.100g, siendo el 17,4% prematuros. Los tipos de crisis, pruebas complementarias y resultados están reflejados en la tabla 2.
Características de los pacientes
| Casos | Edad gestacional/sexo | Peso al nacimiento (g) | Apgar 1-5min | Días de vida al ingreso | Etiología | Orden de uso | Indicación | Vía inicial | Dosis de carga | Dosis de mantenimiento máxima en el hospital | Días de ingreso uso LEV | Mejoría de respuesta a las 24h | Días de tratamiento hospitalario | Tratamiento al alta | Efectos adversos |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 41/M | 3.000 | 9-10 | 2 | Hemorragia cerebral | 2 | No cede con FB | iv | 40mg/kg | No | 2 | No | 1 | FB | No |
| 2 | 39/V | 3.337 | 4-6 | 7 | Asfixia | 1 | Crisis | Oral | 30mg/kg en 2 dosis oral | 3 | Sí | 6 | LEV | No | |
| 3 | 38/M | 2.420 | 9-10 | 25 | Malformación cerebral | 1 | Crisis | iv | 10mg/kg | 35mg/kg en 2 dosis oral | 3 | Sí | 66 | LEV, FB | No |
| 4 | 38/V | 3.200 | 1-4 | 1 | Asfixia | 2 | No cede con FB | iv | 30mg/kg | No | 1 | No | 1 | No | No |
| 5 | 35/M | 2.154 | 0-0 | 1 | Asfixia | 2 | No cede con FB | iv | 20mg/kg | 10mg/kg iv | 1 | No | 2 | Muerte | No |
| 6 | 40/V | 3.100 | 9-10 | 15 | Asfixia extrahospitalaria | 2 | No cede con FB | iv | 10mg/kg | 20mg/kg en 2 dosis oral | 1 | Sí | 6 | LEV | No |
| 7 | 39/V | 3.591 | 5-8 | 1 | Asfixia | 2 | No cede con FB | iv | 20mg/kg | 40mg/kg/día en 2 dosis oral | 2 | No | 8 | LEV | No |
| 8 | 39/V | 4.100 | 9-10 | 1 | Malformación cerebral | 2 | Paso a LEV | Oral | 60mg/kg/día en 2 dosis | 2 | Sí | 23 | LEV, VAL | No | |
| 9 | 34/M | 2.415 | 0-4 | 1 | Asfixia | 2 | No cede con FB | iv | 50mg/kg | 40mg/kg/día en 2 dosis | 1 | No | 45 | LEV | No |
| 10 | 38/M | 2.935 | 1-3 | 1 | Asfixia | 3 | No cede con FB | iv | 10mg/kg | 10mg/kg iv | 3 | Sí | 5 | Muerte | No |
| 11 | 40/V | 3.650 | 7-9 | 2 | Idiopática | 2 | No cede con FB | iv | 40mg/kg | 60mg/kg/día en 2 dosis | 5 | No | 40 | LEV | No |
| 12 | 40/M | 3.400 | 3-7 | 1 | Asfixia | 2 | No cede con FB | iv | 20mg/kg | 40mg/kg/día en 2 dosis | 1 | Sí | 11 | LEV | No |
| 13 | 34/M | 2.230 | 7-8 | 1 | Idiopática | 1 | Crisis | Oral | 20mg/kg/día en 2 dosis oral | 3 | Sí | 5 | LEV | No | |
| 14 | 39/M | 3.200 | 9-10 | 3 | Infarto arterial | 1 | Crisis | Oral | 10mg/kg oral en 2 dosis | 7 | Sí | 5 | LEV | No | |
| 15 | 37/M | 1.610 | 6-9 | 1 | Sindrómico | 2 | Paso a LEV | Oral | 30mg/kg en 2 dosis oral | 6 | Sí | 29 | LEV | No | |
| 16 | 39/V | 2.500 | 9-10 | 8 | Malformación cerebral | 2 | Paso a LEV | Oral | 30mg/kg en 2 dosis oral | 3 | Sí | 25 | LEV | No | |
| 17 | 41/M | 3.900 | 9-10 | 9 | Hemorragia cerebral | 2 | No cede con FB | iv | 10mg/kg | 10mg/kg iv | 1 | Sí | 2 | Muerte | No |
| 18 | 37/M | 2.120 | 9-9 | 1 | Hipoglucemia | 2 | No cede con FB | iv | 10mg/kg | 35mg/kg en 2 dosis oral | 2 | No | 11 | LEV | No |
| 19 | 37/V | 3.000 | 9-10 | 20 | Meningitis neumocócica | 2 | No cede con FB | iv | 15mg/kg | 20mg/kg iv | 1 | No | 10 | Muerte | No |
| 20 | 41/V | 3.890 | 9-10 | 3 | Malformación cerebral | 2 | No cede con FB | iv | 10mg/kg | 10mg/kg oral en una dosis | 4 | Sí | 7 | LEV | No |
| 21 | 39/V | 3.200 | 9-10 | 4 | Idiopática | 2 | No cede con FB | iv | 20mg/kg | 30mg/kg en 2 dosis oral | 2 | Sí | 10 | FEN, OXC | No |
| 22 | 41/V | 3.490 | 9-10 | 1 | Idiopática | 5 | Paso a LEV | Oral | 25mg/kg en 2 dosis | 15 | Sí | 5 | LEV | No | |
| 23 | 35/V | 3.680 | 3-6 | 1 | Asfixia | 2 | Paso a LEV | Oral | 30mg/kg en 2 dosis oral | 6 | Sí | 13 | LEV | No |
FB: fenobarbital; FEN: fenitoína; M: mujer; LEV: levetiracetam; OXC: oxcarbazepina; V: varón; VAL: ácido valproico.
Características de las crisis y pruebas diagnósticas
| N.° (%) | |
|---|---|
| Tipos de crisis | |
| Clónicas | 21 (91,2) |
| Solo sutiles | 1 (4,4) |
| Tónicas | 1 (4,4) |
| Causas | |
| Asfixia | 9 (39,1) |
| Malformación cerebral | 5 (21,7) |
| Hemorragias | 3 (13) |
| Idiopática | 3 (13) |
| Infecciones | 1 (4,4) |
| Metabólicas | 1 (4,4) |
| Hipoglucemia | 1 (4,4) |
| RMN con difusión | 21 (91,2) |
| RMN patológica | 15 (71,4) |
| Solo ecografía cerebral | 2 (8,8) |
| Patológica | 2 (100) |
| EEGa* | 21 (91,2) |
| Crisis | 17 (81) |
| Solo alteración patrón de fondo | 4 (19) |
| EEG | 22 (95,6) |
| Patológico | 14 (63,6) |
EEG: electroencefalograma; RMN: resonancia magnética nuclear.
EEGa* Electroencefalograma integrado por amplitud.
Se usó como primera opción terapéutica en el 17,4% de los casos, siendo la segunda opción en el 73,9%, mayoritariamente tras fenobarbital. En 15 casos (65,2%) se usó una dosis de carga intravenosa, ente 10-50mg/kg. Se usó dosis de mantenimiento en el 91,3%, entre 10-40mg/kg/2 dosis, con aumento de 10mg/kg/3-5 días. De los 19 casos en los que se usó como segunda opción, se consiguió la reducción del primer medicamento en el 63,1% en la primera semana tras el inicio de LEV. En 8 casos no mejoraron las crisis clínicas o eléctricas en las primeras 24h, pero en 15 (65,2%) sí mejoraron (entendiendo mejoría como cese de las crisis o reducción al menos al 50% de frecuencia). No se identificaron efectos adversos en ningún caso. En 4 casos se realizó limitación del esfuerzo terapéutico, sin relación con el uso de LEV. De los 19 restantes, el 88,9% fueron dados de alta con LEV (77,8% en monoterapia).
El uso de LEV en las CN es cada vez más frecuente, pese a no estar aprobado su uso, como la mayoría de fármacos antiepilépticos en lactantes. Se recomienda más por parte de neuropediatras que de neonatólogos1,2. Un estudio3 encontró retrospectivamente, 72 neonatos tratados con LEV, siendo la mayoría prematuros, sin encontrar efectos secundarios que interrumpieran el tratamiento. El criterio de crisis fue únicamente clínico, ya que no se usó aEEG o EEG, por lo que los resultados de eficacia son discutibles. Estudios previos han reclutado entre 6 y 38 neonatos2, algunos solo con prematuros (n=12)4. Un estudio prospectivo5, de 38 neonatos, con uso de LEV como primera opción, encontró mejoría clínica, y en EEG a la semana de vida en 30 de ellos, sin efectos secundarios, aunque permitió 2 dosis de fenobarbital mientras se incrementaban gradualmente las dosis de LEV, por lo que el fenobarbital o la propia evolución de las crisis pudieron influir en los resultados. Se ha comunicado un caso de shock anafiláctico tras la infusión de LEV en un neonato6, y es posible que en niños con situaciones clínicas complejas y con mediación previa no sean fáciles de detectar. Recientemente se ha asociado el LEV a la apoptosis neuronal en asfixias no tratadas con hipotermia6. Dada la escasez de trabajos en neonatos, aún no es posible determinar la seguridad de este fármaco como primera opción en el tratamiento de las CN, y la mayoría de las guías actuales que incluyen el LEV lo relegan a una segunda opción.
Esta revisión tiene limitaciones. Además de ser retrospectiva, el número de casos es pequeño, aunque no hemos encontrado ninguna publicación española sobre el tema; no disponemos de vídeo-EEG para el diagnóstico de las crisis, aunque se ha usado el aEEG y el EEG para guiar el tratamiento. Un mayor número de casos podría determinar si la edad gestacional o la causa de las crisis tiene relación con la respuesta a LEV.
En conclusión, el LEV es cada vez más usado en las CN, en general como segundo fármaco. Parece tener una efectividad al menos similar a los antiepilépticos clásicos. Los escasos efectos secundarios encontrados y el menor daño cerebral que parece tener, hace del LEV un fármaco a considerar, incluso en prematuros. Son necesarios estudios prospectivos para conocer los efectos a corto y largo plazo de esta medicación.
Esta revisión tiene la conformidad del comité de ética hospitalaria.