El síndrome de apneas-hipopneas del sueño (SAHS) es altamente prevalente en la edad pediátrica y un problema importante de salud pública. Se pretende conocer la presentación clínica y polisomnográfica del SAHS infantil en nuestro medio.
Pacientes y métodosEstudio descriptivo retrospectivo de los estudios del sueño realizados a menores de 14 años desde 1999 hasta 2012 en la Unidad del Sueño del Complejo Hospitalario Universitario de Albacete. Se recogen edad, sexo, datos antropométricos, clínicos, indicación y variables del estudio del sueño, tratamiento y evolución.
ResultadosDoscientos treinta y cuatro niños. SAHS el 71,8%: moderado 42,3% y grave 44,6%. 60,7% varones y mediana de edad 5 años; el 78% en edad preescolar o escolar. Presentaban sobrepeso/obesidad 44%, ronquidos 93,4%, apneas 84,5% y somnolencia diurna 5,4%; 23 polisomnografías y 145 poligrafías: mediana de índice de apneas-hipopneas (IAH) 10, de SatO2 mínima 84% y de índice de desaturaciones 8, y media de sueño en supino 53,65% y de eventos en supino 57,61%. El tratamiento fue medidas higiénico-dietéticas en el 29,2%, CPAP el 6% y cirugía el 42,9%. Mejoraron los ronquidos y/o apneas el 69,4% y el peso el 32,4% de los niños con sobrepeso/obesidad.
ConclusionesLa mayoría de los niños estudiados tenían un IAH patológico. Casi la mitad presentaban sobrepeso/obesidad y un alto porcentaje tenía SAHS moderado-grave. El tratamiento más indicado fue la cirugía. La evolución clínica fue favorable en casi el 70%. Menos de un tercio con SAHS y sobrepeso/obesidad mejoraron el peso.
Obstructive sleep apnoea (OSA) is highly prevalent in children and a major public health problem. An attempt is made to determine the clinical and polysomnographic presentation of paediatric OSA in our area.
Patients and methodsRetrospective descriptive study of sleep tests conducted on children up to 14 years-old from 1999 to 2012 in the Sleep Unit of the University Hospital of Albacete. Age, gender, anthropometric, clinical data, indication and variables of sleep study, treatment, and outcomes were collected.
ResultsThe study included 234 children. OSA was found in 71.8%, with 42.3% moderate and 44.6% severe. The majority were male (60.7%) and the mean age 5 was years, of whom 78% were pre-school or school age. There was overweight/obesity in 44%, with 93.4% snoring, apnoea 84.5%, and 5.4% daytime sleepiness. There were 23 polysomnographies and 145 polygraphies, with a median apnoea/hypopnoea index (AHI) of 10, Sat.O2 minimum 84%, desaturation index 8, and mean sleep supine 53.65% and supine events 57.61%. Treatment was lifestyle modifications 29.2%, CPAP 6%, and surgery 42.9%. Improved snoring and/or apnoea 69.4%, and weight 32.4% of overweight/obesity children.
ConclusionsMost of the studied children had a pathological AHI. Almost half were overweight/obese, and a high percentage had moderate-severe OSA. Most frequent treatment was surgery. The clinical outcome was favourable in almost 70%. Less than a third with OSA and overweight/obesity improved weight.
El síndrome de apneas-hipopneas del sueño (SAHS) consiste en «episodios repetidos de limitación completa (apnea) o parcial (hipopnea) del paso del aire durante el sueño, consecuencia de una alteración anatómico-funcional de la vía aérea superior (VAS), que conduce a su colapso, pudiendo acompañarse de desaturaciones de oxígeno y de múltiples despertares no conscientes (microdespertares), que producen un sueño no reparador». Puede asociarse a somnolencia diurna excesiva (SDE), trastornos neuropsiquiátricos, respiratorios, endocrino-metabólicos y cardíacos1. Aunque cierto número de apneas-hipopneas aparecen en la cuarta parte de la población, nos referimos a SAHS cuando su número es elevado y causa problemas de salud2.
El SAHS afecta al 4-6% de varones y al 2-4% de mujeres en edades medias3,4 y su frecuencia aumenta con la edad5. Es un problema de salud pública de primera magnitud6. Sin embargo, solo se ha diagnosticado y tratado al 5-9% de los 1.200.000-2.150.000 sujetos afectados que se calcula que hay en España7.
El SAHS ocurre también en la edad pediátrica y tiene características específicas. El niño presenta particularidades anatómico-funcionales de la VAS y peculiaridades madurativas en la neurofisiología del sueño que lo diferencian del adulto. El SAHS infantil comprende una entidad clara con perfiles muy diferenciados en su etiología, presentación clínica y tratamiento. Tanto la clínica como las consecuencias físicas, cognitivas y madurativas difieren en muchos aspectos2. En este sentido, la Academia Americana de Medicina del Sueño separa ambas entidades y las incluye en apartados diferentes en su clasificación8.
En 2011 se publicó el Documento de consenso del síndrome de apneas-hipopneas durante el sueño en niños9, que define el SAHS infantil como un trastorno respiratorio del sueño caracterizado por una obstrucción parcial prolongada de la VAS y/u obstrucción intermitente completa, que interrumpe la ventilación normal durante el sueño y sus patrones normales. Asocia síntomas que incluyen ronquido, dificultades con el sueño y/o problemas de comportamiento y aprendizaje10. Los casos graves pueden ocasionar alteraciones del crecimiento y neurocognitivas y cor pulmonale. Existen varios factores de riesgo11, siendo la hipertrofia adenoamigdalar el más frecuente, seguido por la obesidad, que ha aparecido en los últimos años como factor etiológico emergente en niños. También están las malformaciones craneofaciales, las enfermedades neurológicas como la parálisis cerebral infantil, las enfermedades neuromusculares y el reflujo gastroesofágico9.
El SAHS es altamente prevalente en la infancia. Afecta al 2-4% de niños entre 2 y 6 años10, con un pico de incidencia entre 2 y 5 años. Las edades más frecuentes son la preescolar y escolar, pero puede manifestarse en los primeros meses de vida. Afecta por igual a ambos sexos2. Por tanto, el SAHS constituye un problema preferente de salud pública infantil por su elevada prevalencia, porque se comporta como trastorno comórbido de diferentes procesos crónicos, empeora el curso de diferentes entidades a las que se asocia e influye en la calidad de vida del niño y sus cuidadores9.
Nuestra unidad realiza estudios del sueño a niños desde 1999. El número de estudios está aumentando en los últimos años. Los pacientes son remitidos, principalmente, por sospecha clínica de SAHS o como evaluación previa a cirugía en candidatos a adenoamigdalectomía. Con este trabajo se pretende conocer cuál es la presentación clínica y polisomnográfica del SAHS en < 14 años de nuestra área y, secundariamente, determinar cuáles son los tratamientos más empleados y cuál es la evolución clínica y ponderal su instauración.
Pacientes y métodosSe trata de un estudio retrospectivo y descriptivo en el que se incluyen, de forma consecutiva, los 234 estudios del sueño que se realizaron a < 14 años desde octubre de 1999 hasta agosto del 2012 en la Unidad del Sueño del Servicio de Neumología del Complejo Hospitalario Universitario de Albacete.
Se registraron las siguientes variables: sexo, edad, indicación del estudio, comorbilidad, clínica, peso, talla, IMC, tipo de estudio, variables polisomnográficas/poligráficas, diagnóstico, gravedad, tratamiento y evolución clínica y del peso.
Todas las variables se obtuvieron mediante la revisión de las historias clínicas hospitalarias de los niños, con una búsqueda activa. La presencia o ausencia de ronquidos, apneas o SDE estaba registrada en todos los casos.
Se consideró que existía comorbilidad y/o hipertrofia adenoamigdalar cuando así lo determinaban en la historia clínica hospitalaria, a su criterio, los especialistas en Pediatría y en Otorrinolaringología.
Se consideró obesidad un percentil de IMC ≥ 95 (P95) y sobrepeso un percentil de IMC > 85 (P85) y < P9512,13.
Todas las polisomnografías (PSG) y poligrafías respiratorias (PR) se realizaron en nuestra unidad, siendo analizadas e interpretadas por el mismo neumólogo. La decisión del tipo de estudio fue tomada por el responsable de la unidad, en función de los recursos disponibles y las indicaciones vigentes en cada momento.
Las variables polisomnográficas/poligráficas incluyen: índice de apneas-hipopneas (IAH)/índice de eventos respiratorios (IER), SatO2 basal, media y mínima, porcentaje de tiempo con SatO2 < 90% (T90), índice de desaturaciones≥3% por hora de sueño/registro, porcentaje de sueño/registro en decúbito supino y porcentaje de eventos respiratorios en decúbito supino.
El Grupo Español de Sueño, en el Consenso del SAHS, considera un IAH entre 1 y 3 como línea de corte de normalidad2. Por tanto, un IAH/IER menor de 3 no se consideró patológico. En relación con la gravedad del SAHS, se clasificó como leve un IAH/IER < 5, moderado 5-10 y grave > 109.
El tratamiento fue instaurado por Otorrinolaringología en los casos en los que existía hipertrofia adenoamigdalar y por Pediatría y/o Neumología en el resto de los casos, de acuerdo con las indicaciones y las recomendaciones vigentes en cada momento.
La evolución ponderal y clínica se clasificó en mejor, igual o peor, recogiéndose esta variable de los datos registrados en la historia clínica hospitalaria de los pacientes en las revisiones posteriores al tratamiento instaurado, siempre y cuando hubieran pasado, al menos, 6 meses del mismo. La sintomatología se consideró mejor si los familiares referían disminución de los ronquidos y las apneas, igual si persistían y peor si aumentaban en frecuencia o intensidad, siempre de forma subjetiva. El peso se consideró mejor si el percentil de IMC bajaba de subgrupo (de≥95 a 86-94 o a≤85 y de 86-94 a≤85), igual si no cambiaba de subgrupo y peor si subía de subgrupo (de≤85 a 86-94 y de 86-94 a≥95).
El estudio descriptivo ha consistido en el cálculo de proporciones para variables cualitativas y de medidas de dispersión y centralización para cuantitativas. En muestras normales se utilizaron la media y la desviación estándar, y en muestras no normales la mediana y rango intercuartil (RI).
Los análisis estadísticos, gráficos y tablas fueron realizados con el programa SPSS versión 19.0 para Windows.
ResultadosSe realizaron 234 estudios, 148 (63,2%) en varones, con una mediana de edad de 5 años (RI 3-8,25). El motivo por el que se realizó fue valorar la necesidad de cirugía por hipertrofia adenoamigdalar en 112 (47,9%) niños, por sospecha clínica de SAHS en 108 (46,2%) y por otros motivos en 14 (6%).
De los 234 niños estudiados, 168 (71,8%) presentaban un IAH/IER ≥ 3 eventos por hora, por lo que fueron diagnosticados de SAHS. De ellos, 102 (60,7%) eran varones, con una mediana de edad de 5 años (RI 3-8), encontrándose 82(48,8%) en edad preescolar y 49 (29,2%) en edad escolar. Por tanto, 131 (78%) niños estaban en edad preescolar/escolar.
La mayoría de los niños diagnosticados de SAHS no presentaban comorbilidad de importancia. La patología encontrada con mayor frecuencia fue la neumológica, en 35 (20,8%) de ellos, y dentro de ella, el diagnóstico más frecuente fue el de asma bronquial en 24 (14,3%). No obstante, no había asociación estadísticamente significativa entre la presencia de patología neumológica y SAHS (20,8% vs. 21,2%; p=0,949) ni entre la presencia de asma y SAHS (14,3% vs. 15,2%; p=0,866).
El ronquido estaba presente en 157 (93,4%), las apneas presenciadas en 142 (84,5%) y la SDE en 9 niños (5,4%). Presentaban sobrepeso/obesidad 74 (44%) niños, hipertrofia adenoamigdalar 100 (59,5%) y ambas condiciones 35 (20,8%).
El diagnóstico se alcanzó mediante PSG en 23 pacientes y por PR en 145. Se obtuvieron como resultados de interés los mostrados en la tabla 1.
Resultados de las variables del estudio del sueño analizadas
| Variable | Resultado |
|---|---|
| IAH/IER (mediana de eventos por hora) | 10 (RI 6-15) |
| SatO2 basal (mediana) | 97% (RI 97-98) |
| SatO2 media (mediana) | 95% (RI 94-96) |
| SatO2 mínima (mediana) | 84% (RI 74-88) |
| T90 (mediana) | 0% (RI 0-2) |
| Desaturaciones ≥ 3% por hora de sueño/registro (mediana) | 8 (RI 4-14) |
| Sueño/registro en supino (media) | 53,65±30,94% |
| Eventos en supino (media) | 57,61±30,94% |
IAH: índice de apneas-hipopneas; IER: índice de eventos respiratorios; RI: rango intercuartil; SatO2: saturación de oxígeno; T90: porcentaje de sueño/registro en el que la saturación de oxígeno es menor del 90%.
El SAHS resultó leve en 22 (13,1%) pacientes, moderado en 71 (42,3%) y grave en 75 (44,6%).
En los 168 niños con SAHS, el tratamiento realizado fue adenoamigdalectomía en 72 (42,9%), medidas higiénico-dietéticas (pérdida de peso/dieta, medidas antirronquido, medidas higiénicas del sueño) en 49 (29,2%), CPAP en 10 (6%) y otras terapias en 37 (22%), entre las que se encuentran observación y seguimiento, tratamiento antiinflamatorio tópico, dispositivos de avance mandibular y terapias endodóncicas/ortodóncicas.
Tras el tratamiento instaurado, de los 157 niños que presentaban ronquidos y/o apneas presenciadas, mejoraron esta sintomatología 109 (69,4%), estaban igual 47 (29,9%) y empeoró 1 (0,6%). De los 74 niños con diagnóstico de SAHS y sobrepeso/obesidad, mejoraron el peso 24 (32,4%), permanecieron igual 36 (48,6%) y empeoraron 14 (18,9%).
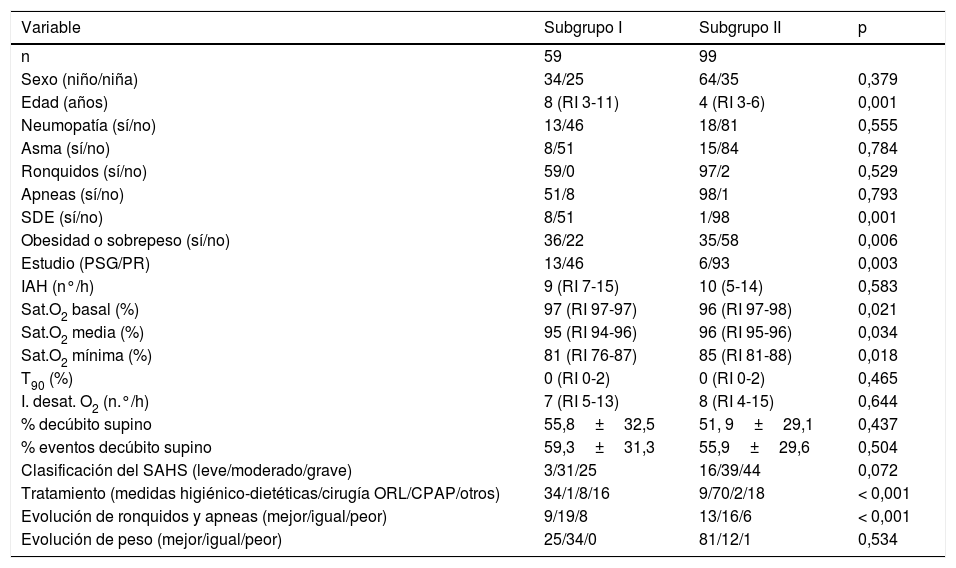
Se evaluaron también las características de 2 subgrupos de pacientes con SAHS, elaborados en función de la indicación del estudio del sueño: por sospecha clínica de SAHS (subgrupo i) o para valorar la necesidad de cirugía por presencia de hipertrofia adenoamigdalar (subgrupo ii), reflejándose los resultados y el análisis comparativo entre ambos subgrupos en la tabla 2.
Diferencias entre los 2 subgrupos planteados
| Variable | Subgrupo I | Subgrupo II | p |
|---|---|---|---|
| n | 59 | 99 | |
| Sexo (niño/niña) | 34/25 | 64/35 | 0,379 |
| Edad (años) | 8 (RI 3-11) | 4 (RI 3-6) | 0,001 |
| Neumopatía (sí/no) | 13/46 | 18/81 | 0,555 |
| Asma (sí/no) | 8/51 | 15/84 | 0,784 |
| Ronquidos (sí/no) | 59/0 | 97/2 | 0,529 |
| Apneas (sí/no) | 51/8 | 98/1 | 0,793 |
| SDE (sí/no) | 8/51 | 1/98 | 0,001 |
| Obesidad o sobrepeso (sí/no) | 36/22 | 35/58 | 0,006 |
| Estudio (PSG/PR) | 13/46 | 6/93 | 0,003 |
| IAH (n°/h) | 9 (RI 7-15) | 10 (5-14) | 0,583 |
| Sat.O2 basal (%) | 97 (RI 97-97) | 96 (RI 97-98) | 0,021 |
| Sat.O2 media (%) | 95 (RI 94-96) | 96 (RI 95-96) | 0,034 |
| Sat.O2 mínima (%) | 81 (RI 76-87) | 85 (RI 81-88) | 0,018 |
| T90 (%) | 0 (RI 0-2) | 0 (RI 0-2) | 0,465 |
| I. desat. O2 (n.°/h) | 7 (RI 5-13) | 8 (RI 4-15) | 0,644 |
| % decúbito supino | 55,8±32,5 | 51, 9±29,1 | 0,437 |
| % eventos decúbito supino | 59,3±31,3 | 55,9±29,6 | 0,504 |
| Clasificación del SAHS (leve/moderado/grave) | 3/31/25 | 16/39/44 | 0,072 |
| Tratamiento (medidas higiénico-dietéticas/cirugía ORL/CPAP/otros) | 34/1/8/16 | 9/70/2/18 | < 0,001 |
| Evolución de ronquidos y apneas (mejor/igual/peor) | 9/19/8 | 13/16/6 | < 0,001 |
| Evolución de peso (mejor/igual/peor) | 25/34/0 | 81/12/1 | 0,534 |
CPAP: continuous positive airway pressure; I. desat. O2: índice de desaturaciones de oxígeno ≥ 3%; IAH: índice de apneas/hipopneas; ORL: otorrinolaringológica; PR: poligrafía respiratoria; PSG: polisomnografía; RI: rango intercuartil; SatO2: saturación de oxígeno; SDE: somnolencia diurna excesiva; T90: porcentaje de sueño en el que la saturación de oxígeno está por debajo de 90%.%.
La importancia de los trastornos del sueño en niños en nuestra área va en aumento (hasta el año 2009 se habían estudiado 90 niños en nuestra unidad, pasando esta cifra a 234 en 2012). En los últimos años, el SAHS era clínicamente significativo hasta en un 90% de los niños y el tratamiento permitió el control de los síntomas en la mayoría.
La prevalencia del SAHS en niños es alta, situándose, según los estudios consultados, en el 2-4% de la población infantil10.
La edad más frecuente de presentación de SAHS infantil en nuestro medio se encontraba entre los 2 y los 5 años, seguida muy de cerca por la edad escolar. En la bibliografía consultada, al igual que en nuestro estudio, las edades más frecuentes de presentación son la preescolar y escolar, y afecta por igual a ambos sexos2.
La hipertrofia adenoamigdalar y la obesidad son los principales factores de riesgo de SAHS en niños, por lo demás, sanos. Tal y como se aprecia en los resultados de nuestro trabajo, la causa más frecuente de SAHS en la edad pediátrica es el aumento de tamaño de las amígdalas y/o la presencia de adenoides, encontrándose hipertrofia adenoamigdalar en el 59,5% de nuestros pacientes con SAHS.
El SAHS también puede estar asociado a obesidad, alteraciones anatómicas, neurológicas, metabólicas o musculares2,9. La susceptibilidad individual, así como las condiciones ambientales y el estilo de vida (actividad física e intelectual, dieta…), desempeñan un importante papel en la variabilidad fenotípica. Por este motivo, y por los cambios comportamentales y dietéticos de la población infantil durante los últimos años, en los que ha aumentado la obesidad y el sedentarismo, el fenotipo clásico está siendo progresivamente sustituido por un patrón similar al que se encuentra en la edad adulta.
En nuestro trabajo, 74 (44%) de los pacientes con SAHS presentaban sobrepeso/obesidad. La presencia de esta condición era la causa más probable del SAHS en 39 (23,2%), ya que no asociaban hipertrofia adenoamigdalar. Hannon et al., en un estudio de 37 adolescentes con obesidad (percentil de IMC > 97), encontraron que el 45% presentaba SAHS en la PSG (definido por IAH > 1,5)14. Otros estudios muestran que el 47% de los niños obesos tienen cuadros de SAHS moderados-graves y el 39% leves15,16. Redline et al. encontraron que la obesidad era el factor de riesgo más significativo para SAHS, con una OR de 4,59 (IC del 95%, 1,58-13,33)17. En una revisión de 27 estudios18, un tercio de los menores de 10 años presentaba una asociación significativa obesidad-SAHS. De hecho, en una revisión de publicaciones de Ng et al. se señala que la gravedad del SAHS se relaciona con el grado de obesidad19. Existe disparidad en el porcentaje de niños con SAHS que presentan obesidad, oscilando entre el 10 y el 50,6%20-23. No obstante, no hay igualdad de criterios en la definición de obesidad y se suele excluir el sobrepeso. En un estudio más reciente, que incluye a 197 menores de 18 años con trastornos respiratorios del sueño, encontraron que un 45,1% presentaba sobrepeso/obesidad. De ellos, no presentaban hipertrofia amigdalar 34, por lo que en el 17,2% del total de la muestra el factor de riesgo más importante era el sobrepeso/obesidad24.
El 93,4% de los niños con SAHS de nuestra muestra presentaban ronquido y el 84,5% apneas presenciadas por los padres. Los 3 síntomas con mayor poder de predicción de la presencia de SAHS son el ronquido, la respiración dificultosa y las pausas respiratorias durante el sueño. Muchos estudios retrospectivos han demostrado que el SAHS no puede distinguirse del ronquido simple basándonos exclusivamente en la historia clínica y la exploración física25. Una historia ronquido intenso no tiene la suficiente sensibilidad diagnóstica para indicar la cirugía en el niño11. De igual manera, la revisión de cintas de vídeo26 y audio27 del sueño de niños, junto con la valoración clínica, no tiene la suficiente especificidad para confirmar el diagnóstico de SAHS. En una revisión sistemática de la bibliografía se comprobó que los resultados de la valoración clínica comparados con los resultados de la PSG nocturna tenían un valor predictivo positivo medio de solo el 55% y, además, ninguno de los estudios analizados demostró que la clínica tuviera una sensibilidad y especificidad > 65%28. Por estas razones, la American Thoracic Society11 y la American Academy of Pediatrics10 recomiendan la PSG para evaluar el SAHS infantil antes de la cirugía.
En nuestro estudio, un 5,4% de los niños con SAHS presentaba SDE. Quizá la diferencia clínica más importante con los adultos radica en que el niño con problemas respiratorios nocturnos no presenta una SDE de manera obvia en la mayoría de las ocasiones y, si está presente, no es predictiva de SAHS en niños pequeños29.
En nuestra serie, se utilizó la PR como método diagnóstico en 208 niños y la PSG en 26. La PSG nocturna es el método de referencia para detectar y graduar la gravedad del SAHS en niños. No obstante, la PR podría utilizarse en la extensa población infantil susceptible de SAHS y de esta forma disminuir el infradiagnóstico, reservándose la PSG para niños con comorbilidad derivados de forma urgente para estudio de sueño y en casos de dudas diagnósticas o sospecha de otras patologías de sueño diferentes del SAHS9. En casos no complicados, la PR puede tener una alta correlación con los hallazgos de la PSG. Varios autores indican que el empleo de criterios clínicos, junto con una exploración minuciosa de la VAS, un vídeo doméstico y una PR con un equipo validado es una buena alternativa para el diagnóstico de certeza de niños con sospecha clínica de SAHS30,31. Hay pocos estudios realizados con PR en niños y son en población de alta probabilidad de SAHS, con escaso número de pacientes y sin comparar simultáneamente con la PSG, obteniéndose resultados discordantes32. En un estudio realizado en España en el que se comparan ambas técnicas concluyen que la PR realizada en el laboratorio de sueño es un método válido para el diagnóstico de SAHS en niños33.
La extirpación amigdalar y adenoidea es, habitualmente, el tratamiento de elección en los niños con SAHS demostrado y presencia de hipertrofia adenoamigdalar. En nuestro estudio, la adenoamigdalectomía fue el tratamiento más indicado y supuso mejoría de los síntomas en 68 (94,4%) de los 72 intervenidos. No obstante, esta mejoría registrada es subjetiva y no objetivada por medio de un nuevo estudio del sueño poscirugía, lo que supone una limitación en este aspecto, ya que desconocemos el número de pacientes con SAHS residual real y, por tanto, subsidiarios de otros tratamientos. En la bibliografía, la eficacia de la adenoamigdalectomía es de aproximadamente el 78% de los casos de SAHS infantil2,10,34,35, pero es variable. Una revisión de la Cochrane del año 200935 muestra la ausencia de estudios doble ciego en el tratamiento del SAHS infantil y concluye que la literatura disponible sobre los efectos de la adenoamigdalectomía en el SAHS pediátrico presenta problemas metodológicos que incluyen la falta de aleatorización y controles, así como variaciones en las definiciones y variables tenidas en cuenta. En un estudio multicéntrico retrospectivo del 201022, encuentran una tasa de curación del 27,2% si se consideraba como criterio de eficacia un IAH < 1/h. En cambio, el porcentaje de eficacia ascendía a 78,4% si se consideraba un IAH ≤ 5. Concluyen que la adenoamigdalectomía se asocia a mejoras significativas en la mayoría de los niños. Sin embargo, hasta que aparezcan los resultados de estudios multicéntricos prospectivos, deberían efectuarse estudios del sueño pre y poscirugía a los niños con mayor riesgo de SAHS residual, entre los que se encuentran los mayores de 7 años, los obesos y los no obesos con asma o SAHS intenso.
En nuestro grupo de pacientes, se utilizó la CPAP como tratamiento en 10, presentando todos ellos sobrepeso/obesidad. Los tratados con CPAP se revisaban en la Consulta Externa de Neumología Monográfica de Sueño, registrándose en 9 (90%) de ellos una mejoría de la sintomatología. La CPAP constituye la segunda línea de tratamiento del SAHS en la infancia36, ya que la mayoría de los niños con SAHS mejora con la adenoamigdalectomía, quedando un pequeño grupo de pacientes que requerirán tratamientos adicionales o en los que la CPAP será la primera opción. Suelen ser niños con obesidad, alteraciones craneofaciales o enfermedades neuromusculares añadidas a la hipertrofia adenoamigdalar o sin hipertrofia adenoamigdalar10.
Además de la limitación ya mencionada, somos conscientes de aquellas derivadas del carácter retrospectivo del estudio, del uso predominante de la PR como método diagnóstico y de la no inclusión de cierta sintomatología que resulta relevante en el SAHS infantil.
Podemos concluir que la mayoría de los niños estudiados en nuestra unidad tenían un IAH patológico y un alto porcentaje de ellos fueron diagnosticados de SAHS moderado o grave. Casi la mitad de los niños con SAHS presentaban sobrepeso/obesidad. El tratamiento más frecuentemente indicado fue la adenoamigdalectomía. La evolución clínica tras el tratamiento instaurado fue favorable en casi el 70% de los niños con SAHS y menos de un tercio con SAHS y sobrepeso/obesidad consiguieron mejorar el peso.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Presentación previa: 48.° Congreso Nacional SEPAR, Gran Canaria, 5-8 de junio del 2015.