El diagnóstico precoz es esencial para disminuir la morbimortalidad en la sepsis neonatal precoz (SNP). La procalcitonina (PCT) en sangre de cordón permitiría identificar al nacimiento a los pacientes infectados.
ObjetivoEstudiar la utilidad y seguridad de un protocolo de valoración de recién nacidos con riesgo de SNP, basado en los valores de procalcitonina en sangre de cordón.
Pacientes y métodosSe incluyeron los nacidos en nuestro hospital de octubre de 2013 a enero de 2015, con factores de riesgo infeccioso. Se procedió según un algoritmo basado en los valores de procalcitonina (<0,6ng/ml frente a ≥0,6ng/ml). Posteriormente se clasificaron como infección comprobada, probable o no infección.
Resultados y conclusionesDe 2.519 nacidos en el periodo de estudio 136 cumplieron criterios de inclusión. De 120 casos con PCT <0,6ng/ml ninguno desarrolló SNP (valor predictivo negativo 100%). Por el contrario, de 16 casos con PCT ≥0,6ng/ml, diez presentaron infección comprobada o probable (valor predictivo positivo 62,5%). La sensibilidad de la PCT frente a infección fue 100% y la especificidad 95,2% (área bajo la curva operador receptor 0,969). La incidencia de infección en el grupo de estudio fue de 7,4%; en RN de madre con corioamnionitis 26,1%. Recibieron antibioterapia 21 recién nacidos (15,4%).
El protocolo clínico estudiado ha demostrado ser efectivo y seguro para diferenciar entre pacientes con mayor riesgo de SNP, en los que la aproximación diagnóstica y terapéutica fue más intervencionista, frente a aquellos con menor probabilidad de sepsis, que se beneficiaron de un manejo más conservador.
Early diagnosis of early-onset neonatal sepsis (EONS) is essential to reduce morbidity and mortality. Procalcitonin (PCT) in cord blood could provide a diagnosis of infected patients from birth.
ObjectiveTo study the usefulness and safety of a procedure for the evaluation of newborns at risk of EONS, based on the determination of PCT in cord blood.
Patients and methodsNeonates with infectious risk factors, born in our hospital from October 2013 to January 2015 were included. They were processed according to an algorithm based on the values of cord blood procalcitonin (< 0.6ng/ml versus ≥0.6ng/ml). They were later classified as proved infection, probable, or no infection.
Results and conclusionsOf the 2,519 infants born in the study period, 136 met inclusion criteria. None of 120 cases with PCT<0.6ng/ml in cord blood developed EONS (100% negative predictive value). On the other hand, of the 16 cases with PCT ≥0.6ng/ml, 10 were proven or probably infected (62.5% positive predictive value). The sensitivity of the PCT against infection was 100%, with a specificity of 95.2% (area under the receiver operator curve 0.969). The incidence of infection in the study group was 7.4%, and 26.1% in cases with maternal chorioamnionitis. 21 newborn (15.4%) received antibiotic therapy.
The studied protocol has shown to be effective and safe to differentiate between patients with increased risk of developing an EONS, in those where the diagnostic and therapeutic approach was more interventionist, versus those with less likelihood of sepsis, who would benefit from a more conservative management.
La incidencia de sepsis neonatal precoz (SNP) ha disminuido drásticamente desde la utilización de profilaxis antibiótica materna1. Sin embargo, el recién nacido (RN) con factores de riesgo infeccioso continúa siendo motivo de ingreso frecuente en las Unidades Neonatales, ya que, para disminuir la morbimortalidad en la SNP, es imprescindible un diagnóstico precoz2.
Todavía no existe un patrón diagnóstico definido para esta situación. Los síntomas clínicos son sutiles e inespecíficos y se producen de forma tardía, por lo que es necesario el diagnóstico presintomático. Este se basa en la identificación de RN con riesgo de sepsis precoz, por factores que no son sensibles ni específicos2–4, y en determinaciones analíticas, que resultan dolorosas, anemizantes y costosas, especialmente lesivas para el pretérmino5–7. La utilización de test diagnósticos no es sistemática ni decisiva y conlleva la realización de pruebas seriadas, que incluyen hemograma con recuento leucocitario, hemocultivo y determinaciones de reactantes de fase aguda, especialmente PCR cuya elevación en la sepsis se produce pasadas las 6-12 h de vida3,5,6. Se han estudiado otros mediadores de inflamación (interleuquina IL-6, IL-8, IL-1 y TNF-α) con resultados variables y poco aplicables en la práctica clínica8–12.
La única forma de diagnóstico definitivo es el hallazgo de un cultivo central positivo. Este patrón de referencia no es óptimo por su baja rentabilidad en periodo neonatal, debida a varios factores: escaso volumen de muestra, bacteriemia intermitente, antibioterapia materna intraparto5…y por la demora en la obtención de resultados, que obliga en muchos casos al tratamiento antibiótico empírico de pacientes no infectados6,13.
La procalcitonina (PCT) es una prohormona secretada en la mayoría de los tejidos parenquimatosos. Como marcador inflamatorio ha sido estudiada en adultos y niños10–14. Se eleva de forma fisiológica en RN sanos los primeros días de vida, con un pico máximo a las 24h, siendo esta elevación mayor, más precoz y más prolongada en los RN prematuros14–16. Su utilidad en el diagnóstico de las infecciones neonatales ha sido demostrada en revisiones sistemáticas, aunque las variaciones fisiológicas durante las primeras horas de vida hacen difícil su interpretación como marcador de SNP16–21. Estudios recientes aportan evidencia de que los niveles de PCT en sangre de cordón, con un punto de corte de 0,6ng/ml, permitirían distinguir precozmente pacientes infectados de los no infectados22,23.
ObjetivoEstudiar la utilidad y seguridad de un protocolo asistencial de valoración de RN con factores de riesgo de SNP, en el que la aproximación diagnóstica y terapéutica inicial se realizaría según los niveles de PCT en sangre de cordón y sintomatología.
Un algoritmo ayudaría al manejo de RN de forma que aquellos con menor riesgo podrían manejarse de forma más conservadora, frente a los pacientes con mayor riesgo infeccioso, en los que la actuación diagnóstica y terapéutica habría de ser más agresiva.
Material y métodosEstudio para valorar un protocolo de actuación clínica. Se realiza la evaluación retrospectiva de la efectividad y seguridad del mismo.
Criterios de inclusión: neonatos nacidos en el Hospital Universitario Príncipe de Asturias de Alcalá de Henares desde el 1 de octubre de 2013 hasta el 31 de enero de 2015, a los que se realizó determinación de PCT en sangre de cordón por los factores de riesgo de SNP que se detallan a continuación:
- a)
Sospecha clínica de corioamnionitis materna, diagnosticada según los criterios de Gibbs24 por fiebre materna intraparto >38° y dos o más de los siguientes: líquido amniótico maloliente; taquicardia materna (>120 latidos por minuto (lpm)); taquicardia fetal (>160 lpm); leucocitosis materna (leucocitos >15.000/μl) o elevación de PCR materna, dolor pélvico o hipercontractilidad uterina materna.
- b)
Parto pretérmino de inicio espontáneo antes de la 34.ª semana de gestación.
- c)
Parto con al menos 2 factores de riesgo de los siguientes: amniorrexis de más de 18 h; edad gestacional (EG) inferior a 37 semanas; colonización materna por estreptococo del grupo B (SGB) desconocida o positiva, con profilaxis incompleta (menos de 4 h, salvo si cesárea con bolsa íntegra y sin trabajo de parto) o fiebre materna intraparto.
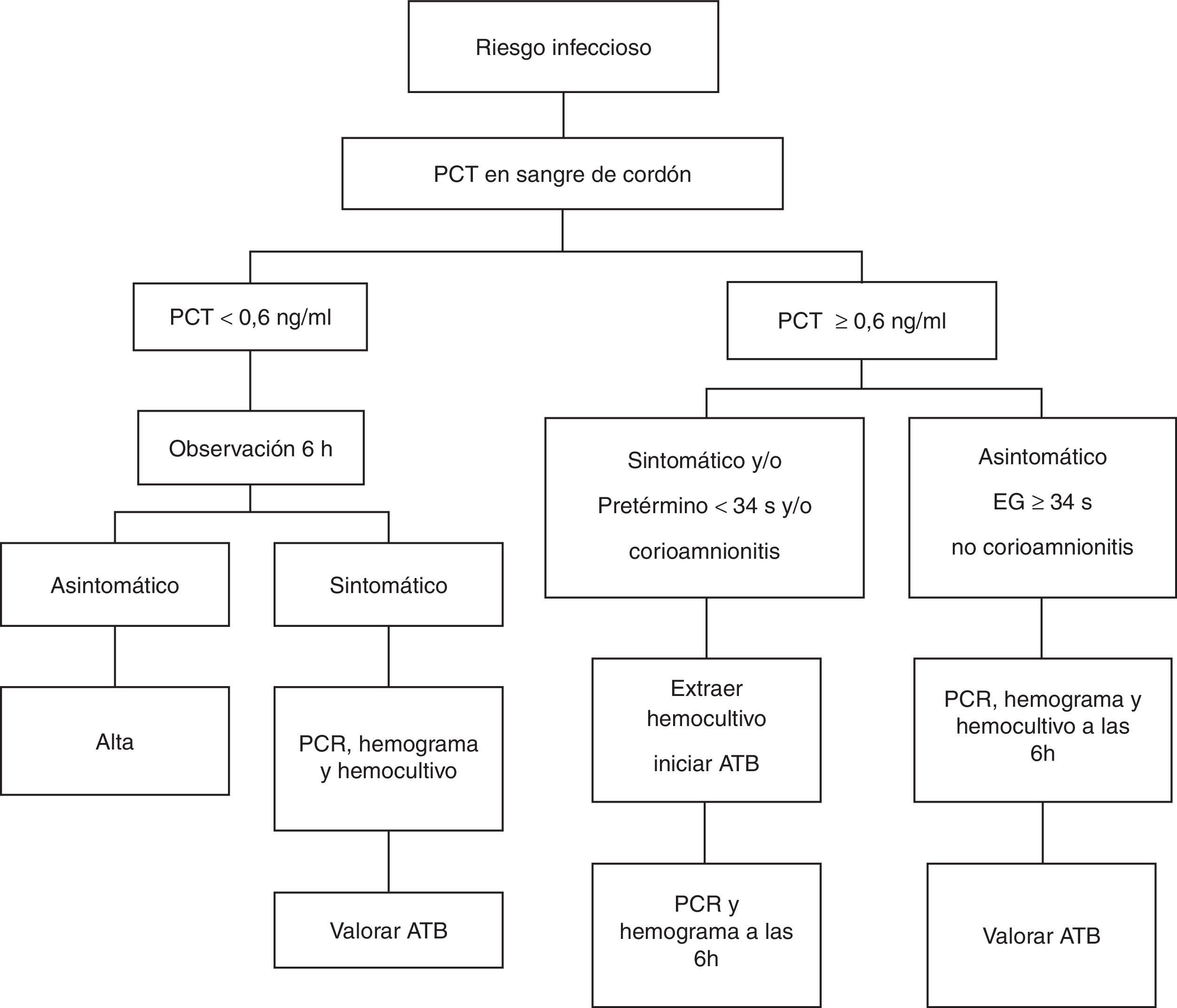
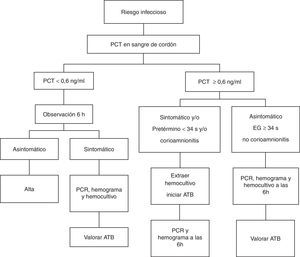
Todos los RN fueron observados clínicamente. Según los valores de PCT en sangre de cordón se procedió según el algoritmo de la figura 1.
Los RN con valores de PCT <0,6ng/ml y asintomáticos se mantuvieron en observación durante un tiempo mínimo de 48h, inicialmente ingresados y posteriormente en la maternidad. Solo se realizó analítica (hemograma con recuento diferencial de leucocitos, PCR, hemocultivo) a aquellos RN con síntomas. Según las alteraciones hematológicas y bioquímicas se valoró el iniciar antibioterapia, así como la realización de otras pruebas diagnósticas (punción lumbar, radiografía de tórax). En los RN con valores de PCT en sangre de cordón ≥0,6ng/ml se realizó a la hora de vida hemocultivo y se inició tratamiento precoz en los siguientes casos: pacientes sintomáticos o pretérminos de EG inferior a 34 semanas o con antecedente de coriamnionitis. Otras determinaciones analíticas (hemograma con recuento y PCR) se realizaron a partir de las 6 h de vida, por ser entonces más valorables8,25–27.
En el resto de RN con PCT ≥0,6ng/ml se realizó analítica a las 6h de vida, siendo individualizada la necesidad o no de antibioterapia. En aquellos pacientes en los que se inició tratamiento se reevaluó la necesidad de continuar con el mismo tras 48-72 h, según evolución clínica y de los parámetros hematológicos y bioquímicos.
A posteriori se clasificó el diagnóstico final según criterios clínicos, biológicos y bacteriológicos, como infección comprobada, probable o no infección.
Se definió como infección comprobada el aislamiento positivo en una muestra central (hemocultivo o cultivo de líquido cefalorraquídeo); como infección probable la alteración de signos biológicos o clínicos posnatales sin otra causa aparente, en al menos dos áreas clínicas (tabla 1) y que hubiera requerido al menos cinco días de antibioterapia. Se clasificaron como no infectados los RN que no presentaron cultivos centrales positivos ni los criterios anteriormente definidos de infección probable.
Signos clínicos o biológicos de infección
| Respiratorio | Taquipnea, apneas, hipoxemia, distrés respiratorio |
| Cardiológico | Taquicardia (≥180 lpm). Episodios de bradicardia (<80 lpm) |
| Hemodinámico | Mala coloración de piel, hipoperfusión periférica, hipotensión en ausencia de hipovolemia |
| Neurológico | Irritabilidad, letargia o hipoactividad |
| Digestivo | Pobre alimentación, intolerancia o distensión abdominal |
| Regulación térmica | Fiebre (>38°C), hipotermia (<36°C) |
| Metabólico | Acidosis metabólica (exceso de bases<-10). Hiperglucemia (>140mg/dl) |
| Alteración hematológica | Leucopenia (<5.000 leucocitos/μl) o neutropenia (<2.000 neutrófilos/μl) Índice de neutrófilos inmaduros (INI) >0,2 Trombocitopenia (<100.000 plaquetas/μl) |
| Aumento de reactantes | Proteína C reactiva PCR>15mg/l (6-12h) o >20mg/l a partir de 24h |
lpm: latidos por minuto.
La determinación de PCT se realizó de forma urgente, obteniéndose el resultado en 20 min. Las muestras fueron analizadas mediante inmunoanálisis por quimioluminiscencia automatizado, con sensibilidad analítica de 0,02ng/ml. Se usó la metodología ADVIA Centaur XP® BRAMHS PCT de Siemens Healthcare Diagnostics. El valor de corte de 0,6ng/ml aplicado en el protocolo se basa en los estudios realizados por Joram et al.22,23. En el estudio estadístico las características se han descrito en porcentajes para variables cualitativas, calculando la precisión por medio del intervalo de confianza (IC) del 95% y en porcentajes y mediana con desviación estándar para datos cuantitativos.
Se obtuvieron las curvas características operativas del receptor para niveles de PCT, así como el índice de Youden, mediante el programa MedCalc y se determinaron los puntos de corte, así como la sensibilidad, la especificidad y valores predictivos, con los correspondientes IC. Se utilizó la calculadora Excel para pruebas diagnósticas de la red CASPe (URL: http://www.redcaspe.org). Se analizaron los resultados agrupando casos de infección confirmada y probable. La probabilidad posprueba positiva se halló por el teorema de Bayes.
ResultadosDescripción de la población. De un total de 2.519 nacimientos en nuestro hospital en el periodo de estudio, 153 RN (6%) presentaron los factores de riesgo infeccioso descritos. Fueron excluidos 17 por no haber seguido correctamente el protocolo. La población de estudio la constituyen 136 RN con factores de riesgo infeccioso para SNP, que cumplieron criterios de inclusión y en los que se aplicó correctamente el protocolo.
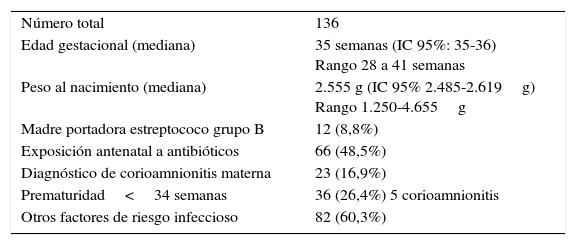
Las características de la población se resumen en la tabla 2.
Características de la población de estudio
| Número total | 136 |
| Edad gestacional (mediana) | 35 semanas (IC 95%: 35-36) Rango 28 a 41 semanas |
| Peso al nacimiento (mediana) | 2.555 g (IC 95% 2.485-2.619g) Rango 1.250-4.655g |
| Madre portadora estreptococo grupo B | 12 (8,8%) |
| Exposición antenatal a antibióticos | 66 (48,5%) |
| Diagnóstico de corioamnionitis materna | 23 (16,9%) |
| Prematuridad<34 semanas | 36 (26,4%) 5 corioamnionitis |
| Otros factores de riesgo infeccioso | 82 (60,3%) |
Variables expresadas en mediana con intervalo de confianza para el 95% (IC 95%), número total y porcentaje.
La colonización materna para SGB fue positiva en 12 casos; negativa en 52 y desconocida en el momento del parto en 72. El 30% de las madres con corioamnionitis eran portadoras de SGB.
Recibieron profilaxis antibiótica materna 66 casos: 16 de 23 casos con sospecha materna de corioamnionitis (de los que 5 eran también <34 semanas); 20 de 36 casos de pretérmino de EG<34 semanas y 35 casos del resto de RN de riesgo.
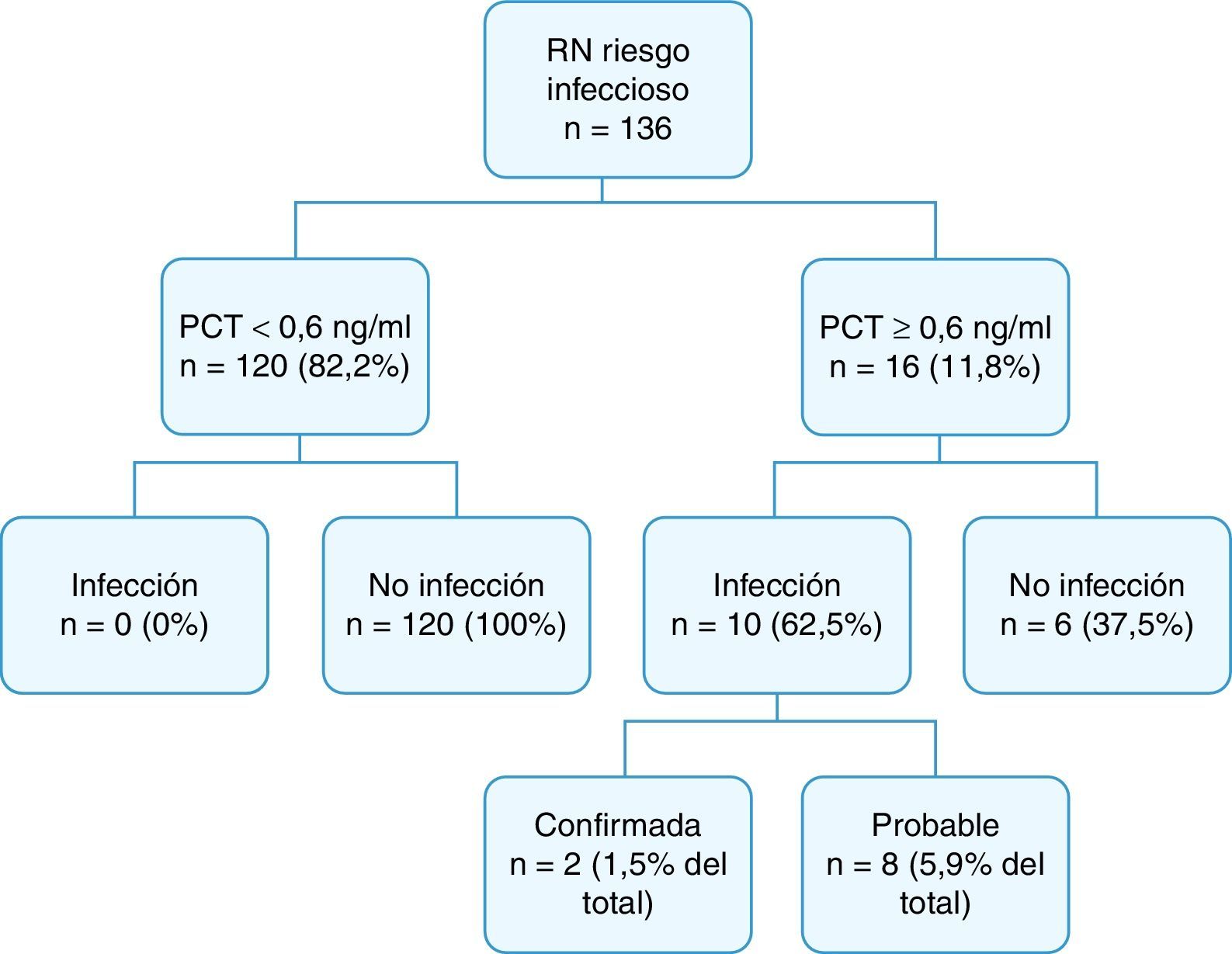
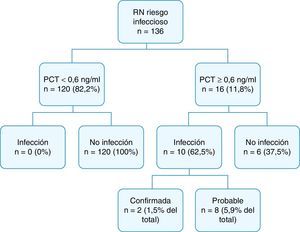
Los resultados diagnósticos finales del estudio se recogen en la figura 2.
En 120 RN (82,2%) la PCT en sangre de cordón fue <0,6ng/ml, de los cuales ninguno desarrolló una sepsis. En 16 casos (11,8%) la PCT en sangre de cordón fue ≥0,6ng/ml. Diez de ellos presentaron infección: confirmada (2 casos) o probable (8 casos). La incidencia global de infección en nuestro estudio fue de 7,4% (de infección comprobada el 1,5% y de infección probable el 5,9%). De 16 casos con PCT positiva 9 (56,2%) eran hijos de madre con corioamnionitis; 6 de ellos (37,5%) infectados.
Entre los RN infectados solo en un caso la madre era portadora de SGB.
Recibieron antibioterapia 21 RN (15,4%): 7 casos (5,8%) de entre los 120 con PCT <0,6ng/ml y 14 (87,5%) de los 16 RN con PCT ≥0,6ng/ml. Ninguno de los RN con PCT<0,6ng/ml en los que se inició tratamiento antibiótico fue diagnosticado a posteriori como infección confirmada ni probable por no cumplir criterios para ello. La mayoría (85,7%) fueron prematuros (5 menores de 34 semanas) con distrés respiratorio, secundario en 2 casos a enfermedad de membrana hialina y en 4 a taquipnea transitoria; además de un RN a término con síndrome de aspiración meconial. En todos se suspendió la antibioterapia antes de 4 días. De los 6 casos considerados falsos positivos (con PCT ≥0,6ng/ml pero no infectados) 4 fueron tratados: 3 hijos de madre con corioamnionitis y un pretérmino de 29 semanas.
En veintitrés casos (16,9%) existía antecedente de corioamnionitis materna. Once (48%) recibieron antibioterapia posnatal (6 con diagnóstico final de infección y 5 menores de 34 semanas).
Por el contrario ninguno de los 36 RN de EG inferior a 34 semanas (26% de la muestra) fue diagnosticado finalmente de infección. De ellos habían recibido antibioterapia materna el 56%.
La clasificación diagnóstica final fue la siguiente: dos casos de infección confirmada (uno por Streptococcus pneumoniae y otro por Escherichia coli) y ocho casos de infección probable. La mayoría de los RN (92,6%) fueron clasificados como no infectados. El rango de EG de los infectados fue de 34 a 41 semanas. Siete tenían como antecedente fiebre materna, 6 de ellos hijos de madre con corioamnionitis. Tres tenían cultivos periféricos positivos. El tiempo de antibioterapia en los diagnosticados de infección fue de 6 a 14 días, no observando en ningún caso recurrencia, con mortalidad del 0%.
Evaluación del algoritmo diagnóstico:
No encontramos en nuestra serie ningún falso negativo: de 120 casos con PCT <0,6ng/ml ninguno desarrolló SNP (valor predictivo negativo 100%; IC 95%: 96,9-100%). No se produjo ningún reingreso por infección.
Por el contrario, de los 16 casos con PCT ≥0,6ng/ml, diez fueron diagnosticados de infección comprobada o probable (valor predictivo positivo 62,5% con IC 95%: 38,6-81,5%), siendo los 6 restantes falsos positivos (4,8%).
En los RN con antecedente de corioamnionitis materna la incidencia de infección (probabilidad preprueba) fue de 26,1%, siendo la probabilidad posprueba positiva, por el teorema de Bayes de 88,1% (IC 95% 64,7-96,8%).
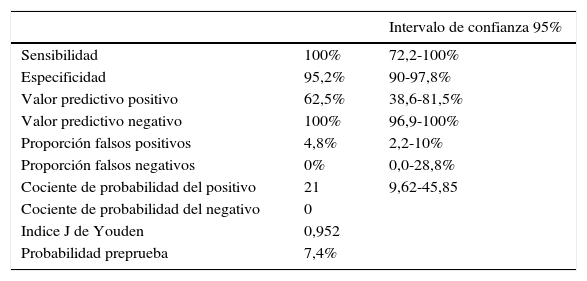
La tabla 3 muestra los parámetros de eficacia diagnóstica de la PCT en sangre de cordón frente a infección para un punto de corte ≥ 0,6ng/ml.
Parámetros de eficacia diagnóstica de la procalcitonina en sangre de cordón en el diagnóstico de infección neonatal precoz para un punto de corte ≥ 0,6 ng/ml
| Intervalo de confianza 95% | ||
|---|---|---|
| Sensibilidad | 100% | 72,2-100% |
| Especificidad | 95,2% | 90-97,8% |
| Valor predictivo positivo | 62,5% | 38,6-81,5% |
| Valor predictivo negativo | 100% | 96,9-100% |
| Proporción falsos positivos | 4,8% | 2,2-10% |
| Proporción falsos negativos | 0% | 0,0-28,8% |
| Cociente de probabilidad del positivo | 21 | 9,62-45,85 |
| Cociente de probabilidad del negativo | 0 | |
| Indice J de Youden | 0,952 | |
| Probabilidad preprueba | 7,4% |
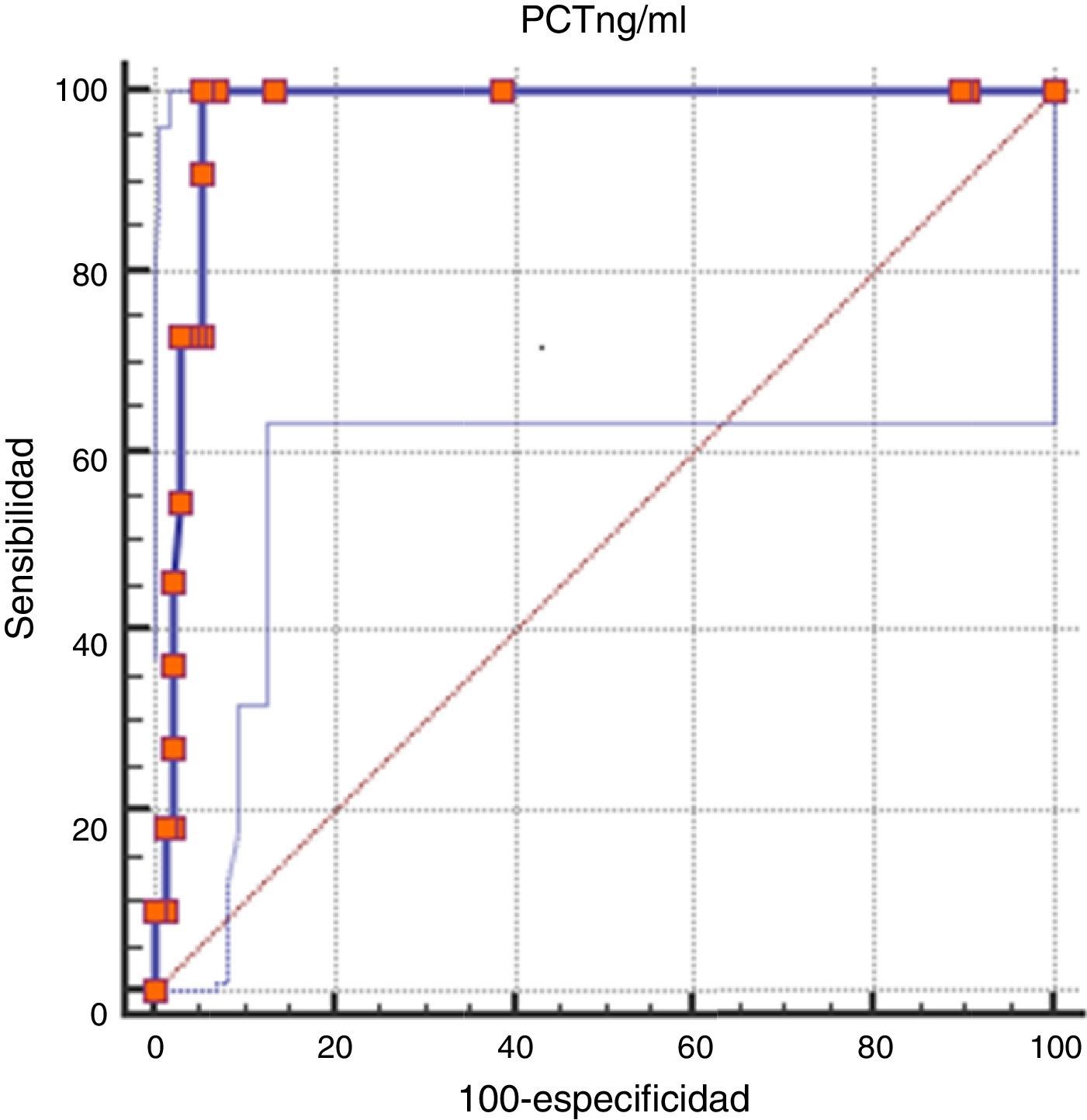
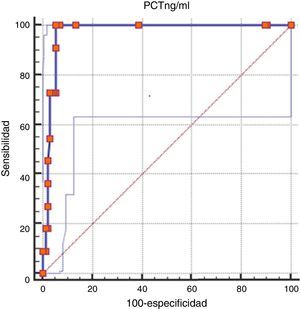
El área bajo la curva operador receptor fue 0,978 (IC 95%: 0,94-0,99). El índice de Youden para ese punto de corte fue de 0,952 (fig. 3).
Durante el periodo de estudio se diagnosticaron otros 3 casos de SNP en nuestra Unidad, no incluidos en el protocolo por no cumplir criterios. En dos existía como único factor de riesgo la amniorrexis de más de 24 h y en el otro antecedente de bacteriuria materna. El total de sepsis estimada de la población neonatal atendida en nuestro hospital en el periodo del estudio fue de 5,2 ‰.
DiscusiónCuando se evalúa un protocolo diagnóstico para SNP la primera dificultad es la ausencia de un patrón de referencia adecuado. La clasificación de casos como infección comprobada es clara. Para el diagnóstico de infección probable hemos adaptado un baremo clínico analítico similar al empleado por otros autores3,4,8,11,17–21. En esta situación compleja por la falta de especificidad de la clínica y el resultado poco rentable y diferido de los cultivos centrales, un protocolo del manejo inicial debería discriminar precozmente entre pacientes infectados y no infectados.
Por la baja incidencia de la SNP y por la gravedad de la misma es imprescindible, en la selección de la prueba diagnóstica, que esta nos aporte la seguridad de detectar los casos infectados (alta sensibilidad) permitiendo descartar infección cuando no la haya (alto valor predictivo negativo)16–18,21.
En numerosos trabajos se demuestra la utilidad de la PCT para el diagnóstico de sepsis neonatal, con valores de sensibilidad y especificidad de 81 y 79%20. Sin embargo, la gran variabilidad, en función de la EG y sobre todo de las horas de vida, ha interferido hasta ahora con la aplicación clínica en el diagnóstico precoz de la SNP14–21, en el que la precocidad y fiabilidad diagnóstica son irrenunciables. Este inconveniente desaparece si se evalúan los niveles de PCT en sangre de cordón. Joram et al. encuentran valores muy elevados de sensibilidad y especificidad, junto con un valor predictivo negativo del 99% para un punto de corte de 0,6ng/ml. La PCT en sangre de cordón puede ser clave en el diagnóstico precoz de la SNP22,25. En nuestro trabajo hemos estudiado la aplicación clínica de estos hallazgos, encontrando resultados similares e incluso mejores que los de estos autores, tanto en sensibilidad (100%), especificidad (95,2%), valor predictivo negativo (100%) y valor predictivo positivo (62,5%). El espectro de pacientes de nuestra muestra, seleccionada por factores de riesgo infeccioso conocidos para la etapa neonatal inmediata1–4, es adecuado, ya que la probabilidad preprueba de infección en la misma fue de 7,4%. Por otra parte no hemos observado ningún falso negativo. Un estudio similar de reciente publicación obtiene resultados parecidos, aunque la selección de muestra es menos estricta27. Estudios con otros marcadores en sangre de cordón obtienen peores resultados en sensibilidad y especificidad28–30.
La ventaja de la aplicación en la clínica de un protocolo que distinga, dentro de los pacientes con riesgo infeccioso, aquellos que puedan manejarse de forma conservadora es evidente, puesto que la mayor parte de esta población de RN de riesgo no va a presentar una sepsis. En nuestro estudio el 92,6% de los RN con factores de riesgo de SNP no fueron diagnosticados finalmente de infección.
Por otro lado, el identificar al nacimiento qué pacientes van a tener mayor probabilidad de sepsis implica el inicio muy precoz de antibioterapia en los infectados, lo que evitaría la progresión de la infección, disminuyendo el tiempo de tratamiento. En nuestro estudio todos los RN con diagnóstico final de infección recibieron antibioterapia desde la primera hora de vida.
En la balanza entre tratamiento precoz frente a tratamiento innecesario, la determinación de PCT en sangre de cordón disminuye el número de RN sometidos a tratamiento antibiótico empírico. Es bien conocido que la antibioterapia de amplio espectro en la etapa neonatal puede ocasionar efectos adversos sobre la microbiota intestinal, en la maduración del sistema inmune, riesgo de alergias, de sepsis tardía, resistencias bacterianas e infección nosocomial, así como de enterocolitis necrotizante31–34; todos ellos efectos yatrógenos no desdeñables.
Los síntomas iniciales de SNP son inespecíficos y pueden solaparse con patologías no infecciosas propias de la adaptación a la vida extrauterina. En RN con PCT <0,6ng/ml el protocolo permite valorar el inicio de antibioterapia de forma individualizada, de manera que un pequeño porcentaje de estos RN (5,8%) recibió antibiótico al nacimiento, la mayoría pretérminos con dificultad respiratoria atribuible a otra causa. Evolutivamente ninguno de ellos cumplió criterios clínicos ni analíticos para poder ser clasificados finalmente como infección probable ni confirmada. En nuestro estudio no hemos encontrado ningún falso negativo, pero el tamaño muestral es pequeño, lo cual, junto con la baja incidencia de SNP probada, limita el poder del mismo. Sería interesante realizar estudios más amplios multicéntricos y prospectivos con el objeto de validar estos resultados, lo que permitiría evitar en un mayor número de casos la antibioterapia inicial en el RN pretérmino con PCT <0,6ng/ml.
La rentabilidad de la prueba es mayor en los hijos de madre con corioamnionitis, en los que la probabilidad posprueba positiva fue del 88,1%. Recibieron antibioterapia empírica un 48% de estos RN, frente a recomendaciones que preconizan tratamiento antibiótico en todos los RN de madre con corioamnionitis3,34.
El valor predictivo positivo fue en nuestro estudio del 62,5%, que implica una proporción baja de tratamientos antibióticos innecesarios. Podría postularse que la precocidad de la antibioterapia evitaría el desarrollo de síntomas y alteraciones analíticas en pacientes que, si no hubieran sido tratados, habrían desarrollado una sepsis clínicamente significativa, lo que influiría en el valor predictivo de la prueba. Pero este es un sesgo difícilmente evitable. Llama la atención el que ninguno de los RNPT de EG <34 semanas fuera diagnosticado finalmente de infección en nuestra serie; esto podría relacionarse con la alta proporción de ellos con antibioterapia materna previa al parto (56%). Asimismo podría deducirse que, actualmente, la causa infecciosa ha perdido peso entre los factores desencadenantes del parto pretérmino.
En la práctica clínica hemos observado que la determinación de PCT en sangre de cordón ha disminuido el número de pruebas analíticas y de pacientes sometidos a tratamiento antibiótico, ha identificado precozmente a los infectados y, al discriminar entre RN con mayor o menor riesgo, ha permitido la disminución del tiempo de ingreso para observación en estos últimos, favoreciendo el establecimiento del vínculo maternofilial y de la lactancia materna.
ConclusionesLa determinación de PCT en sangre de cordón ha demostrado utilidad y fiabilidad en la valoración de los RN con riesgo de SNP, con una muy alta sensibilidad y especificidad. El protocolo de decisión clínica estudiado, con limitaciones por la incidencia de SNP y tamaño muestral, ha confirmado ser efectivo y seguro para discriminar entre pacientes con un mayor riesgo, en los que la aproximación diagnóstica y terapéutica fue más intervencionista, frente a aquellos con menor probabilidad de sepsis, la mayoría, que se beneficiaron de un manejo más conservador, con una disminución de pruebas complementarias, exposición innecesaria a antibióticos, así como del tiempo de ingreso.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Presentada Comunicación con opción a premio en el XXV Congreso de Neonatología y Medicina Perinatal. Sevilla, mayo 2015.