Como han expuesto Manuel Sánchez Luna et al., la pulsioximetría es un método eficaz, no invasivo, de bajo coste y bien tolerado para la detección de cardiopatías congénitas1. No obstante, cuando el cribado es positivo también hay que considerar la posible presencia de hemoglobinopatías, ya que estas pueden causar hipoxia en ausencia de cualquier otra alteración clínica o analítica2.
Presentamos el caso clínico de un neonato que, en su día 2 de vida, durante el cribado de cardiopatías congénitas, presentó una saturación periférica (SpO2) que oscilaba entre el 85 y el 90%. La SpO2 no aumentó con la administración de oxígeno al 100%, mientras que el paciente no mostraba signos de dificultad respiratoria o enfermedad cardiovascular. La investigación inicial incluyó hemograma, proteína C-reactiva, hemocultivo, panel metabólico y radiografía de tórax, con resultados negativos o normales en todas las pruebas. El electrocardiograma y el ecocardiograma 2D no detectaron signos de alteraciones del ritmo cardíaco, hipertensión pulmonar o cardiopatía estructural. Durante la estancia, el paciente continuó mostrando valores bajos de SpO2 (SpO2: 83-86%) medidos por pulsioximetría, a pesar de que los resultados de gasometrías repetidas fueron normales (PaO2: 90-140mm; SaO2: 97-99%). La persistencia de dicha discrepancia llevó a la sospecha de una posible hemoglobinopatía. Se realizó secuenciación por PCR en el neonato, identificándose una mutación en heterocigosis en el exón 2 del gen HBG1 que codifica la subunidad 1 de la cadena γ (γ1-globina), c.202G>A (pVal68Met), asociada a un polimorfismo compatible con hemoglobina fetal (HbF)-Sardinia en homocigosis. Esta «falsa hipoxia» persistió hasta que el paciente cumplió 1,5-2 meses de edad.
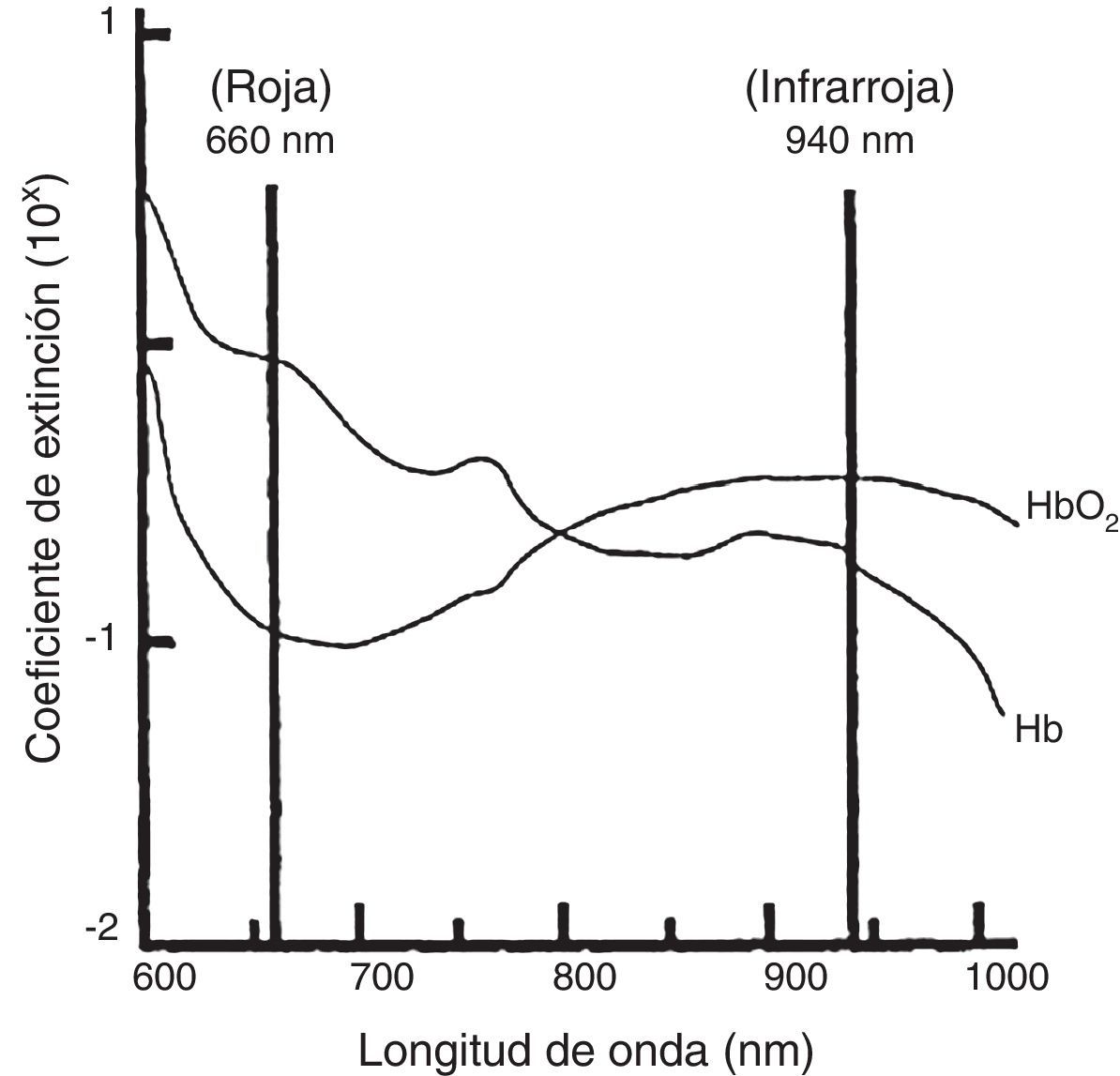
La pulsioximetría emplea solo 2 longitudes de onda para calcular los valores de saturación de la hemoglobina: 940nm (hemoglobina oxigenada) y 660nm (hemoglobina desoxigenada) (fig. 1), de modo que la presencia de una variante de HbF con un espectro de absorción alterado puede dar lugar a lecturas incorrectas de SpO23. Por fortuna, el patrón de oro diagnóstico, la cooximetría, emplea longitudes de onda adicionales y puede detectar la mayoría de estas variantes4.
Extinción de hemoglobina oxigenada y hemoglobina desoxigenada en adultos con valores normales.
Fuente: Sinex3.
La mutación Val68Met en la γ1-globina de la HbF fue descrita por primera vez muy recientemente, en 2015, y su prevalencia aún se desconoce2. La HbF-Sardinia es un polimorfismo frecuente sin alteraciones funcionales o clínicas conocidas4. Hasta donde sabemos, esta es la segunda vez que se detecta la mutación Val68Met en la γ1-globina y la primera que se describe en asociación con la HbF-Sardinia.
Al nacer, la HbF representa del 70 al 80% de la hemoglobina circulante, con una transición progresiva a los tetrámeros del adulto, en su forma predominante (HbA) y minoritaria (HbA2). A los 6 meses la HbF representa menos del 4-5% del total2. La mutación encontrada en nuestro paciente afectaba al gen de la γ-globina, de manera que solo afectaba a la conformación de la hemoglobina fetal, impidiendo su detección por pulsioximetría. Esto explica la normalización de los valores de SpO2 a los 2 meses de edad, coincidiendo con el descenso fisiológico de la HbF.
En este caso en particular, el valor anormalmente bajo de la SpO2 en un neonato sin manifestaciones clínicas probablemente no se hubiera detectado de no haber efectuado el cribado de cardiopatías congénitas de manera rutinaria. La utilidad de dicho cribado es innegable, ya que permite la detección temprana de enfermedades potencialmente fatales1, pero su uso generalizado puede dar lugar a falsos positivos conducentes a su vez a investigaciones extensas que suponen una carga para la familia y los sistemas de salud. Por lo tanto, sería aconsejable considerar la posibilidad de una alteración de la hemoglobina en pacientes con lecturas bajas de SpO2 en ausencia de otras manifestaciones clínicas.