Evaluar la correlación entre hallazgos de la ecografía pulmonar realizada precozmente con las escalas de gravedad clínica y su asociación con la evolución posterior en la bronquiolitis aguda (BA) leve-moderada.
Pacientes y métodosEstudio observacional prospectivo. Se incluyó a lactantes con BA leve-moderada evaluados mediante ecografía pulmonar en las primeras 24 h tras la atención hospitalaria. Se graduó la afectación pulmonar (rango 0-50 puntos) sobre la base de un score ecográfico (ScECO). Se evaluó la correlación entre el ScECO y 2escalas clínicas de uso habitual: escala de Wood Downes Ferres modificada (WDFM) y escala del Hospital Sant Joan de Déu (HSJD). Así mismo se valoró la asociación entre el ScECO y la evolución clínica posterior (ingreso en la Unidad de Cuidados Intensivos Pediátricos [UCIP], días de hospitalización y días de oxigenoterapia).
ResultadosSe incluyó a 59 pacientes con una edad mediana de 90 días (RIQ: 30-270 días). La puntuación mediana del ScECO fue de 6 puntos (2-8) en los pacientes que no requirieron ingreso, 9 (5-13,7) en los ingresados en planta y 17 (14,5-18) en los pacientes que precisaron traslado de planta a la UCIP (p=0,001). El ScECO tuvo una correlación lineal moderada con la escala de WDFM (rho=0,504, p<0,001) y HSJD (rho=0,518; p <0,001). El ScECO se asoció al ingreso en UCIP (OR 2,5 [IC del 95%: 1,1-5,9]; p=0,035), mayor estancia hospitalaria (1,2 días [IC del 95%: 0,55, 1,86]; p=0,001) y duración de oxigenoterapia (0,87 días [IC del 95%: 0,26, 1,48]; p=0,006).
ConclusionesLa ecografía pulmonar precoz se correlaciona de forma moderada con la gravedad de la BA evaluada por escalas clínicas y guarda cierta relación con la evolución clínica.
To determine the correlation between the findings seen in early lung ultrasound with the clinical severity scales, and its association with the subsequent progression of the mild-moderate acute bronchiolitis (AB).
Patients and methodsAn observational prospective study conducted on infants with mild-moderate BA, using lung ultrasound in the first 24hours of hospital care. The lung involvement was graded (range 0-50 points) based on an ultrasound score (ScECO) and 2routinely used clinical scales: the modified Wood Downes Ferres (WDFM), and the Hospital Sant Joan de Deu (HSJD). The relationship between the ScECO and the subsequent clinical progression (admission to the Paediatric Intensive Care Unit (PICU), days in hospital, and days of oxygen therapy), was also determined.
ResultsThe study included a total of 59 patients, with a median age of 90 days (IQR: 30-270 days). The median ScECO score was 6 points (2-8) in the patients that did not require hospital admission, with 9 points (5-13.7) admitted to the ward, and 17 (14.5-18) in the patients who needed to be transferred from the ward to the PICU (P=.001). The ScECO had a moderate lineal association with the WDFM scale (rho=0.504, P<.001) and the HSJD (rho=0.518; P<.001). The ScECO was associated with admission to PICU [OR 2.5 (95% CI: 1.1-5.9); P=.035], longer hospital stay [1.2 days 95% CI: 0.55-1.86); P=.001] and duration of oxygen therapy [0.87 days (95% CI: 0.26-1.48); P=.006].
ConclusionsThere is a moderate correlation between early lung ultrasound findings with the severity of the AB evaluated by the clinical scales, as well as some relationship with the clinical progression.
La bronquiolitis aguda (BA) es la causa más frecuente de hospitalización en lactantes, suponiendo una importante demanda asistencial y una considerable carga económica. Aunque la mayoría de las BA sigue un curso benigno, un grupo de pacientes tiene una evolución desfavorable precisando ingreso en Unidad de Cuidados Intensivos Pediátricos (UCIP), soporte ventilatorio y considerable morbimortalidad. Muchas veces es difícil predecir qué pacientes evolucionarán desfavorablemente, lo que obliga a mantener una observación hospitalaria prolongada en determinados grupos de riesgo. Las escalas clínicas de gravedad se utilizan frecuentemente, siendo útiles para valorar de forma objetiva y reproducible la evolución clínica y la respuesta al tratamiento. No obstante, su utilidad para predecir la evolución en los casos de BA leve-moderada no está demostrada1-3. El poder disponer de una herramienta a pie de cama que nos permita anticipar qué pacientes pueden seguir un curso desfavorable sería muy útil a efectos de evitar eventos adversos, intensificar la monitorización y adecuar la gestión de recursos disponibles (traslado a centros con UCIP, inicio precoz del soporte respiratorio, etc.).
La ecografía pulmonar permite evaluar la extensión de afectación pleuro-pulmonar a pie de cama, de forma dinámica y sin efectos adversos. Se ha demostrado su utilidad y en muchos casos su superioridad a la radiografía de tórax en el diagnóstico de la taquipnea transitoria del recién nacido, el síndrome de distrés respiratorio agudo (SDRA), la neumonía, el derrame pleural o el neumotórax4-11. Pese a la evidencia acumulada en otras enfermedades pulmonares agudas, apenas existen estudios que hayan evaluado la utilidad de la ecografía pulmonar en la BA. Hasta ahora los estudios realizados coinciden en que la extensión de las anomalías pulmonares guarda relación con la gravedad clínica de la BA12-14. Podría pensarse que la extensión de la afectación pulmonar puede tener valor para predecir la evolución clínica de la BA como sucede en otras enfermedades, como el SDRA, donde ha demostrado su capacidad predictiva en la mortalidad o la respuesta a tratamientos como la ventilación en prono o maniobras de reclutamiento alveolar15-20. Sin embargo, ningún estudio ha evaluado la capacidad de la ecografía pulmonar realizada precozmente para predecir la evolución de la BA.
Nuestro estudio tiene 2objetivos principales: por un lado, evaluar la relación entre la ecografía pulmonar y la gravedad en la BA leve-moderada indicada por 2 escalas de valoración clínica utilizadas en nuestro medio, y por otro analizar si la ecografía pulmonar realizada precozmente guarda relación con la evolución clínica en pacientes que se presentan en el hospital con diagnóstico de BA leve-moderada.
Pacientes y métodosPoblaciónEstudio observacional prospectivo de octubre del 2016 a marzo del 2017. Se definió BA como un episodio de dificultad respiratoria dominado por signos de afectación de las vías respiratorias bajas (sibilancias, estertores) tras una infección de vías respiratorias altas en lactantes menores de un año, independientemente de que se tratara del primer episodio1,2. Se incluyó a pacientes con diagnóstico clínico de BA leve-moderada menores de un año atendidos en nuestro centro, siempre y cuando la realización de la ecografía pulmonar a cargo de los investigadores estuviera disponible en las primeras 24 h de la asistencia. Se excluyó a los pacientes que se presentaron con BA grave en el momento de ser atendidos en el hospital (escala de Wood Downes Ferres modificada [WDFM] > 8 y escala del Hospital Sant Joan de Déu [HSJD] > 10), los que ingresaron en UCIP en las primeras 24 h desde la atención, pacientes con diagnóstico ecográfico de neumonía, cardiopatías congénitas con repercusión hemodinámica y prematuros con antecedente de broncodisplasia, cuyos hallazgos ecográficos son muy similares en la BA.
MedidasSe recogieron los datos demográficos y clínicos de los pacientes a su llegada al hospital. La valoración clínica del paciente incluyó la toma de constantes vitales, saturación de oxígeno y el cálculo de 2escalas clínicas de uso común en nuestro medio (WDFM y HSJD) por parte del médico responsable21,22. Se siguió la evolución de los pacientes en el siguiente mes a su consulta (reasistencia a Urgencias, necesidad de ingreso o complicaciones posteriores precoces), mediante revisión de la historia electrónica y contacto telefónico. Los pacientes ingresados se siguieron hasta el alta recogiéndose los tratamientos recibidos y su evolución clínica. Las variables principales de estudio fueron necesidad de ingreso en UCIP, ventilación mecánica invasiva, días de hospitalización y duración de oxigenoterapia. El criterio de ingreso general en UCIP fue el desarrollo de dificultad respiratoria grave según escalas clínicas. Otras circunstancias consideradas como indicación de traslado a UCIP fueron la presencia de apneas, hipoxemia significativa (necesidad de oxígeno suplementario a concentración mayor del 50% para saturación mayor del 90%) o hipercapnia.
Ecografía pulmonarSe realizó una ecografía pulmonar, según el protocolo diseñado, a todos los participantes dentro de las primeras 24 h desde su asistencia al hospital.
Se utilizó un ecógrafo portátil (Sonosite Turbo M, Fujifilm, Japón) con una sonda lineal de 6-13 MHZ en todos los pacientes. Las ecografías fueron realizadas e interpretadas por 2pediatras residentes (observador A y observador B) con experiencia previa en ecografía pulmonar. Dichos residentes habían realizado más de 25 ecografías pulmonares en su práctica clínica (fundamentalmente para diagnóstico de neumonía y sus complicaciones). Fueron específicamente entrenados para el estudio mediante 2 sesiones teórico-prácticas de 2 h de duración con revisión y comentario de los hallazgos ecográficos en BA y la realización de al menos 10 ecografías pulmonares supervisadas en pacientes con BA (no incluidos en el estudio)23-25.
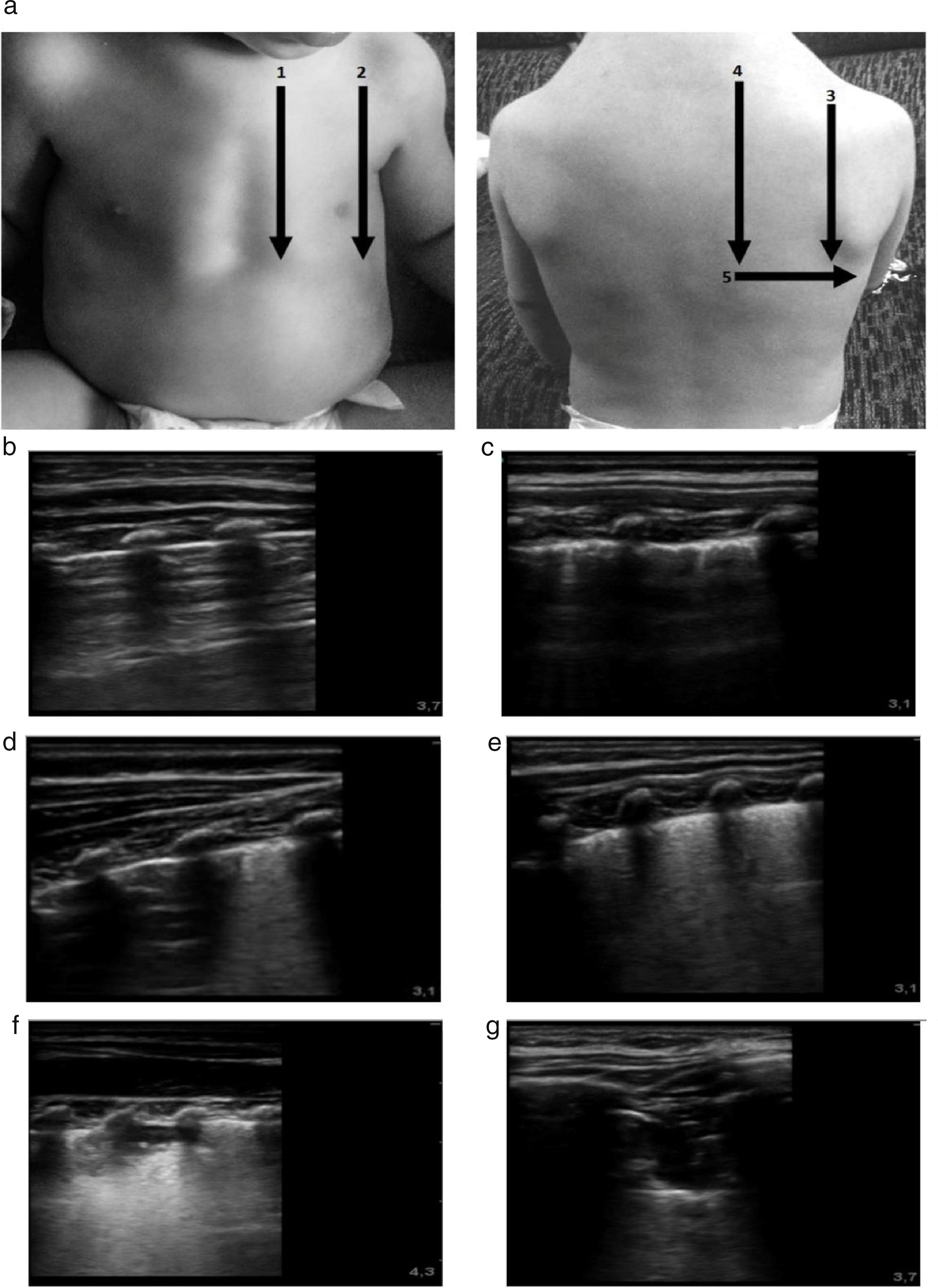
El protocolo de adquisición de imágenes incluyó la evaluación de 10 zonas pulmonares (5 en cada pulmón), obteniendo un vídeo de 10 s de duración en cada zona (fig. 1). Todas las imágenes se archivaron en soporte digital para su análisis posterior. Las imágenes se analizaron en orden aleatorio y sin disponer de los datos clínicos del paciente para asegurar una valoración objetiva y ciega. En cada zona pulmonar se valoraron 3 componentes diferentes de la enfermedad pulmonar en la BA: anomalías de la línea pleural (AP), extensión del síndrome intersticial (SI) y presencia de consolidaciones subpleurales (CS). Las AP valoradas fueron engrosamiento o pérdida del deslizamiento pleural normal; se puntuó como 0 (ausencia de cualquier anomalía) y 1 punto (presencia de cualquier anomalía) para una puntuación máxima de 10 puntos. La presencia de SI se puntuó 0 (patrón normal con predominio de líneas A), 1 (SI con líneas B confluentes definidas como 3 o más líneas B por espacio intercostal o aspecto de pulmón blanco en 1 espacio intercostal) o 2 (SI con líneas B confluentes definidas como 3 o más líneas B por espacio intercostal o aspecto de pulmón blanco en 2 espacios intercostales adyacentes) para una puntuación máxima de 20 puntos. Las CS se puntuaron 0 (ausentes), 1 (una consolidación <1cm) y 2 (consolidaciones >1cm o CS múltiples) para una puntuación máxima de 20 puntos. El score global (ScECO) se calculó como la suma de las puntuaciones de cada zona individual. Así la puntuación máxima posible fue 50 (rango 0-50) (fig. 1).
a) Protocolo de adquisición e interpretación de la ecografía pulmonar. Las áreas exploradas se señalan con números. La puntuación de la ecografía se indica en las imágenes identificadas con letras. En las imágenes se muestra la puntuación asignada a cada anomalía detectada. b) Pulmón normal: 0 puntos. c) Engrosamiento pleural. Puntuación SCORE: 1 punto. d) SI focal. Puntuación SCORE: 1 punto. e) SI difuso. Puntuación SCORE: 2 puntos. f) CS < 1cm. Puntuación SCORE: 1 punto. g) CS > 1cm. Puntuación SCORE: 2 puntos.
CS: consolidaciones subpleurales; SI, síndrome intersticial; 1: área anterior paraesternal; 2: área anterior axilar anterior; 3: área posterior línea axilar posterior; 4 área posterior paravertebral; 5: área posterior infraescapular.
Los datos se resumen en mediana (rango intercuartil) y número (porcentaje). En un primer análisis se valoró el acuerdo interobservador entre los pediatras formados en ecografía pulmonar con un pediatra con más de 5 años de experiencia en ecografía pulmonar. Se valoró el grado de concordancia en la valoración de AP, SI y presencia y extensión de las CS mediante el análisis de 30 vídeos de 10 s de pacientes con BA seleccionadas al azar. Se utilizó el coeficiente kappa de Cohen para valorar la concordancia, considerándose muy buena si kappa era > 0,8 y buena si kappa era > 0,6 según los límites propuestos por Landi y Koch. Se utilizó el coeficiente de correlación intraclase para valorar el grado de acuerdo absoluto entre los observadores. Posteriormente, se evaluó la asociación entre el ScECO (puntuación global y sus componentes de AP, SI y CS) y los parámetros clínicos de gravedad de BA mediante coeficientes de correlación de Spearman. Finalmente, se investigó mediante regresión multivariante si existía asociación independiente entre el ScECO y la necesidad de ingreso en UCIP, días de hospitalización o duración de la oxigenoterapia. Se consideró estadísticamente significativa una p <0,05. Se utilizó el software SPSS versión 22.0 para el análisis estadístico.
Aspectos éticosEl protocolo del estudio fue evaluado y aprobado por el Comité Ético de Investigación Clínica y los padres o tutores legales dieron su consentimiento informado escrito para la participación en el estudio y la publicación de los resultados.
ResultadosSe incluyó a 59 pacientes con BA leve-moderada con una edad de 90 días (RIQ: 30-270) y un peso de 6,1kg (4,8-7,9). Cuarenta y cuatropacientes precisaron ingreso hospitalario con estancia de 5 días (3-7,5) y 37 (84%) precisaron oxigenoterapia durante 3 (2-6) días. La ecografía pulmonar se realizó en 41 pacientes al ingreso en Planta de Hospitalización y en 18 en el servicio de Urgencias. Cuatro pacientes (6,7%) ingresaron en la UCIP y ninguno necesitó ventilación mecánica invasiva. Las características de los pacientes se resumen en la tabla 1y el anexo 1, material suplementario.
Características de los pacientes
| Características de las BA | |
| Sexo | 37 (62,7) |
| Edad (días) | 90 (30-270) |
| Peso (g) | 6.1 (4,8-7,9) |
| Longitud (cm) | 61 (56-68) |
| Factores de riesgo de BA | 29 (49,2) |
| Tiempo de evolución de los síntomas | 3 (2-4) |
| Gravedad de la BA | |
| Score WDFM | 5 (4-6) |
| a. Leve | 12 (20,3) |
| b. Moderada | 47 (79,7%) |
| Score HSJD | 6 (4-7) |
| a. Leve | 25 (42,4) |
| b. Moderada | 34 (57,6%) |
| Ingreso hospitalario | 44 (74%) |
| Tratamiento intrahospitalario | |
| a. Oxígeno | 37 (84%) |
| b. SSH 3% | 14 (31,8%) |
| c. Broncodilatadores | 4 (9%) |
| d. Broncodilatadores+SSH 3% | 26 (59%) |
| d. Corticoides sistémicos | 4 (9%) |
| e. Antibióticos | 2 (4,5) |
| f. Fluidoterapia intravenosa | 6 (13,6%) |
| Evolución | |
| Días de la oxigenoterapia | 3 (2-6) |
| Días de la hospitalización | 5 (3-7,5) |
| Ingreso en UCIP | 4 (6,7%) |
| Ventilación mecánica invasiva | 0 (0%) |
| Ecografía pulmonar (Score global) | 8 (5-13) |
| Anomalías pleurales (0-10) | 5 (3-6) |
| Síndrome intersticial (0-20) | 2 (0-5) |
| Consolidaciones subpleurales (0-20) | 2 (0-3) |
Factores de riesgo de BA: edad < 6 semanas, prematuridad < 35 semanas, enfermedad cardiorrespiratoria crónica, inmunodeficiencia y ausencia de lactancia materna exclusiva.
La concordancia interobservador entre los pediatras que realizaron e interpretaron los estudios y un pediatra experto en ecografía pulmonar fue muy buena en la valoración de las AP (observador A: kappa 0,851; observador B: kappa 0,841) y el SI (observador A: kappa 0,836; observador B: kappa 0,877) y buena para las CS (observador A: kappa 0,620; observador B: kappa 0,695). El coeficiente de correlación intraclase interobservador (acuerdo absoluto en las medidas individuales) para la puntuación total del ScECO fue 0.917 (IC 95%: 0.854-0.956).
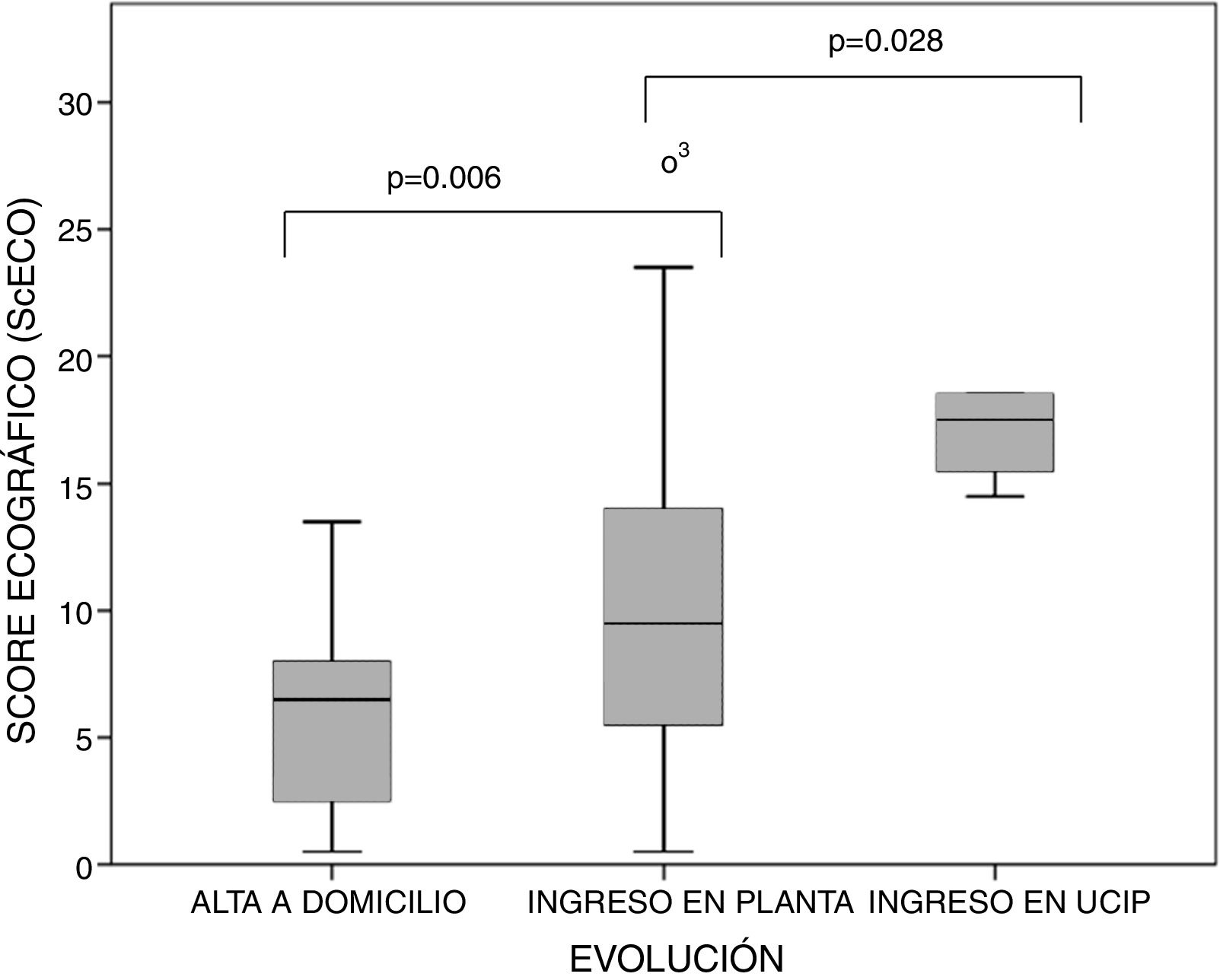
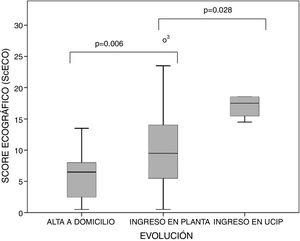
La ecografía se realizó a una mediana de 3 (2-4) días desde el inicio de los síntomas de BA. Ningún paciente recibía soporte respiratorio (exceptuando oxigenoterapia convencional por cánulas nasales) previamente a la realización de la ecografía. Las áreas pulmonares más frecuentemente afectadas fueron las áreas posteriores paravertebral y subescapular del tórax (tabla 2). La puntuación mediana del ScECO fue 8 (5-13) puntos en toda la cohorte y 6 (2-8) en los pacientes dados de alta a domicilio, 9 (5-13,7) en los ingresados en planta y de 17 (14,5-18) en los que precisaron traslado de planta a UCIP (p <0,001) (fig. 2). También hubo diferencias estadísticamente significativas en la extensión del SI: alta a domicilio 0 (0-2), ingreso en planta 4,5 (3-6) y traslado a UCIP 5,5 (5-6), p<0,001 y en la extensión de las CS: alta a domicilio 0 (0-2), ingreso en planta 2 (0-3,7) e ingreso en UCIP 5 (4,2-5,7), p=0,004, pero no en la extensión de las AP. No hubo diferencias significativas en la gravedad clínica entre lactantes menores de 3 meses y mayores de 3 meses: escala WDFM 5 (4-6) vs. 4,5 (4-7), p=0,459, y escala HSJD 6 (4-7) vs. 5,5 (4-7), p=0,662, respectivamente. Sin embargo, los lactantes menores de 3 meses tuvieron un ScECO mayor: 9 (6-13) vs. 7,5 (2-13), p=0,069, mayor SI 3 (1-5) vs. 1 (0-4.5), p=0,127, y más CS 4,5 (3-6) vs. 2 (0-4), p=0,106, aunque las diferencias no fueron significativas.
Porcentaje de afectación pulmonar en la ecografía en las áreas pulmonares estudiadas (para cada área se calcula la media de ambos pulmones)
| Área pulmonar | |||||
|---|---|---|---|---|---|
| Anterior paraesternal | Línea axilar anterior | Línea axilar posterior | Posterior paravertebral | Posterior subescapular | |
| AP | 34,7% | 39,7% | 22% | 74% | 65% |
| SI | 9,4% | 11,1% | 5,1% | 34% | 27% |
| CS | 9,4% | 10,2% | 5,1% | 25,5% | 27,1% |
AP: anomalía pleural; CS: consolidación subpleural; SI: síndrome intersticial.
Box-plot con la distribución de los valores del score ecográfico en función de la evolución del paciente.
Las barras indican la comparación por parejas (alta a domicilio vs. ingreso en planta e ingreso en planta vs. ingreso en UCIP) en el test de comparaciones múltiples.
p = 0,001 (test de Kruskal-Wallis).
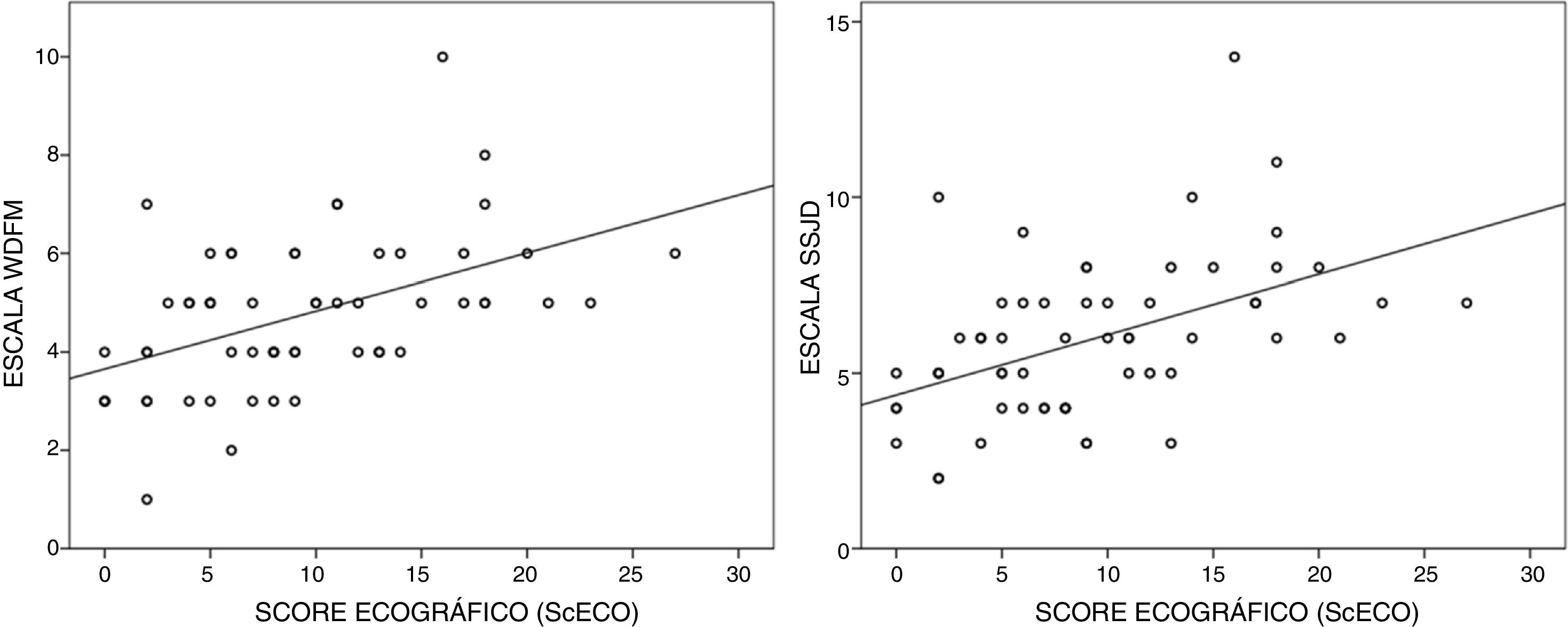
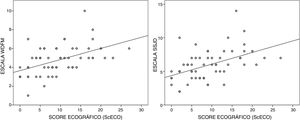
Los valores del ScECO, especialmente la extensión del SI y las CS, mostraron una correlación lineal estadísticamente significativa con los parámetros clínicos con la excepción de la frecuencia respiratoria (tabla 3). La correlación más fuerte se observó entre el score global y las escalas WDFM (rho de Spearman 0,504, p<0,001) y HSJD (rho de Spearman 0,518; p <0.001). Se muestran los gráficos de dispersión correspondientes a estas correlaciones (fig. 3)
Coeficientes de correlación de Spearman entre la ecografía pulmonar y los parámetros clínicos. Valores de los parámetros clínicos en función de la mediana del score ecográfico
| FR | FC | SatO2 | Escala WDFM | Escala HSJD | |
|---|---|---|---|---|---|
| ScECO | 0,092 | 0,366** | –0,296* | 0,504*** | 0,518*** |
| Anomalías pleurales | –0,060 | 0,3343** | –0,097 | 0,383** | 0,355** |
| Síndrome intersticial | 0,115 | 0,268** | –0,327* | 0,458*** | 0,484*** |
| Consolidaciones subpleurales | 0,213 | 0,403** | –0,303* | 0,463*** | 0,502*** |
| FR | FC | SatO2 | Escala WDFM | Escala HSJD | |
|---|---|---|---|---|---|
| ScECO | |||||
| <8 puntos | 53 (42-62) | 143 (130-160) | 96 (94-98) | 4 (3-5) | 5 (4-6) |
| >8 puntos | 54 (44-60) | 160 (144-172)* | 93 (90-98) | 5 (4-6)* | 7 (5-8)* |
FC: frecuencia cardiaca; FR: frecuencia respiratoria; HSJD: escala del Hospital Sant Joan de Déu; SatO2: saturación de oxígeno; WDFM: escala de Wood Downes Ferres modificada.
Por cada 5 puntos de incremento en el ScECO, aumentó la probabilidad de ingreso en UCIP (OR 2,5 [IC del 95%: 1,1-5,9); p=0.035), estancia hospitalaria en 1,2 días (IC del 95%: 0.55, 1.86; p <0,001) y duración de la oxigenoterapia en 0.87 días (IC del 95%: 0,26, 1,48; p=0.006). Estas asociaciones se mantuvieron significativas tras ajuste por sexo, peso, edad, tiempo de evolución de la BA y presencia de factores de riesgo de BA grave (tabla 4).
Asociación entre el score ecográfico global y la evolución clínica en el análisis multivariante
| Ingreso en la UCIP | |||
|---|---|---|---|
| Univariante | Multivariante | ||
| OR (IC del 95%) | p | OR (IC del 95%) | p |
| 2,5 (1,1-5,9) | 0,035 | 3,75 (1,12-12,52) | 0,032 |
| Días de hospitalización | |||
|---|---|---|---|
| Univariante | Multivariante | ||
| Coeficiente B (IC del 95%) | p | Coeficiente B (IC del 95%) | p |
| 1,2 (0,55, 1,86) | <0,001 | 1,09 (0,29, 1,79) | 0,003 |
| Días de oxígeno | |||
|---|---|---|---|
| Univariante | Multivariante | ||
| Coeficiente B (IC del 95%) | p | Coeficiente B (IC del 95%) | p |
| 0,87 (0,26-1,48) | 0,006 | 0,75 (0,10, 1,4) | 0,024 |
La asociación entre el score ecográfico se evaluó mediante regresión logística para el ingreso en UCIP y regresión lineal para los días de hospitalización y oxigenoterapia. Las OR y los coeficientes B se expresan para incrementos de 5 puntos en el score ecográfico con sus intervalos de confianza del 95% y el valor de p. El modelo está ajustado por sexo, peso, edad, tiempo de evolución de la BA y la presencia de algún factor de riesgo de BA grave (edad <6 semanas, prematuridad <35 semanas, enfermedad crónica previa o ausencia de lactancia materna exclusiva).
En este estudio preliminar hemos observado que la ecografía pulmonar se correlaciona con la gravedad clínica en BA leve-moderada y que puede tener cierto valor para predecir la evolución clínica posterior. Sin embargo, no hemos podido demostrar que tenga una utilidad añadida a las escalas de valoración clínica para anticipar una evolución desfavorable.
Existen muy pocos estudios que hayan utilizado la ecografía pulmonar en la BA, pese a que se trata de una herramienta ampliamente utilizada en la valoración del paciente con enfermedad pulmonar aguda tal como neumonía, derrame pleural o edema de pulmón donde ha demostrado tener un rendimiento diagnóstico superior a la radiología convencional evitando el uso de radiación ionizante5-7,12.
En 2011 Caiulo et al. compararon los hallazgos ecográficos y radiológicos en pacientes con BA mostrando que la extensión de las CS y del SI guardaba relación con la gravedad y que el número de CS seguía un curso paralelo a la escala de Downes12. En 2015, Basile et al.Valoraron, en pacientes con BA, las anomalías ecográficas en función de la presencia y extensión de CS y la extensión del SI para identificar a los pacientes que precisaban oxigenoterapia13. Nuestros resultados están en concordancia con los estudios mencionados; también hemos encontrado que las anomalías ecográficas se correlacionan linealmente y de forma similar con 2escalas clínicas validadas26.
Un aspecto a destacar es que en nuestro estudio no encontramos una correlación lineal entre la frecuencia respiratoria (considerada de forma generalizada como marcador sensible de afectación respiratoria) y la ecografía pulmonar. No tenemos una explicación clara para este hallazgo. Tal vez la mayor variabilidad de la frecuencia respiratoria y su falta de especificidad (relación con la fiebre, obstrucción nasal, agitación del paciente, etc.) junto con la falta de tamaño muestral puedan estar detrás de este hallazgo inesperado.
Los hallazgos ecográficos como las AP, las CS o la presencia de SI no son específicos de la BA y son muy similares a los que se observan en otras enfermedades con afectación intersticial difusa, como la broncodisplasia o el SDRA6,27. No obstante, nuestro estudio y otros previos son una prueba de concepto, indicando que la extensión de las anomalías ecográficas refleja en cierto modo la gravedad del proceso fisiopatológico subyacente en la BA. Sabemos que las BA más graves son aquellas que tienen comportamiento similar al SDRA con afectación intersticial grave y disminución de la distensibilidad pulmonar en contraposición con el patrón obstructivo y atrapamiento aéreo. Es plausible que detectar precozmente un pulmón con una aireación comprometida mediante ecografía pueda tener valor para anticipar la evolución clínica. En este estudio hemos observado que los pacientes que acabarán precisando ingreso en UCIP tienen mayor afectación ecográfica inicialmente que los que son dados de alta a domicilio o los que ingresan en planta, y que también tiene cierto valor para identificar pacientes que requerirán más días de ingreso y oxigenoterapia. No obstante, en nuestros modelos estadísticos no se ha podido demostrar que dichas asociaciones persistan cuando se tiene en cuenta las escalas de gravedad clínica. Ello no debe servir para descartar definitivamente el uso de la ecografía en BA, sino que debe animarnos a estudiar más profundamente cuál puede ser su papel. En esta línea hemos observado que, a similar gravedad clínica, los lactantes <3 meses tienen más afectación de la aireación pulmonar que los lactantes más mayores, lo cual también podría relacionarse con la peor evolución de este grupo en que la afectación alvéolo-intersticial pudiera dominar, en contraposición con la obstrucción y atrapamiento aéreo de los lactantes mayores.
Todas las guías de práctica clínica coinciden en que las exploraciones complementarias no se recomiendan de rutina en la BA1,2. No obstante, la ecografía podría resultar útil en aquellos casos en que pese a la valoración clínica habitual dudemos, por ejemplo, sobre la necesidad de observación hospitalaria. Una afectación extensa en la ecografía debiera hacernos pensar que la evolución puede ser desfavorable. Así en nuestro estudio una puntuación > 13,5 según nuestro ScECO tuvo una sensibilidad y una especificidad del 100 y el 82%, respectivamente, para predecir el ingreso en UCIP.
LimitacionesLos hallazgos de nuestro estudio deben interpretarse teniendo en cuenta sus limitaciones. La ecografía se realizó a una mediana de 3 días desde el inicio de la BA, aunque este momento suele coincidir con la máxima afectación clínica, es posible que existieran diferencias entre pacientes en el grado de afectación pulmonar y además, es posible que la administración de tratamiento nebulizado pudiera modificar los hallazgos ecográficos. No obstante, no existen publicaciones que demuestren que los broncodilatadores modifiquen la evolución ni la afectación pulmonar ecográfica en la BA. Nuestro estudio incluye a pocos pacientes y presenta puntuaciones relativamente bajas (mediana de 8 puntos) en un score ecográfico máximo de 50 puntos. Este hecho ha podido limitar la detección de una relación independiente entre la ecografía y la evolución clínica, que en la temporada epidémica estudiada fue relativamente benigna (estancia hospitalaria corta y pocos ingresos en la UCIP).
En nuestro score ecográfico se evalúan más áreas pulmonares por pulmón respecto a los previos, de manera que, aunque pudiera aportar más información, podría comprometer su reproducibilidad y aplicación clínica. Nuestros datos indican que la valoración del tamaño y el número de CS puede tener cierto grado de subjetividad, la concordancia interobservador fue solo buena. Así mismo, parece que las AP tienen poco valor añadido a las CS y el SI, por lo que en futuros estudios puede ser conveniente simplificar el score obviando este aspecto.
En el futuro, con la creciente disponibilidad de equipos y entrenamiento de los pediatras, es posible que la utilización de ecografía en enfermedades respiratorias se generalice. Sin embargo, para poder desarrollarla en toda su potencialidad es preciso generar evaluaciones sistemáticas y validadas. En nuestra opinión, los futuros estudios deberían centrarse en detectar qué hallazgos tienen más valor predictivo en la evolución de la BA. Para ello será necesario incluir a suficientes pacientes con evolución desfavorable y necesidad de soporte ventilatorio, por lo que dichos estudios deberían ser multicéntricos para asegurar el reclutamiento.
ConclusionesExiste una correlación moderada entre las escalas de gravedad clínica y la extensión de la afectación pulmonar en la ecografía realizada precozmente en lactantes con BA leve-moderada. Los hallazgos ecográficos de más valor son la extensión del SI y las CS. La ecografía pulmonar podría relacionarse con la evolución clínica y resultar útil para identificar a aquellos pacientes en riesgo de una evolución desfavorable.
FinanciaciónXIX Convocatoria Ayuda a la Investigación Clínica y Epidemiológica-2016, Fundación Ernesto Sánchez Villares, Sociedad de Pediatría de Asturias, Cantabria y Castilla y León. Proyecto 02/2016: «Utilidad de la ecografía pulmonar en la valoración de la gravedad y pronóstico de la bronquiolitis aguda». Investigador principal: Elia Zoido Garrote. Dotación económica de 3.000 euros.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.