La renovación de las guías de práctica clínica sobre la bronquiolitis aguda (BA) obliga a reevaluar las consecuencias de su implantación. Pretendemos actualizar las principales variables clínico-epidemiológicas en pacientes ingresados por BA en el sur de Europa y analizar las causas de la estancia prolongada.
Pacientes y métodoEstudio retrospectivo de ingresos por BA durante 5 epidemias (2010-2015), con descripción de las principales variables clínico-epidemiológicas y análisis por regresión logística de los factores asociados a mayor estancia.
ResultadosEl inicio de la epidemia ocurrió entre las semanas cuarta de septiembre y tercera de octubre. De los menores de 2 años (42.530 niños), el 15,21% (6.468 pacientes) acudieron a urgencias por BA y el 2,36% ingresaron (1.006 pacientes), con un 18,5% de prematuros. El 12,2% tenían peso al nacimiento inferior a 2.300g. El 21,1% eran menores de un mes, consultaron por apnea asociada el 10,8%, ingesta inferior al 50% en el 31,1% y presentaban sobreinfección bacteriana el 13,1%. Estos factores se asociaron de forma independiente a la estancia prolongada. La mediana de estancia fue de 5 días y la proporción de ingresos en la unidad de cuidados intensivos pediátricos (UCIP) del 8,5% de los casos.
ConclusionesEl inicio de la epidemia de la bronquiolitis mostró una variabilidad de hasta 4 semanas en nuestro medio. Tras 5 años de la implantación de la guía de práctica clínica, la incidencia de ingresos está en torno al 2,3% y parece estable respecto a estudios previos. La edad media de los pacientes desciende a 2,4 meses, aunque con una proporción similar de ingresos en la UCIP de un 8,5%.
Los factores de riesgo independiente asociados a una estancia hospitalaria más prolongada fueron: bajo peso al nacimiento, edad menor de un mes, apneas previas al ingreso, ingesta inferior al 50% y la sobreinfección bacteriana grave, donde la infección respiratoria superó la prevalencia de infección del tracto urinario grave.
The renewal of clinical practice guidelines on acute bronchiolitis (AB) requires the re-assessment of the consequences of their implementation. An update is presented on the main clinical and epidemiological variables in patients hospitalised due to AB in Southern Europe and an analysis made of the causes associated with longer hospital stay.
Patients and methodA retrospective study was conducted on patients admitted to hospital due to AB during 5 epidemics (2010-2015), with an analysis of the major clinical and epidemiological variables. A logistic regression analysis was performed on the factors associated with a longer hospital stay.
ResultsThe beginning of the epidemic occurred between the 4th week of September and the 3rd week of October. Of those children under 2 years (42,530), 15.21% (6,468 patients) attended paediatric emergency department due to having AB, and 2.36% (1,006 patients) were admitted. Of these, 18.5% of were premature, 12.2% had a birth weight <2,300g, 21.1% were younger than 1 month, 10.8% consulted for associated apnoea, 31.1% had an intake <50%, and 13.1% had bacterial superinfection. These factors were independently associated with prolonged stay. The median length of stay was 5 days, and 8.5% of cases were admitted to a paediatric intensive care unit (PICU).
ConclusionsThe beginning of the bronchiolitis epidemic showed a variability of up to 4 weeks in this region. Five years after implementing the new guidelines, the incidence of admissions was approximately 2.3%, and appeared stable compared to previous studies. The mean age of the patients decreased to 2.4 months, although with a similar proportion of PICU admissions of 8.5%.
Independent factors associated with prolonged stay were: low birth weight, age less than one month, apnoea prior-to-admission, intake of less than 50%, and severe bacterial superinfection. Respiratory bacterial infection exceeded the prevalence of urinary tract infection.
A pesar del paso del tiempo no existe ninguna patología infecciosa, reconocida ya desde los inicios de la pediatría europea1, que genere mayor carga asistencial en los servicios de salud, que la bronquiolitis aguda (BA)2-6. El virus respiratorio sincitial (VRS) es el responsable en aproximadamente el 60-75% de los casos6,7. Como en los primeros abordajes terapéuticos1, no existe un tratamiento etiológico disponible para la enfermedad una vez establecida, y la terapéutica se basa en cuidados generales y medidas de soporte respiratorio de mayor o menor intensidad, que se han actualizado en los últimos años en diversas guías de práctica clínica (GPC)8-11.
La posibilidad de la vacunación en el lactante o en la embarazada está cada vez más cerca12 y la estrategia para combatir esta enfermedad pasa por conocer adecuadamente su comportamiento epidemiológico según las características geográficas y ambientales de cada zona, para poder así establecer medidas ajustadas a cada circunstancia. Los estudios epidemiológicos sobre BA publicados en Europa, sobre todo de pacientes ingresados, presentan cierta disparidad en los resultados2,5,13-16. La actualización de las GPC para el tratamiento de la BA y su implementación —como en nuestro caso— desde el año 201011, obliga a evaluar las consecuencias de su implantación y su repercusión en la dinámica hospitalaria.
Nuestro objetivo es describir y contrastar las principales variables epidemiológicas y clínicas en pacientes ingresados en un hospital de tercera referencia, de una población costera situada al sur de Europa, durante 5 epidemias recientes de BA tras la implantación estable de una GPC desde el año 201011. Analizaremos la incidencia de ingresos en relación con las consultas en urgencias y la necesidad de atención en unidades de cuidados intensivos pediátricos (UCIP), así como la gravedad en términos de estancia hospitalaria y sus factores asociados. Pretendemos además determinar el inicio de la situación de epidemia en nuestro medio y su variabilidad anual.
Pacientes y métodoEstudio retrospectivo de pacientes ingresados en un hospital pediátrico de tercer nivel desde el 1 de octubre de 2010 al 31 marzo de 2015 con diagnóstico clínico al alta de BA según los criterios clásicos de McConnochie, definidos como el primer episodio agudo de dificultad respiratoria de vías bajas asociado a un cuadro catarral previo en menores de 24 meses17. Este hospital materno-infantil es la cabecera asistencial de referencia de un servicio de salud, con una población de 1,2 millones de habitantes y una población pediátrica adscrita directa de unos 100.000 niños, de los cuales se estimó en 42.530 los menores de 24 meses susceptibles al inicio del periodo de estudio. Su situación geográfica costera en el paralelo 36° 43’ 0” N, con un clima mediterráneo, hace que se trate del hospital pediátrico de referencia más al sur de Europa.
La historia clínica de nuestros pacientes recoge de forma homogénea las principales variables al ser una patología recurrente y estandarizada. Los criterios de ingresos seguidos fueron los de la GPC previamente referida11. En nuestro hospital todos los pacientes fueron investigados al ingreso, para la ubicación de cohortes, respecto a la presencia del VRS a partir del análisis antigénico del aspirado nasofaríngeo al ingreso (RSV Card letitest©, Leti Diagnostics, Barcelona, España)18. Durante la estancia, todos los pacientes fueron monitorizados mediante oximetría de pulso al ingreso hasta la completa estabilidad clínica en una planta de hospitalización específica para lactantes con BA.
Los investigadores también revisaron los registros de pacientes atendidos en urgencias para determinar el número e incidencia de casos distintos con código diagnóstico al alta de BA durante el periodo de estudio. De los pacientes ingresados, se revisó la historia clínica informatizada para recoger variables demográficas y clínicas. De cada paciente se recogieron las variables: sexo, edad, mes de ingreso, peso al nacimiento, edad gestacional, edad de la madre, edad posmenstrual, parto múltiple, cesárea, exposición ambiental y/o durante la gestación al tabaco, lactancia materna, hermanos menores de 6 años y de 6 a 14 años, atopia en familiares de primer grado, enfermedades crónicas (antecedentes de cardiopatía, enfermedad neurológica incapacitante y displasia broncopulmonar), días de evolución previa al ingreso, fiebre, grado hiporexia, bajo peso (por debajo del percentil 3), gravedad al ingreso mediante escala validada19, presencia de apneas, días de estancia en planta y en cuidados intensivos e infección bacteriana grave asociada, confirmada o sospechada. Los casos de ITU y sepsis, mediante confirmación por urocultivos y/o hemocultivos positivos junto con clínica compatible. En casos de sobreinfección respiratoria sospechada, esta se estableció según criterios clínicos y analíticos previamente descritos20–22, con elevación de reactantes por encima de 70mg/l para la PCR y de 0,5ng/ml para la procalcitonina.
El inicio de la epidemia se consideró cuando la incidencia semanal de BA en urgencias fue mayor del límite superior del intervalo de confianza al 95% de la línea base de incidencia de casos fuera del periodo epidémico (de abril a septiembre), durante 2 semanas consecutivas según el método clásico de Serfling23.
Se contrastó el comportamiento de las variables según la presencia del VRS y se analizaron los factores de riesgo de prolongación del ingreso, tomando como referencia la mediana de días de estancia hospitalaria según estudios previos7. Se excluyeron en este caso los pacientes con enfermedad de base, para centrarnos en los pacientes sanos que suponen alrededor del 95% en la mayoría de las series14,24,25. El análisis estadístico se realizó mediante el programa libre PSPP. Las variables cualitativas se resumieron mediante porcentajes y las cuantitativas, con la media y la desviación estándar. La asociación entre variables cualitativas se analizó mediante la prueba Chi-cuadrado. El análisis multivariante de los factores asociados con una estancia prolongada se realizó mediante regresión logística, incluyendo en el modelo final aquellas variables con una significación p<0,25 en el análisis bivariante. Se consideraron estadísticamente significativos todos los contrastes de hipótesis con una p<0,05 y todos los intervalos de confianza se estimaron con un nivel de confianza del 95%.
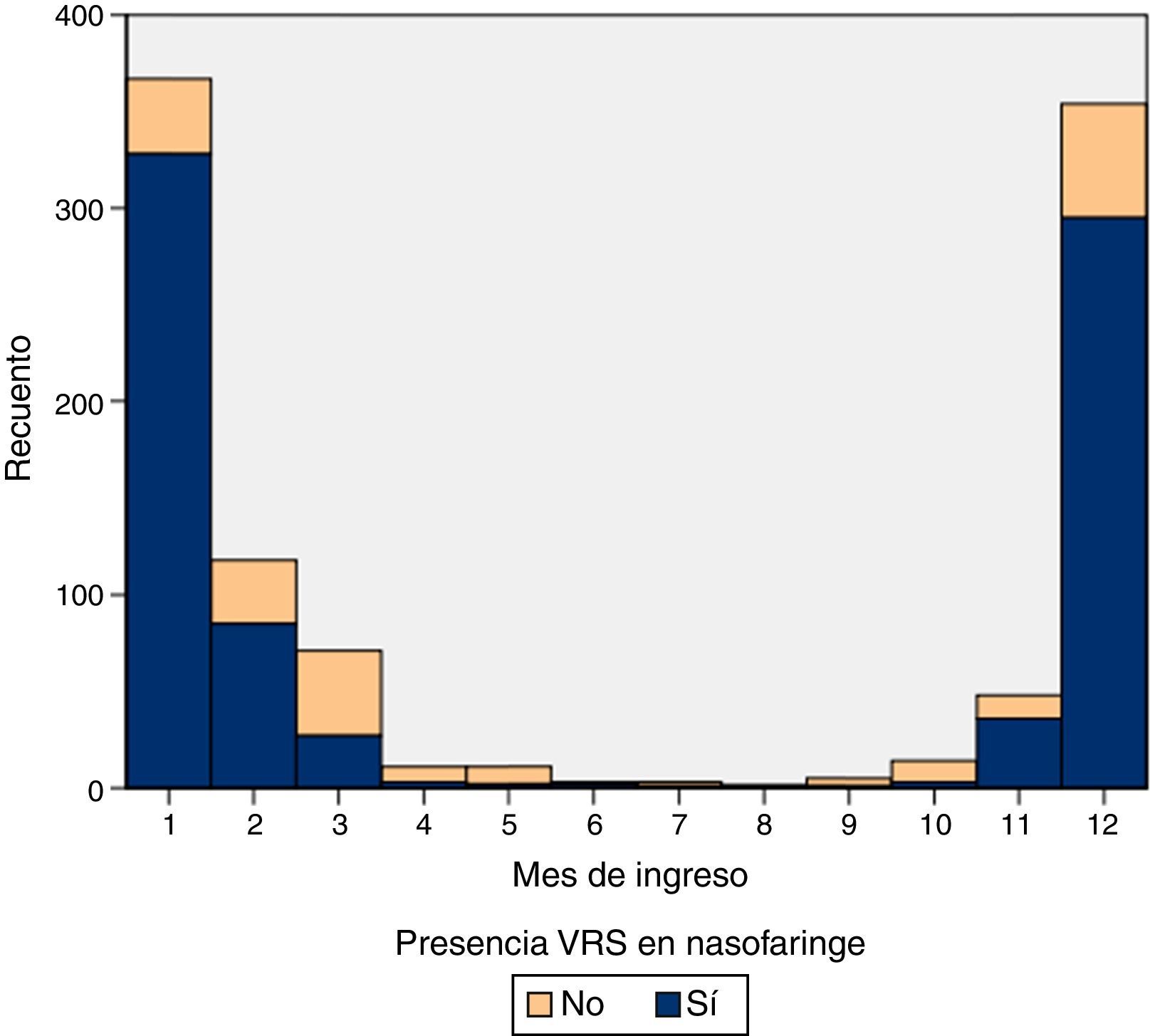
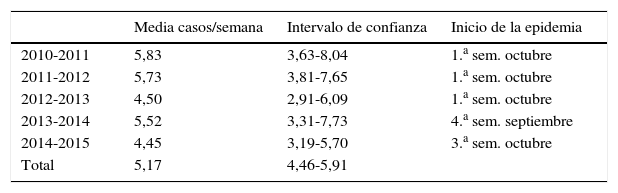
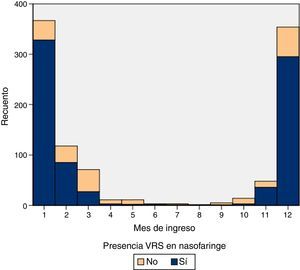
ResultadosDurante el periodo de estudio, el 15,21% (6.468 pacientes) de los menores de 24 meses consultaron en urgencias de nuestro hospital por BA y el 2,36% de los casos fueron ingresados (1.006 pacientes). Las características de nuestra muestra se resumen en la tabla 1. La línea base de incidencia semanal calculada en los periodos de abril a octubre fue de 5,17 casos por semana (IC 95%: 4,46-5,91). El inicio de la epidemia para cada temporada, según nuestra densidad de incidencia, se muestra en la tabla 2. La diferencia de inicio en nuestra serie fue de 4 semanas. La frecuencia mensual de ingresos se muestra en la figura 1.
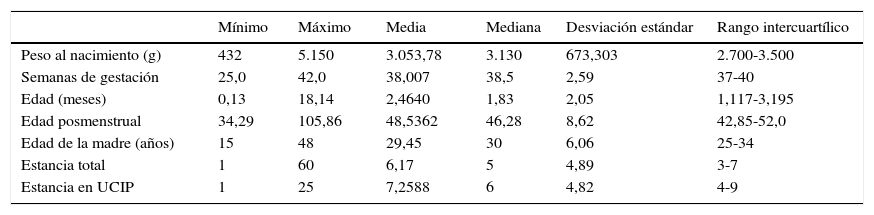
Variables cuantitativas de los pacientes ingresados con bronquiolitis del estudio (n=1.006)
| Mínimo | Máximo | Media | Mediana | Desviación estándar | Rango intercuartílico | |
|---|---|---|---|---|---|---|
| Peso al nacimiento (g) | 432 | 5.150 | 3.053,78 | 3.130 | 673,303 | 2.700-3.500 |
| Semanas de gestación | 25,0 | 42,0 | 38,007 | 38,5 | 2,59 | 37-40 |
| Edad (meses) | 0,13 | 18,14 | 2,4640 | 1,83 | 2,05 | 1,117-3,195 |
| Edad posmenstrual | 34,29 | 105,86 | 48,5362 | 46,28 | 8,62 | 42,85-52,0 |
| Edad de la madre (años) | 15 | 48 | 29,45 | 30 | 6,06 | 25-34 |
| Estancia total | 1 | 60 | 6,17 | 5 | 4,89 | 3-7 |
| Estancia en UCIP | 1 | 25 | 7,2588 | 6 | 4,82 | 4-9 |
UCIP: unidad de cuidados intensivos pediátricos.
Media de casos semanales de pacientes con bronquiolitis atendidos en urgencias fuera del periodo epidémico (1 de abril a 30 de septiembre), intervalo de confianza al 95% y semana de inicio de la epidemia
| Media casos/semana | Intervalo de confianza | Inicio de la epidemia | |
|---|---|---|---|
| 2010-2011 | 5,83 | 3,63-8,04 | 1.a sem. octubre |
| 2011-2012 | 5,73 | 3,81-7,65 | 1.a sem. octubre |
| 2012-2013 | 4,50 | 2,91-6,09 | 1.a sem. octubre |
| 2013-2014 | 5,52 | 3,31-7,73 | 4.a sem. septiembre |
| 2014-2015 | 4,45 | 3,19-5,70 | 3.a sem. octubre |
| Total | 5,17 | 4,46-5,91 |
sem.: semana.
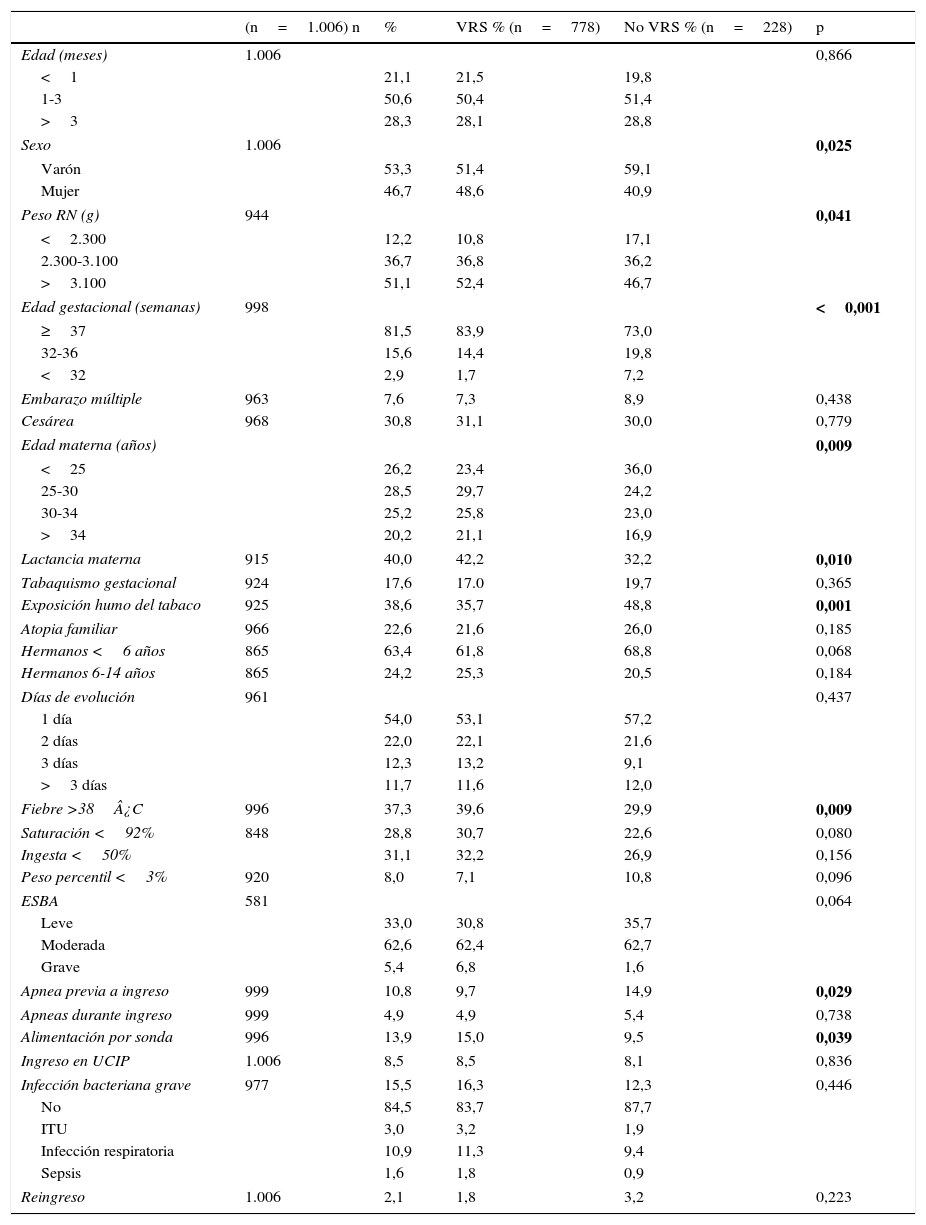
De los pacientes ingresados, en el 77,9% se pudo identificar el VRS en el aspirado. En la tabla 3 se muestran las variables según la presencia del VRS junto a la muestra n alcanzada por cada variable. La media de edad fue de 2,46 meses (IC 95%: 2,34-2,59). El 71,8% eran menores de 3 meses, el 93,6% eran menores de 6 meses y solo el 0,5% eran mayores de 12 meses. El 53,3% eran varones y el 81,5% fueron de más de 37 semanas de gestación; el 15,6% de 32 a 37 semanas y el 2,9% eran de menos de 32 semanas. El 7,6% eran embarazos múltiples y el 30,8% fueron cesáreas. El 40% fueron alimentados con lactancia materna exclusiva. El 17,6% sufrieron tabaquismo gestacional y el 38,6% tabaquismo ambiental. Tenían antecedentes de atopia en familiares de primer grado el 22,6%. El 63,4% tenían hermanos menores de 6 años y el 24,2% tenían hermanos de 6 a 14 años. Los antecedentes de cardiopatía, enfermedad neurológica y displasia broncopulmonar se detectaron en el 2,9, 1,3 y 1,7% respectivamente. En 9 casos que recibieron alguna dosis de palivizumab se detectó el VRS. El 53,9% consultaron en el primer día de aparición de la dificultad respiratoria.
Comparación de variables epidemiológicas y clínicas según la presencia de VRS en casos de bronquiolitis en los pacientes ingresados, mediante la prueba de Chi-cuadrado
| (n=1.006) n | % | VRS % (n=778) | No VRS % (n=228) | p | |
|---|---|---|---|---|---|
| Edad (meses) | 1.006 | 0,866 | |||
| <1 | 21,1 | 21,5 | 19,8 | ||
| 1-3 | 50,6 | 50,4 | 51,4 | ||
| >3 | 28,3 | 28,1 | 28,8 | ||
| Sexo | 1.006 | 0,025 | |||
| Varón | 53,3 | 51,4 | 59,1 | ||
| Mujer | 46,7 | 48,6 | 40,9 | ||
| Peso RN (g) | 944 | 0,041 | |||
| <2.300 | 12,2 | 10,8 | 17,1 | ||
| 2.300-3.100 | 36,7 | 36,8 | 36,2 | ||
| >3.100 | 51,1 | 52,4 | 46,7 | ||
| Edad gestacional (semanas) | 998 | <0,001 | |||
| ≥37 | 81,5 | 83,9 | 73,0 | ||
| 32-36 | 15,6 | 14,4 | 19,8 | ||
| <32 | 2,9 | 1,7 | 7,2 | ||
| Embarazo múltiple | 963 | 7,6 | 7,3 | 8,9 | 0,438 |
| Cesárea | 968 | 30,8 | 31,1 | 30,0 | 0,779 |
| Edad materna (años) | 0,009 | ||||
| <25 | 26,2 | 23,4 | 36,0 | ||
| 25-30 | 28,5 | 29,7 | 24,2 | ||
| 30-34 | 25,2 | 25,8 | 23,0 | ||
| >34 | 20,2 | 21,1 | 16,9 | ||
| Lactancia materna | 915 | 40,0 | 42,2 | 32,2 | 0,010 |
| Tabaquismo gestacional | 924 | 17,6 | 17.0 | 19,7 | 0,365 |
| Exposición humo del tabaco | 925 | 38,6 | 35,7 | 48,8 | 0,001 |
| Atopia familiar | 966 | 22,6 | 21,6 | 26,0 | 0,185 |
| Hermanos <6 años | 865 | 63,4 | 61,8 | 68,8 | 0,068 |
| Hermanos 6-14 años | 865 | 24,2 | 25,3 | 20,5 | 0,184 |
| Días de evolución | 961 | 0,437 | |||
| 1 día | 54,0 | 53,1 | 57,2 | ||
| 2 días | 22,0 | 22,1 | 21,6 | ||
| 3 días | 12,3 | 13,2 | 9,1 | ||
| >3 días | 11,7 | 11,6 | 12,0 | ||
| Fiebre >38¿C | 996 | 37,3 | 39,6 | 29,9 | 0,009 |
| Saturación <92% | 848 | 28,8 | 30,7 | 22,6 | 0,080 |
| Ingesta <50% | 31,1 | 32,2 | 26,9 | 0,156 | |
| Peso percentil <3% | 920 | 8,0 | 7,1 | 10,8 | 0,096 |
| ESBA | 581 | 0,064 | |||
| Leve | 33,0 | 30,8 | 35,7 | ||
| Moderada | 62,6 | 62,4 | 62,7 | ||
| Grave | 5,4 | 6,8 | 1,6 | ||
| Apnea previa a ingreso | 999 | 10,8 | 9,7 | 14,9 | 0,029 |
| Apneas durante ingreso | 999 | 4,9 | 4,9 | 5,4 | 0,738 |
| Alimentación por sonda | 996 | 13,9 | 15,0 | 9,5 | 0,039 |
| Ingreso en UCIP | 1.006 | 8,5 | 8,5 | 8,1 | 0,836 |
| Infección bacteriana grave | 977 | 15,5 | 16,3 | 12,3 | 0,446 |
| No | 84,5 | 83,7 | 87,7 | ||
| ITU | 3,0 | 3,2 | 1,9 | ||
| Infección respiratoria | 10,9 | 11,3 | 9,4 | ||
| Sepsis | 1,6 | 1,8 | 0,9 | ||
| Reingreso | 1.006 | 2,1 | 1,8 | 3,2 | 0,223 |
ESBA: escala de severidad de la bronquiolitis aguda; ITU: infección del tracto urinario; RN: recién nacido; UCIP: unidad de cuidados intensivos pediátricos; VRS: virus respiratorio sincitial.
p significativa en negrita.
El 37,3% presentaban fiebre y el 28,8% tenían una saturación de oxígeno menor del 92% al consultar. El 31,1% tenían una ingesta inferior al 50%. Presentaban bajo peso, por debajo del percentil 3, el 8,0%. Según la escala de gravedad al ingreso, el 62,6% se catalogaron de intensidad moderada y el 5,4% de graves. El 10,8% refirieron apnea previa al ingreso, pero solo el 4,9% de los pacientes presentaron apneas durante el ingreso. El 13,9% requirieron alimentación por sonda enteral y el 8,5%, ingreso en la UCIP (85 casos: 53 CPAP, 21 VMI, 4 VM alta frecuencia, 7 cánulas alto flujo). Solo el 11,4% no precisaron oxigenoterapia. El 15,5% padecieron una infección bacteriana grave (en 3 variedades detectadas: ITU, sobreinfección respiratoria y sepsis [tabla 2]), de las que solo un 1,9% se catalogaron de nosocomiales. Se registró reingreso en el 2,1% de los casos. Hubo 2 fallecimientos, lo que supone un 0,19% de los pacientes hospitalizados.
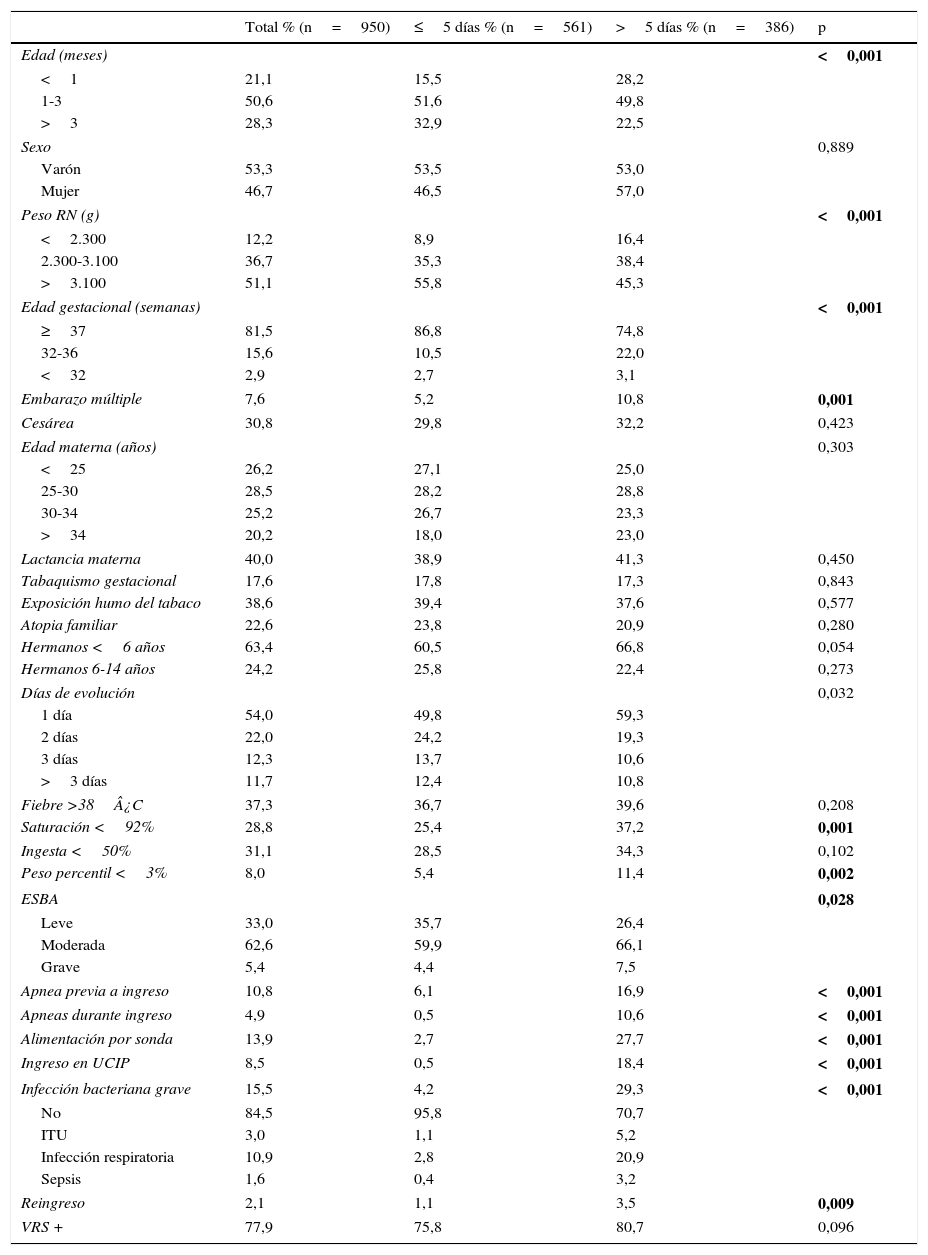
La estancia media por temporadas no presentó diferencias significativas. El análisis comparativo de los pacientes con mayor estancia respecto de la mediana de estancia, que se situó en 5 días, se presenta en la tabla 4. En el modelo final, fueron significativas la edad, la presencia de apnea antes del ingreso, la infección bacteriana asociada y la ingesta inferior al 50% al ingreso (tabla 5).
Comparación de variables epidemiológicas y clínicas según días de estancia de los pacientes con bronquiolitis mediante la prueba de Chi-cuadrado
| Total % (n=950) | ≤5 días % (n=561) | >5 días % (n=386) | p | |
|---|---|---|---|---|
| Edad (meses) | <0,001 | |||
| <1 | 21,1 | 15,5 | 28,2 | |
| 1-3 | 50,6 | 51,6 | 49,8 | |
| >3 | 28,3 | 32,9 | 22,5 | |
| Sexo | 0,889 | |||
| Varón | 53,3 | 53,5 | 53,0 | |
| Mujer | 46,7 | 46,5 | 57,0 | |
| Peso RN (g) | <0,001 | |||
| <2.300 | 12,2 | 8,9 | 16,4 | |
| 2.300-3.100 | 36,7 | 35,3 | 38,4 | |
| >3.100 | 51,1 | 55,8 | 45,3 | |
| Edad gestacional (semanas) | <0,001 | |||
| ≥37 | 81,5 | 86,8 | 74,8 | |
| 32-36 | 15,6 | 10,5 | 22,0 | |
| <32 | 2,9 | 2,7 | 3,1 | |
| Embarazo múltiple | 7,6 | 5,2 | 10,8 | 0,001 |
| Cesárea | 30,8 | 29,8 | 32,2 | 0,423 |
| Edad materna (años) | 0,303 | |||
| <25 | 26,2 | 27,1 | 25,0 | |
| 25-30 | 28,5 | 28,2 | 28,8 | |
| 30-34 | 25,2 | 26,7 | 23,3 | |
| >34 | 20,2 | 18,0 | 23,0 | |
| Lactancia materna | 40,0 | 38,9 | 41,3 | 0,450 |
| Tabaquismo gestacional | 17,6 | 17,8 | 17,3 | 0,843 |
| Exposición humo del tabaco | 38,6 | 39,4 | 37,6 | 0,577 |
| Atopia familiar | 22,6 | 23,8 | 20,9 | 0,280 |
| Hermanos <6 años | 63,4 | 60,5 | 66,8 | 0,054 |
| Hermanos 6-14 años | 24,2 | 25,8 | 22,4 | 0,273 |
| Días de evolución | 0,032 | |||
| 1 día | 54,0 | 49,8 | 59,3 | |
| 2 días | 22,0 | 24,2 | 19,3 | |
| 3 días | 12,3 | 13,7 | 10,6 | |
| >3 días | 11,7 | 12,4 | 10,8 | |
| Fiebre >38¿C | 37,3 | 36,7 | 39,6 | 0,208 |
| Saturación <92% | 28,8 | 25,4 | 37,2 | 0,001 |
| Ingesta <50% | 31,1 | 28,5 | 34,3 | 0,102 |
| Peso percentil <3% | 8,0 | 5,4 | 11,4 | 0,002 |
| ESBA | 0,028 | |||
| Leve | 33,0 | 35,7 | 26,4 | |
| Moderada | 62,6 | 59,9 | 66,1 | |
| Grave | 5,4 | 4,4 | 7,5 | |
| Apnea previa a ingreso | 10,8 | 6,1 | 16,9 | <0,001 |
| Apneas durante ingreso | 4,9 | 0,5 | 10,6 | <0,001 |
| Alimentación por sonda | 13,9 | 2,7 | 27,7 | <0,001 |
| Ingreso en UCIP | 8,5 | 0,5 | 18,4 | <0,001 |
| Infección bacteriana grave | 15,5 | 4,2 | 29,3 | <0,001 |
| No | 84,5 | 95,8 | 70,7 | |
| ITU | 3,0 | 1,1 | 5,2 | |
| Infección respiratoria | 10,9 | 2,8 | 20,9 | |
| Sepsis | 1,6 | 0,4 | 3,2 | |
| Reingreso | 2,1 | 1,1 | 3,5 | 0,009 |
| VRS + | 77,9 | 75,8 | 80,7 | 0,096 |
ESBA: escala de severidad de la bronquiolitis aguda; ITU: infección del tracto urinario; RN: recién nacido; UCIP: unidad de cuidados intensivos pediátricos; VRS: virus respiratorio sincitial.
p significativa en negrita.
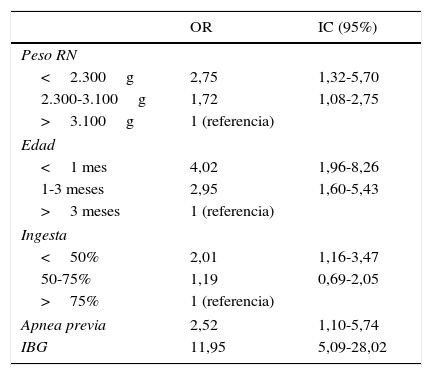
Resultados del análisis de regresión logística de las variables asociadas a mayor estancia en pacientes ingresados por bronquiolitis, con su odds ratio e intervalo de confianza
| OR | IC (95%) | |
|---|---|---|
| Peso RN | ||
| <2.300g | 2,75 | 1,32-5,70 |
| 2.300-3.100g | 1,72 | 1,08-2,75 |
| >3.100g | 1 (referencia) | |
| Edad | ||
| <1 mes | 4,02 | 1,96-8,26 |
| 1-3 meses | 2,95 | 1,60-5,43 |
| >3 meses | 1 (referencia) | |
| Ingesta | ||
| <50% | 2,01 | 1,16-3,47 |
| 50-75% | 1,19 | 0,69-2,05 |
| >75% | 1 (referencia) | |
| Apnea previa | 2,52 | 1,10-5,74 |
| IBG | 11,95 | 5,09-28,02 |
IBG: infección bacteriana grave; IC: intervalo de confianza; OR: odds ratio; RN: recién nacido.
Tras la implementación de la GPC del año 2010, la perspectiva de 5 epidemias son un tiempo razonable para evaluar su impacto. En la latitud de este centro hospitalario, se suele considerar octubre como el mes de inicio de la epidemia de BA, pero existió una variabilidad de 4 semanas, como ha sido descrito2. En otras latitudes europeas, como en Grecia, la epidemia se inicia en diciembre, con un pico en febrero15. Los abordajes que puedan tener su actuación a través de la inmunidad de la embarazada, como se establece con la tosferina, deben tener en cuenta estos aspectos a la hora de planificar la estrategia de prevención12.
Aunque clásicamente se ha considerado 24 meses la edad límite para el diagnóstico de BA, cada vez son más los autores que centran su estudio en los primeros 12 meses como una edad más adecuada para definir esta enfermedad14,26. El comportamiento real de la fisiopatología de la BA en los lactantes menores de 6 meses difiere de forma significativa de aquellos de mayor edad, tanto por el grado de maduración inmunológica y funcional, como por el tamaño de las vías respiratorias. En nuestra serie, el 93% de los ingresos eran menores de 6 meses y solo el 0,5% de los ingresos por BA superaron el año de edad para una edad media de 2,46 meses. En publicaciones de nuestro entorno, cerca del 2,7% de los ingresos por BA son mayores de un año2.
La edad media de los ingresados muestra amplia variabilidad según se recoge en un extenso análisis epidemiológico de la evidencia27, lo que sin duda condiciona otras variables como los ingresos en la UCIP y la estancia media. Tanto la estancia media en planta como en UCIP debe necesariamente estar referida a la edad media de los ingresos y a la proporción de prematuros en la serie. Sin esta estandarización no son comparables los resultados publicados. En estudios de tendencias, se ha observado una disminución de la edad de ingreso5,24 en los últimos años. Globalmente, de lo revisado y de acuerdo con nuestros resultados, la edad de ingreso parece sensiblemente inferior respecto a publicaciones de nuestro entorno de antes de la implantación de la GPC, con edades medias de 3,4 meses28, 3,9 meses5 y 5,5 meses29.
El 15,21% anual de nuestra población susceptible consultó en urgencias por bronquiolitis y el 2,36% de la población susceptible precisó ingreso. En estudios previos este dato oscila entre el 2,12, el 2,324 o el 4,5%26, con una tendencia dispar según las publicaciones que va desde estable24, en disminución4 o en aumento26.
En todas las series publicadas existe un predominio de varones2,3,7,14, que es más acusado (con una significación p<0,05) para el caso de BA no infectadas con el VRS. También el menor peso al nacimiento y la menor edad gestacional están en relación con la BA no-VRS, muy probablemente por el efecto que la administración de palivizumab tiene en nuestro medio (tabla 3).
La lactancia materna tiene un comportamiento que parece proteger más a la BA de virus distintos del VRS, lo que ya ha sido referido previamente25. Dado que el VRS es un virus estacional con menor estabilidad inmunogénica (induce una respuesta pobre y poco duradera30,31), es probable que la leche materna no tenga el nivel de IgA secretora respecto al nivel conseguido frente a los virus no-VRS con mayor estabilidad a lo largo de las distintas epidemias. Ello también explica que en nuestra serie se observe la estabilidad de la prevalencia de ingresos por BA con VRS con independencia de la edad de las madres, al contrario que en los casos no-VRS, en los que la prevalencia va disminuyendo con la edad materna con una significación p<0,01 (tabla 3). La distribución de casos de las bronquiolitis no-VRS es menos explosiva y más uniforme que la del VRS, tal como se aprecia en la figura 1.
La exposición ambiental y gestacional al humo del tabaco ha sido considerada clásicamente como un factor de riesgo de ingreso aun claramente vigente26,32, que en nuestra serie parece afectar en mayor medida a los casos de BA no-VRS (p<0,01; tabla 3) aunque no se relacionó con mayor estancia (tabla 4). Tampoco la fiebre mostró relación con mayor estancia y su presencia se asoció al debut de la BA en el 37,3% de los casos, con predominio para los casos por VRS (p<0,01; tabla 3).
La apnea previa al ingreso, como motivo de consulta asociada a la BA, tiene un comportamiento diferente y es más frecuente en los casos no-VRS. La prevalencia del 5% de apneas durante el ingreso no muestra diferencias con las series publicadas33. Las apneas en la BA pueden ser obstructivas, centrales y mixtas. Es probable que las apneas previas al ingreso sean de predominio obstructivo y, tras el ingreso, con los cuidados respiratorios hospitalarios, tengan menor incidencia durante la estancia. El comportamiento, en este sentido, parece diferente en los casos por VRS respecto a los no-VRS (tabla 3). La presencia de apneas previas al ingreso detectadas por los cuidadores se mostró como factor de riesgo de mayor estancia (tablas 4 y 5).
Respecto a la necesidad de cuidados especiales, la alimentación por sonda es más frecuente en los casos VRS, probablemente por la mayor gravedad de la BA, pero no hay diferencia en la prevalencia de ingresos en la UCIP, que en nuestro estudio fue globalmente del 8,5% de los ingresos en planta. En nuestra unidad no se utilizan cánulas de alto flujo (CAF) en planta por su coste y por la falta de estudios sobre su eficacia y seguridad. Los pacientes que la precisan ingresan en la UCIP sin que nuestra cifra de ingresos sea superior a la publicada y que oscila entre un 6 y un 13%5,14,15,25. Aunque ampliamente utilizada y con resultados prometedores, no ha sido recomendada para utilizarla en plantas de hospitalización a día de hoy en una reciente revisión34.
Los antecedentes de cardiopatía, enfermedad neurológica y displasia broncopulmonar son semejantes a otros trabajos24,27. Su presencia es un criterio de riesgo de ingreso en la UCIP y de prolongación de la estancia por sí mismas. Por ello, en nuestro análisis de estancia prolongada, han sido excluidos.
La presencia de hermanos en el entorno familiar, la atopia familiar y los días de evolución no mostraron relación con la etiología de la BA ni con la prolongación de la estancia. Del resto de variables estudiadas en la tabla 4, el análisis de regresión logística multivariante mostró como factores de riesgo de estancia prolongada el bajo peso al nacimiento, la edad, la presencia de apneas previas al ingreso y la ingesta inferior al 50% (tabla 5), muy en consonancia con trabajos previos7.
La coinfección bacteriana en vías respiratorias bajas en un epitelio destruido por virus como el VRS, en pacientes que aún no tienen edad o no han completado la vacunación antineumocócica, no tiene la relevancia que merece en los diversos estudios publicados, si bien existe evidencia suficiente para afirmar su implicación frecuente en casos que acaban precisando ingreso en una UCIP21,25. Su concurrencia es un claro factor de riesgo de prolongación de la estancia. En estudios recientes se ha implicado hasta en el 29% de las viriasis respiratorias en niños22. En nuestra serie, el diagnóstico clínico de sobreinfección bacteriana respiratoria, ya fuera confirmada o sospechada, superó con creces al de ITU grave.
Las limitaciones de nuestro trabajo son las inherentes a cualquier estudio retrospectivo, como las dificultades de recogida y pérdidas de información. Hay que añadir el hecho de estar circunscrito a pacientes ingresados y de un solo hospital. No se han documentado las consultas en centros de atención primaria previas al ingreso, que en otras series alcanzan el 21% de la cohorte anual2. Tampoco se han tenido en cuenta los efectos de las coinfecciones virales que se estiman en torno a un 30% de los casos7, aunque no sean imprescindibles para el diagnóstico, como se ha comentado anteriormente. Por último, las sobreinfecciones bacterianas son difíciles de delimitar sobre todo en infecciones respiratorias, en las cuales se puede producir elevación de reactantes de fase aguda en algunas infecciones víricas.
ConclusionesEl inicio de la epidemia de la bronquiolitis mostró una variabilidad de hasta 4 semanas en nuestro medio. Tras 5 años de la implantación de la GPC11, la incidencia de ingresos está en torno al 2,3% y parece estable respecto a estudios previos. La edad media de los pacientes desciende a 2,4 meses, aunque con una proporción similar de ingresos en la UCIP de un 8,5%.
Los factores de riesgo independiente asociados a una estancia hospitalaria más prolongada fueron: bajo peso al nacimiento, edad menor de un mes, apneas previas al ingreso, ingesta inferior al 50% y sobreinfección bacteriana grave, donde la infección respiratoria superó la prevalencia de ITU grave.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.